2665例多柔比星脂质体用药人群的严重超敏反应自动监测研究
2021-03-16刘思源郭代红孔祥豪于承暄解放军总医院医疗保障中心药剂科北京00853重庆医科大学药学院重庆40006
刘思源,郭代红,孔祥豪,2,于承暄,朱 雨(.解放军总医院医疗保障中心药剂科,北京 00853;2.重庆医科大学药学院,重庆 40006)
多柔比星属于蒽环类抗肿瘤药物,通过嵌入DNA碱基对,干扰转录过程,起到抗肿瘤作用[1]。该药常见的药品不良反应(adverse drug reaction,ADR)有骨髓抑制、心脏毒性和手足综合征,其中心脏毒性通常呈进展性和不可逆性,极大限制了其临床应用[2]。多柔比星脂质体以脂质体作为外壳包载多柔比星,具有作用时间长、毒性小的特点[2-4]。同时,其在乳腺癌、卵巢癌等多种肿瘤治疗中取得较好疗效[5-7],临床应用日益广泛;但有研究结果显示,其相关过敏反应发生率较修饰前增高[8-9],国内外均有其致严重过敏反应甚至致死的个案报道[10-12]。有文献报道,该药引起的过敏反应可能并非免疫机制介导,而是类过敏反应[13],因此依据国际共识[14],本文称其为超敏反应。
查阅国内外文献,关于多柔比星脂质体相关严重超敏反应的研究大多局限于个案报道和文献分析,尚缺乏基于用药人群的发生率和风险因素研究。本研究依托郭代红团队自主研发的“临床药物不良事件主动监测与智能评估警示系统-Ⅱ”(active surveillance and assessment system of adverse drug events-Ⅱ,ADEASAS-Ⅱ)[15],筛选我院住院人群中发生多柔比星脂质体相关严重超敏反应的病例,计算发生率,深入分析发生特征,探究风险因素,为临床用药提供参考。
1 资料与方法
1.1 数据来源
依托ADE-ASAS-Ⅱ与医院信息系统(hospital information system,HIS)对接,回顾性监测我院2012年1月1日- 2019年12月31日期间所有使用多柔比星脂质体的住院患者。经系统自动筛选(禁用所有排除条件,纳入全部用药人群)、智能报警后,再由两名临床药师背靠背逐一甄别,确定阳性病例,对于有争议的病例,提请专家做最终评判。
运用倾向性评分匹配(propensity score matching,PSM)方法平衡阳性组和阴性组间的混杂因素,匹配因素包括患者性别、年龄、身体质量指数(body mass index,BMI),比例为1∶4,卡钳值为0.01。
1.2 判定标准
参照我国《药品不良反应报告和监测管理办法》中的五项评价标准,判定评价结果为“肯定”、“很可能”、“可能”的为阳性病例。人工评价时,部分皮肤症状与手足综合征症状相似,如红斑、麻木等,但手足综合征为剂量依赖性,最早可能在初始治疗的3~5 d后出现,大多仅表现为皮肤症状[2],而本研究中的阳性病例大多发生于给药过程中,仅有1例发生于输注刚结束,且除皮肤症状外,还累及呼吸等系统,两种类型ADR基本能够区分。此外,心脏毒性也可能在初次用药后发生[2],因此对用药后仅表现为心慌的病例予以剔除。
根据《严重过敏反应急救指南》推荐意见[16],对严重超敏反应进行严重程度分级。
1.3 数据处理
采用K-S检验对计量资料进行正态性检验,满足正态分布的数据用均值±标准差表示,组间比较采用t检验,不满足正态分布的数据用中位数表示,组间比较采用Mann-Whitney U检验。计数资料用频数(构成比)表示,组间比较采用χ2检验,检验水准α= 0.05。单因素Logistic回归结果中,筛选P< 0.05的因素,纳入多因素Logistic回归,进一步探究风险因素。统计分析软件:Excel 2016、SPSS 23。
2 结果
2.1 发生率变化趋势
2012-2019年,我院住院人群中使用多柔比星脂质体的患者共计2665人,10 541例次,人均用药3.96次。经ADE-ASAS-Ⅱ系统自动筛选,获得报警病例175例次,双人评价后,最终确定阳性病例31例,其中关联性评价:“肯定”1例,“很可能”29例,“可能”1例;严重程度分级:Ⅰ级2例,Ⅱ级27例,Ⅲ级2例。逐年统计发现,用药人数从2012年的48例增长至2019的934例,严重超敏反应发生率从0到1.64%不等,严重超敏反应总发生率为1.16%。
2.2 阳性患者的药物溶媒及合并用药
31例阳性病例中,27例多柔比星脂质体溶媒为5%葡萄糖注射液250 mL,2例为5%葡萄糖注射液500 mL;另外2例为0.9%氯化钠注射液250 mL,其中1例患者从2018年2月-7月,连续使用多柔比星脂质体+5%葡萄糖注射液250 mL 12次,间隔7个月后,再次用药时,以0.9%氯化钠注射液250 mL为溶媒,发生严重超敏反应,经抗过敏对症治疗且换用5%葡萄糖注射液250 mL为溶媒后,完成治疗,在下一周期用药过程中无超敏反应发生。
阳性患者化疗方案以AC(多柔比星脂质体+环磷酰胺)为主(29.03%),详见表1。合并用药种类(溶媒除外)平均12种,最少6种,最多17种。化疗前或化疗时给予止吐(甲氧氯普胺、昂丹司琼等)、抑酸(西咪替丁、泮托拉唑等)、保肝(复方甘草酸苷、多烯磷脂酰胆碱等)、保护心肌(磷酸肌酸钠、右雷佐生)、抗过敏(地塞米松、异丙嗪、苯海拉明)等预防性治疗。

表1 阳性患者化疗方案Tab 1 Chemotherapy regimens of positive patients
2.3 严重超敏反应发生特征
阳性患者的总用药周期大多在4周期内(74.19%),最短1周期,最长25周期,人均用药4.68周期,中位数为3周期(1,6);83.87%(26例)的严重超敏反应发生于用药第1周期,4例发生于第2周期,1例发生于第13周期。
31例发生严重超敏反应患者中,30例发生于输注过程中,仅有1例发生于输注刚结束时;8例患者(25.81%)因超敏反应停药未完成治疗,其余23例经暂停输注、抗过敏对症治疗、减慢输注速度等措施完成治疗,其中1例经对症处置、继续输注时,又发生严重超敏反应,再次处置后完成治疗,关联性判定为“肯定”。
严重超敏反应累及系统例次最多的是呼吸系统(38.39%),其次为皮肤系统(31.25%),详见表2。
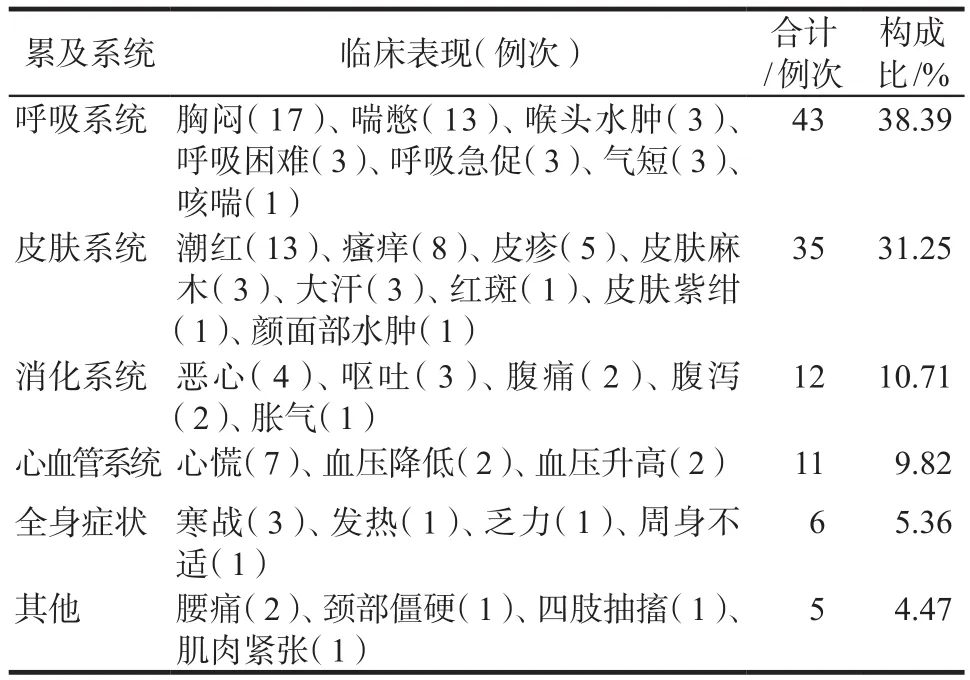
表2 严重超敏反应累及系统和临床表现Tab 2 Systems and clinical manifestations involved in severe hypersensitivity reactions
治疗用药主要为地塞米松(23例次,46.94%)、异丙嗪(13例次,26.53%),其次为苯海拉明6例次,甲泼尼龙琥珀酸钠4例次,葡萄糖酸钙2例次,氯雷他定1例次。2例过敏性休克病例中,抗过敏药物分别为地塞米松+异丙嗪+甲泼尼龙琥珀酸钠、地塞米松+异丙嗪+葡萄糖酸钙,两病例均未使用肾上腺素。
2.4 风险因素分析
为减少混杂因素影响,本研究运用PSM方法,依据患者性别、年龄、BMI,在阴性病例中匹配得到对照组119例,匹配后阳性组与对照组各项信息无显著差异,详见表3。对照组中,化疗方案以R-CHOP(16.81%)、AC(14.29%)为主,分布较分散,详见表4,给药前均给予止吐、抗过敏等预防用药。阳性患者中排名前5位的化疗方案,分布于对照组的前7种内。
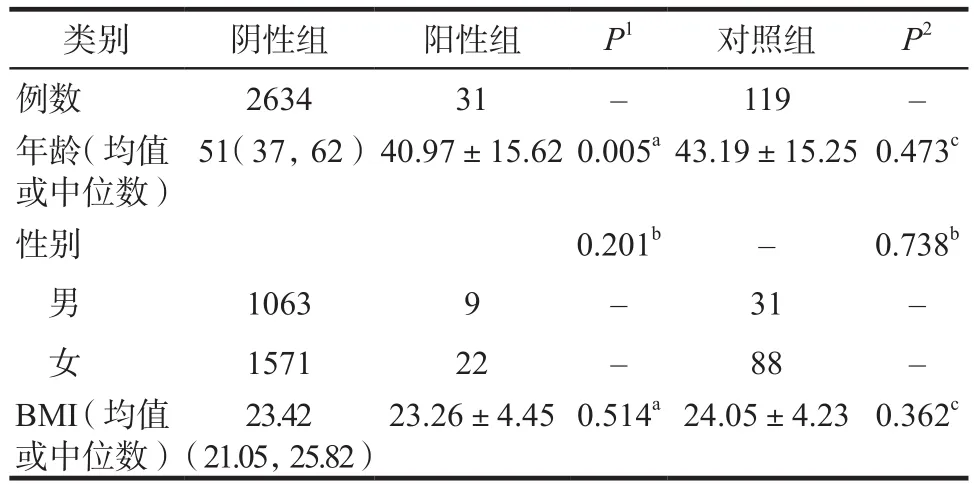
表3 PSM匹配前后人群信息对比Tab 3 Comparison of basic information of patients before and after PSM
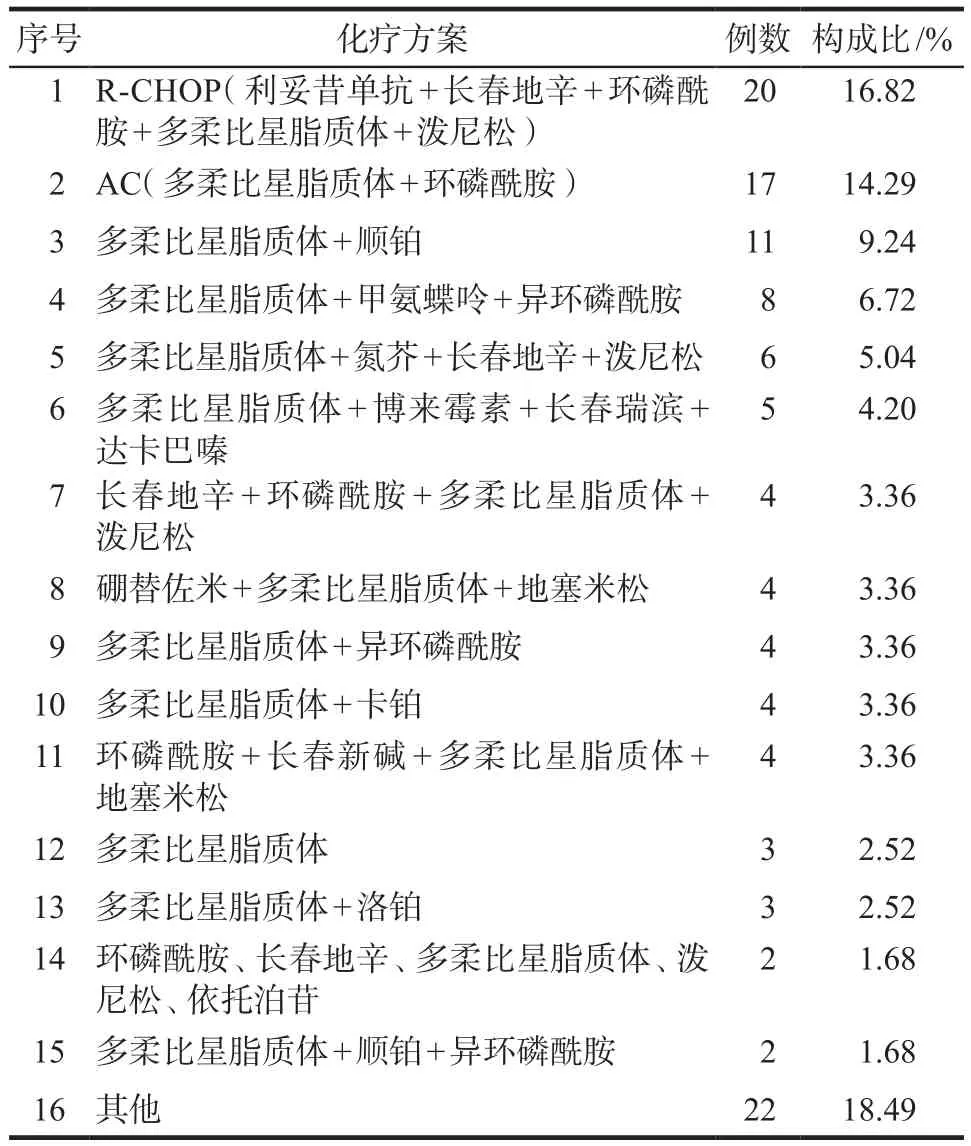
表4 对照组化疗方案Tab 4 Chemotherapy regimens of the control group
比较阳性组和对照组各项信息,单因素Logistic回归结果显示,既往有药物过敏史、霍奇金淋巴瘤、非霍奇金淋巴瘤为影响因素;将以上三个因素纳入多因素Logistic回归,结果显示既往有药物过敏史为独立风险因素(AOR:4.899,95%CI:1.411~17.008)。此外对同期4511例次多柔比星用药人群进行主动监测的结果显示,严重超敏反应发生为0例次。详见表5。
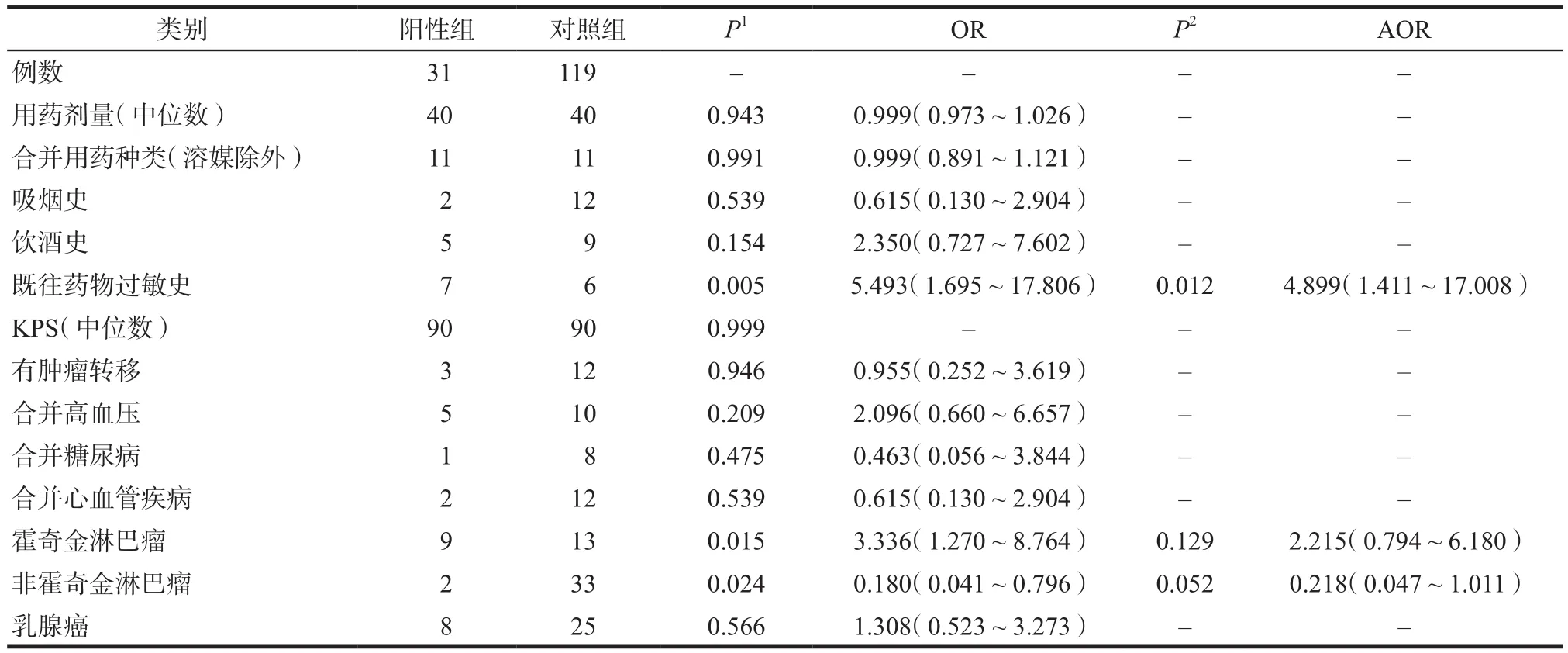
表5 单因素和多因素Logistic回归结果Tab 5 Univariate and multivariate Logistic regression results
3 讨论
3.1 严重超敏反应发生率
统计发现,近年来多柔比星脂质体的用药人群逐年增多,严重超敏反应例数也随之增多,2014年严重超敏反应发生率最高(4%),但例数较少,代表性较差;2015年后严重超敏反应发生率在0~1.64%间波动,总发生率为1.16%。多柔比星脂质体说明书提示,10%的用药患者可发生急性输注反应;查阅文献,其相关超敏反应发生率差异较大。有研究[13]表明,未预防使用抗过敏药物、仅控制滴注速度的情况下,29例患者中有13例(44.83%)发生超敏反应;给予预防用药的研究中,超敏反应发生率为3.08%~9.00%[3,12,17],严重超敏反应发生率为1.32%~2.00%[8,18]。多柔比星脂质体说明书中并未提示需要预防给予抗过敏药物,但我院在使用该药前给予了以地塞米松、异丙嗪为主的预防用药,一定程度上减少了ADR发生,可能导致本研究中严重超敏反应发生率偏低。
Chanan-Khan等人的研究[13]为前瞻性研究,医护人员能够密切关注并及时记录患者相关超敏反应症状,这可能也是其发生率较高的原因。本研究回顾性分析患者的电子病历,由于部分轻微的超敏反应症状,如瘙痒、皮疹等,医护人员可能并未发现或并未记录于电子病历中,因此基于病历分析获得的超敏反应发生率结果可能并不准确。此外,人用药品注册技术要求国际协调会(ICH)E2A指导原则中提示,研究者应重点关注严重ADR信息。因此本研究仅针对严重超敏反应开展自动监测研究,获取更加准确的真实世界数据,为临床提供参考。
3.2 发生周期
多柔比星脂质体说明书和相关文献报道[2,13,19],超敏反应大多发生于首次用药,减慢滴速后可恢复。本研究与上述报道结果基本一致,但其中1例患者经对症处理后再次用药时仍发生类似反应。因此输注时应密切关注患者症状,以便及时采取措施。
研究中还发现有4例ADR发生于第2周期,与相关报道一致[20];1例患者发生于第13周期,该例患者连续用药12周期后,间隔7个月,再次用药时发生ADR,可能与间断用药有关,也可能与患者此次以0.9%氯化钠注射液作为溶媒有关。多柔比星脂质体说明书提示“本品用5%葡萄糖注射液稀释后供静脉滴注”、“其他稀释剂都可能使本品产生沉淀”,有研究[21]也提示“该药不宜与0.9%氯化钠注射液配伍,宜与5%葡萄糖注射液配伍”。本研究150例阳性组和对照组中,仅有2例使用0.9%氯化钠注射液稀释,另外1例也发生ADR。提示临床用药时,应严格按照说明书推荐的稀释方法,以减少ADR的发生。
3.3 发生机制
Szebeni等人的研究结果显示[13,19,22-23],多柔比星脂质体相关的超敏反应可能由于脂质体引起补体激活反应(complement activation-related pseudo-allergy,CARPA),导致肥大细胞释放介质,引起一系列症状,而并非由多柔比星引起的IgE介导的Ⅰ型过敏反应,也有其他研究得到类似结论[24]。本研究也对多柔比星脂质体与多柔比星做了比较,我们对八年间4511例次多柔比星用药人群进行监测,并未发现严重超敏反应发生。从发生率方面来看,超敏反应可能与脂质体的关联性更强。有研究[8]显示多柔比星脂质体组严重超敏反应发生率为1.32%,而表柔比星组为0。
此外,虽然两种反应在临床症状方面基本一致[19],但也有各自的发生特征,IgE介导的Ⅰ型过敏反应,需要致敏过程,一般在多次用药后发生,再激发后更为严重,而CARPA不需致敏过程,一般在首次用药后发生、再激发后症状轻微或消失[13,19,23]。本研究中,ADR大多发生于首次用药,多周期用药后发生较少,从发生特征方面来看,也与CARPA特征更为吻合。
3.4 风险因素分析
本研究运用PSM方法减少混杂因素干扰,匹配后组间信息无统计学差异。两组的预防用药方案和化疗方案也基本一致。比较组间其他信息,用药剂量、合并用药种类、合并心血管疾病等,均未发现风险信号,仅发现既往有药物过敏史为独立风险因素(AOR:4.899,95%CI:1.411~17.008),提示临床用药应关注重点人群。多柔比星脂质体说明书中指出,由于其心脏毒性,有心血管病史的患者需评估利弊才能使用;回归结果显示,在严重超敏反应方面,未见心血管病史对其有显著影响。
3.5 信息化技术在真实世界研究中的应用
本研究依托ADE-ASAS-Ⅱ中基于文本识别技术的过敏反应模块,提取八年间我院住院患者中所有多柔比星脂质体的用药人群10 541例次,耗时仅90 min,快捷高效。模块设置中,禁用所有排除条件,纳入全部用药人群,为开展真实世界研究提供数据支持。该模块依据过敏反应特征词集对病例进行智能报警,词集中不仅涵盖过敏反应相关症状描述(皮疹、呼吸困难、过敏性休克等),还包括治疗药物描述(地塞米松、异丙嗪等)以及辅助用语描述(抗过敏、停药等),尽可能全面的覆盖病历文本中对过敏反应的描述词语,以纳入更多的可疑病例。本研究中,系统共报警175例次,经双人逐一甄别,最终获得31例严重超敏反应病例(报警阳性率为17.71%),极大节省了人力物力,研究人员得以将大部分精力投入到病例评价,获得更加准确、全面的数据,充分体现了运用信息化技术开展真实世界研究的优势。
综上,近年来多柔比星脂质体的用药人数递增,在给予预防用药情况下,严重超敏反应发生率为1.16%,这可能与脂质体的关联性更强,大多发生于首次用药,多数患者经对症治疗后能够完成治疗,也有25.81%的阳性患者中断治疗,需警惕ADR发生的风险,既往有药物过敏史为独立风险因素,临床应重点予以关注。
