基于网络药理学探讨散寒除湿抗毒方治疗COVID-19的物质基础和作用机制
2021-03-01廖金花彭双凤韦祖猛
廖金花 王 兴 彭双凤 凌 利 田 鑫 韦祖猛 邵 婧 李 林*
1.江西中医药大学,江西 南昌 330006; 2.江西中医药大学附属医院,江西 南昌 330006
2019年末以来,新型冠状病毒肺炎(COVID-19)逐渐在全国乃至全球爆发,引起国内外的高度重视,而中医药在COVID-19的治疗中发挥着至关重要的作用。COVID-19属于中医学“疫”病范畴[1],病因以“湿”为主,可称之为“湿毒疫”,病位以上焦为主[2]。散寒除湿抗毒方为国医大师伍炳彩的自拟方,被纳入到“江西省新型冠状病毒肺炎中医药防治方案(试行第三版)”(以下简称江西方案)中,作为治疗寒湿郁肺证的推荐方,在江西省的疫情防治中取得了良好的效果[3]。
寒湿郁肺证是由于疫毒湿寒与伏燥搏结所致[4];国医大师伍炳彩以“寒温一统”思想为指导,以《伤寒论》-麻黄加术汤合《温病条辨》-杏苏散加减而成,起到散寒祛湿,理肺化痰的功效。方中麻黄为君,开腠理、透毛窍,宣肺平喘;桂枝功效有三:一则解肌发表,助君药解表逐邪,二则温通血脉,畅行营阴,三则化气行水以利寒湿;白术“主风寒湿痹”(《神农本草经》),长于健脾祛湿,配麻黄以发汗祛湿;杏仁降气平喘、苏子降气化痰、止咳平喘,杏、苏与麻黄相伍,一宣一降,以助肺气之宣降;前胡降气化痰、桔梗与枳壳配伍宣降肺气,既疏理胸膈气机,又化痰止咳祛邪,三药合用,气顺津布则痰消;陈皮、半夏行气燥湿化痰,以上共为臣药。茯苓健脾以杜生痰之源;生姜、大枣滋脾行津,调和脾胃;炙甘草益气和中,助正达邪,缓和药性,防温燥之麻、桂辛散太过而伤元气之弊,是使药而兼佐药之用。诸药合用,邪正兼顾,共奏散寒除湿,宣降肺气,理肺化痰之功,为散寒除湿抗毒之方剂。
文章通过网络药理学分析散寒除湿抗毒方的潜在有效化学成分、治疗靶点及相关通路,为本方治疗COVID-19提供理论基础和科学依据,亦为本方更好的在国际抗疫中发挥积极作用提供理论支撑。
1 材料与方法
1.1 筛选与获取散寒除湿抗毒方药物成分 在TCMSP(http://tcmspw.com/tcmsp.php)数据库据库中分别输入散寒除湿抗毒方全方生麻黄、杏仁、桂枝、炙甘草、炒白术、紫苏、法半夏、陈皮、前胡、桔梗、枳壳、茯苓、生姜、大枣,以口服生物利用度(OB)≥30%,类药性指数(DL)≥0.18为条件进行筛选,获得14味中药潜在的有效成分。
1.2 收集散寒除湿抗毒方对应靶点 基于TCMSP数据库,根据上述筛选出的散寒除湿抗毒方中14味中药潜在的有效成分预测作用靶点。
1.3 获取COVID-19疾病靶点 分别在GeneCard(https://www.genecards.org/)和OMIM(https://omim.org/)数据库以“Coronavirusdisease 2019”和“coronavirus”为关键词,得到与COVID-19疾病相关的靶点。
1.4 获取潜在作用靶点 利用Uniprot(https://www.uniprot.org/)数据库查询散寒除湿抗毒方可能的作用靶点蛋白对应的基因名,将其基因名和1.3获取的疾病靶点基因名分别录入到Venny2.1在线软件作图工具平台(https://bioinfogp.cnb.csic.es/tools/venny/),制作韦恩图,获得交集靶点基因名,作为潜在作用靶点。
1.5 构建药物-成分-靶点-疾病网络图 将中药化学成分的靶点中与潜在作用靶点相合部分,以及“1.4”所得的潜在作用靶点导入Cytoscape 3.7.2软件,构建“药物-成分-靶点-疾病”相互作用网络,使用Network Analyzer功能对药物中的主要化学成分进行分析,节点的大小代表度(degree)值的大小。
1.6 构建清热化湿抗毒方对COVID-19疾病的作用靶点蛋白网络图 将获得的潜在作用靶点导入STRING网络平台(https://string-db.org/cgi/input.pl),选择物种为Homosapiens进行分析,获得蛋白相互作用关系表,将蛋白相互作用表导入Cytoscape 3.7.2软件,构建蛋白相互作用网络图(PPI),其中节点的大小、颜色的深浅变化代表度值的大小,并根据节点的度值筛选出核心作用靶点。
1.7 GO和KEGG富集分析 通过Metascape(https://metascape.org/)基因注释及分析平台对潜在作用靶点进行富集分析,得到GO(Geneontology)和KEGG(Kyotoencyclopediaofgenesandgenomes)富集分析的柱状图,并进行分层聚类,预测散寒除湿抗毒方化学成分主要作用靶点和潜在生物活动机制。为了进一步获得相关生物活动之间的关系,运用Metascape对GO和KEGG富集通路进行聚类分析,获取散寒除湿抗毒方治疗COVID-19最可能的作用机制。
2 结果
2.1 中药活性化合物及靶点的筛选 通过TCMSP数据库以OB≥30%、DL≥0.18筛选后得到散寒除湿抗毒方活性化合物共266个,其中白术7个、半夏13个、陈皮5个、大枣29个、茯苓15个、甘草92个、桂枝7个、桔梗7个、杏仁19个、麻黄23个、前胡25个、生姜5个、枳壳5个、紫苏14个;通过TCMSP数据库获取中药成分对应的靶点,其中白术23个、半夏172个、陈皮30个、大枣435个、茯苓30个、甘草1769个、桂枝74个、桔梗92个、杏仁207个、麻黄498个、前胡373个、生姜75个、枳壳123个、紫苏151个,去掉重复项后共289个。
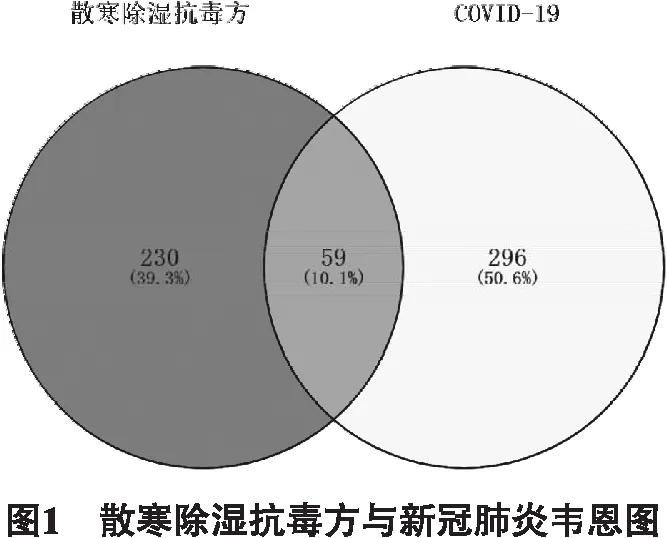
2.2 潜在作用靶点的预测 根据GeneCards、OMIM数据库检索到COVID-19的疾病靶点355个,在Venny2.1在线软件作图工具平台输入药物靶点与疾病靶点,绘制韦恩图(如图1所示),两者交集部分为潜在作用靶点共59个。
2.3 药物-成分-靶点-疾病网络图的构建 将散寒除湿抗毒方潜在的有效成分靶点与59个潜在作用靶点输入Cytoscape软件,筛除与靶点无交集的孤立成分,绘制药物-成分-靶点-疾病网络图(如图2所示)。节点度值(Degree)>15(3倍中位数)的中药潜在有效成分有7种(详见表1),分别为槲皮素、β-谷甾醇、木犀草素、柚皮素、山柰酚、川陈皮素、(+)儿茶素,Degree>40的潜在作用靶点有14个,分别为MAPK3、TNF、IL6、TP53、CASP3、MAPK8、ALB、MAPK1、IL10、IL1B、PTGS2、CXCL8、CCL2、FOS;从表1中发现大部分为多味中药的共有化学成分,且每种成分与多个靶点对应,一个靶点又可对应多种成分,体现了散寒除湿抗毒方多味中药可共同作用于同一靶点,每味中药又可作用于多个靶点的干预特点,能有效干预COVID-19的多靶点,达到较好的治疗效果。
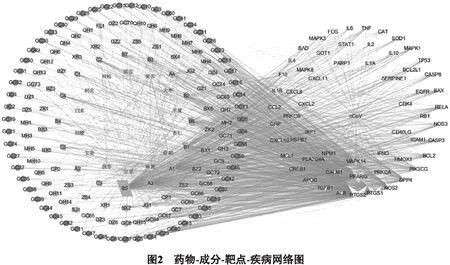
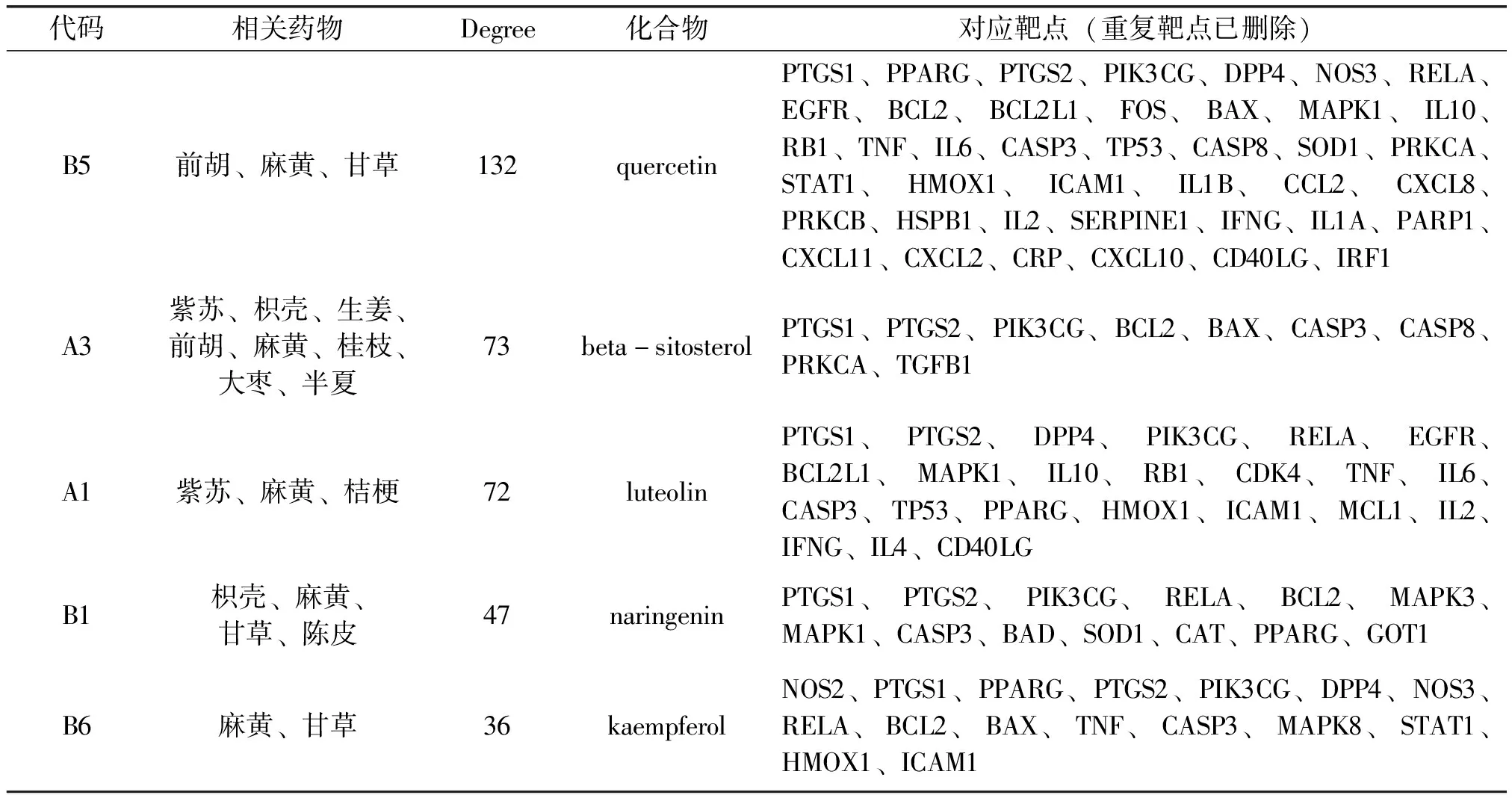
表1 Degree>10的药物主要化学成分信息
2.4 PPI网络图的构建 将59个潜在作用靶点录入STRING数据库中,得到PPI网络关系信息表,使用Cytoscape软件对网络关系信息表进行可视化分析,构建PPI网络图(如图3所示)。Degree>32.5(中位数)的靶点基因有29个,与2.3中Degree>40的潜在作用靶点相互映射,取交集得到潜在核心靶点IL6、TNF、CASP3、MAPK、PPARG,推测散寒除湿抗毒方可能主要通过以上5个靶点对COVID-19进行干预治疗。
为了进一步探讨这些潜在靶点之间相互作用的生物过程,运用Metascape以MCODE算法识别靶点之间最密切的生物过程,收集P<0.01,最小计数为3和富集因子>1.5(富集因子是观察到的计数与偶然期望的计数之比)的术语,并根据其成分靶点之间相互关系的密切程度得到前3个具有丰富生物过程的核心富集模块,进行富集分析后按P值划分,选取3个最佳功能描述(表2),图4中左上核心富集模块主要涉及乙型肝炎、细胞凋亡和弓形虫病,右上核心富集模块主要涉及糖尿病并发症中的AGE-RAGE信号通路、癌症的途径和鞘脂信号通路,左下核心富集模块主要涉及趋化因子信号通路、细胞因子与细胞因子受体的相互作用和IL-17信号通路。
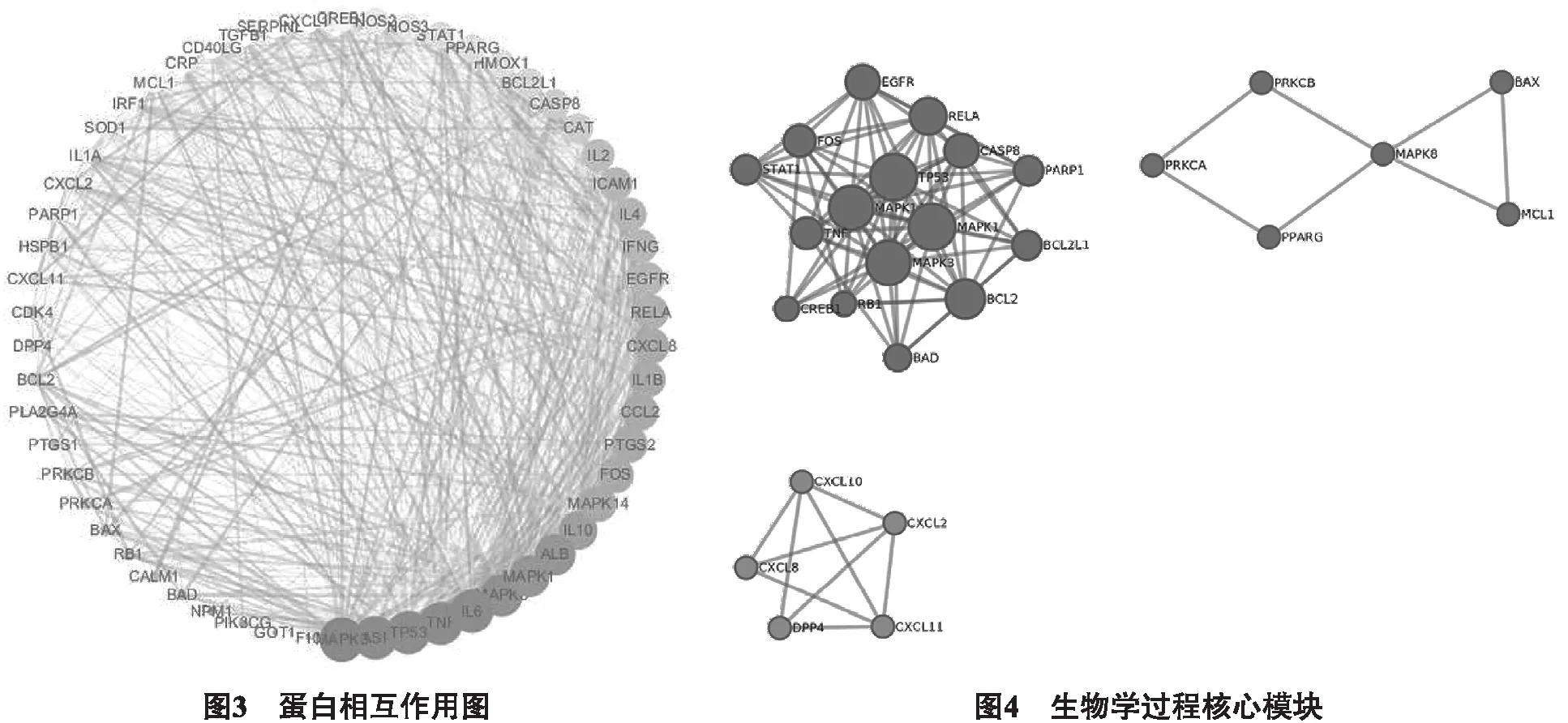
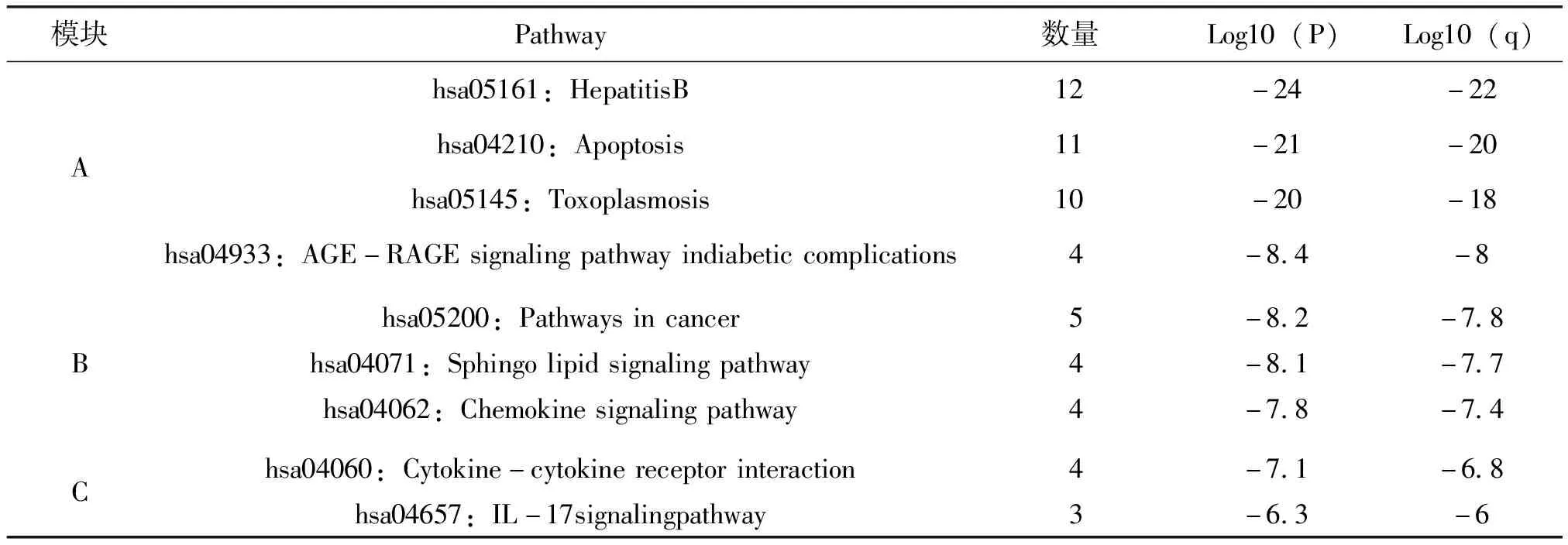
表2 核心富集模块功能描述
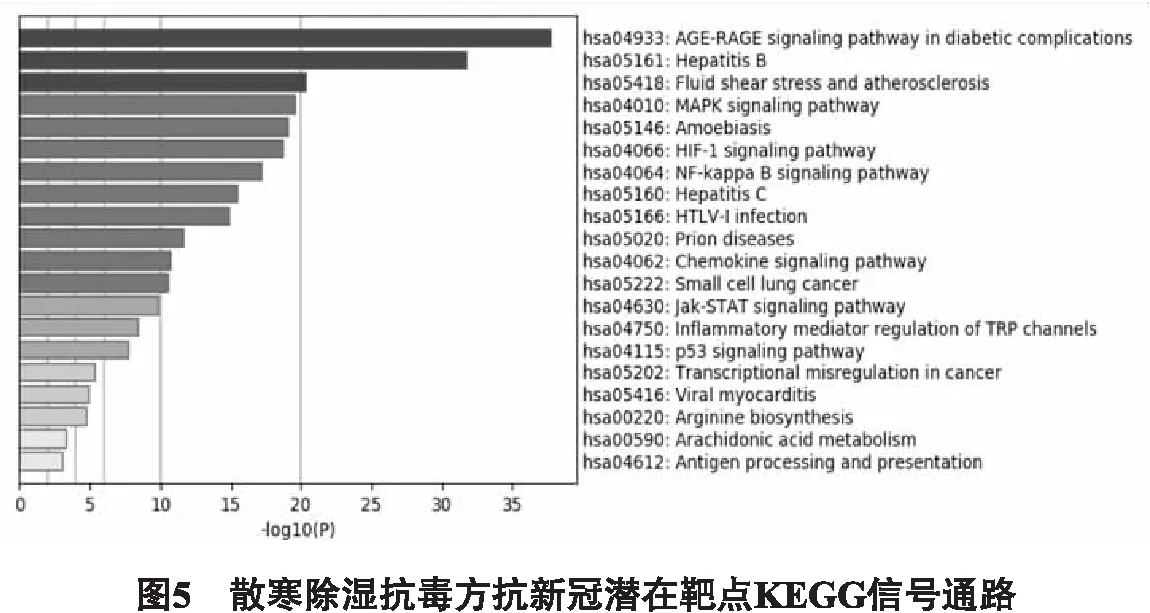
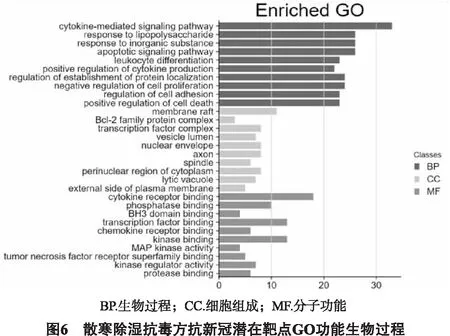
2.5 富集分析 为探讨上述59个交集靶点在治疗COVID-19中的作用机制,运用Metascape对59个的靶点进行KEGG(如图5所示)和GO(如图6所示)富集分析,KEGG分析得到206条通路途径,GO分析得到419分子功能、4435个生物学过程、323个细胞组分,KEGG取前20条通路,GO 分子功能、生物学过程和细胞组分分别取前10个作为重点展示。主要涉及的KEGG富集通路主要涉及:糖尿病并发症的年龄-愤怒信号通路、MAPK信号通路、趋化因子信号通路;GO生物学过程:细胞因子介导的信号通路、凋亡信号通路、调节细胞粘附等;GO细胞组成:膜筏、Bcl-2家族蛋白复合物、转录因子复合体等;GO分子功能:细胞因子受体结合、磷酸酶结合、BH3域绑定、转录因子结合、趋化因子受体结合等。
3 讨论
《说文解字》中提到“疫者,民皆病也”,疫病具有强烈的传染性,本次COVID-19亦属于中医“疫”病范畴[5]。针对此次疫情,仝小林院士等[6]通过实际调查,初步提出本病归属于“寒湿疫”,认为“寒湿”是COVID-19爆发的关键因素。国医大师伍炳彩认为对于COVID-19寒湿兼燥者,当以麻黄加术汤去寒湿,合用杏苏散治凉燥,故自拟散寒除湿抗毒方用于治疗寒湿兼燥的新冠肺炎[7],现已被纳入到江西方案中作为推荐方,为新冠肺炎治疗提供了江西方案。
本研究共筛选出散寒除湿抗毒方治疗COVID-19的148个成分,运用Cytoscape 3.7.2通过中位Degree值筛选得到7个主要潜在成分,其中6种为黄酮类化合物,分别为槲皮素、β-谷甾醇、木犀草素、柚皮素、山柰酚、川陈皮素,另1种为黄烷衍生物(+)儿茶素。散寒除湿抗毒方与COVID-19有59个交集靶点,通过PPI网络与“药物-成分-靶点-疾病网络”相映射发现本方可能主要通过作用于IL6、TNF、CASP3、MAPK、PPARG等潜在核心靶点,改善新冠肺炎患者临床症状,从而达到干预COVID-19的效果。
3.1 散寒除湿抗毒方通过调节免疫-炎症反应干预COVID-19 COVID-19入侵人体后可诱导过度的炎症反应,导致弥漫性肺损伤、ARDS、多器官衰竭甚至死亡。因此,调控免疫-炎症反应是治疗COVID-19,改善临床症状的途径之一[8];涉及的化合物有:槲皮素、β-谷甾醇、木犀草素、柚皮素、山柰酚、川陈皮素;涉及的靶点有:PTGS2、TNF、IL6、IL-10。
有研究发现,槲皮素能抑制巨噬细胞分泌PTGS2,刺激巨噬细胞进一步分化成熟,成为活化巨噬细胞,增强吞噬功能,从而调节免疫炎症反应[9];又有研究发现槲皮素可以抑制单纯疱疹病毒1型感染诱导的IRF-3和NF-JB的激活,减少RAW264.7细胞产生的炎症因子:肿瘤坏死因子-α(TNF-α)[10]。β-谷甾醇可通过下调IL6和TNF-α水平,改善炎症反应[11];柚皮素能通过抑制环氧合酶(COX),减少前列腺素PGE2的合成,减少炎性因子的释放,调节免疫炎症反应[12];山柰酚可减少促炎细胞因子(IL-12和TNF-α)的释放,并通过抑制IKK的磷酸化和IKBα的降解来调节NF-KB的水平,从而改善CPL介导的炎症[13];川陈皮素能抑制肾小球系膜细胞HBZY-1炎症因子MCP-1和IL6的表达水平,减轻炎症反应[14];(+)儿茶素中所含的要表没食子儿茶酚没食子酸(EGCG)及表没食子儿茶酚(EGC)在MDCK细胞中对流感病毒的复制具有抑制活性,其中EGCG可能与病毒粘合,防止病毒入侵MDCK细胞,间接减轻炎症反应[15]。
3.2 散寒除湿抗毒方可能通过调控细胞凋亡干预COVID-19 细胞凋亡主要有三种途径:线粒体通路、死亡受体通路和内质网通路。冠状病毒主要通过外在途径(死亡受体通路)诱导细胞凋亡。散寒除湿抗毒方可通过PARP1、CASP3、CASP8、MAPK1、MAPK3、MAPK8、TNF、TP53等靶点调控细胞凋亡。
研究发现:SADS-CoV感染时细胞可出现明显的CPE,显微镜下可见凋亡细胞胞质固缩和细胞膜融合、染色质凝缩并附在核膜周边,形成凋亡小体[16]。Fas/CD95 是细胞膜上主要的死亡受体,许多冠状病毒的S蛋白可诱导激活细胞膜死亡受体,最终引起由 Caspase 级联信号途径诱导的细胞凋亡[17]。SARS-CoV诱导的细胞凋亡依赖于Caspase家族,Caspase抑制剂过表达可抑制细胞凋亡[18]。木犀草素既能通过调控CASP8、CASP3的表达干预流感病毒诱导的细胞凋亡[18],又能通过降低过氧化物酶活性、TNF-α和IL6水平,以及提高IL-4和IL-10水平,抑制NF-KB,从而抑制细胞凋亡途径[18];新冠患者心肌细胞或激活后白细胞释放的TNF、IL6具有启动凋亡程序的作用[23]。散寒除湿抗毒方可通过调控细胞凋亡过程,进而对COVID-19进行干预。
3.3 散寒除湿抗毒方可能通过鞘脂类信号通路干预COVID-19 鞘脂类通路激活,可使血管通透性增加,表面活性剂钝化,肺泡上皮细胞凋亡,诱发肺水肿[24]。散寒除湿抗毒方可通过靶点:BAX、BCL2、MAPK14、NOS3、PRKCA、PRKCB、MAPK1、MAPK3、MAPK8、RELA、TNF、TP53调节鞘脂类信号通路,缓解肺水肿及肺组织损伤。
国内第一例新冠尸体解剖发现:右肺严重淤血,肺水肿,心外膜水肿。故调节血管屏障对新冠肺炎的治疗具有重要的临床意义[25-26]。而鞘脂类物质是一种极其重要的血管生成因子和具有强大的血管屏障调节特性的信号介质。鞘氨醇1-磷酸(S1P)是神经鞘磷脂代谢产生的一种有生物活性的脂类,由神经酰胺代谢产生,S1P已在体外被证实了具有增强肺血管屏障的功能[27-29];血小板一直被认为可以降低血管内皮通透性,研究发现,S1P是人类血小板产生的关键屏障保护性介质[30];S1PR4和S1PR5可与Giand G12/13偶联,通过G12/13的信号可以抑制迁移,降低内皮屏障功能,并通过促进GTPase Rho和Rho相关激酶(ROCK)的激活来诱导血管收缩;S1P还能有效减轻NOS2刺激的肺损伤[30]。散寒除湿抗毒方中的化合物山奈酚、槲皮素、木犀草素都具有调控鞘脂类信号通路的作用。
综上可知,散寒除湿抗毒方可通过调节免疫-炎症反应,以及通过调控细胞凋亡及鞘脂类信号通路,对COVID-19进行干预。散寒除湿抗毒方作为国医大师伍炳彩的自拟方,被选入“江西方案”中作为推荐方,其对于新冠肺炎的治疗效果在临床中也已经得以证实。本研究通过对散寒除湿抗毒方的药物潜在有效成分、潜在作用靶点及相关通路进行分析,预测散寒除湿抗毒方治疗COVID-19的潜在作用机制,为中医药治疗COVID-19提供一定的理论基础和科学依据,为后续研究及开发院内制剂提供参考。
