尼妥珠单抗联合放化疗治疗局部晚期头颈部恶性肿瘤的临床效果观察
2021-02-28苏家兴崔英强
苏家兴,崔英强
(1.云浮市人民医院 肿瘤科,广东 云浮 527300;2.高州市人民医院 肿瘤内科一区,广东 高州 525200)
0 引言
头颈部恶性肿瘤的治疗方式主要是手术+放化疗,但如果癌症进展到晚期,上述治疗方式最佳时机已错过,往往只能利用化疗手段来自制机体肿瘤细胞的生长速度[1]。但临床实践可知,放化疗虽然能提高局部晚期头颈部恶性肿瘤患者的局部控制率,降低患者的淋巴转移率,控制肿瘤局部复发率,但整体疗效欠佳,且放化疗会严重损害患者的机体,因而受到一定限制[2]。随着临床医学不断深入研究癌症的发病机制,临床逐渐将研究重点放在分子靶向治疗上。临床研究发现,表皮生长因子受体(EGFR)在多种恶性肿瘤细胞上均有分布,其和肿瘤细胞的增殖、分化、浸润、凋亡等都存在相关性,因此临床将其作为肿瘤靶向治疗的一个关键靶点[3]。尼妥珠单抗(nimotuzumab)属于一种人源化单克隆抗体(lgG1,亚型),能够抑制内源性配体和EGFR产生结合,以此阻断EGFR的细胞学效应,阻止介导下游信号的传导通路,从而对肿瘤细胞增殖、转移、浸润产生抑制,促使肿瘤细胞凋亡[4]。本研究针对局部晚期头颈部恶性肿瘤实施妥珠单抗联合放化疗来治疗,具体内容报道如下。
1 资料与方法
1.1 一般资料
选择2016年1月至2020年12月本院收治的86例局部晚期头颈部恶性肿瘤开展研究。入组条件:通过病理活检确诊是恶性肿瘤;临床诊断属于局部晚期(T3N1M0~T4N3M0)头颈部恶性肿瘤;患者的与预期生存时间>3个月;无手术适应证;肝肾功能正常;了解研究目的并签署知情同意书。排除标准:无法完成完整的治疗;在研究期间更换或者加用其他治疗药物;无法评定治疗效果者。随机将86例分配法分成参照组与实验组,各组有病患43例。两组患者的性别、年龄、肿瘤部位、血常规指标等对比无统计学意义(P>0.05)。见表1。本研究经过医院伦理委员会批准。

表1 两组患者基线资料对比
1.2 治疗方式
参照组只采取根治性同步放化疗,每一周采取25~40mg/m2的顺铂(江苏豪森药业集团有限公司,国药准字:H20040813,规格:6mL:30mg)进行化疗治疗,每周治疗1次,同时给予患者适形调强放疗,将照射范围设置成为淋巴结区域与原发灶区域,如果肿瘤体积较大(GTV),药物剂量66~72Gy,转移淋巴结GTV剂量64~68Gy,临床高危靶区体积(CTV1)剂量为60~64Gy,临床低危靶区体积(CTV2)剂量50~54Gy,疗程为6~7周。
在上述基础上,实验组联合尼妥珠单抗(50mg:10mL/瓶,国药准字:S20080001,百泰生物药业有限公司生产)进行治疗,患者每次使用100~200mg,将尼妥珠单抗加入250mL的生理盐水中,为患者进行脉滴注,滴注时间应当超过1h,一天治疗1次,疗程共6周。
1.3 观察指标
1.3.1 疗效判断标准
①完全缓解(CR):所有的目标病灶都不见,不见的时间教育超过1个月;②部分缓解(PR):基线病灶体积明显缩小,缩小范围超过原本范围的30%;③稳定(SD):患者的基线病灶的体积没有改善,或者增大<20%;④进展(PD):患者的基线病灶体积发生增大,且增大>20%。治疗有效率=完全缓解率+部分缓解率;临床控制率=完全缓解率+部分缓解率+稳定率。
1.3.2 随访观察
对所有患者进行为期1年的随访观察,统计两组的1年生存率;统计患者出现的不良反应,包括脱发、骨髓抑制、食欲下降、消化道反应、口腔黏膜损害等。
1.4 统计学方法
选用SPSS 19.0统计学软件处理分析,计数资料实施χ2检验,计量资料采取t检验,P<0.05表示差异有统计学意义。
2 结果
2.1 对比两组近期疗效
实验组的治疗有效率为69.77%、临床控制率为95.35%、1年生存率为88.37%均显著高于参照组的治疗有效率为48.84%、临床控制率为72.09%、1年生存率为69.77%,对比有统计学意义(P<0.05)。详见表2。
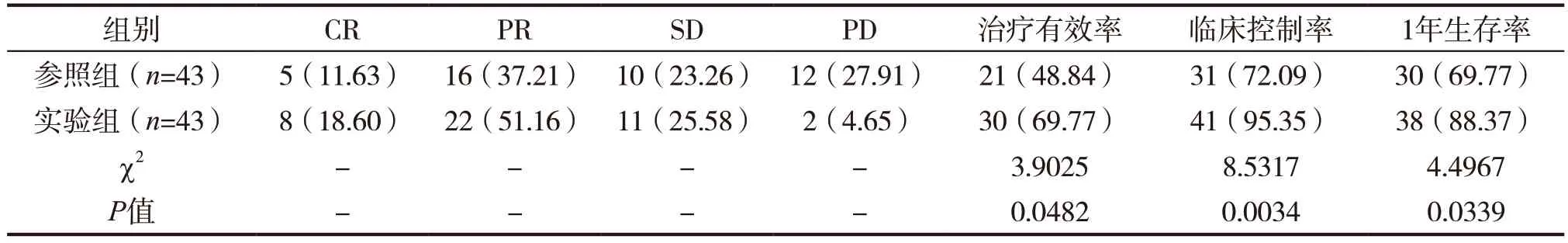
表2 两组近期疗效对比[n(%)]
2.2 两组不良反应发生率对比
实验组出现的不良反应例数与参照组比较P>0.05。见表3。
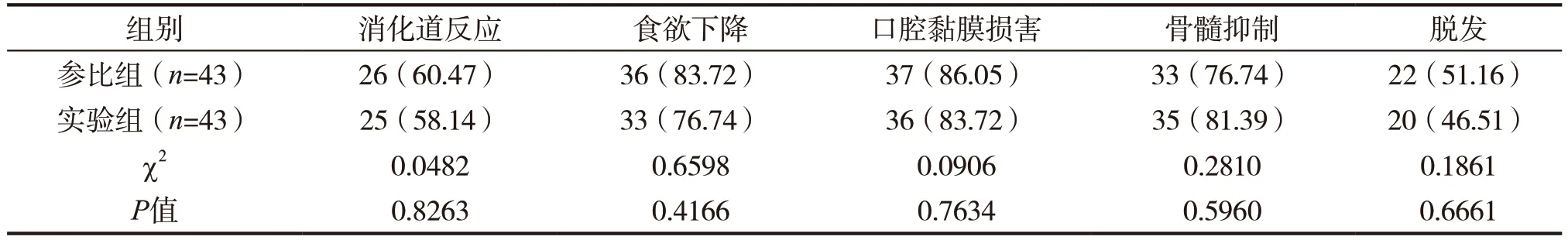
表3 两组不良反应发生率对比[n(%)]
3 讨论
放化疗治疗局部晚期头颈部恶性肿瘤主要是将一定放射剂量施加在局部病灶区域,将肿瘤细胞直接破坏,以此抑制肿瘤发展;化疗时,经患者的静脉滴注顺铂,利用细胞毒作用让患者的肿瘤细胞相关DNA形成一种双链加合,以此抑制肿瘤细胞DNA的合成,以此达到抑制肿瘤的治疗目的,同时还可以对肿瘤新生血管的形成产生抑制[5]。临床实践可知,放化疗虽然可以有一定的肿瘤细胞抑制作用,能够避免患者机体内的肿瘤避发生扩散或者转移。但是,放化疗治疗效果有效,有数据显示,有25.00%~33.33%的患者因对放化疗抵抗性及肿瘤细胞多药耐药性等发生了肿瘤细胞扩散或者转移现象[6]。
靶向治疗主要是根据肿瘤细胞生物特性改变视作治疗的靶点,在提高抗肿瘤活性的强度时,减少对人体正常细胞的毒副作用。近些年,临床更进一步的了解局部晚期头颈部恶性肿瘤的病因学及药物抵抗机制等生物学行为,并针对局部晚期头颈部恶性肿瘤的特定靶点,制定了分子靶向治疗[7]。随着小分子抑制物与单抗等药物的相继产出,临床发现这些药物能够对肿瘤细胞的产生及进展过程中的相关机制进行有效抑制,包括肿瘤细胞的增殖、血管生成、残存、转移等,以此获得有效的治疗效果。在局部晚期头颈部恶性肿瘤中,有较多肿瘤的靶点能够进行靶向治疗,例如EGFR、基因突变、血小板衍生生长因子(PDGF)、血管内皮生长因子(VEGF)等,其中相关研究最多的是EGFR[8]。在局部晚期头颈部恶性肿瘤中,大多数肿瘤疾病的EGFR一般都是过表达的,EGFR通道一般会被非正常激活。有研究显示,EGFR表达也是局部晚期头颈部恶性肿瘤一个重要的预后因素,其过表达会相应预示患者的总生存与无病生存率,同时存在EGFR表达显示肿瘤患的局部复发率更高[9]。目前临床已经证实EGFR的自分泌途径和肿瘤发生、发展等多个过程存在密切相关性,例如血管形成、细胞增殖、细胞凋亡、细胞调控、转移扩散。EGFR已成为了局部晚期头颈部恶性肿瘤最常用的靶点之一。王凤[10]研究表明,头颈部恶性肿瘤采取EGFR治疗时表现为高表达,而采取肿瘤活检标本来进行免疫组化法检测,可见鼻咽癌患者中的EGFR表达率大约为80%~95%,这表明了EGFR高表达属于头颈部恶性肿瘤预后不良的一项高独立危险因素。因此,局部晚期头颈部恶性肿瘤进行靶向治疗已经是当前临床治疗的一种新选择。目前,临床上的表皮生长因子受体抑制剂(EGFRI)根据相应的作用原理有很多种分类,包括抗毒素、单克隆抗体、酪氨酸激酶抑制剂等,而在临床应用较多的单克隆抗体主要包括尼妥珠单抗、西妥昔单抗、帕尼单抗等。
尼妥珠单抗能够和EGFR发生特异性结合,这是一种人源化单克隆抗体,能够选择性地结合目标受体进,对EGFR酪氨酸激酶的活性产生抑制,将EGFR介导的下游信号传导通路进行阻断,将EGFR的细胞学效应实施抑制,避免肿瘤的再次增殖;同时这种药物还有较高的人源化程度,能够选择性作用在患者的在肿瘤EGFR、皮肤上,不会对人体的皮肤修复及更新产生影响,同时临床过敏概率相对角度,不会导致患者发生较多的皮疹不良反应,即便导致患者出现皮疹,其程度也较轻[11]。临床已有研究证实,对于头颈部鳞癌存在EGFR高表达的患者实施靶向治疗,其获得疗效较佳,患者的耐受性好。国内外有大量研究显示,尼妥珠单抗联合放化疗协同治疗,对头颈恶性肿瘤、神经胶质瘤等均能够增强化疗效果[12]。本研究结果显示,实验组的治疗有效率为69.77%、临床控制率为95.35%、1年生存率为88.37%均显著高于参照组的治疗有效率为48.84%、临床控制率为72.09%、1年生存率为69.77%,对比有统计学意义(P<0.05)。实验组出现的不良反应例数与参照组对比(P>0.05)。这证明尼妥珠单抗联合放化疗对局部晚期头颈部恶性肿瘤实施治疗,能够很好的抑制患者的肿瘤,让患者长期生存期得到延长,可以将其作为局部晚期头颈部恶性肿瘤的一种创造新治疗方法。
综上所述,局部晚期头颈部恶性肿瘤患者采取尼妥珠单抗联合放化疗治疗,有助于患者提高近期疗效,为患者开辟新治疗选择,值得推广应用。
