腹腔镜超声引导微波消融治疗原发性肝癌的疗效分析
2021-02-27金一帮童晓春徐智锋潘江华李幼林胡逸人
金一帮,陈 璐,童晓春,徐智锋,潘江华,李幼林,胡逸人
(温州市人民医院普通外科,浙江 温州,325000)
原发性肝癌是常见的消化道恶性肿瘤,目前传统手术仍是治疗肝脏恶性肿瘤最可靠的手段,但由于肿瘤本身的生物学特性等原因,最终有机会接受手术根治的患者仅约占20%[1]。随着微波技术在医学领域的广泛应用,微波消融在治疗肝癌方面具有疗效确切、损伤小、安全性高等优点,尤其腹腔镜技术的联合应用,相较传统经皮微波消融具有一定优势。我院采用腹腔镜B超引导下微波消融治疗原发性肝癌取得满意疗效,现总结报道如下。
1 资料与方法
1.1 临床资料 选择2016年1月至2017年12月诊断原发性肝癌并在我院行微波消融治疗的124例患者,根据治疗术式分为观察组(行腹腔镜超声引导微波消融术,n=62)与对照组(行经皮超声引导微波消融术,n=62)。选择标准:(1)依据病史、甲胎蛋白(alpha fetal protein,AFP)、异常凝血酶原(PIVKA-Ⅱ)、影像学检查及病理报告等证实为原发性肝癌;(2)无大血管浸润,无淋巴结或肝外转移;(3)术前检查评估均为肝功能分级Child-Pugh A或经内科治疗达到此标准;(4)无合并其他严重内科疾病或轻微内科疾病;(5)病灶直径<5 cm,数量≤4。术前向患者或家属充分告知手术过程及可能风险,并签署知情同意书。排除标准:(1)合并门静脉癌栓或下腔静脉癌栓;(2)心、脑、肾、血管等严重内科疾病;(3)肿瘤直径≥5 cm;(4)各种原因不能耐受手术。两组患者临床资料差异无统计学意义,具有可比性,见表1。
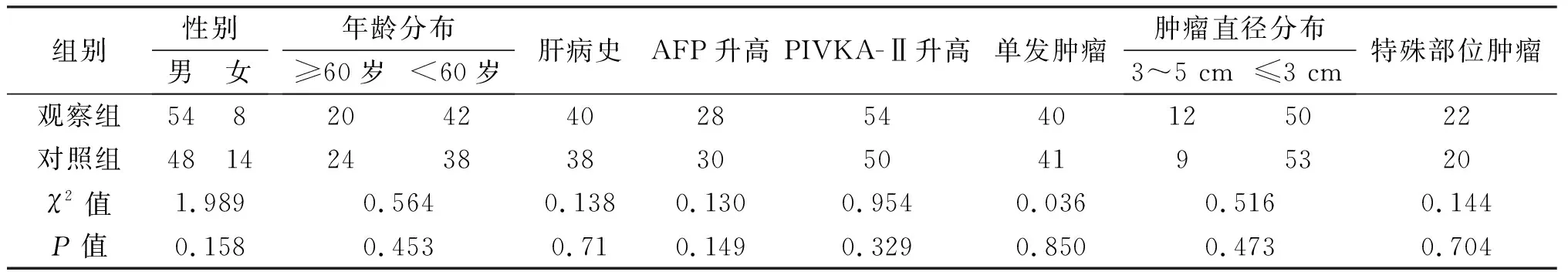
表1 两组患者临床资料的比较(n)
1.2 手术方法
1.2.1 观察组 患者取仰卧位,采用全身麻醉,建立人工气腹。腹腔镜直视下使用腹腔镜超声再次扫描肝脏,根据肿瘤位置、大小、数量等确定腹腔镜微波消融治疗方案。超声刀游离肝脏,通过超声探头引导,腹壁插入微波消融针,针芯超过肿瘤中心,功率设置为80~100 W,根据实际情况设置4~10 min的消融时间进行微波消融治疗,并在腹腔镜直视下观察是否发生异常。通过术中B超动态实时监测,治疗过程中消融处回声逐渐增强并覆盖肿瘤,保证消融范围达肿瘤周边1.0 cm的肝脏组织,达到标准后将针退出适当位置并进行再次消融,直至肿瘤完全消融,拔出针尖前对针道进行适当消融,以预防针道种植及出血。治疗后1周复查血清肿瘤指标,并行腹部增强CT或腹部MRI判断肿瘤灭活情况,针对未完全消融病例,再次行微波消融治疗,以确保病灶完全灭活。
1.2.2 对照组 患者取左侧卧位或仰卧位,必要时予以静脉麻醉辅助,B超再次扫描肝脏,确定病灶并定位,局部浸润麻醉后进行穿刺,具体消融方法、术后处理同观察组。
1.3 观察指标 (1)术中新发现肿瘤数量:术中再次进行肝脏扫描,观察有无术前检查未发现的病灶。(2)术后并发症情况:观察术后出现的并发症,主要包括:较严重的消融后综合征及胸腹腔积液、肝肾功能障碍等常见并发症。(3)肿瘤完全消融率:为完全消融病例占所有病例的百分比。判定方法:术后1个月复查MRI或增强CT,观察消融区域有无肿瘤信号,若无则判定为完全消融,否则为未完全消融[2]。(4)局部复发率、肿瘤再发率:术后随访2年,期间如发现原消融区域病灶,则判定为局部复发,如出现其他位置新发病灶,则判定为再发。(5)相关肿瘤标志物:术后1周对两组患者AFP及PIVKA-Ⅱ进行复查并比较降低情况。(6)生存率:术后随访2年,计算两组生存率。
1.4 统计学处理 应用SPSS 17.0软件进行数据分析,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结 果
两组术中新发现病灶情况、肿瘤完全消融率差异有统计学意义(P<0.05),两组AFP、PIVKA-Ⅱ术后1周降低情况差异无统计学意义(P>0.05),见表2。观察组并发症发生率为9.7%(6/62),对照组为24.2%(15/62),两组差异有统计学意义(P<0.05)。见表3。术后随访2年,两组局部复发率、肿瘤再发率、1年生存率、2年生存率差异无统计学意义(P>0.05),见表2。
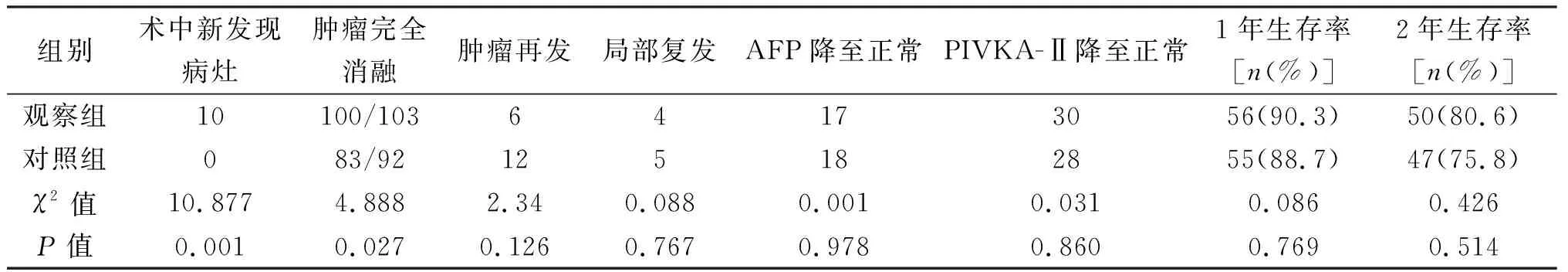
表2 两组患者观察指标的比较(n)
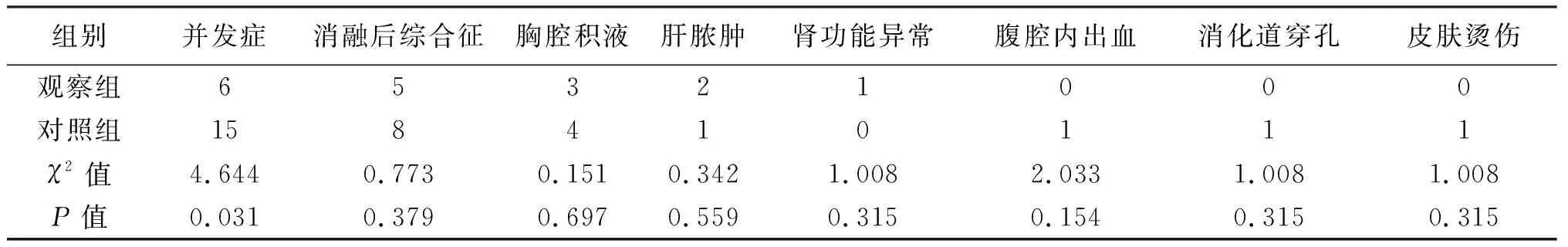
表3 两组患者术后并发症的比较(n)
3 讨 论
原发性肝癌是世界范围内多发的消化道恶性肿瘤,具有较高的病死率。我国是肝脏恶性肿瘤的高发国家之一。由于原发性肝癌本身的生物学特性,多数患者确诊时往往已错过手术根治的时机。随着微波消融技术在医学领域的应用与发展,其在治疗肝癌方面疗效确切,且具有创伤小、热效率高、凝固坏死率显著等优点,已逐渐成为成熟可靠的治疗肝癌的新手段。目前,经皮微波消融治疗原发性肝癌的应用最为广泛,在临床疗效方面得到公认。随着腹腔镜技术的不断发展,越来越多的研究表明,腹腔镜超声引导微波消融治疗原发性肝癌具有诸多优势,尤其在排除遗漏病灶、提高特殊部位肝癌的完全消融率等方面优势明显;在疗效方面,针对直径≤3 cm,甚至直径为3~5 cm的原发性肝癌均取得确切疗效,具有较高的肿瘤坏死率与生存率[3-4],可与手术切除媲美。
目前临床腹腔镜技术发展相对成熟,手术创伤小,相较经皮穿刺微波消融术,腹腔镜技术具有更清晰、灵活的视野,不仅扩大了监测范围及手术适用性,而且可更好地定位肿瘤,提高穿刺定位的准确性[5],避免与减少术中因定位或进针困难对邻近腹腔内脏器的误伤,如果术中出现意外情况,腹腔镜直视下可帮助我们及时发现问题并处理。本研究中病例均较顺利完成手术,完成时间较稳定且出血量相对较少。在术后并发症方面,观察组发生率为9.7%,优于对照组的24.2%(P<0.05);其中术后腹腔出血、邻近脏器损伤、皮肤烫伤等并发症均见于对照组,并未出现在观察组,考虑腹腔镜直视下精准定位、精准穿刺及实时术中监测等优势在减少或避免此类并发症方面可能发挥重要作用,需进一步研究证实。通过腹腔镜技术,术中再次超声扫描有助于对肿瘤进行准确分期,并能发现术前影像学未能发现的病灶[3],腹腔镜超声探头的应用,与体外超声相比具有信号强、干扰小、图像清晰、观察角度灵活等优势,术中更容易发现微小病灶。本研究中,观察组新发现病灶18处,均为术前B超、MRI检查未发现病灶,而对照组术中并未发现新增病灶,两组差异有统计学意义,提示腹腔镜B超的应用能较好地排除遗漏病灶,进一步提高疗效。术后1个月复查增强CT显示,观察组共103处消融病灶,未见明显强化的病灶100处,统计完全消融率达97.1%,高于对照组的90.2%(P<0.05);两种治疗方法均体现出较好的局部疗效。肿瘤病灶是否完全消融,与术中消融针的穿刺精确度密切相关,腹腔镜技术的应用为此创造了有利条件,这在特殊部位(如毗邻膈肌、空腔脏器、肝内大血管、胆管等)的肝脏肿瘤行微波消融治疗时优势更为明显[5]。通过两年的随访复查,观察组局部复发率为6.5%,与文献报道接近[6],肿瘤再发率为9.7%,与对照组相比差异无统计学意义,显示与传统经皮微波消融相比,本治疗方法同样具有较低的局部复发率与肿瘤再发率,治疗效果满意。此外,针对局部复发、再发的病灶,腹腔镜下超声引导的微波消融也可进行重复性治疗,在临床上还适于肝切除术后复发、其他介入治疗后复发及肝转移癌的治疗等诸多方面,适用性广、安全性强。
AFP与PIVKA-Ⅱ是反应原发性肝癌较敏感的肿瘤标志物,是目前用于筛查与诊断原发性肝癌的常用指标,也是病情评估、疗效判定的参考指标[7-8]。本研究中两组术后AFP、PIVKA-Ⅱ降低情况相近,差异无统计学意义,表明微波消融治疗原发性肝癌具有确切的肿瘤灭活效果。通过随访,观察组1年、2年生存率分别为90.3%与80.6%,与文献报道的94.7%、81.9%相似[9],与对照组(88.7%与75.8%)相比,差异无统计学意义(P>0.05),提示腹腔镜下超声引导的微波消融与经皮微波消融相似,具有较好的远期疗效。
综上所述,与经皮微波消融治疗相比,腹腔镜超声引导微波消融治疗直径<5 cm的原发性肝癌疗效确切,能更好地排除遗漏病灶,具有术后并发症少、肿瘤完全消融率高等优势,是安全、有效的治疗方法,值得进一步推广应用。
