姜黄素对冈田酸损伤的HT⁃22细胞的保护作用
2021-02-26许传先凌卫明张岳春欧萌萌方斌斌
许传先,凌卫明,张岳春,欧萌萌,方斌斌*
1无锡市儿童医院检验科,江苏 无锡 214023;2南京医科大学附属无锡精神卫生中心检验科,江苏 无锡 214151
阿尔茨海默病(Alzheimer’s disease,AD)是一种神经系统退行性疾病,起病隐匿并呈进行性发展。AD 病变主要发生在大脑皮层及脑区,AD 的病理特征包括认知功能障碍[1]、脑皮质神经元减少退化[2]、神经细胞内神经原纤维缠结、细胞外老年斑及脑实质血管淀粉样变性等。Tau蛋白是一种微管相关蛋白,在脑细胞中的功能是与其他微管蛋白结合形成微管,并保持其稳定性。相关研究证实了AD 患者脑中磷酸化Tau(p⁃Tau)蛋白数量异常增加[3],同时动物实验表明,AD 模拟动物的相关脑细胞内p⁃Tau水平出现同样变化,因此Tau 蛋白的过磷酸化成为AD病变评估的关键标志物,对抗Tau蛋白过磷酸化也成为AD治疗的一个重要切入点[4]。
姜黄色素(curcuminoids)是我国传统中药姜黄的主要活性成分,姜黄素(curcumin,Cur)是其中一种单体,通过抑制β淀粉样蛋白(amyloid β⁃protein,Aβ)的产生和聚集,对神经系统显示出保护作用[5]。大脑中细胞外大量淀粉样蛋白的沉积是AD的主要病理变化之一,动物试验表明姜黄素可以使AD 鼠大脑中相关神经细胞外的Aβ淀粉样蛋白减少,并能预防这种蛋白的生成[6]。但姜黄素对AD 相关细胞内另一主要病理变化,即p⁃Tau的影响有待深入研究。
AD 的发病机制尚未明确。目前研究表明,神经元细胞在Tau蛋白磷酸化后可产生多种神经毒性损害,如缺血缺氧[7-8]、氧化应激[9]、炎症[10]和老化[11]等。本研究用冈田酸(okadaic acid,OA)诱导HT⁃22小鼠海马神经元细胞,并以一定浓度的姜黄素处理,探讨姜黄素对OA诱导的HT⁃22细胞的作用及其对凋亡及氧化应激的影响,对AD 的治疗有重要临床指导意义。
1 材料和方法
1.1 材料
小鼠海马神经元来源的HT⁃22 细胞系,购自赛百慷(上海)生物技术股份有限公司,姜黄素、冈田酸(Sigma公司,美国),MEM培养液(Invitrogen公司,美国),胎牛血清、N2培养基添加剂、Neurobasal培养基(Gibco 公司,美国),活性氧检测试剂盒、MTT 细胞增殖及细胞毒性检测试剂盒、Annexin V⁃FITC/PI细胞凋亡检测试剂盒、DCFH⁃DA荧光探针检测试剂盒(上海碧云天生物技术有限公司),ChemiDocTMXRS凝胶成像系统(Bio⁃Rad 公司,美国),BD FACS⁃Verse 流式细胞仪(BD 公司,美国),Leica DM14000荧光显微镜(莱卡公司,德国)。
1.2 方法
1.2.1 细胞培养
小鼠海马神经元来源的HT⁃22 细胞,用含10%胎牛血清的MEM 高糖培养液(100 U/mL 青霉素和100 mg/L 链霉素),在37 ℃、5%CO2、100%饱和湿度条件下培养,细胞贴壁生长后加入分化液(Neuro⁃basal 培养基和N2 添加剂)培养24 h。当细胞呈对数生长时,进行分组实验。
1.2.2 实验分组
HT⁃22 细胞以不同浓度的OA(20、40、60、80、100 nmol/L)处理,不加OA的细胞作为对照,分别进行MTT 实验和Annexin V⁃FITC/PI 双染色检测细胞活性及凋亡情况。后续实验以OA 作用HT⁃22 细胞的半数抑制浓度(IC50)作为实验浓度,分为对照组:HT⁃22 细胞未经任何处理因素;Cur 组:姜黄素(20 μg/mL)作用HT⁃22 细胞24 h;OA 组:80 nmol/L OA作用HT⁃22细胞24 h;OA+Cur 组:OA(80 nmol/L)加入HT⁃22细胞12 h后加姜黄素(20 μg/mL)处理细胞12 h进行后续检测。
1.2.3 MTT检测细胞活力
HT⁃22细胞生长至对数生长期时,0.25%胰酶消化贴壁细胞,完全培养基终止消化,并调整至100 μL 5 000个细胞后接种于96孔培养板,每组5个复孔,待细胞贴壁后进行分组实验,设立调零孔,分别培养12、24、48 h后,向各孔内加10 μL MTT溶液,置于培养箱继续培养1 h后中反应,在酶标仪上于波长450 nm处测各孔吸光值。细胞活力(%)=(实验组吸光值-调零孔吸光值)/(对照组吸光值-调零孔吸光值)×100%。
1.2.4 Annexin V⁃FITC/PI 双染色检测细胞凋亡
按照Annexin V⁃FITC/PI 双染色凋亡检测试剂盒说明书进行操作。取胰酶处理后的对数生长期细胞,调整细胞浓度接种于6孔培养板(2×105个/孔),待细胞贴壁后,进行分组实验,分别培养24 h,PBS 轻轻洗涤2 次,各组依次加入195 μL Annexin V⁃FITC结合液、5 μL AnnexinV⁃FITC 混匀,5 μL PI 混匀,暗盒中放置10 min后,置于荧光显微镜下观察并拍照记录,并以流式细胞仪(绿色荧光FITC和红色荧光PI分别采用FL1和FL3通道)检测凋亡细胞数。
1.2.5 DCFH⁃DA 荧光探针荧光显微镜测定细胞活性氧(reactive oxygen species,ROS)水平
取胰酶处理后的对数生长期细胞,调整细胞浓度接种于6孔培养板(2×105个/孔),分组处理后,收集各组细胞,将DCFH⁃DA稀释为终浓度10 μmol/L。去除细胞培养液,加入1 mL稀释好的DCFH⁃DA。荧光显微镜和流式细胞仪检测各组细胞ROS生成水平。
1.2.6 免疫印迹法检测蛋白表达
HT⁃22 细胞分组处理后,收集各组细胞,采用BCA 法进行蛋白质含量测定。等量蛋白经SDS⁃PAGE电泳分离后,转移到PVDF 膜上。用封闭液封闭60 min,分别加入Bcl⁃2、Cleaved⁃caspase⁃3、t⁃Tau、p⁃Tau和β⁃actin抗体,4 ℃作用过夜,然后用TBST 清洗10 min 3次,加入二抗室温孵育90 min,再用TBST清洗10 min 3次。ECL发光液将PVDF膜显色,凝胶成像系统扫描分析结果,Image J软件分析条带灰度值。
1.3 统计学方法
采用GraphPad Prism7.0 进行统计学分析,实验结果以均数±标准差()表示,多组实验数据比较采用方差分析,任意两组间比较用LSD⁃t检验。P<0.05表示差异有统计学意义。
2 结果
2.1 OA对HT⁃22细胞的作用
2.1.1 OA对HT⁃22细胞活力的影响
MTT 结果显示,与对照组相比,不同浓度的OA(20、40、60、80、100 nmol/L)分别作用HT⁃22 细胞12、24、48 h 后,细胞活力随OA 浓度和作用时间的增加而逐渐降低。OA 对HT⁃22 细胞活力的抑制作用具有浓度和时间依赖性,差异有统计学意义(图1)。说明OA 对HT⁃22 细胞活力有抑制作用,OA 作用HT⁃22细胞的IC50接近80 nmol/L。

图1 冈田酸对HT⁃22细胞活力的影响(n=3)Figure 1 Effect of OA on viability of HT⁃22 cells(n=3)
2.1.2 OA对HT⁃22细胞凋亡的影响
流式细胞仪检测细胞凋亡实验结果显示,与对照组相比,不同浓度的OA分别作用HT⁃22细胞24 h后,OA 组细胞凋亡率明显升高,呈浓度依赖性,差异有统计学意义(图2)。说明OA 促进HT⁃22 细胞的凋亡,其IC50接近80 nmol/L。
2.1.3 OA对HT⁃22细胞ROS生成水平的影响
流式细胞仪检测结果显示,与对照组相比,不同浓度的OA(40、60、80 nmol/L)分别作用HT⁃22 细胞24 h后,OA组细胞内ROS生成水平随OA浓度的增高而增高(图3)。说明OA 的损伤造成HT⁃22 细胞内ROS水平增高。
2.1.4 OA作用HT⁃22细胞后Bcl⁃2、Cleaved⁃caspase⁃3、t⁃Tau、p⁃Tau蛋白表达量的变化

图2 OA对HT⁃22细胞凋亡的影响Figure 2 Effect of OA on HT⁃22 cells apoptosis

图3 OA对HT⁃22细胞内活性氧水平的影响Figure 3 Effect of OA on the level of reactive oxygen species in HT⁃22 cells
Western blot 蛋白实验结果显示,不同浓度的OA(20、40、80 nmol/L)作用HT⁃22细胞48 h后,与对照组相比,凋亡蛋白Cleaved⁃caspase⁃3 表达量明显上升,抗凋亡蛋白Bcl⁃2表达量降低,差异有统计学意义(图4)。这一改变与流式细胞仪检测细胞凋亡实验结果相符。
用不同浓度OA 作用HT⁃22 细胞后,经Western blot检测,被诱导后的HT⁃22细胞出现类似于AD的t⁃Tau、p⁃Tau蛋白表达量明显升高(图4),说明OA处理HT⁃22细胞后模拟了AD的病理特征。根据MTT实验及流式细胞仪检测,OA作用HT⁃22细胞的IC50接近80 nmol/L,后续实验将使用80 nmol/L的OA对HT⁃22细胞进行诱导。
2.2 姜黄素对OA损伤的HT⁃22细胞的影响
2.2.1 姜黄素对OA损伤的HT⁃22细胞活力的影响
MTT结果显示,与对照组相比,Cur组对细胞活力无明显影响,差异无统计学意义。与对照组相比,OA组和OA+Cur组细胞活力明显降低,且OA组细胞活力低于OA+Cur 组细胞,差异有统计学意义(图5)。说明姜黄素可以减轻OA损伤所造成的HT⁃22细胞活力降低。
2.2.2 姜黄素对OA损伤HT⁃22细胞凋亡的影响

图4 OA对HT⁃22细胞Bcl⁃2、cleaved⁃caspase⁃3、t⁃Tau、p⁃Tau蛋白表达量的影响Figure 4 Effect of OA on the expression levels of Bcl⁃2,cleaved⁃caspase⁃3,t⁃Tau,p⁃Tau protein in HT⁃22 cells

图5 姜黄素对OA损伤的HT⁃22细胞活力的影响Figure 5 Effect of curcumin on the cell viability in HT⁃22 cells damaged by OA
Annexin V⁃FITC/PI双染色荧光显微镜观察结果显示,与对照组相比,Cur组细胞无明显变化,OA组和OA+Cur 组细胞早期凋亡细胞明显增多(图6A)。流式细胞仪检测细胞凋亡结果显示,与对照组相比,Cur组细胞凋亡率无明显变化,差异无统计学意义。与对照组相比,OA组和OA+Cur组细胞凋亡率增高,且OA 组细胞凋亡率高于OA+Cur 组细胞,差异有统计学意义(图6B、C)。说明姜黄素可抑制OA损伤造成的HT⁃22细胞凋亡。
2.2.3 姜黄素对OA 损伤的HT⁃22细胞ROS 水平的影响

图6 姜黄素对OA损伤HT⁃22细胞凋亡的影响Figure 6 Effect of curcumin on the cell apoptosis in HT⁃22 cells damaged by OA
DCFH⁃DA荧光探针荧光显微镜观察显示,与对照组相比,Cur 组细胞无明显变化,OA 组细胞内DCFH 的荧光强度增高,OA+Cur组细胞内荧光强度高于Cur组低于OA组(图7A)。流式细胞仪检测结果显示,与对照组相比,Cur组细胞无明显变化,OA组、OA+Cur组细胞ROS含量增多,且OA组细胞ROS含量高于OA+Cur组(图7B、C)。说明姜黄素可以抑制OA损伤造成的HT⁃22细胞内的ROS水平增高。
2.2.4 姜黄素对OA 损伤HT⁃22 细胞内多种蛋白表达水平的影响
Western blot 蛋白实验结果显示,与对照组相比,Cur 组细胞t⁃Tau、p⁃Tau 蛋白、凋亡蛋白Cleaved⁃caspase⁃3、抗凋亡蛋白Bcl⁃2表达量的差异无统计学意义。与对照组相比,OA 组与OA+Cur 组细胞t⁃Tau,p⁃Tau蛋白、凋亡蛋白Cleaved⁃caspase⁃3表达量明显上升,抗凋亡蛋白Bcl⁃2表达量显著降低,且OA组t⁃Tau、p⁃Tau、Cleaved⁃caspase⁃3 蛋白表达量明显高于OA+Cur 组,Bcl⁃2表达量明显低于OA+Cur 组,差异具有统计学意义。说明姜黄素可以降低OA损伤的HT⁃22 细胞的AD 相关蛋白表达量,Bcl⁃2 表达量升高与凋亡检测结果相符,说明姜黄素对OA 损伤的HT⁃22细胞有保护作用(图8A、B)。
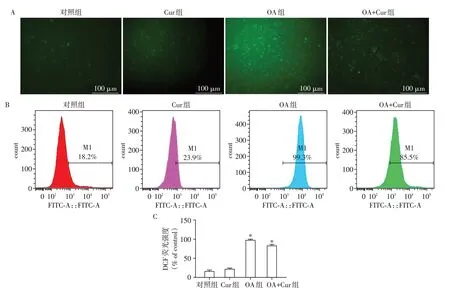
图7 姜黄素对OA损伤的HT⁃22细胞内ROS水平的影响Figure 7 Effect of curcumin on the level of reactive oxygen species in HT⁃22 cells damaged by OA
3 讨论
AD病因尚未完全阐明,由于AD临床病理进程缓慢,其病理变化多由尸检脑部异常的组织结构获取,未能明确病程早期的损伤机制[12]。在神经病理学方面,AD患者相关脑区细胞内Tau蛋白过度磷酸化和神经原纤维缠结以及细胞外丰富的淀粉样蛋白沉积被认为是神经元细胞损伤的主要原因[13-14]。

图8 姜黄素对OA损伤的HT⁃22细胞Bcl⁃2、cleaved⁃caspase⁃3、t⁃Tau、p⁃Tau蛋白表达量的影响Figure 8 Effect of curcumin on the expression levels of Bcl⁃2,cleaved⁃caspase⁃3,t⁃Tau,p⁃Tau protein in HT⁃22 cells in⁃jured by OA
Tau蛋白是神经细胞内含量最高的微管结合蛋白,通过微管组装维持微管的稳定性,Tau蛋白过度磷酸化后,微管稳定性下降而出现神经原纤维缠结。AD 患者因Tau 蛋白过磷酸化而出现相关症状。OA 是蛋白磷酸酶2A 的抑制剂,可诱导细胞和动物体内Tau 过度磷酸化及神经元死亡,从而提供研究AD的理想模型[15-16]。本研究用不同浓度的OA处理HT⁃22细胞,结果细胞凋亡率增加,细胞内ROS量增加,细胞内p⁃Tau蛋白表达量异常增多。p⁃Tau蛋白表达量增多是AD典型的分子生物学表现,我们认为,HT⁃22细胞经OA处理后p⁃Tau表达量的显著增加可以作为一种模型研究AD病理特征的改变。
Aβ是一种淀粉样蛋白沉积,是AD 患者脑内细胞外老年斑的主要组成部分[17],病理证实,AD 患者Aβ主要沉积于脑部相关细胞的外部,同时动物实验后的病理检查也证实AD 模拟动物的Aβ也同样沉积于相关细胞外[18]。Aβ沉积与相关细胞的凋亡进程及细胞凋亡后的变化有关[19]。
有研究显示,OA 作用于PC12 等细胞进行AD造模后细胞内Aβ表达量上升[20],也有文献表明,AD模型细胞内虽然有Aβ的增加,但其表达量因条件不同而具有摆动性[19-21]。由于本研究用OA 处理HT⁃22细胞后,有更加直观的细胞内p⁃Tau、t⁃Tau表达量变化作为造模指标测定,而Aβ沉积部位主要位于细胞外并且其生成过程有阶段性,对后续实验可能会造成干扰,所以本研究未将细胞内Aβ表达量增加作为AD造模成功的另一个观测指标,未检测OA应用前后细胞内Aβ表达量的变化。
不同浓度的OA(20、40、60、80、100 nmol/L)分别作用小鼠海马神经元HT⁃22 细胞24 h 后,细胞活力受到抑制,呈浓度依赖性下降,其中80 nmol/L OA 处理组,细胞活力下降接近IC50,我们选择80 nmol/L OA 作为后续实验的损伤浓度。ROS主要由线粒体在能量代谢过程中产生,线粒体损伤等多种途径可引起细胞内ROS 蓄积。氧化应激反应可使ROS 量增多,如果组织细胞内ROS量升高超过机体清除能力,ROS 的产生和清除将处于失衡状态,可导致细胞死亡。流式细胞仪检测结果显示OA 诱导后,细胞内ROS 异常增高,细胞发生早期凋亡,并且早期凋亡率随OA浓度的增加呈明显上升的趋势。免疫印迹实验证明了此结论,OA 诱导HT⁃22 细胞后,抗凋亡蛋白Bcl⁃2 表达量下降,凋亡蛋白Cleaved⁃cas⁃pase⁃3表达量明显增高。
慢性炎症反应是AD 的重要发病机制之一,姜黄素可抑制主要炎症介质,包括环氧合酶⁃1、环氧合酶⁃2、干扰素⁃C 以及抑制调节转录因子(AP⁃1、NF⁃κB)的活性,激活NF⁃κB 信号转导通路后可以促进下游基因的表达,发挥抗炎效应[22-24]。本研究中,与OA组相比,姜黄素作用OA损伤的HT⁃22细胞后,促进细胞活性,降低其凋亡率,减弱OA损伤导致的氧化应激反应,减弱细胞内活性氧生成,同时Bcl⁃2表达量增高、Cleaved⁃caspase⁃3蛋白表达量降低,表明姜黄素对OA损伤的HT⁃22细胞起到一定的保护作用。
目前,Tau蛋白过磷酸化被公认为对AD的发生有重要意义,过度磷酸化的Tau 蛋白可降低微管稳定性,损害神经元功能[25-26]。在AD模型小鼠中,Tau蛋白水平明显高于正常对照小鼠,并且过度磷酸化Tau蛋白在其发病机制中起主要作用[27]。研究表明,OA 诱导HT⁃22 细胞后,t⁃Tau、p⁃Tau 蛋白表达量增高,而姜黄素作用OA损伤的细胞后,t⁃Tau、p⁃Tau蛋白表达量降低,说明姜黄素的应用可抑制OA 诱导的HT⁃22细胞内总Tau蛋白的表达及其过磷酸化,姜黄素对OA损伤的HT⁃22细胞有保护作用。
总之,本研究结果表明,OA 诱导HT⁃22 细胞后细胞内ROS 含量增高,细胞早期凋亡细胞增加,凋亡相关蛋白表达量变化明显,细胞内t⁃Tau、p⁃Tau蛋白量增高,而应用姜黄素后可以有效改善OA 损伤后HT⁃22细胞的状态,促进细胞增殖,降低损伤蛋白的表达量,对细胞起到明显的保护作用。姜黄素作为一种抗氧化剂,所具有的抗AD作用,可作为AD治疗的新思路,提示有必要对抗氧化剂在AD发生发展中的作用进行更深入的研究。
