植酸-金属离子螯合物改性层状黏土及其在聚己内酯中的增强与抗菌效应研究
2021-02-25刘小超吴慧青刘跃军
毛 龙,刘小超,谢 斌,吴慧青,刘跃军
(1 厦门理工学院 福建省功能材料及应用重点实验室,福建 厦门 361024;2 湖南工业大学 先进包装材料与技术湖南省重点实验室,湖南 株洲 412007)

近年来利用聚多巴胺(PDA)、单宁酸(TA)等对LDHs进行表面包覆改性已经有不少研究,并且取得了较好的效果。如Phua等[13]采用DA在LDHs表面自聚得到PDA改性LDHs,并将其应用到聚氨酯中来增强复合材料的力学性能和形状记忆性能。又如Mao等[14]利用TA的多个邻位酚羟基结构与金属离子Fe(Ⅲ)发生络合反应,从而在LDHs表面通过螯合和沉积作用形成稳定的核壳结构(LDHs@TA-Fe(Ⅲ)),最终提高了纳米复合材料的力学和气体阻隔等性能。研究发现,植酸(PA),又为肌醇正六磷酸酯,是自然界中普遍存在的天然物质,广泛存在于豆类、谷类、干果、蔬菜和水果等植物中[15]。相比于PDA和TA来说,PA具有来源广泛、价格低廉、螯合能力强、光稳定性好等优点。特别指出的是,植酸与乙二胺四乙酸一样具有较强的螯合能力,并且在很宽的pH值范围内都具有螯合能力[16]。在生产实践中,PA被用来作为金属材料表面涂层达到耐腐蚀的目的,将其应用于纳米材料的表面改性工作具有很好的研究意义,可丰富纳米材料的表面改性方法。因此,通过简单的一步法利用金属离子与PA在水溶液中发生沉积和螯合作用形成稳定的配位化合物,实现对LDHs有效的表面包覆改性,形成核壳结构,为LDHs的表面改性方法提供更多的选择性,具有简单、有效和环保等优点,符合材料表面改性方法的发展趋势。这种利用PA与金属离子螯合对LDHs表面包覆改性的方法在文献中鲜有报道[17],是本研究的创新点。
本研究利用Ag+,Cu2+,Fe3+和Zn2+与PA发生螯合作用并沉积吸附在LDHs表面,制备出不同金属离子负载的表面包覆改性LDHs(LDHs@PA-M),研究LDHs@PA-M在不同金属离子负载下的微观形貌和抗菌特性。同时,这些表面包覆改性层状纳米黏土用来改性绿色可降解的脂肪族聚酯——聚己内酯(PCL),提高PCL基材的阻隔性能和力学性能,赋予抗菌等功能性,提高其在绿色活性包装领域的应用潜力。
1 实验材料与方法
1.1 主要实验原料
植酸水溶液,植酸(C6H18O24P6)质量分数为70%,上海阿拉丁生化科技股份有限公司;AgNO3,CuCl2·2H2O,ZnCl2,FeCl3·6H2O,分析纯,上海阿拉丁生化科技股份有限公司;N,N-二甲基甲酰胺(C3H7NO),分析纯,西陇科学股份有限公司;MgAl-CO3LDHs,参考文献[14]方法制备;PCL,6800型,熔融指数为7.3 g/10 min,重均分子量为80000,瑞典Perstorp公司。
1.2 LDHs@PA-M的制备
为了验证何种金属离子与PA通过螯合沉积作用能形成稳定和均匀的核壳结构,利用Ag+,Cu2+,Fe3+和Zn2+与PA发生螯合作用沉积吸附在LDHs表面,原理如图1所示。将0.05 g的MgAl-CO3LDHs加入到100 mL去离子水中,超声分散30 min,然后加入0.05 g的70% PA水溶液,室温下磁力搅拌吸附15 min,得到溶有PA的MgAl-CO3LDHs分散液。
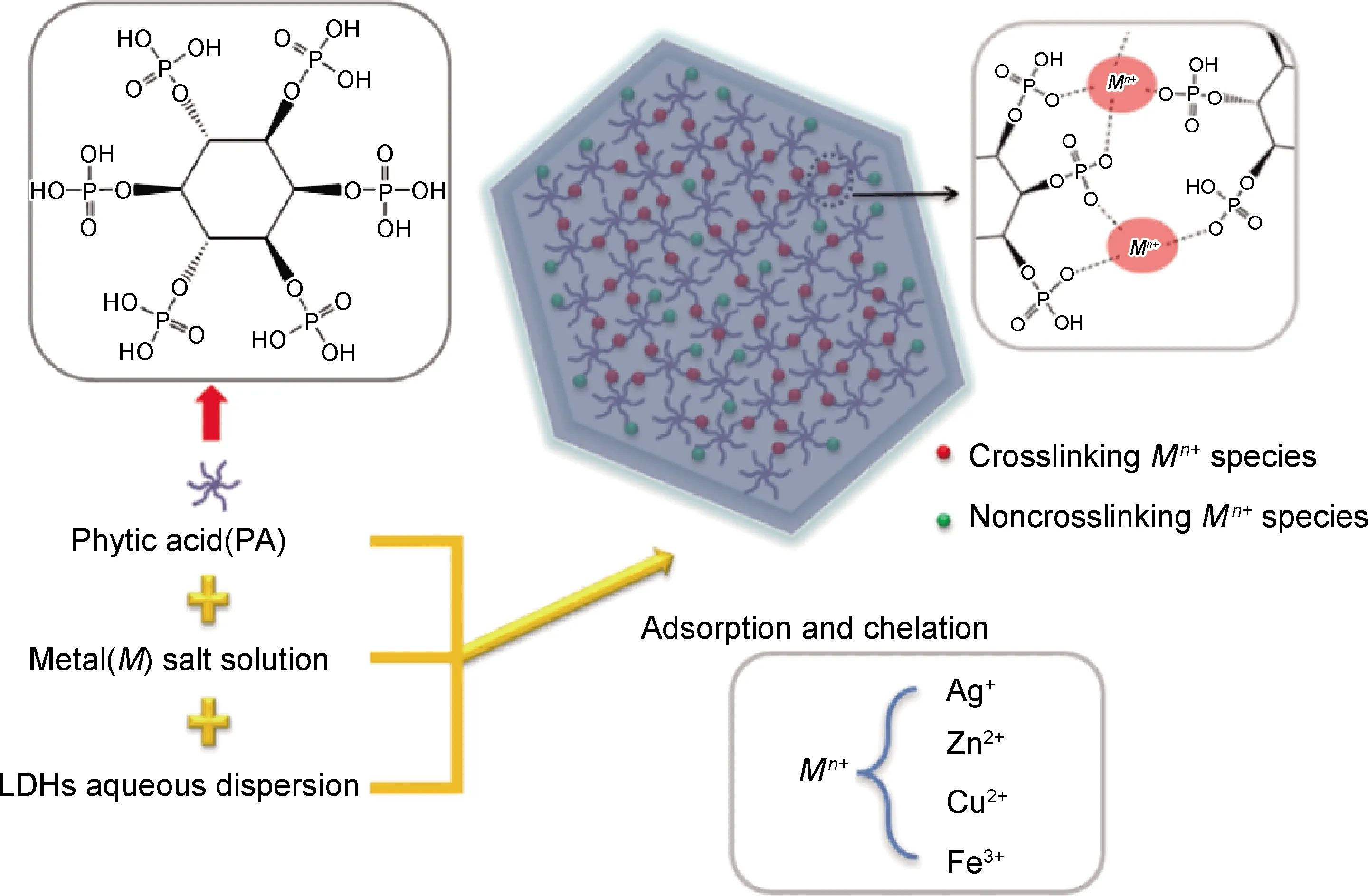
图1 一步法制备LDHs@PA-M
1.2.1 LDHs@PA-Ag+的制备
称取0.0090 g的AgNO3(0.053 mmol)加入到上述分散液中,70 ℃下反应2 h,反应过程中溶液颜色越来越深,反应结束后将反应液离心,洗涤3次后,冷冻干燥得到灰白色的LDHs@PA-Ag+。
1.2.2 LDHs@PA-Cu2+的制备
称取0.0090 g的CuCl2·2H2O(0.053 mmol)加入到上述分散液中,常温下反应2 h,反应结束后将反应液离心,洗涤3次后,冷冻干燥得到淡蓝色的LDHs@PA-Cu2+。
1.2.3 LDHs@PA-Zn2+的制备
称取0.0074 g的ZnCl2(0.053 mmol)加入到上述分散液中,常温下反应2 h,反应结束后将反应液离心,洗涤3次后,冷冻干燥得到LDHs@PA-Zn2+。
1.2.4 LDHs@PA-Fe3+的制备
称取0.0143 g的FeCl3·6H2O(0.053 mmol)加入上述到分散液中,常温下反应2 h,反应结束后将反应液离心,洗涤3次后,冷冻干燥得到LDHs@PA-Fe3+。
1.3 LDHs@PA-M/PCL纳米复合材料的制备
称取0.014 g的LDHs@PA-M加入到14 mL的N,N-二甲基甲酰胺中,超声分散15 min,再加入1.4 g PCL,于40 ℃下磁力搅拌45 min后,升温至80 ℃继续搅拌30 min,随后超声15~20 min去除反应液中的气泡,最后将反应液倒入水平放置的聚四氟乙烯模具中,置于60 ℃烘箱中烘干12 h,至溶剂挥发完全,即得到LDHs@PA-M/PCL复合薄膜。复合薄膜(分别命名为LDHs@PA-Ag+/PCL,LDHs@PA-Cu2+/PCL)中LDHs@PA-M的质量分数均为1%,并将MgAl-CO3LDHs以相同的质量分数与PCL复合作为对比样(命名为LDHs/PCL)。
1.4 表征与测试
采用傅里叶变换红外光谱(FTIR)仪对样品进行化学结构的表征,KBr压片,扫描区间为400~4000 cm-1;采用扫描电子显微镜(SEM)对样品的表面微观形貌进行了表征,样品表面喷金;采用场发射透射电子显微镜(TEM)对样品的微观形貌进行了表征;采用能量色散X射线光谱仪(EDS)对样品表面元素分布和含量进行了表征;采用万能力学试验机对样品的力学性能进行了表征,测试样条用裁刀裁切成型,样品为哑铃型,总长度为35 mm,标距长度为10 mm,宽度2 mm,厚度由厚度计测量得到,拉伸速率为20 mm/min。
1.5 抗菌性能测试
采用平板菌落计数法测试抗菌性能,抗菌对象为革兰氏阴性菌大肠杆菌(E.coli)。用接种环将保存的菌种接种到LB固体培养基中,于37 ℃培养箱中培养24 h;取生长好的菌落接种于LB液体培养基中,在恒温培养摇床中37 ℃恒温振荡培养24 h,再将LB液体培养基稀释,通过分光光度计调节吸光度至约0.1,即相应细菌浓度为1×108CFU/mL。在LB液体培养基中培养细菌12 h,稀释细菌悬浮液直到600 nm吸光度值为≈0.1。将150 μL菌液滴至装有15 mL液体培养基的锥形瓶中,此时菌液浓度为1×105CFU/mL。分别将粉末样品(取50 mg)和复合薄膜样品(直径为10 mm的圆片)浸泡到含有菌液的锥形瓶中,使样品充分浸润在菌液中,再将锥形瓶放置于恒温培养摇床中,37 ℃恒温振荡培养,24 h后取适量的稀释菌液,涂布在培养皿上,置于恒温培养摇床中继续培养24 h,用菌落计数器统计培养皿上的菌落数,测试得到的数值单位是CFU/cm2,指每平方厘米样品中含有的细菌群落总数。通过抗菌率来评估样品的抗菌活性,抗菌率=[(对照的菌落数-样品的菌落数)/对照的菌落数]×100%[18]。
2 结果与分析
2.1 LDHs@PA-M的化学结构分析


图2 MgAl-CO3 LDHs和LDHs@PA-M的傅里叶红外光谱图
2.2 LDHs@PA-M的微观形貌分析
图3为不同视野下MgAl-CO3LDHs的SEM图。从图3中可以看到,合成的MgAl-CO3LDHs呈现出六边形的层状结构,这是一种典型的水滑石形貌,其直径约为1500 nm,厚度约为40 nm,长径比约为37.5。图4为不同视野下LDHs@PA-M的SEM图。从图4中可以看到,4种LDHs@PA-M均呈现和MgAl-CO3LDHs相似的六边形层状结构,然而LDHs@PA-Zn2+和LDHs@PA-Fe3+表面粗糙,这表明LDHs@PA-Zn2+和LDHs@PA-Fe3+没有实现有效均匀的包覆。因此在复合材料的制备中采用LDHs@PA-Ag+和LDHs@PA-Cu2+,后面复合材料的讨论只涉及LDHs@PA-Ag+和LDHs@PA-Cu2+制备的复合材料。尽管LDHs@PA-Ag+和LDHs@PA-Cu2+表面光滑平整,但是仅通过SEM无法判断LDHs@PA-M的包覆厚度,需要进一步验证LDHs@PA-Ag+和LDHs@PA-Cu2+的表面包覆效果,故采用TEM来进行表征。

图3 MgAl-CO3 LDHs的SEM图

图4 不同视野下LDHs@PA-M的SEM图
将PA-Ag+沉积吸附在MgAl-CO3LDHs上,形成的LDHs@PA-Ag+的TEM照片如图5所示。从标尺为500 nm,100 nm的图中可以明显看到,在MgAl-CO3LDHs表面出现一层约20 nm的包覆物。TEM表明PA-Ag+已经成功对MgAl-CO3LDHs表面包覆改性。从标尺为10 nm的图中可以看到,在LDHs@PA-Ag+上还存在一定数量纳米尺寸的Ag+聚集体,尺寸大约在35 nm。LDHs@PA-Ag+的EDS元素分析结果如图6所示。从EDS元素分布图中可以看到六边形MgAl-CO3LDHs中的金属元素(Mg和Al)、PA中的P元素、Ag元素,这进一步表明PA-Ag+配位化合物的存在。同时,EDS能谱分析表明LDHs@PA-Ag+中Ag元素的质量分数达到了3.02%。

图5 LDHs@PA-Ag+的TEM照片
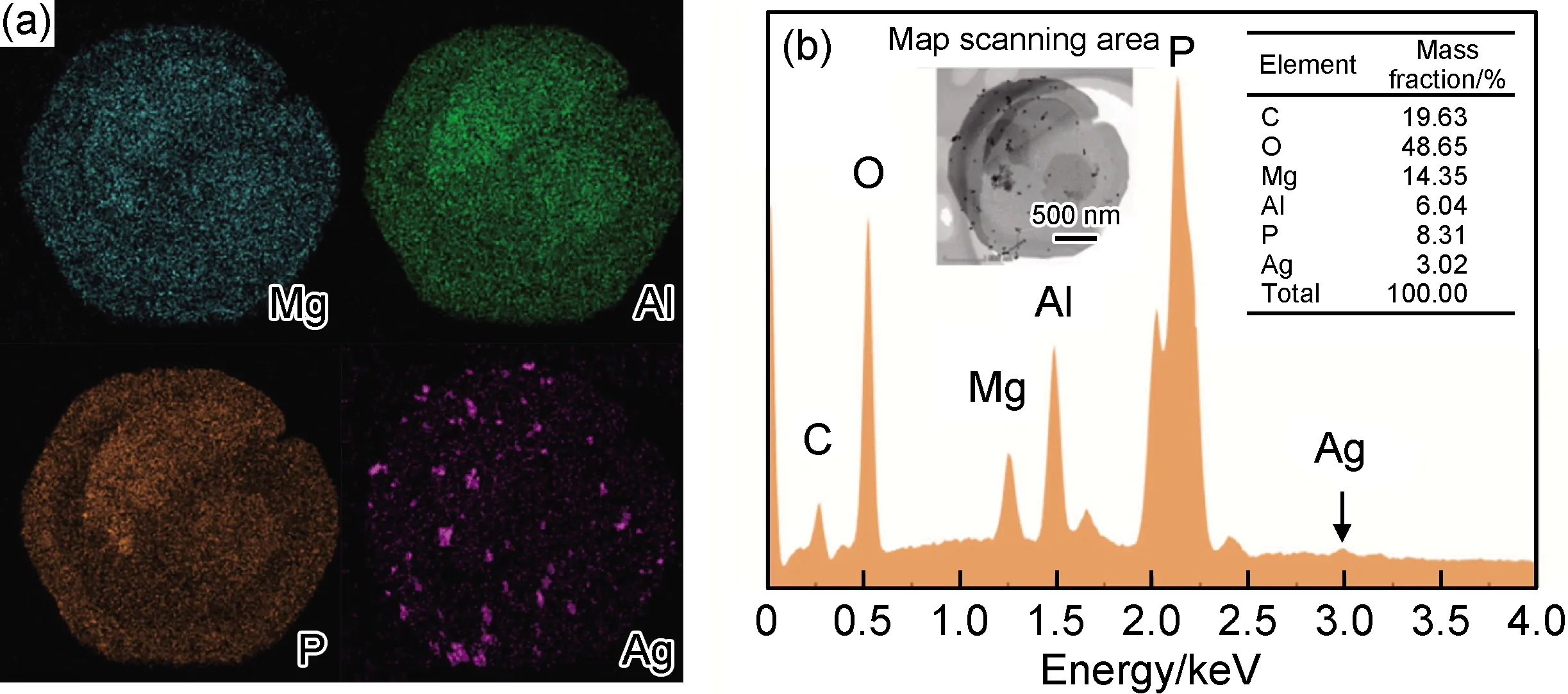
图6 LDHs@PA-Ag+ EDS面扫描元素分析结果
将PA-Cu2+沉积吸附在MgAl-CO3LDHs上,形成的LDHs@PA-Cu2+的TEM照片如图7所示。从图7中可以看到,在MgAl-CO3LDHs表面存在厚度约为12 nm的包覆物,但衬度区别并不是很明显,需要采用线扫描进一步确认。LDHs@PA-Cu2+的EDS元素分析结果如图8所示。从面扫描的元素分布图(图8(a),(b))中可以看到,P元素和Cu元素均匀分布在MgAl-CO3LDHs表面,这表明PA-Cu2+在MgAl-CO3LDHs表面上均匀分布。EDS能谱分析表明LDHs@PA-Cu2+中Cu元素的质量分数为1.52%。EDS线扫描结果(图8(c))表明Mg元素含量在MgAl-CO3LDHs的边缘处开始显著降低,而Cu元素含量没有显著变化,这更加确认了PA-Cu2+包覆物的存在。

图7 LDHs@PA-Cu2+的TEM照片
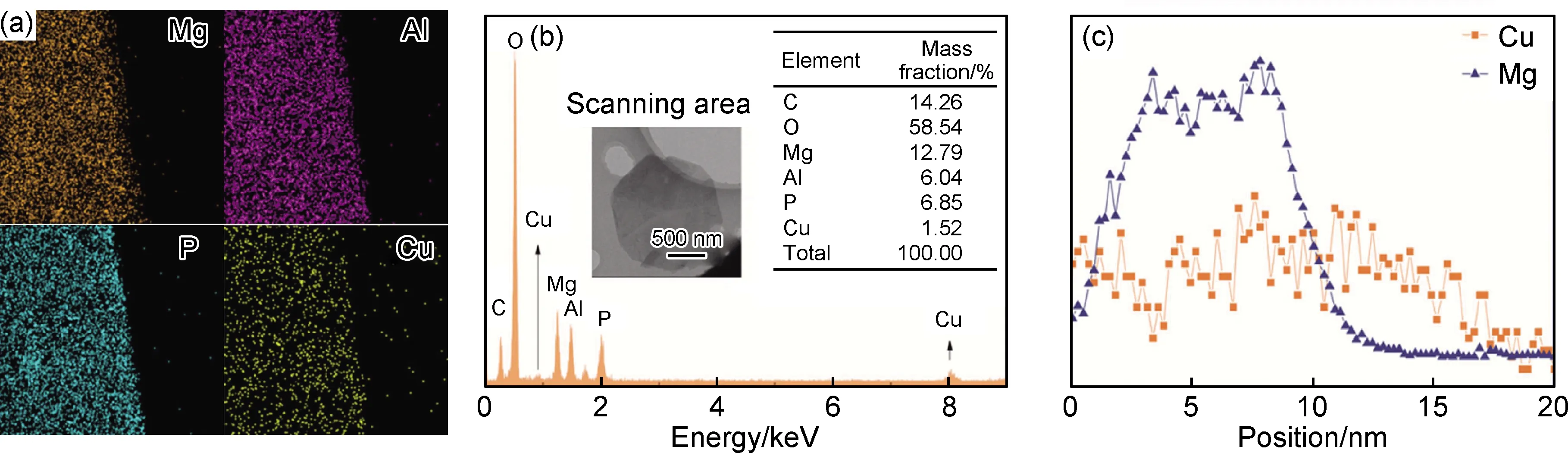
图8 LDHs@PA-Cu2+ EDS元素分析结果
2.3 LDHs@PA-M和LDHs@PA-M/PCL纳米复合材料的抗菌活性
为了定量评价LDHs@PA-M和LDHs@PA-M/PCL纳米复合材料的抗菌性能,采用菌落计数器统计浸有不同样品的培养皿中的菌落数,利用抗菌率来评价样品的抗菌活性,如图9所示。图9(a)为LDHs@PA-Cu2+和LDHs@PA-Ag+的抗菌测试结果。从图9(a)中可以看到,MgAl-CO3LDHs对革兰氏阴性菌-大肠杆菌(E.coil)表现出一定的抗菌活性,E.coli浓度仅从2.6×1013CFU/cm2降低到1.7×1013CFU/cm2,抗菌率为34.62%;LDHs@PA-Cu2+具有更强的抗菌能力,培养皿中细菌数量进一步降低为5.8×107CFU/cm2,抗菌率超过99.99%;LDHs@PA-Ag+则表现出了极其优异的抗菌性能,从图中可以看出,培养基中并无菌落存在,抗菌率达到100%。这主要是由于负载在LDHs@PA-M上的Cu2+和Ag+与细菌的细胞膜接触并破坏其结构,从而使细胞失去了生存和增殖的能力[20-21]。
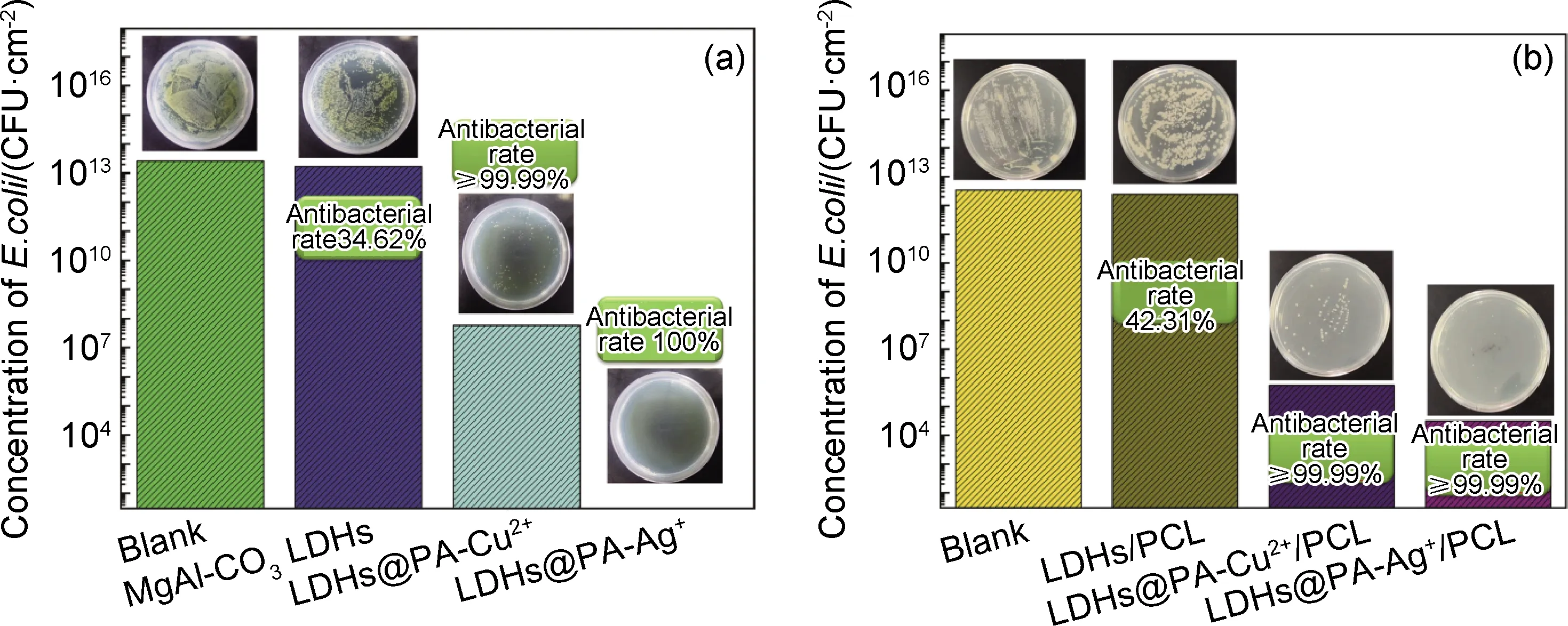
图9 LDHs@PA-M(a)和LDHs@PA-M/PCL纳米复合材料(b)的抗菌性能测试结果
图9(b)为LDHs@PA-Cu2+/PCL和LDHs@PA-Ag+/PCL纳米复合材料抗菌测试结果。从图9(b)中可以看到,LDHs@PA-M/PCL纳米复合材料的抗菌性与LDHs@PA-M的抗菌性呈现良好的相关性。LDHs/PCL的抗菌率仅为42.31%;LDHs@PA-Cu2+/PCL复合材料对应的E.coli浓度从空白对比样的3.4×1012CFU/cm2降低到5.5×105CFU/cm2,抗菌率超过99.99%;LDHs@PA-Ag+/PCL纳米复合材料对应的E.coli浓度更是降低至3.4×104CFU/cm2,抗菌率超过99.99%,表现出最为优异的抗菌活性。
2.4 LDHs@PA-M/PCL纳米复合材料的力学性能
图10为LDHs@PA-M/PCL纳米复合材料的力学性能。从图10中可以看到,纯PCL的拉伸强度和断裂伸长率分别为31.3 MPa和612%;在MgAl-CO3LDHs加入到纯PCL之后,LDHs/PCL纳米复合材料的拉伸强度得到一定程度的提高。在利用PA-Ag+包覆层对MgAl-CO3LDHs进行改性之后,LDHs@PA-Ag+/PCL纳米复合材料的拉伸强度和断裂伸长率达到了38.8 MPa和762%,力学增强效果显著。在利用PA-Cu2+包覆层对MgAl-CO3LDHs进行改性之后,LDHs@PA-Cu2+/PCL纳米复合材料的拉伸强度和断裂伸长率分别提高了30.7%和33.3%,达到了40.9 MPa和816%,力学性能增强效果最为显著。复合材料的强度与样品缺陷和裂缝大小及分布密切相关,这些缺陷和裂缝大小及分布的负载程度显著恶化材料抗断裂的能力[22]。力学分析结果表明,LDHs@PA-M对PCL基材力学性能改善效果更好,这是由于表面包覆改性能提高MgAl-CO3LDHs与基材PCL的界面相容性,减少界面缺陷[14]。此外,LDHs@PA-Cu2+/PCL纳米复合材料表现出更好的力学性能,结合前面的LDHs@PA-M微观形貌分析,原因可能是LDHs@PA-Cu2+的包覆表面更加均匀,而LDHs@PA-Ag+表面还是存在一定的不均匀性。因此,合适添加量的LDHs@PA-M能够在PCL基材中起到较好的增强与增韧作用。
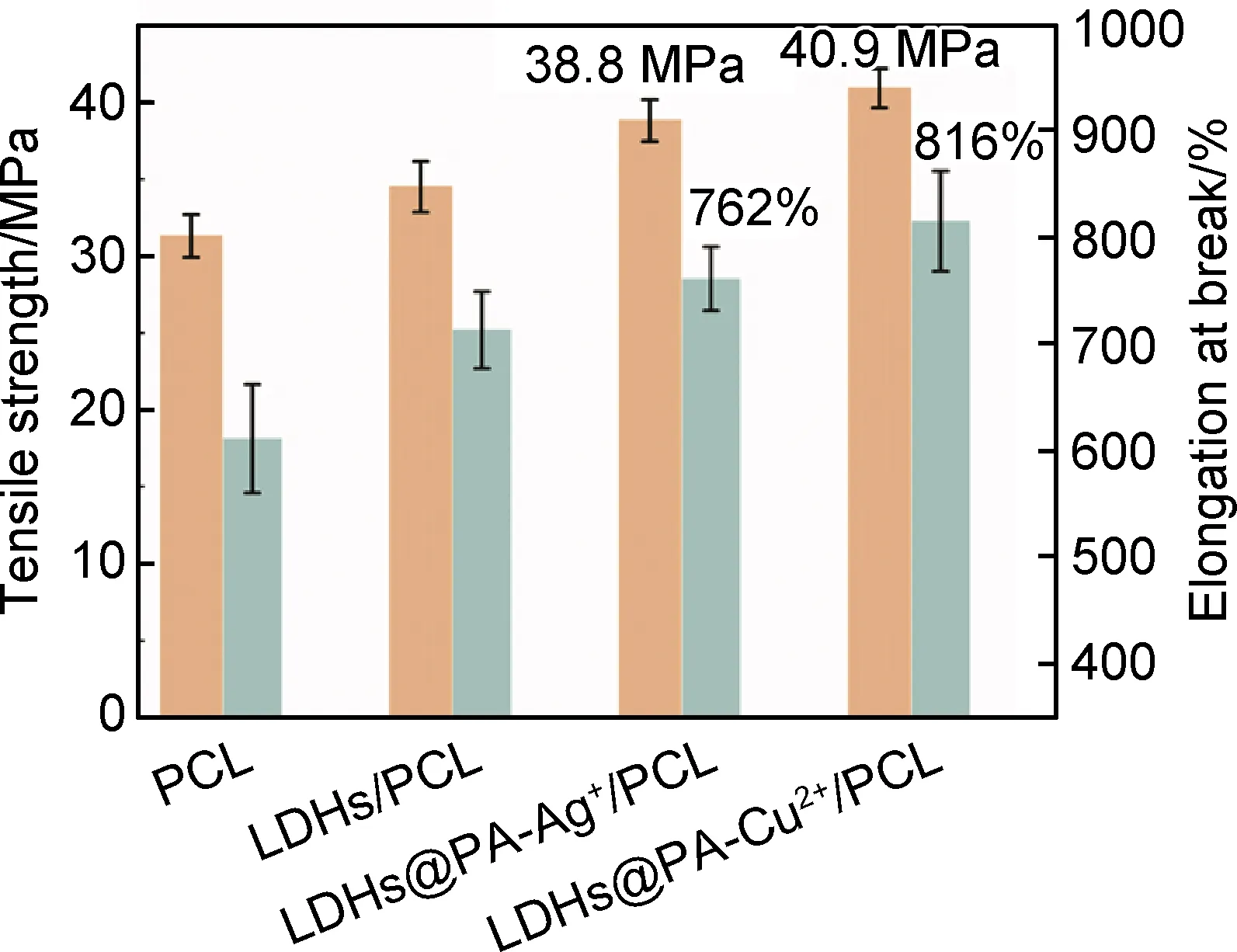
图10 LDHs@PA-M/PCL纳米复合材料的力学性能
为了解释力学性能变化的原因,对LDHs/PCL,LDHs@PA-Ag+/PCL和LDHs@PA-Cu2+/PCL纳米复合材料的断面进行微观形貌分析,如图11所示。在MgAl-CO3LDHs加入到PCL之后,MgAl-CO3LDHs与PCL基材之间出现较为明显的界面缺陷(箭头所指的区域,图11(a));而LDHs@PA-Ag+和LDHs@PA-Cu2+表现出更好的界面相容性,没有出现明显的界面缺陷,在塑性破坏的过程中能够更好地抵抗外力产生的形变。结合LDHs@PA-Ag+和LDHs@PA-Cu2+的微观形貌,LDHs@PA-Cu2+/PCL比LDHs@PA-Ag+/PCL表现出更好的力学性能原因可能是由于LDHs@PA-Ag+表面存在一定尺寸Ag+聚集体,对LDHs@PA-Ag+与PCL基材的界面结合力和相容性有一定的负面作用。
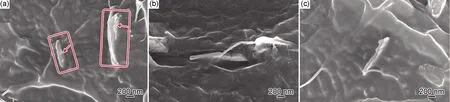
图11 LDHs/PCL(a),LDHs@PA-Ag+/PCL(b)和LDHs@PA-Cu2+/PCL(c)的断面扫描电镜图
3 结论
(1)Ag+和Cu2+与PA能够在MgAl-CO3LDHs表面形成稳定、均匀的纳米包覆层,而Fe3+和Zn2+未能与PA在LDHs表面形成稳定、均匀的包覆层。
(2)利用金属Ag+和Cu2+优异的抗菌活性,LDHs@PA-Cu2+对大肠杆菌(E.coli)的抗菌率超过99.99%,LDHs@PA-Ag+的抗菌率更是达到了100%,而MgAl-CO3LDHs的抗菌性仅为34.62%。
(3)相比于纯的PCL,制备的LDHs@PA-Cu2+/PCL纳米复合材料的拉伸强度和断裂伸长率分别提高了30.7%和33.3%,达到了40.9 MPa和816%,力学性能增强效果最为显著;LDHs@PA-Ag+/PCL纳米复合材料的拉伸强度和断裂伸长率也分别达到了38.8 MPa和762%,力学性能增强效果次之。
(4)LDHs@PA-Cu2+/PCL和LDHs@PA-Ag+/PCL纳米复合材料对E.coli的抗菌率均超过99.99%,表现出优异的抗菌活性,拓展了层状黏土/生物基高分子复合材料在活性包装领域的应用。
