贝伐珠单抗联合化疗对转移性直肠癌患者血清学肿瘤标志物水平及预后的影响
2021-02-24付岳亚
付岳亚
(河南省南阳市第二人民医院肿瘤二科 南阳 473003)
直肠癌早期缺乏特异性临床表现,确诊时约有20%的患者发生转移,即使实施根治性手术治疗,术后仍有40%左右的患者复发转移,5 年生存率较低[1~2]。对于转移性直肠癌患者的治疗临床首选化疗,FOLFIRI 方案较为常见,能促使肿瘤细胞凋亡,拮抗肿瘤细胞纺锤体形成,改善患者病情[3]。因肿瘤细胞存在耐药现象,单一使用FOLFIRI 方案治疗患者无瘤生存期较短,预后欠佳。贝伐珠单抗(BV)属于重组抗人血管内皮生长因子(VEGF)单克隆抗体,可结合VEGF,拮抗肿瘤新生血管形成,发挥抗肿瘤作用[4]。本研究分析BV 联合化疗治疗转移性直肠癌患者效果,为后期制定治疗方案提供参考。现报道如下:
1 资料与方法
1.1 一般资料 选择我院于2016 年2 月~2018 年1 月收治的90 例转移性直肠癌患者,按随机数字表法分为联合组和对照组,各45 例。联合组女10 例,男 35 例;年龄 37~78 岁,平均(46.32±2.10)岁;盆腔转移15 例,肺转移12 例,肝转移27 例,其他9例;黏液癌5 例,腺癌40 例。对照组女13 例,男32例;年龄 35~79 岁,平均(46.25±2.03)岁;盆腔转移14 例,肺转移 11 例,肝转移 29 例,其他 6 例;黏液癌7 例,腺癌38 例。两组一般资料对比,差异无统计学意义(P>0.05)。本研究经医院医学伦理委员会审核批准。
1.2 入组标准 纳入标准:符合《现代肿瘤学》[6]中转移性直肠癌诊断标准,经病理检查确诊;年龄≥18岁;预计生存期>3 个月;患者及其家属签署知情同意书;凝血功能正常。排除标准:长期使用免疫抑制剂;精神疾病或认知功能障碍;合并内分泌系统疾病;合并严重心脑血管疾病;过敏体质。
1.3 治疗方法 对照组行FOLFIRI 方案化疗,第1天静脉滴注盐酸伊立替康注射液(国药准字H20143126)180 mg/m2、注射用亚叶酸钙(国药准字H20060198)400 mg/m2、氟尿嘧啶注射液(国药准字H21024236)400 mg/m2,连续化疗 4 个周期,每个周期2 周。联合组在此基础上使用BV(国药准字S20190040) 治疗,0.9%氯化钠溶液 100 ml+BV 1 mg/kg 静脉滴注,时间控制在 30~60 min,每 2 周给药1 次,共治疗4 次。
1.4 观察指标 (1)临床疗效:肿瘤病灶完全消失,维持4 周以上未复发为完全缓解(CR);肿瘤体积缩小≥50%,维持4 周以上未复发为部分缓解(PR);肿瘤体积缩小<50%,或增大<20%为稳定(SD);肿瘤体积增大≥20%,或无明显缩小,或出现新的病灶为进展(PD)。治疗总有效=CR+PR。(2)采集治疗前、治疗4 个周期后两组患者空腹肘静脉血5 ml,离心取上清液,采用酶联免疫吸附试验(ELISA)测血清环氧化酶-2(COX-2)、VEGF、基质金属蛋白酶-9(MMP-9)。(3)随访 3 年,比较两组预后情况:生存时间和无疾病进展时间。(4)两组不良反应(胃肠道反应、骨髓抑制、周围神经炎、肾功能不全、脱发、肝功能不全等)发生情况。
1.5 统计学方法 应用SPSS21.0 统计学软件分析处理数据,计数资料以%表示,采用χ2检验,计量资料以()表示,采用t检验,P<0.05 为差异有统计学意义。
2 结果
2.1 两组临床疗效比较 与对照组相比,联合组治疗总有效率更高,差异有统计学意义(P<0.05)。见表1。
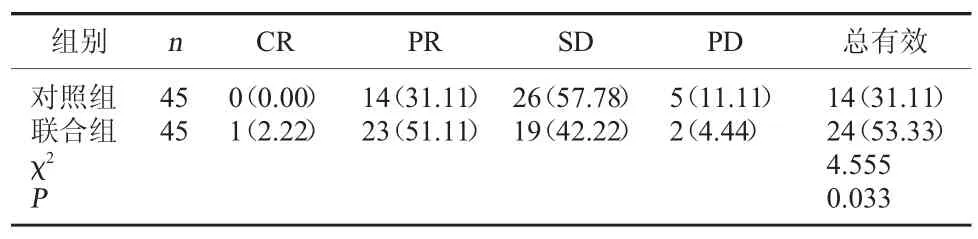
表1 两组临床疗效比较[例(%)]
2.2 两组预后情况比较 联合组生存时间和无疾病进展时间较对照组长,差异有统计学意义(P<0.05)。见表 2。
表2 两组预后情况比较(月,)
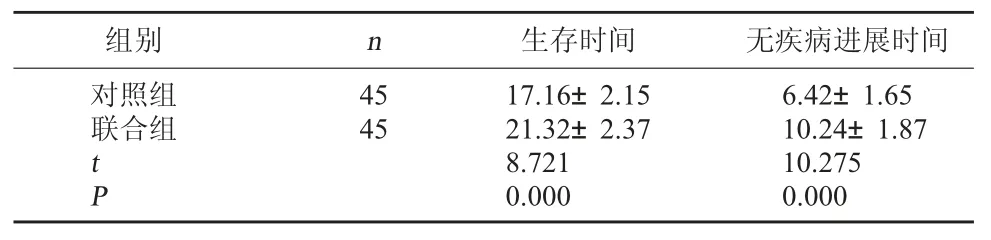
表2 两组预后情况比较(月,)
组别 n 生存时间 无疾病进展时间对照组联合组45 45 tP 17.16±2.15 21.32±2.37 8.721 0.000 6.42±1.65 10.24±1.87 10.275 0.000
2.3 两组肿瘤标志物比较 治疗前两组肿瘤标志物各指标比较无明显差异(P>0.05),治疗后联合组肿瘤标志物各指标较对照组低(P<0.05)。见表3。
表3 两组肿瘤标志物比较()
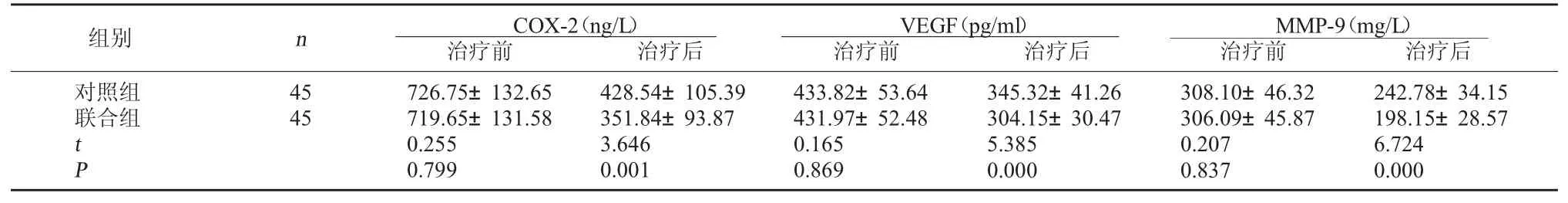
表3 两组肿瘤标志物比较()
MMP-9(mg/L)治疗前 治疗后对照组联合组组别 n COX-2(ng/L)治疗前 治疗后VEGF(pg/ml)治疗前 治疗后45 45 tP 726.75±132.65 719.65±131.58 0.255 0.799 428.54±105.39 351.84±93.87 3.646 0.001 433.82±53.64 431.97±52.48 0.165 0.869 345.32±41.26 304.15±30.47 5.385 0.000 308.10±46.32 306.09±45.87 0.207 0.837 242.78±34.15 198.15±28.57 6.724 0.000
2.4 两组不良反应发生情况比较 两组不良反应发生率对比,差异无统计学意义(P>0.05)。见表4。
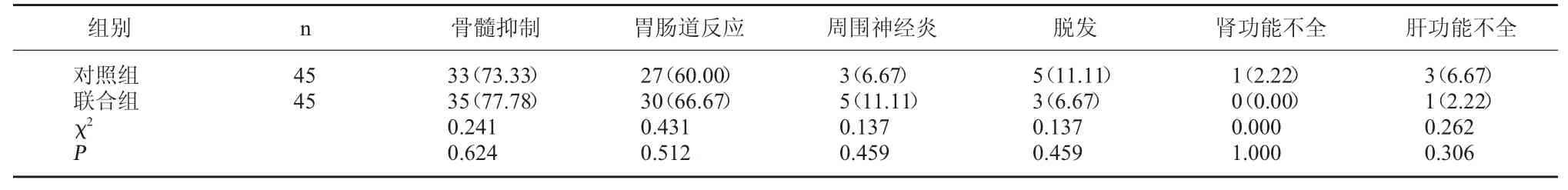
表4 两组不良反应发生情况比较[例(%)]
3 讨论
直肠癌发生与吸烟、高蛋白饮食、家族性肠息肉密切相关,患者早期无典型性表现,不易受到重视,确诊时多已发生转移,根治手术治疗效果欠佳。FOLFIRI 化疗方案是治疗转移性直肠癌常用手段,其中伊立替康可经代谢产物SN-38 损伤DNA 单链,对肿瘤细胞DNA 复制造成影响,起到抗肿瘤目的;5-氟尿嘧啶可杀伤增殖期肿瘤,尤其S 期细胞,还可抑制胸腺嘧啶核苷酸合成酶活性,阻止细胞DNA 形成;亚叶酸钙可提供大量还原性叶酸,增强5-氟尿嘧啶作用[7~8]。诸药合用可改善机体肿瘤负荷,降低病灶转移、扩散风险。但单一治疗方案临床缓解率较低,且患者5 年生存率无明显提高。
BV 可阻碍VEGF 结合血管内皮细胞受体,降低肿瘤血管内皮细胞损伤修复能力,促进肿瘤血管萎缩,致使肿瘤细胞凋亡、坏死,还可对肿瘤细胞核DNA 扩增速度造成影响,致使纺锤体分裂速度减慢,进而有效抑制肿瘤细胞扩散、复制,发挥抗肿瘤作用[9~10]。本研究结果显示,与对照组相比,联合组治疗总有效率更高,治疗后 COX-2、VEGF、MMP-9 水平更低,生存时间和无疾病进展时间较对照组长(P<0.05),两组各项不良反应发生率比较无显著性差异(P>0.05),提示BV 联合化疗可提高转移性直肠癌患者临床疗效,降低血清学肿瘤标志物水平,且未增加毒副作用,有利于患者预后。BV 可使肿瘤细胞缺血时间延长,增加对肿瘤细胞器、细胞膜结构的破坏,使肿瘤标志物释放减少,并可使肿瘤细胞氧化应激性损伤提高,导致肿瘤细胞核DNA 分裂速度减慢,进而抑制肿瘤生长。同时BV 可优化肿瘤组织微血管结构,改善血管通透性、组织密度,提高肿瘤组织对细胞毒药物摄取率,增强化疗效果。
综上所述,在转移性直肠癌患者中行BV 联合化疗不会增加毒副作用,并可提高临床疗效,降低肿瘤标志物水平,改善患者预后。
