基于质量源于设计(QbD)理念优化七叶神安分散片的制备*
2021-02-23纪晓燕陈志伟陈王燕王伟影
纪晓燕,朱 婷,陈志伟 ,陈王燕 ,王伟影
(1 浙江维康药业股份有限公司,浙江 丽水 323000;2 丽水市质量检验检测研究院,浙江 丽水 323000)
人用药品注册技术国际协调会议(ICH)在2009年发布的ICH Q8(R2)提出了质量源于设计(quality by design,QbD)理念[1],推动药品质量管理理念从“质量源于检验(quality by testing,QbT)”向“质量源于设计(quality by design,QbD)”转变[2-3]。QbD理念关注药物制剂原料属性、制备工艺、成品质量之间的关系,预先设定好目标质量属性,基于科学知识和风险管理确定关键因素,通过实验设计(Design of Experiment,DOE)对生产工艺进行控制[4],确定最佳方式。
七叶神安分散片的主要药效成分为三七叶总皂苷,临床主要用于心气不足、心血瘀阻所致的心悸、失眠、胸痛、胸闷等症,是2008年获国家食品药品监督管理局批复的在七叶神安片的基础上为提高生物利用度而开发的便于服用且起效快的新制剂[5]。现行制备方法以预胶化淀粉为填充剂和黏合剂、羧甲基淀粉钠(羧甲淀粉钠)为崩解剂、微粉硅胶(二氧化硅)为润滑剂和助流剂、硬脂酸镁为润滑剂,用量分别占处方的14.2%、21.3%、46.1%和0.7%,因作为润滑剂和助力剂的微粉硅胶(二氧化硅)用量过大,生产中制剂成型困难,制成的颗粒细粉较多,颗粒较松散,产尘较大,较难顺利压片,出现裂片概率较高;而崩解剂羧甲基淀粉钠遇水膨胀会形成透明胶团,部分胶团易吸附在崩解仪吊篮的不锈钢筛孔上,不能完全通过筛网。本实验基于QbD的指导理念,在生产实际和原有研发基础上[6]对七叶神安分散片进行二次开发,优化制备工艺,旨在提高七叶神安分散片质量的稳定性和一致性。
1 仪器与试药
1.1 仪 器
BP211D电子天平,德国赛多利斯公司;LC-2030C高效液相色谱仪,日本岛津公司;ZRS-8G溶出度试验仪,天津大学精密仪器厂;ZB-1E崩解仪,天津市天大天发科技有限公司;FT-2000A脆碎度检测仪,天津市天大天发科技有限公司;Milli-Q Advantage A10超纯水仪。
1.2 试 药
人参皂苷Rb3对照品(批号:111686-201504,质量分数:97.0%),中国食品药品检定研究院;乙腈(色谱纯),赛默飞;甲醇(色谱纯),赛默飞;磷酸(色谱纯),上海展云;水为自制超纯水。
三七叶总皂苷(批号:20161032),浙江维康药业股份有限公司;羧甲淀粉钠(批号:20160936),湖州展望药业有限公司;羧甲纤维素钠(批号:160708),安徽山河药用辅料股份有限公司;交联羧甲纤维素钠(批号:160503),安徽山河药用辅料股份有限公司;低取代羟丙纤维素(批号:20160705),湖州展望药业有限公司;预胶化淀粉(批号:150320),安徽山河药用辅料股份有限公司;微晶纤维素(批号:161062),安徽山河药用辅料股份有限公司;二氧化硅(批号:20161014),湖州展望药业有限公司;硬脂酸镁(批号:160919),安徽山河药用辅料股份有限公司。
2 方法与结果
2.1 关键质量属性(Critical Quality Attributes,CQAs)分析
基于七叶神安分散片现行法定标准[5]的质量控制项目,对安全性、有效性的影响程度进行CQAs分析。结果见表1。

表1 七叶神安片关键质量属性分析表
2.2 基于风险评估确定关键因素
由CQAs分析结果可知,溶出度和分散均匀性为七叶神安分散片制备工艺优化中重点评估的CQAs。影响CQAs的因素有环境(温度、湿度)、设备(型号、功率)、处方和生产工艺等4类因素,因本实验在同一环境中使用同一设备,环境和设备影响CQAs的风险极低,可忽略;七叶神安分散片片重为0.28 g,片较小,生产方式为制粒后压片,生产工艺带来的风险忽略;片重0.28 g,其中三七叶总皂苷用量约为0.05 g,辅料约为0.23 g,处方影响CQAs的风险极高,将风险因素处方细化,如图1所示。针对处方因素进行风险分析,原料药用量少(约占处方的17.9%),其粒度不会对药物的溶出度和分散均匀性产生大的影响;辅料中,骨架材料的种类和用量将是影响影响药物溶出度和分散均匀性的关键物料属性,即关键因素;其他辅料为次关键因素。

图1 处方因素风险分析鱼刺图
2.3 制备设计及优化
本实验采用粉末直接压片技术,在筛选辅料种类时考虑选择同时具备多种作用的材料。
2.3.1 骨架材料(填充剂)、崩解剂的选择
选择分散片制备中最常用的骨架材料(填充剂)预胶化淀粉、羧甲纤维素钠、交联羧甲纤维素钠、微晶纤维素4种材料进行单因素考察,以分散片的外观、硬度[5]、溶出度[5]为考核指标,结果见表2。

表2 填充剂的筛选
选择常用的羧甲淀粉钠(羧甲基淀粉钠)、羧甲纤维素钠、交联羧甲纤维素钠、低取代羟丙纤维素4种崩解剂,以分散均匀性[5]为考核指标,进行单因素试验,结果见表3。
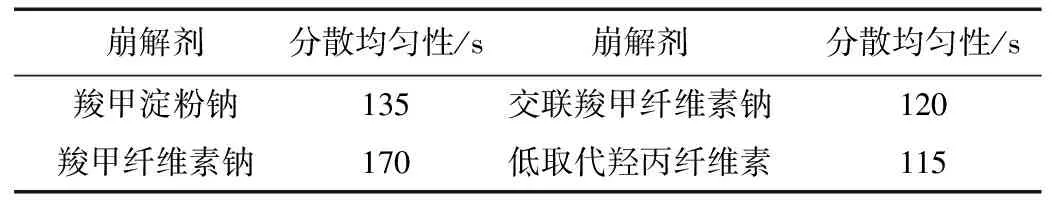
表3 崩解剂的筛选
由表2、表3可知,微晶纤维素做为骨架材料(填充剂)兼具黏合剂的作用,较其他材料有优势,外观、硬度和溶出度都得到了较好的改善;低取代羟丙纤维素作为崩解剂,分散均匀性时间最佳,且分散片全部崩解并通过筛网,无胶团易吸附在崩解仪吊篮的不锈钢筛孔上,不能完全通过筛网的情况。
2.3.2 正交试验确定最佳制备处方
项目组小试发现选用微晶纤维素、低取代羟丙纤维素作为骨架材料(填充剂)、崩解剂之后,微粉硅胶(二氧化硅)的使用量可大幅度减少;依据大量小试实验,确定低取代羟丙纤维素(A)、微晶纤维素(B)和二氧化硅(C)进行三因素三水平正交试验(表4),以颗粒休止角、外观、硬度、分散均匀性为评价指标,确定最佳处方配比,结果见表5。

表4 正交因素水平表

表5 正交试验结果
由表5可知,休止角和分散均匀性的最佳组合均为A1B3C3;外观和硬度的最佳组合均为A2B3C1;综合考虑整体最佳方案为A3B3C2,即低取代羟丙纤维素14.3%、微晶纤维素66.5%和二氧化硅0.4%。
综合考虑,确定七叶神安分散片的制备工艺为,取三七叶总皂苷50 g,加入微晶纤维素约186.2 g、二氧化硅2.8 g、低取代羟丙纤维素40 g,混匀,制粒,加入硬脂酸镁1 g,混匀,压制成1000片,即得。
2.4 验证试验
根据确定的制备工艺进行连续3批放大生产七叶神安分散片,对成品得率、脆碎度、溶出度、分散均匀性、含量测定和重量差异进行考察[5,7];同时考察3批相同原料制备工艺优化前七叶神安分散片的脆碎度、溶出度、分散均匀性、含量测定和重量差异,结果见表6、表7。
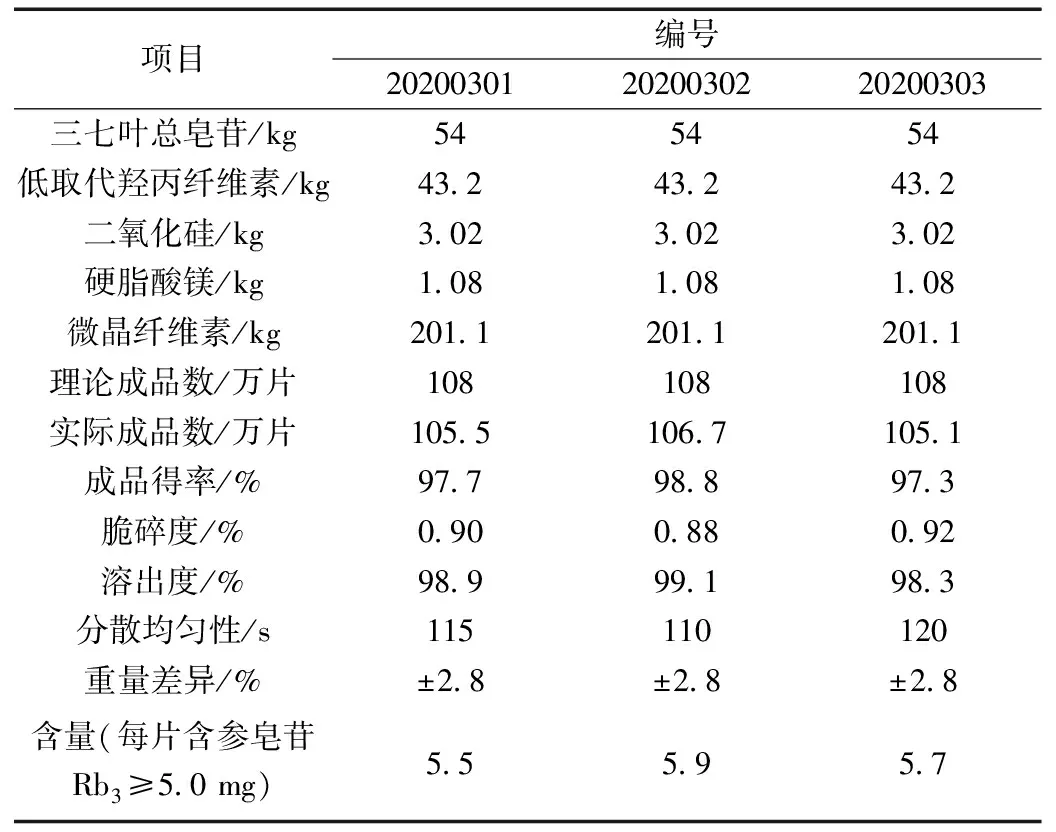
表6 三批放大生产数据

表7 三批制备工艺优化前的七叶神安片
3 结 论
七叶神安片分散片在初始研发时也进行了制备工艺的筛选[6],多年生产过程中发现,初始研发筛选的助流剂(微粉硅胶<二氧化硅>)和崩解剂(羧甲基淀粉钠<羧甲淀粉钠>)存在不易压片、易出现裂片、重量差异波动较大、分散均匀性接近标准要求限度等不利于大宗生产中控制药物质量的情况,项目组从QbD的指导理念出发,对CQAs进行分析,并基于风险评估、使用鱼刺图对CQAs的影响因素进行识别和排序,确定辅料的重量和用量是关键影响因素。
项目组在二次开发时不改变压片技术,以外观、硬度、溶出度为考核指标,筛选了可同时作为填充剂和黏合剂的微晶纤维素、兼具崩解剂和黏合剂作用的低取代羟丙纤维素,解决了压片不易的情况,改善了片剂外观的光亮度、提高了片剂的溶出度,同时也加快了片剂的崩解速度。
3批放大生产的七叶神安分散片的验证结果显示,基于QbD理论优化的制备工艺,提高了七叶神安分散片批次间质量的一致性,可为大宗生产提供参考,也可为其他品种药物的二次开发提供参考。
