两种结核感染T细胞检测试剂盒性能评估
2021-02-23潘建华李艳红周锐雄余俊鹏杨锦鸿
潘建华,张 玲,李艳红,周锐雄,余俊鹏,杨锦鸿
广州金域医学检验中心血液室/广州医科大学金域检验学院,广东广州 510330
结核病是由结核分枝杆菌(MTB)感染导致的一种慢性传染病。肺外结核感染临床表现较为隐匿,症状不典型,容易导致误诊、漏诊[1]。常规的MTB培养需要时间较长,培养条件要求较高,而且易受到标本质量和MTB数量的影响,阳性率仅为30%,痰涂片检出率也相对较低[2]。近年来,MTB感染T细胞斑点试验(T-SPOT.TB)越来越受到关注,其利用酶联免疫斑点法(ELISPOT)检测是否存在MTB感染T淋巴细胞后分泌的特异性细胞因子干扰素-γ(IFN-γ)来判断有无MTB感染[3]。多项研究表明,T-SPOT.TB在诊断MTB感染方面具有灵敏度高、特异性强的特点,目前已在临床上广泛应用[4-8],而目前市场推广较为广泛的进口试剂由于价格昂贵,不能在临床上普及使用,因此,选择一种经济、快速、准确地诊断MTB感染的检测方法对于结核病的防治至关重要。本研究通过多家实验室验证评估国产与进口同类T-SPOT.TB产品的检测性能,现报道如下。
1 材料与方法
1.1标本来源 来自广州金域(112份)、杭州金域(88份)、福州金域(64份)、成都金域(80份)、沈阳金域(64份)检验中心的临床标本,共408份,来源患者中男215例,女193例;年龄2~83岁,中位年龄47岁。金域体检中心50份T-SPOT.TB检测体检标本,体检者中男25例,女25例;年龄25~48岁,中位年龄35岁;所有体检人员HIV抗体检测均为阴性。
1.2仪器与试剂 参比试剂盒由英国Oxford Immunnotec公司提供,考核试剂由北京同生时代生物技术有限公司提供。使用仪器包括安徽嘉文仪器装备有限公司生产的JW-1050R低速冷冻离心机、日本Panasonic生产的CO2培养箱,济南鑫贝西生物技术有限公司生产的BIOBASEⅡ级生物安全柜,美国CTL公司生产的酶联免疫荧光斑点分析仪。淋巴细胞分离液、RPMI-1640培养基分别由上海复星医学科技发展有限公司和北京同生时代生物技术有限公司提供。
1.3方法 对458份标本分别使用参比试剂(进口)和考核试剂(国产)进行ELISPOT,提取外周血单个核细胞刺激培养进行斑点计数判断结果,对两种试剂检测结果进行Kappa检验,以Kappa值≥0.75为两者一致性较好。
1.3.1标本采集 采血量:肝素抗凝全血,2岁以下儿童2~3 mL,其他年龄受试者4~6 mL,免疫力低下或白细胞计数降低的受试者6~8 mL。标本存储:标本室温(15~25 ℃)保存及运输,不得冷冻或冷藏,建议24 h内送至实验室,室温保存不应超过32 h。
1.3.2检测方法 所有操作均按照试剂盒说明书进行,参比试剂采用ELISPOT对早期分泌抗原靶6 000(ESAT-6)和培养滤液蛋白10 000(CFP-10)有反应的T细胞进行斑点计数;考核试剂采用ELISPOT对复合抗原ESAT-6/CFP-10/Esx-1底物蛋白Rv3615c(Rv3615c)有反应的T细胞进行斑点计数。
1.4判断标准
1.4.1参比试剂结果判断 参比试剂检测结果包括阴性对照孔和阳性对照孔、抗原A和抗原B结果。(1)试验有效的标准:阴性对照孔内斑点计数<10个,且阳性对照孔内斑点计数>20个。(2)阳性结果判断标准:①阴性对照孔斑点计数<6个,且抗原A或抗原B孔的斑点计数—阴性对照孔斑点计数的结果>6个;②阴性对照孔斑点计数>6个,且抗原A 或抗原B孔的斑点计数>2倍阴性对照孔斑点计数。满足阳性结果判断标准任意一条即为阳性,否则为阴性。
1.4.2考核试剂结果判断 考核试剂结果包括阴性对照孔、检测孔、阳性对照孔结果。当阴性对照孔斑点计数为0~5个时,考核试剂结果判断方法见表1。
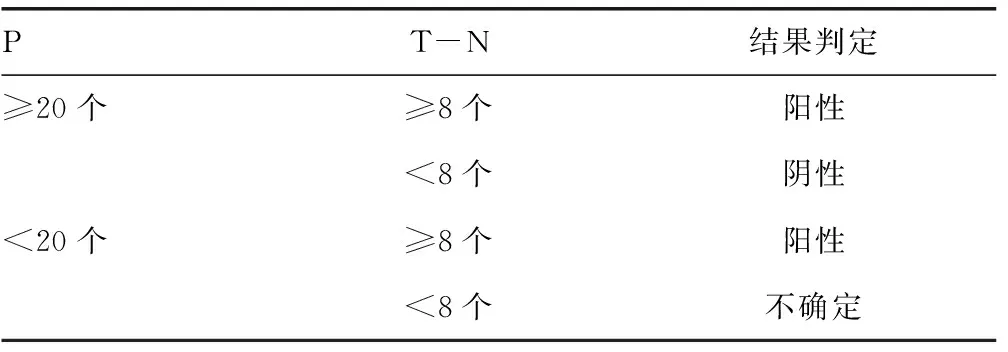
表1 考核试剂结果判断
1.5统计学处理 两种试剂检测的数据采用Kappa一致性检验分析。
2 结 果
2.1考核试剂与参比试剂对临床标本的检测结果一致性 408份临床标本中,400份标本两种试剂检测结果一致,其中有8份标本两种试剂检测结果不一致,考核试剂检测为阳性,参比试剂检测为阴性,两种试剂的检测结果总一致率为98.04% (Kappa=0.96)。广州金域检验中心一致率为96.43%(Kappa=0.93); 杭州金域检验中心一致率为97.73%(Kappa=0.95); 福州金域检验中心一致率为98.44%(Kappa=0.97);成都金域检验中心一致率为98.75%(Kappa=0.97); 沈阳金域检验中心一致率为100.00%(Kappa=1.00)。见表2。
2.2考核试剂与参比试剂对体检标本的检测结果一致性 50份体检标本中,49份标本两种试剂检测结果均与临床诊断符合,1份标本考核试剂检测结果为阳性(斑点计数为5个),参比试剂为阴性,两种检测试剂一致率为98.00%(49/50)。见表2。

表2 两种试剂检测结果比较

续表2 两种试剂检测结果比较
3 讨 论
病原学检查常作为诊断结核病的金标准,如痰涂片常用于肺结核的诊断,但其受制于痰液取样及痰中MTB数量的影响,故灵敏度较低,且无法诊断肺外结核及不咳痰结核病,使其应用受到一定的限制[9]。MTB感染者外周血中存在MTB特异的活化效应T细胞,这些T细胞在受到ESAT-6和CFP-10刺激后分泌细胞因子,其中包括IFN-γ。临床常通过检测IFN-γ的量和ELISPOT提取外周血单个核细胞刺激培养进行斑点计数,从而推测体内是否存在对MTB反应的效应T细胞,进一步对MTB感染情况进行辅助诊断。本研究两种试剂均采用ELISPOT原理,并同时设有阴性和阳性对照评估试验可靠性。ELISPOT应用于结核病诊断已近20年[10-11],能够检测出1/100 000~1/50 000的外周血单个核细胞中经抗原刺激后释放细胞因子的细胞,现已成为最敏感的检测方法之一。
本研究结果显示,考核试剂的检测性能不仅与参比试剂的检测性能一致性较好,而且在MTB阳性检出率方面优势更为突出,文中有8份标本考核试剂检测为阳性,而参比试剂检测为阴性,其中有6份阳性标本来源患者临床诊断为肺部疾病或有结核症状和治疗史,有2份标本阳性待确诊,尚不能排除假阳性的可能,分析原因可能与各自试剂抗原组合有关,参比试剂是通过ELISPOT检测MTB 特异性抗原ESAT-6和CFP-10刺激T淋巴细胞释放的IFN-γ进行检测,为单抗原判读结果,容易造成一定比例的漏检,而考核试剂是采用复合三抗原(ESAT-6/CFP-10/Rv3615c)刺激T淋巴细胞释放的IFN-γ,增加了检测敏感性, MTB引起的机体免疫反应是多个抗原共同起作用的结果,而考核试剂在基础抗原ESAT-6、CFP-10基础上,增加了ESX-1底物蛋白Rv3615c抗原。 Rv3615c是免疫原性较强的靶抗原,其基因表达依赖MTB基因组RD1区,包含了多个肽段的集合体,可被MTB感染者T细胞识别。采用抗原三合一技术,更能模拟人体内MTB引起的免疫反应,在巨噬细胞的吞噬体内活跃表达,更接近体内的真实情况,所以,运用复合抗原EAST-6/CFP-10/Rv3615c筛查MTB可提高结核病患者和潜伏结核感染人群的检出率。
综上所述,金域集团5家连锁检验中心同时用考核试剂和参比试剂对408份临床标本进行验证,均获得较高的检出率,两种试剂检测结果有较高的一致性,检验性能尚未发现有本质区别,对MTB感染的辅助诊断均具有指导意义。