水中溴溶液标准物质的研制
2021-02-04李锋丽孙倩芸许爱华邱黛君周宁宁
李锋丽 孙倩芸 许爱华 邱黛君 孙 华 周宁宁
(山东省计量科学研究院,济南 250014)
1 引言
溴是常温常压下呈液体状的非金属元素,是重要的矿产资源,主要以离子形式散布在地壳水圈中。测定水中溴离子的含量可以确定溴资源的品位,并且为建立提溴方法提供基础数据,对于溴资源的回收利用具有重要意义。现代生活饮用水处理消毒工艺主要采用O3、ClO2和Cl2混合消毒方法,当水中富含溴离子时,臭氧能将其氧化成溴酸盐。毒理学研究表明,饮用水中极低的溴酸盐对人类和动物具有潜在的致癌作用,在国际上被定为2B级的潜在致癌物[1]。我国饮用水卫生标准(GB/T5750-2006)中将溴酸盐列为常规检测项目,规定其最高含量不得超过0.7 mg/L。因此,准确测定水中溴离子含量能间接控制水中溴酸盐含量,保证饮用水安全[2]。
目前, 酚红分光光度法、离子色谱法、离子选择电极法和碘量法是检测溴离子的主要方法。离子色谱法由于操作简单、灵敏度高被作为测定水中溴离子的常用方法[3-5]。水中溴离子的精准测量离不开溴溶液标准物质,其对于保证测量结果的量值准确和溯源性具有重要意义。
2 材料与方法
2.1 主要仪器与材料
离子色谱仪:Thermo公司,型号:ICS-5000+;
分析天平:Sartorius公司,型号:MC210S ;
溴化钾标准物质:GBW(E)060321,国防科技工业应用化学一级计量站;
水中溴成分分析标准物质:GBW(E)080521,中国计量科学研究院;
实验用水均为超纯水。
2.2 实验条件
离子色谱仪:电导检测器;AS11-HC色谱柱;淋洗液:30 mM(KOH);流速:1.0 mL/min;柱温:30℃;进样量:25 μL。
3 标准物质的制备
3.1 样品预处理
将溴化钾标准物质在烘箱中于(110±10)℃下干燥6h,之后将其放入硅胶干燥器中,冷却至室温。
3.2 溴溶液标准物质的制备
在温度(20±2)℃,相对湿度(40±10)%的洁净室中,用分析天平称取2.98001 g3.1中处理好的溴化钾标准物质,置于烧杯内,加入500mL超纯水使其完全溶解后转移至2000 mL容量瓶中,用超纯水定容至刻度,混匀后得到质量浓度为1000μg/mL的溴标准溶液。将100瓶20mL的玻璃安瓿瓶清洗、干燥,然后将溴标准溶液分装至瓶中,每瓶20 mL。放置在阴凉处,常温保存。
4 均匀性和稳定性检验
4.1 均匀性检验
采用方差分析法考察溴溶液标准物质的瓶内均匀性和瓶间均匀性。在标准物质分装过程的前、中、后期随机抽取11瓶样品,用超纯水稀释至10μg/mL,在2.2实验条件下测定其质量浓度。分别以顺序、随机和倒序的顺序测量各瓶样品,每瓶测量3次,以平均值作为测量结果,统计结果见表1。

表1 均匀性检验结果 μg/mL
由表1中的数据计算出瓶间方差S12、瓶内方差S22和F值。结果显示,检验统计量F 将研制的标准物质在50℃下保存,采用离子色谱法在第1、2、3、4、5、6、7d进行50℃条件下的稳定性监测,统计结果见表2。 表2 短期稳定性检验结果 μg/mL 采用直线拟合法进行稳定性检验:以时间为自变量、标准物质的特性量值为因变量进行线性回归,通过t检验,溶液满足|b| 在预定的稳定性周期内,从2018年04月到2019年04月,按照先密后疏的原则,用离子色谱法测定溴溶液标准物质的量值,统计结果见表3。 表3 长期稳定性检验结果 μg/mL 数据处理方法同4.2,满 足|b| 标准物质采用重量-容量法制备,其量值为溶液中溶质的质量和溶液的体积比,定值公式为: (1) 其中标准溶液的质量浓度为ρ,溴化钾标准物质的质量为m,纯度为ω,相对分子量为M0,溴的相对分子量为M,配制的溶液体积为Vρ。 水中溴溶液标准物质的制备浓度为: 参照已有研究[10,11], 研制溴溶液标准物质的过程中引入的不确定度如表4所示。 表4 不确定度分量汇总 溴溶液标准物质质量浓度的相对标准不确定度按下式合成: 研制的溴溶液标准物质的质量浓度为1000μg/mL,相对扩展不确定度为Urel=1.0% (k=2),均匀性良好,12个月内量值稳定,可用于水中溴离子的检测分析。4.2 短期稳定性检验
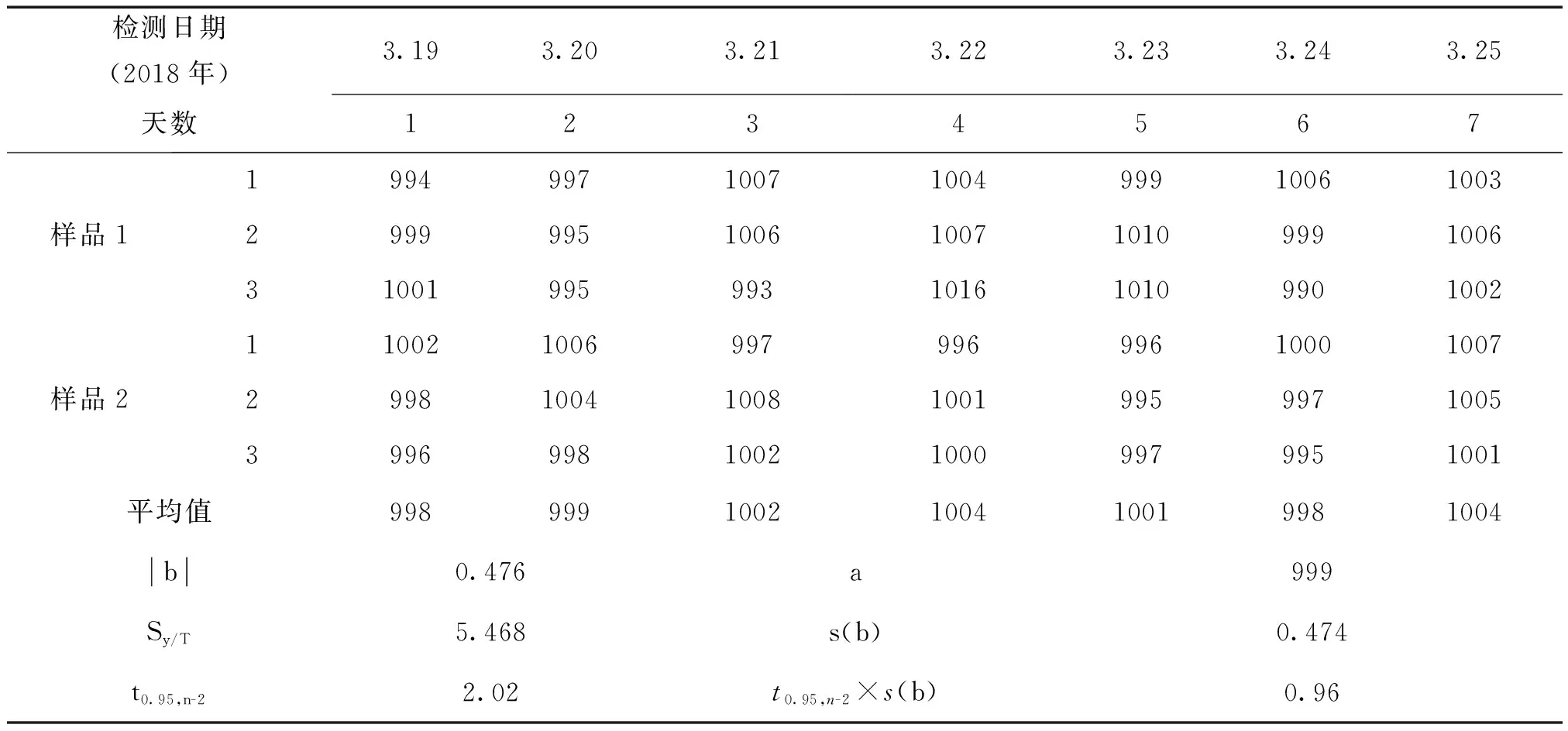
4.3 长期稳定性检验
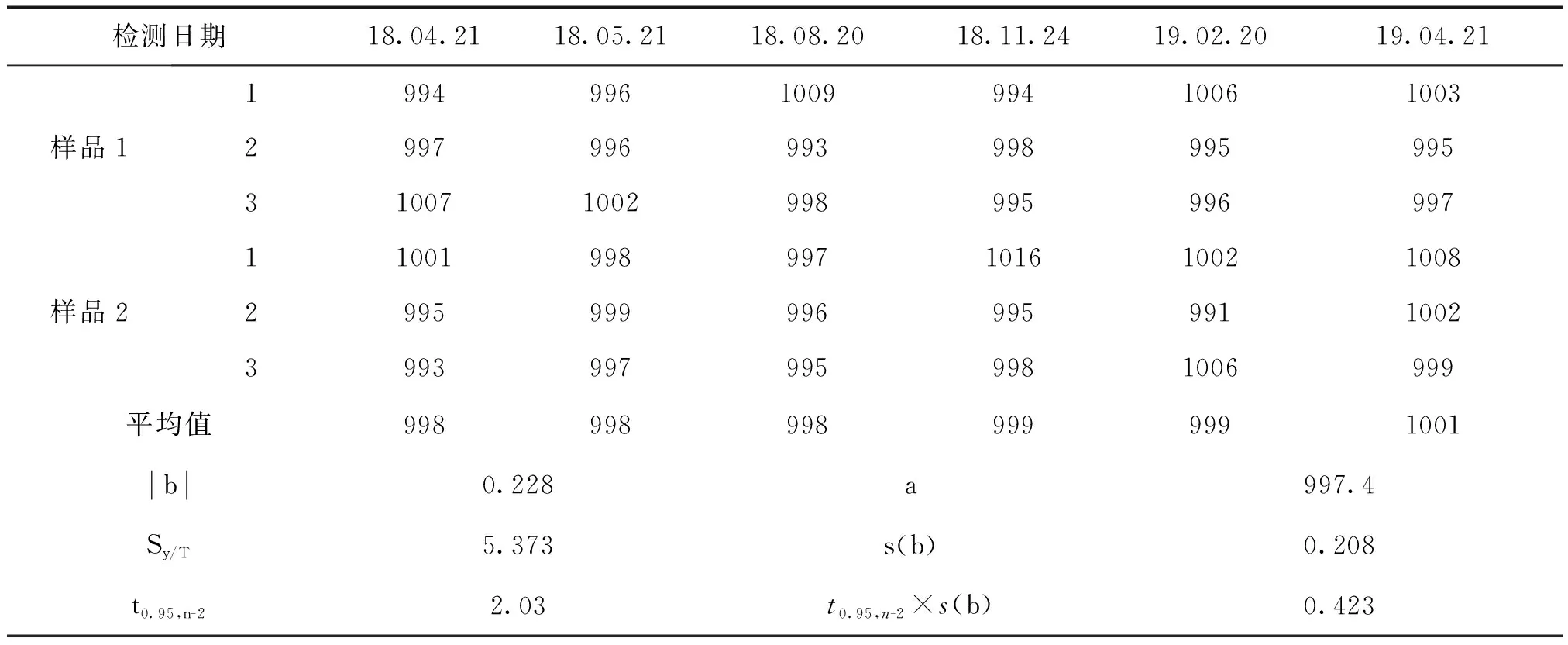
5 定值结果及不确定度评定
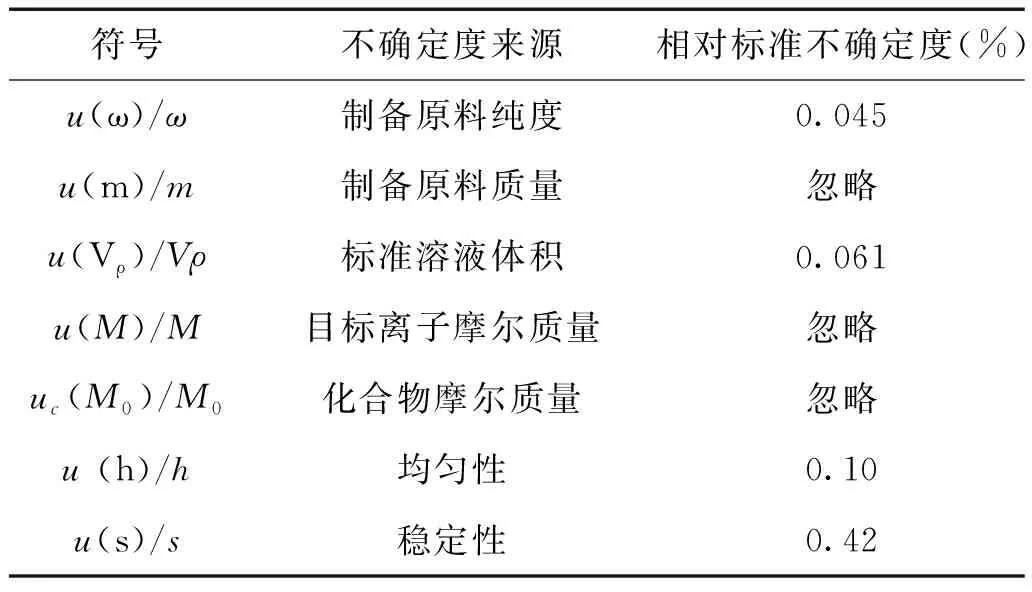

6结语
