聚乙二醇干扰素α-2a联合恩替卡韦治疗慢性乙型肝炎患者疗效及血清Pygo2和GP73水平变化*
2021-02-04郑志恒李维筠回振宇
郑志恒,李维筠,回振宇,陈 莹
慢性乙型肝炎(chronic hepatitis B,CHB)是乙型肝炎病毒(hepatitis B virus,HBV)持续感染引起的肝脏慢性炎症性疾病[1]。目前,临床上主要采取抗病毒、免疫调节、抗炎和护肝等方法治疗CHB患者,以长期抑制或消除病毒感染,保护肝功能。恩替卡韦是主要的抗病毒药物之一,临床试验[2]发现,长期采用恩替卡韦抗病毒治疗CHB患者也存在病毒耐药性问题,后续治疗困难。聚乙二醇干扰素α-2a(peg-IFN-α-2a)是主要的免疫调节性药物之一,能抑制HBV复制和通过免疫调节双重作用起到抗HBV的效果,具有较高的血清学应答和较持久的病毒学应答率[3,4]。本研究应用恩替卡韦联合peg-IFN-α-2a治疗CHB患者,分析了治疗效果及血清人尾肢同源蛋白2(people end limb homologous protein 2,Pygo2)和高尔基体糖蛋白73(Golgi glycoprotein 73,GP73)水平的变化,现将结果报道如下。
1 资料与方法
1.1 一般资料 2018年2月~2019年2月我院收治的CHB患者77例,男42例,女35例;年龄35~56岁,平均年龄为(42.3±5.6)岁;病程3~6年,平均为(4.5±1.3)年。符合中华医学会肝病学分会和感染病学分会联合修订的《慢性乙型肝炎防治指南(2015年版)》[5]的诊断标准。排除标准:合并恶性肿瘤、药物性肝损伤、酒精性肝炎、妊娠或哺乳期妇女、精神障碍、语言障碍或听力障碍者。采用随机数字表法将患者分为对照组36例和观察组41例,两组性别、年龄、病程和肝功能等一般资料比较均无统计学差异(P>0.05),具有可比性。本研究获得我院医学伦理委员会批准,患者及其家属签署知情同意书。
1.2 治疗方法 给予对照组患者恩替卡韦片(正大天晴药业集团股份有限公司,国药准字:H20100019)0.5 mg口服,1次/d;观察组在此基础上给予聚乙二醇干扰素α-2a注射液(上海罗氏制药有限公司,国药准字:S20040007)180 μg皮下注射,1次/w,两组均治疗观察24 w。
1.3检测指标 使用全自动生化分析仪检测血生化指标(美国贝克曼库尔特);采用实时荧光定量聚合酶链式反应法检测血清 HBV DNA水平(四川新先达测控技术有限公司);采用化学发光法检测血清HBeAg和抗HBe(上海联迈生物工程有限公司);采用ELISA法检测血清Ⅲ型前胶原(procollagen type,PCⅢ)、层粘连蛋白(laminin,LN)、透明质酸(hyaluronic acid,HA)、Ⅳ型胶原(collagen Type IV,Ⅳ-C)水平(上海信裕生物科技有限公司)及Pygo2和GP73水平(上海酶联生物科技有限公司)。
2 结果
2.1 两组血清学和病毒学应答率比较 在治疗观察结束时,观察组血清HBeAg转阴率和HBeAg血清转换率均显著高于对照组(P<0.05,表1)。
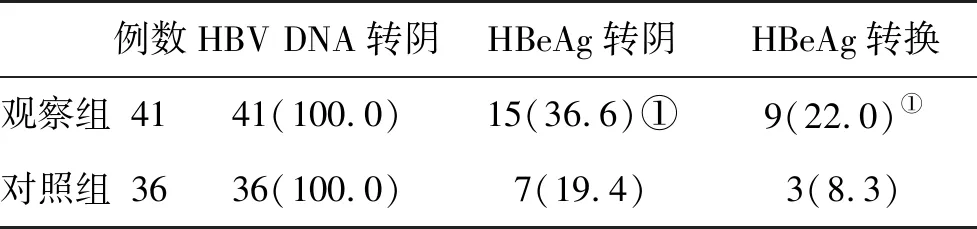
表1 两组血清学和病毒学应答率[n(%)]比较
2.2 两组肝功能指标比较 在治疗结束时,观察组患者血清ALT水平显著低于对照组(P<0.05,表2)。
2.3 两组血清肝纤维化指标比较 在治疗结束时,观察组患者血清LN、Ⅳ-C、PC-Ⅲ和HA水平均显著低于对照组(P<0.05,表3)。
2.4 两组血清肝脏病变相关因子比较 在治疗结束时,观察组患者血清Pygo2和GP73水平均显著低于对照组(P<0.05,表4)。
表2 两组肝功能指标比较

表3 两组血清肝纤维化指标比较

表4 两组血清肝脏病变相关因子水平比较
3 讨论
CHB患者肝纤维化进展可发展为肝硬化,同时疾病进展为肝癌的几率也会增大。调查研究[5]发现,每年死于CHB进展性疾病的患者约有60万人。我国肝硬化和原发性肝癌患者继发于慢性CHB感染的比例分别为60%和80%,每年因原发性肝癌死亡人数超过20万,占世界原发性肝癌死亡总人数的45%。临床研究[6]显示,CHB患者临床治愈的必要条件之一是尽早实现HBV DNA和HBeAg转阴以及HBeAg血清学转换,获得更早的停药时机,减少延长疗程后耐药的风险。欧美肝病研究机构认为,CHB患者实现HBV DNA和HBeAg转阴以及HBeAg血清学转换甚至临床治愈的现实途径之一在于机体免疫功能的激活[7]。恩替卡韦是一种环戊酰鸟苷酸类似物,为治疗CHB的一线药物,其能通过干扰病毒的核苷酸代谢,直接抑制病毒复制,通过体内磷酸化生成具有抑制HBV DNA聚合酶作用的三磷酸核苷类似物,并与HBV多聚酶底物三磷酸脱氧鸟嘌呤核苷相互竞争,从而抑制HBV多聚酶的活性,达到抑制病毒复制的作用,但长期临床实践显示,其抗病毒作用会随着用药时间的延长而减弱。2018年美国肝病学会将聚乙二醇干扰素α-2a列为治疗CHB的优先选择的药物之一,有利于患者机体免疫系统功能的改善,同时规避HBV耐药的发生[8, 9]。聚乙二醇干扰素α-2a的主要代谢部位在肝脏,其作用效果主要表现在抑制HBV复制,增强巨噬细胞活性,增强淋巴细胞对靶细胞的细胞毒性等免疫调控作用[10]。聚乙二醇干扰素α-2a主要作用机制在于通过诱导细胞内抗病毒活性作用,与细胞表面受体结合,激活细胞内多种抗病毒蛋白,促使病毒RNAs降解,从而抑制HBV DNA的复制。同时,它还可增强NK细胞、巨噬细胞和T淋巴细胞的活力,起到免疫调节作用,具有抗纤维化作用。此外,聚乙二醇干扰素α-2a在α-干扰素的基础上结合了一定分子量的聚乙二醇分子,有利于α-干扰素活性的保持和半衰期的延长,使其抗病毒效应得到持续和巩固[11]。临床研究[12]显示,180 μg聚乙二醇干扰素α-2a经皮下注射进入血流,其治疗浓度维持时长可达80~168 h,实现长效提高免疫的抗病毒效果。本研究在治疗结束时,虽然两组HBV DNA转阴率相似,但联合组血清HBeAg转阴率和HBeAg血清转换率均显著高于对照组,说明聚乙二醇干扰素α-2a能通过调节免疫功能发挥其更好的抗病毒效果。
研究指出,基线ALT水平可能与聚乙二醇干扰素α-2a对CHB患者的治疗效果有关,可能是基于药物对肝脏保护作用的关系[13]。本研究在治疗后,观察组血清ALT水平显著低于对照组。分析原因可能为皮下注射聚乙二醇干扰素α-2a后,其会在血液中高度积聚并直接被运输到肝组织,使肝脏维持较高的血药浓度,直接提高了药物的抗病毒活性,可能具有更大的抗病毒作用[14]。研究表明,应用聚乙二醇干扰素α-2a联合恩替卡韦治疗CHB患者,血清ALT复常率显著高于恩替卡韦单独使用组,说明聚乙二醇干扰素α-2a在保护肝功能、促进ALT复常方面,效果良好[15]。临床研究[16,17]发现,良好的护肝作用有助于阻滞CHB患者肝纤维化进展。本研究在治疗后,观察组患者血清LN、Ⅳ-C、PC-Ⅲ和HA水平均显著低于对照组,说明聚乙二醇干扰素α-2a在保护肝脏,缓解肝纤维化方面具有良好的效果。
Pygo2和GP73均是重要的肝脏病变相关标志物。临床研究[18]显示,Pygo2与肝纤维化密切相关,而GP73在肝脏发生病变时表达异常。CHB患者血清GP73水平增高,提示其可能对CHB发生和肝脏病变具有促进作用[19]。本研究在治疗后,观察组血清Pygo2和GP73水平均显著低于对照组,说明聚乙二醇干扰素α-2a联合恩替卡韦治疗能显著缓解CHB患者肝脏病变,抑制疾病进展。临床研究[20]发现,应用聚乙二醇干扰素α-2a能通过诱导细胞内抗病毒活性,激活细胞内多种抗病毒蛋白,促使病毒RNAs降解,从而抑制HBV DNA的复制,同时还可增强NK细胞等免疫细胞的活力,起到免疫调节和抗肝纤维化的双重作用,抑制病毒复制,缓解疾病进展。
