应用肿瘤坏死因子拮抗剂人群结核潜伏感染的检测及预防性治疗
2021-02-03谭雨亭侍效春刘晓清
谭雨亭,侍效春,刘晓清
中国医学科学院 北京协和医学院 北京协和医院感染内科,北京 100730
世界卫生组织(World Health Organization,WHO)发布的《2019年全球结核病报告》指出,全球潜伏结核感染(latent tuberculosis infection,LTBI)人群约为17亿,占全球人口1/4左右。2018年全球新发结核病例约为1000万,其中中国新发结核病例居全球第二位(9%)。结核病是全球重要的公共卫生问题,仍是人类十大死因之一,居于单一传染性疾病死因之首[1]。LTBI的早期发现和治疗对消除和控制活动性结核十分重要。肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)拮抗剂的使用是发生活动性结核的高危因素,2015年WHO发布的LTBI管理指南强烈推荐在接受TNF-α拮抗剂治疗的患者中开展LTBI筛查和治疗[2]。随着越来越多生物制剂疗效和安全性临床试验的开展,TNF-α拮抗剂在临床上的应用越来越被肯定,临床上对于这部分患者LTBI的筛查和治疗越来越重视。由于结核病流行病学和社会经济状况等存在差异,目前不同国家的指南或共识关于该类人群LTBI的管理并不一致。本文对应用TNF-α拮抗剂LTBI的筛查和治疗作一综述,以期为临床诊疗提供借鉴。
1 应用肿瘤坏死因子-α拮抗剂使活动性结核发病风险增加
TNF-α拮抗剂的出现使风湿性疾病的治疗取得突破性进展,虽然其疗效在临床上得到了验证,但其副作用尤其是结核感染等并发症不容忽视。TNF-α拮抗剂的使用是活动性结核发病的高危因素,其风险是普通人群的1.6~25.1倍[3],尤其对于LTBI患者,结核再活动风险更高[4]。研究表明,TNF-α是肉芽肿形成及维持肉芽肿完整性的关键因素,TNF-α拮抗剂可通过诱导体内TNF-α水平的变化破坏肉芽肿的完整性[5]。TNF-α拮抗剂引起结核再活动的机制可能包括:(1)减弱巨噬细胞的抗结核分枝杆菌活性及抑制巨噬细胞凋亡;(2)改变CD4+T细胞的表型;(3)与效应CD8+T细胞亚群消耗有关,减弱其杀伤结核分枝杆菌的能力[6]。
使用不同种类的TNF-α拮抗剂发生活动性结核的风险不同。阿达木单克隆抗体(adalimumab,ADA)、英夫利西单克隆抗体(infliximab,IFX)的结核发病风险明显高于依那西普(etanercept,ETN)[7-9]。目前关于戈利木单克隆抗体(golimumab,GOL)和赛妥珠单克隆抗体(certolizumab pegol,CZP)的数据较少,有Meta分析显示这两种较新的抗TNF-α单克隆抗体并不增加结核发病风险[10-11]。使用不同TNF-α拮抗剂的结核发病风险需要更多研究和更长时间的随访观察加以明确。
2 应用肿瘤坏死因子-α拮抗剂患者潜伏结核感染的管理
2.1 筛查
LTBI是Mtb在体内的持留状态,其诊断缺乏金标准,目前主要依据结核菌素试验(tuberculin skin test,TST)或干扰素-γ释放试验(interferon-γ release assays,IGRAs)阳性,且无活动性结核的证据。由于结核流行情况、社会经济状况等存在差异,目前对于LTBI的筛查方法及标准(单用TST或单用IGRAs或联合TST和IGRAs)各国指南或共识并不一致[12]。2015年WHO发布的LTBI管理指南强烈推荐在应用TNF-α拮抗剂前应进行LTBI筛查,在高/中高收入、结核年发病率低于100/10万人的国家应用TST或IGRAs筛查LTBI,而在低/中等收入国家IGRAs不能代替TST作为LTBI的检测方法[2]。2013年我国结核病预防与管理专家组发表的《肿瘤坏死因子拮抗剂应用中结核病预防与管理专家共识》推荐:对于有条件的患者建议优先选择IGRAs作为LTBI的筛查方法,尤其对于结核病及非结核分枝杆菌感染的高发区人群、卡介苗接种者、曾接受过免疫抑制剂治疗的患者、合并糖尿病的患者以及TST硬结≥10 mm的患者,采用IGRAs筛查更为必要[13]。
由于接受TNF-α拮抗剂治疗的人群均为免疫抑制人群,应用TNF-α拮抗剂治疗前激素和/或免疫抑制剂的使用可能会影响TST和IGRAs筛查LTBI的阳性率[14]。因此,有研究推荐联合应用TST和IGRAs筛查LTBI以提高灵敏度[15],或在应用免疫抑制治疗前筛查LTBI[16-17],以免对TST和IGRAs的结果造成影响。
2.2 不同国家治疗相关指南或共识
一项关于应用TNF-α拮抗剂的类风湿关节炎患者LTBI治疗疗效的Meta分析显示,与未接受治疗的LTBI患者相比,接受治疗的LTBI患者发生活动性结核的风险降低了65%(RR=0.35,95% CI:0.15~0.82)[11]。Kisacik等[18]的多中心大样本病例对照研究发现,未抗结核治疗及抗结核治疗疗程不足是应用TNF-α拮抗剂的LTBI患者发生活动性结核的危险因素(OR=3.15,95% CI:1.43~6.9)。2015年WHO发布的LTBI管理指南肯定了LTBI治疗的有效性和重要性,并强烈推荐以下5种方案:异烟肼治疗6个月(6 INH)、异烟肼治疗9个月(9 INH)、异烟肼联合利福喷丁治疗3个月(3 INH+RFT)、异烟肼联合利福平治疗3~4个月(3~4 INH+RIF)、利福平治疗3~4个月(3~4 RIF)[2]。不同国家指南或共识采用的方案及抗结核治疗后开始TNF-α拮抗剂治疗的时间标准并不一致(表1),关于LTBI治疗后何时开始TNF-α拮抗剂治疗尚存争议[13,19-28]。
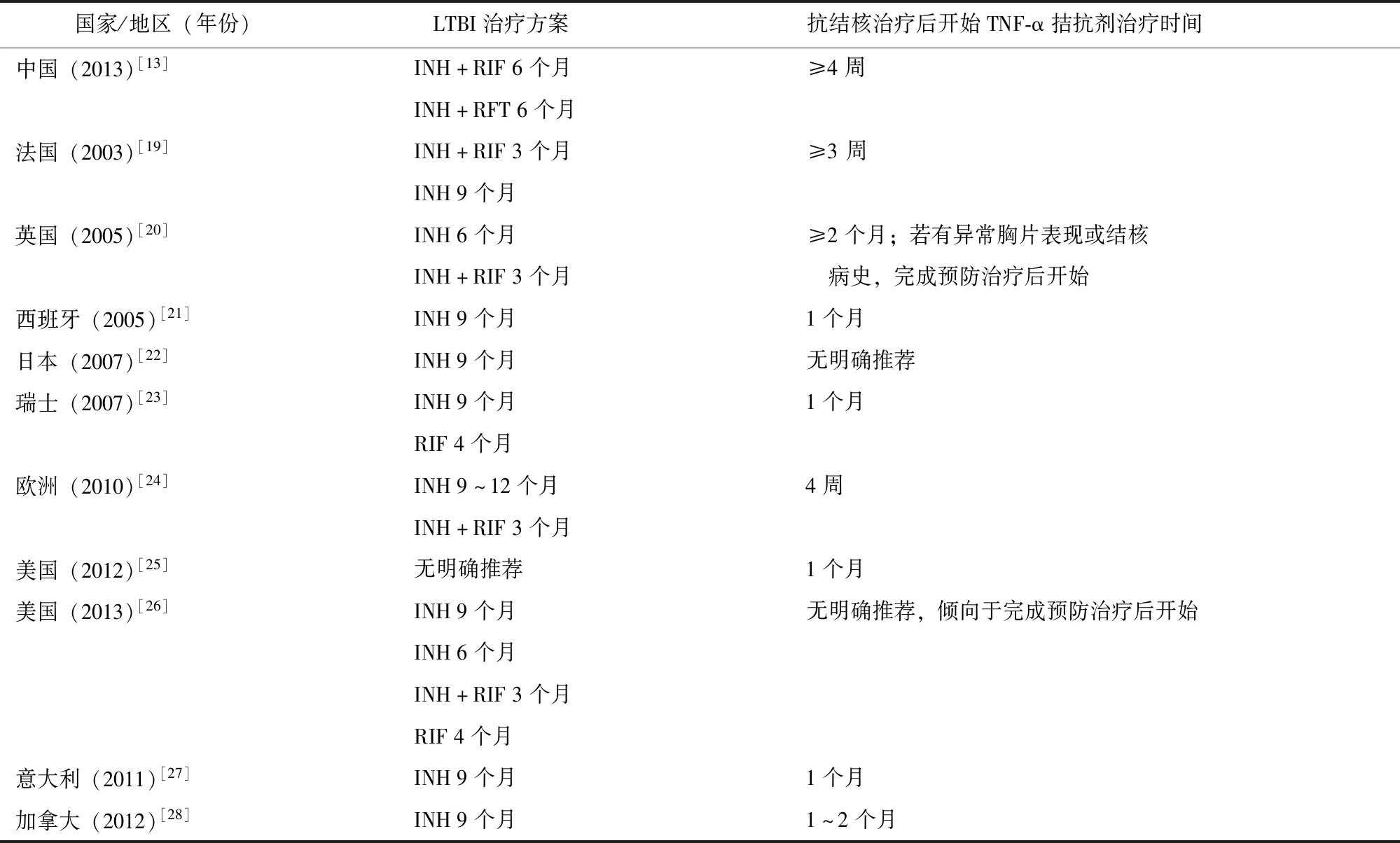
表1 应用TNF-α拮抗剂LTBI治疗方案指南或共识
2.3 疗效及安全性
2.3.1 异烟肼单药治疗方案
西班牙、日本、美国、意大利、加拿大指南或共识均将9 INH方案作为首选的LTBI治疗标准方案[21-22,27-28]。Gómez-Reino等[29]在应用TNF-α拮抗剂的LTBI人群中发现,未抗结核治疗组活动性结核发病率是9 INH方案组的7.09倍(95% CI:1.60~64.69)。Cagatay等[30]的回顾性研究中,583例应用TNF-α拮抗剂的LTBI或既往结核感染患者予以9 INH方案治疗,最终6例(1%)患者发生活动性结核,肝毒性事件发生率为5.3%。在一项更大样本量的回顾性研究中,5704例应用TNF-α拮抗剂的LTBI患者予以9 INH方案治疗,最终43例(0.7%)发生活动性结核,治疗完成率为92.7%[31]。
虽然9 INH方案疗效确切,但因疗程较长、治疗依从性较差导致其疗效并不理想[18,32]。因此,短程方案的疗效和安全性值得进一步探究。2005年英国胸科协会关于应用TNF-α拮抗剂结核感染的风险和管理意见[20]推荐6 INH作为LTBI治疗方案,该共识综合比较了6 INH、3 INH+RIF和利福平联合吡嗪酰胺治疗2个月(2 RIF+PZA)方案的安全性和依从性,认为6 INH方案肝毒性发生率最低且依从性较好。Nobre等[33]的回顾性研究纳入了157例应用TNF-α拮抗剂的患者,其中21例LTBI患者在应用TNF-α拮抗剂前给予6 INH方案,最终1例仅完成3个月治疗疗程的患者发生活动性结核。Gomes等[34]报道了54例接受TNF-α拮抗剂治疗的LTBI患者予以6 INH方案治疗后的随访情况,随访2年活动性结核的发生率为0,不良反应发生率为14.8%。
2.3.2 异烟肼联合利福平或利福喷丁治疗方案
2005年英国胸科协会关于应用TNF-α拮抗剂结核感染的风险和管理意见推荐3 INH+RIF为LTBI治疗方案,认为该方案可能因疗程短而有更好的依从性,且耐药性发生风险较低[20]。既往Sterling等[35]的大样本多中心随机非劣效试验在结核病高危人群中比较了3 INH+RFT方案和9 INH方案的疗效和安全性,发现2种方案疗效相当,而前者治疗完成率明显高于后者,肝毒性事件发生率明显低于后者。Tomsic等[36]在50例应用TNF-α拮抗剂的LTBI患者中给予3 INH+RIF治疗方案,最终2例患者发生活动性结核。Chang等[37]在37例应用TNF-α拮抗剂的LTBI患者中给予3 INH+RIF方案治疗,经过24.5个月的观察,无活动性结核发生。
2.3.3 利福平单药治疗方案
2007年瑞士专家组推荐9 INH和4 RIF作为应用TNF-α拮抗剂LTBI治疗方案,对于不能耐受异烟肼或对异烟肼耐药者可采用4 RIF方案[23]。2013年美国疾病预防与控制中心关于LTBI的管理指南亦推荐4 RIF方案用于不能耐受异烟肼或对异烟肼耐药的患者[25]。Laffitte等[38]的回顾性研究纳入了50例应用TNF-α拮抗剂治疗的银屑病患者,其中9例LTBI患者在应用TNF-α拮抗剂前予以4 RIF方案抗结核治疗,经中位随访时间64周后,1例患者发生活动性结核。
2.3.4 不同治疗方案的比较
2020年美国国家结核病控制协会和疾控中心发布的LTBI管理指南[39]指出,基于疗效肯定(疗效与9 INH方案相当或不劣于9 INH方案)、较低的不良反应发生率和较高的治疗完成率,推荐短程的3 INH+RFT、3 INH+RIF、4 RIF方案作为LTBI患者治疗的首选,异烟肼单药治疗方案(9 INH和6 INH)可作为替代。然而,该指南主要针对结核病发病率较低国家LTBI患者治疗方案的选择,且未涉及接受TNF-α拮抗剂的患者。2015年WHO发布的LTBI管理指南认为3 INH+RFT方案与9 INH、6 INH方案疗效相当,且3 INH+RFT方案的肝毒性事件发生率最低,但该结论是基于对所有结核病高危LTBI人群治疗方案数据的分析[2]。
与上述指南的部分结论类似,韩国Lee等[40]分析了246例使用TNF-α拮抗剂的LTBI患者结核病发生情况,9 INH方案组结核病发生率为5/219(2.3%),3 INH+RIF方案组结核发生率为0;9 INH方案组治疗完成率(84.9%)低于3 INH+RIF 9 INH方案组(96.3%),不良反应发生率(4.1%)高于3 INH+RIF方案组(3.7%)。韩国Park等[41]在408例应用TNF-α拮抗剂的LTBI患者研究中发现,结核病发生率9 INH方案组最高(3.3%),其次为 4 RIF 方案组(2.9%)和3 INH+RIF方案组(0);治疗完成率9 INH方案组(73.8%)最低,4 RIF方案组(87.1%)和3 INH+RIF方案组(94.2%)较高;3种方案总的不良反应发生率相当,肝毒性事件发生率9 INH方案组(9.8%)最高,3 INH+RIF方案组(2.9%)及4 RIF方案组(1.4%)较低。3 INH+RIF或3 INH+RFT方案或可能因疗效肯定、疗程短、依从性高、不良反应发生率较低,成为目前较为适宜的LTBI治疗方案。
目前在应用TNF-α拮抗剂的人群中直接对比不同方案的研究极少,且均为回顾性观察性研究,尚缺乏大样本的随机对照试验比较不同方案在该人群中的有效性和安全性。尽管上述几种LTBI治疗方案不良反应发生率偏低,临床上应用时仍应最大限度地注意抗结核药物的潜在不良反应。基础疾病状态或联合应用肝毒性免疫抑制剂如甲氨蝶呤、来氟米特等均可增加LTBI治疗期间肝毒性事件的发生率[42]。抗结核治疗药物潜在的肝毒性可能导致TNF-α拮抗剂有效性降低或治疗中断耽误病情,因此LTBI治疗期间肝毒性的定期监测尤为重要。此外,应用以利福霉素为基础的方案需注意药物之间的相互作用,包括华法林、口服避孕药、唑类抗真菌药等[43],利福喷丁的药物相互作用比利福平少,有限的临床数据表示当利福平禁用时,或可考虑3 INH+RFT方案[44]。
3 展望
中国是结核病负担最重的国家之一,在高危人群中对LTBI进行筛查和治疗对活动性结核的消除和控制具有重要意义。应用TNF-α拮抗剂是活动性结核发病的高危因素,在该人群中进行LTBI筛查和治疗可有效降低活动性结核的发病。目前,尚缺乏不同方案在该人群中的疗效和安全性评价数据。LTBI治疗方案的选择需综合考虑疗效、安全性、依从性及是否增加耐药风险等因素。短程的3 INH+RIF或3 INH+RFT方案或可成为LTBI治疗较为适宜的方案,然而仍需大样本随机对照试验进一步验证。在应用TNF-α拮抗剂的LTBI人群中开展不同治疗方案的比较研究具有重要意义,有助于医务工作者在循证医学研究的基础上选择最优和个体化的治疗方案。
利益冲突:无
