猪冠状病毒会给猪带来哪些影响
2021-01-27译自Vol362020
孟 霞 译自,Vol.36(2020),№4:6~9
潘雪男 校
如果2019年末就哪种病毒在世界上最知名进行一次调查,那么答案可能会是流感病毒或艾滋病病毒。然而,几个月后,世界上出现了一个新的头号病毒——新型冠状病毒(SARS-CoV-2)[引起新型冠状病毒肺炎(Covid-19)的病原体](图1)。对人和动物而言,冠状病毒并不是一种新的病原体,它们已经在自然界存在了很长的时间,与普通的病毒一样,它们通常会发生变异,并且可以不时地变换宿主。在新型冠状病毒出现之前,已知能够感染人类并影响人类健康的冠状病毒有6种,其中最常见的冠状病毒是引起中东呼吸综合征(Middle East Respiratory Syndrome,MERS)和严重急性呼吸综合征(SARS)的冠状病毒。它们和冠状病毒科的其他成员经常会导致人出现轻度或严重的呼吸道疾病。

图 1 新型冠状病毒模型
不仅人类可以感染冠状病毒,家畜和家禽也会感染其中一些冠状病毒,引起众所周知的疾病,如鸡传染性支气管炎或牛冠状病毒病。
1 能够感染猪的冠状病毒
目前,已知会感染猪的冠状病毒有6种,其中最出名的是感染猪胃肠道的病毒,如猪流行性腹泻病毒(Porcine Epidemic Diarrhoea Virus,PEDV)和传染性胃肠炎病 毒(Transmissible Gastroenteritis Virus,TGEV)。另一种会引起猪发生流行性腹泻(Porcine Epidemic Diarrhoea,PED)的病毒是δ-冠状病毒。2018年以来,相对较新的也会感染猪胃肠道的病毒是猪急性腹泻冠状病毒(Swine Acute Diarrhoea Coronavirus,SADS-CoV)。 可感染猪呼吸道的冠状病毒是猪呼吸道冠状病毒(Porcine Respiratory Coronavirus,PRCV)。最后但同样重要的冠状病毒是血凝性脑炎病毒(Haemagglutinating Encephalitis Virus,HEV,一种乙型冠状病毒),它会导致猪呕吐和消瘦。
2 冠状病毒简介
冠状病毒是一种有囊膜的单链正股RNA病毒。其包膜或外壳由蛋白质刺突组成,对消毒剂和热敏感,因而极易遭到破坏。这些刺突蛋白会与家畜或家禽细胞上的受体相互作用,从而侵入动物体内。
单链RNA病毒的繁殖很简单,在复制过程中可能会吸收其他病毒的RNA片段,或者错误复制时,通过缺失或点突变改变自身的RNA。这些变异的病毒可能无法繁殖,几乎不可能存活下来并感染其他动物,但有些病毒可能会完全或在新的位点定植在某个动物体内,少数病毒会引起疾病。冠状病毒可以从不同种类的动物中分离到,它们能使其中一些动物暴发可识别的疾病或不产生任何影响。蝙蝠能够携带多种冠状病毒,且不表现出明显的病理状况。
3 四种不同的冠状病毒
根据病毒的RNA序列和蛋白质组成,冠状病毒可分为四个不同的组:α-冠状病毒、β-冠状病毒、γ-冠状病毒和δ-冠状病毒。当两种冠状病毒感染同一宿主细胞时,它们的RNA可能会在入侵的细胞中结合并产生新的病毒。研究表明,TGEV和PEDV可以在感染猪的体细胞中重组,这些重组病毒能够从发生腹泻的猪体内分离到。
所有冠状病毒都可以感染动物的细胞,但如果这些细胞未因感染而受到损害或者在感染的细胞中只有很少一部分受到损伤,那么感染动物不会表现出临床症状,并且感染状态不明显。最新研究表明,血凝性脑炎病毒(HEV)和猪流行性腹泻病毒(PEDV)正在意大利的猪群中流行,但不引发临床症状。
3.1 猪呼吸道冠状病毒(PRCV)
3.1.1 PRCV致病机理
PRCV是一种与TGE密切相关的冠状病毒,在细胞培养基中能损伤和融合细胞,感染猪后通常会定植在肺部。当PRCV与其他病毒同时感染猪时,造成的肺部损害远比单独感染PRCV造成的严重。
3.1.2 PRCV的传播方式
PRCV可通过猪与猪的直接接触和气溶胶传播;一旦传入猪群,会在猪群中迅速扩散。猪场之间的传播通常由携带PRCV的猪完成。
3.1.3 临床症状
仔猪感染PRCV后,一些体内有母源抗体的猪会在3~5月龄时产生抗体,其他猪会出现咳嗽和食欲不振。体内无母源抗体的普通仔猪试验感染PRCV后1 d~5 d会出现食欲减退、不愿运动、呼吸困难和发热(40 ℃)等症状。
3.1.4 治疗和预防
目前,控制病毒感染的唯一标记是感染猪呈TGEV血清阳性,因此感染会妨碍对未流行TGE猪群的鉴定,这一问题可以通过严格的检测和隔离以建立和维持无抗体猪群来解决。这一经验证实,建立和维持未感染PRCV的猪群是可行的,但这种做法没有其他商业性价值。猪场应该采取与应对TGE相似的消毒措施。用于预防PRCV感染的试验性疫苗已经研发成功,但还没有上市销售。
3.2 血凝性脑炎病毒(HEV)
3.2.1 HEV致病机理
幼龄猪感染HEV后会呕吐和消瘦。与新型冠状病毒一样,HEV也是β-冠状病毒的成员。HEV在猪群中广泛存在,通过感染猪的呼吸传播到未感染猪的呼吸道。经口鼻感染后,猪会在3 d~5 d内出现临床症状。初乳中的母源抗体可保护仔猪长达15周。
3.2.2 传播方式
HEV会通过感染猪的鼻分泌物在整个猪群中传播。该病毒能够感染生长期后期的猪和育肥期早期的猪,且不会引起临床症状,感染非免疫母猪所产的仔猪后会引发临床症状。HEV似乎会通过病毒携带猪在猪群之间传播。
3.2.3 临床症状
5日龄至3周龄的仔猪感染后会出现临床症状。HEV会侵袭猪的神经,并会侵入大脑。仔猪感染后首先可见的症状是呕吐、扎堆,这可能与感染仔猪体温升高、抑郁、食欲不振和便秘有关。一些感染猪可能会出现脑脊髓炎症状,如后腿无力,或吞咽困难。仔猪感染后会在28 h~36 h内死亡,或逐渐消瘦。
3.2.4 治疗和预防
目前还没有疫苗可预防猪感染HEV。对未发生HEV感染的猪场进行预防可采取闭锁繁育法,或者从已知无该病的猪场引种。对于该病毒已经在猪群中流行的猪场,唯一有效的预防措施是确保仔猪获得初乳,消毒也能起到一定的预防作用。HEV不感染人,不会引发公共卫生问题。
3.3 猪流行性腹泻病毒(PEDV)
3.3.1 PEDV的致病机理
PEDV的一个经典血清型已在欧洲和亚洲的猪群中流行多年,但在最近10年,PEDV的多个变异基因型出现在中国的猪群中,并已传入美国和中美洲的猪群。哺乳仔猪感染PEDV后,会出现消化酶水平下降、肠道绒毛收缩、营养物质吸收减少,未消化的食物和液体进入大肠,引发腹泻。
3.3.2 传播方式
PEDV可以经口传播。由于感染猪发生水样腹泻,通过粪便排出的病毒可通过接触和气溶胶广泛分布于猪群中,并在猪舍中迅速传播。PEDV经冷冻后可以存活很长时间,并在中性环境中保持稳定。PEDV在猪场之间的传播通常由感染猪的移动引起,也可通过饲料传播。
3.3.3 临床症状
无免疫力的断奶猪或所有年龄段的猪感染PEDV后会以暴发性腹泻的形式发病。经过1 d~3 d的潜伏期后,感染仔猪会拉水样粪便,并可能会呕吐。猪场中几乎所有无免疫力的仔猪都会发病,幼龄仔猪感染后的死亡率接近100%,年龄较大的猪感染后20%~30%的猪会出现呕吐和腹泻,繁殖母猪感染后可能会出现食欲不振。
在部分免疫猪群中,哺乳仔猪和体重低于32 kg的幼龄断奶仔猪很少会感染。断奶仔猪感染后反应迟钝,不愿起身(图2),很少有发烧症状。急性期的呕吐和腹泻会持续3 d左右。
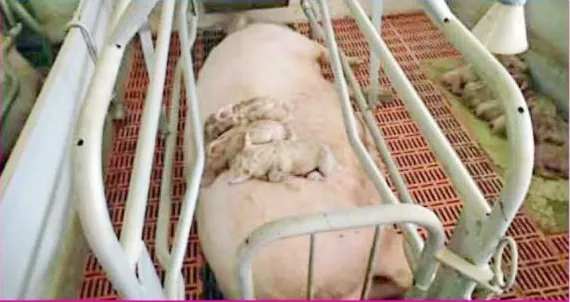
图 2 猪流行性腹泻的典型临床症状
3.3.4 治疗和预防
PED的治疗尚无特效药,感染猪只能接受支持性治疗。哺乳仔猪和刚断奶的仔猪应供给混合葡萄糖和甘氨酸的电解质溶液,并应提供足够数量的饮水器。隔离所有14 d内将要分娩的母猪和感染后14 d内将要产仔的母猪,能够减少该病暴发所产生的影响。一些国家已经推出用减毒活毒株、灭活病毒和病毒亚单位研制的疫苗,但那些用于预防传统PEDV感染的疫苗对PEDV的最新毒株无效。
3.4 传染性胃肠炎病毒(TGEV)
3.4.1 TGEV致病机理
猪传染性胃肠炎(Transmissible Gastroenteritis,TGE)由一种会损坏宿主细胞的冠状病毒引起。TGEV能在猪小肠内衬细胞中繁殖,使成熟的吸收性细胞死亡,导致肠绒毛缩短和肠道消化力下降。由TGEV引发的渗透性腹泻会导致仔猪死于脱水。免疫母猪初乳和常乳中的特异性IgA抗体可保护仔猪免受感染。
3.4.2 传播方式
感染猪粪便中的病毒可经口感染健康猪。由于发病猪的腹泻量大且多水,TGEV通过猪与粪便的接触和空气流动在猪群中广泛分布,并迅速在猪舍内传播。冷冻后TGEV可以存活很长一段时间,且在中性条件下可保持稳定。TGEV在猪场之间的传播通常是通过感染猪的移动来实现,但也有通过运输车辆、衣服和空气进行传播的记录。
3.4.3 临床病状
TGE始于猪暴发性发生腹泻。在未免疫的猪群中,所有年龄段的猪在几天内都会发病,排黄绿色的水样粪便,3周龄内的仔猪可能会出现呕吐。感染猪脱水,24 h~48 h内死亡。易感仔猪出生后3 d~4 d内即发病。在无饮水可饮用的非免疫猪群中,仔猪在第0天至第7天的死亡率为100%,3周龄或更大年龄段的仔猪很少死亡。在TGE呈地方性流行的地区,10日龄至6周龄的猪感染后会出现腹泻和生长受阻,育肥猪感染后可能仅仅表现为生长缓慢。
3.4.4 治疗和预防
TGE尚无有效的治疗方法,可以用电解质溶液维护发病猪。早期断奶、提高猪舍温度和保持卫生都有助于降低发病猪的死亡率,哺乳仔猪用免疫母猪寄养也有利于降低死亡率。断奶仔猪应供给饮水。要防止TGEV传入猪场,可采取隔离、禁止访客或卡车进入、严格执行淋浴或浸水等措施。某些国家或地区已经生产出基于TGEV的减毒株、灭活病毒和病毒亚单位的疫苗,这些疫苗可以单独使用,也可以与PED疫苗一起使用。
4 抗冠状病毒的疫苗
如果冠状病毒已经在动物群中存在很长时间,那么我们从以前的疫苗使用中能获得怎样的经验。这些疫苗肯定是相关人员为防止动物感染冠状病毒研制的,并已用于控制鸡传染性支气管炎、牛冠状病毒(一种类似新型冠状病毒和猪HEV的β-冠状病毒)病以及猪传染性胃肠炎(TGE)和猪流行性腹泻(PED)。有效的疫苗包括减毒活病毒(它们能在宿主中繁殖但不会引发疾病,同时能让动物产生免疫力)、全病毒灭活疫苗以及由病毒片段或单个蛋白质或编码蛋白质的基因制成的疫苗。针对任何一种病毒实际使用的疫苗取决于疫苗的免疫效力、使用的便利性、成本和疾病的重要性(尚未尝试为了预防猪呼吸道冠状病毒感染进行免疫接种)。
抗冠状病毒的疫苗可以预防疾病的发生,但是灭活疫苗和亚单位或RNA疫苗可能无法充分刺激动物产生获得彻底保护所必需的肠道或呼吸道的局部免疫应答反应,这种保护力只能由合适的减毒疫苗提供。当病毒出现突变株时,如鸡传染性支气管炎,以及在接种疫苗时动物体内存在母源抗体时,给动物接种疫苗以预防感染可能会失败。几乎没有疫苗可以消除所有相对应的冠状病毒或预防亚临床感染的发生。
5 猪不易感染新型冠状病毒
猪对冠状病毒的新成员并不敏感。至少有两个不同的研究小组测试了不同种类的动物对该病毒的敏感性。德国联邦动物卫生研究院弗里德里希·勒夫勒研究所(Friedrich-Loeffler-Institut,FLI)率先报道了猪和鸡不易感染新型冠状病毒,而蝙蝠和雪貂易感染。
FLI的相关研究人员检查了动物是否会感染新型冠状病毒,该病原体是否可以在动物体内复制以及动物是否会出现临床症状。他们还测试了动物是否会排泄该冠状病毒,从而是否会对人类健康构成潜在风险。在试验条件下,猪和鸡都不易感染新型冠状病毒。在该感染研究中,研究人员通过鼻腔给动物接种新型冠状病毒,模仿人通过鼻咽发生自然感染的途径。
在中国进行的试验也显示了类似的结果。《科学》杂志发表了来自中国农业科学院哈尔滨兽医研究所、中国疾病预防控制中心病毒病预防控制所以及国家动物疫病防控高级别生物安全实验室的21位研究人员的研究报告。该研究小组测试了各种动物对新型冠状病毒的敏感性,他们得出的结论是新型冠状病毒在狗、猪、鸡和鸭体内的复制能力很差。
