基于烟雾箱模拟的己烯醇与O3气相反应的动力学研究
2021-01-26陈梅芳佟胜睿李伟然张欣然葛茂发
王 振, 陈梅芳, 佟胜睿, 陈 怡, 李伟然, 张欣然, 葛茂发,3*
1.中国科学院化学研究所, 分子动态与稳态结构国家重点实验室, 北京分子科学国家实验室, 北京 100190 2.中国科学院大学, 北京 100049 3.中国科学院城市环境研究所区域大气环境卓越研究中心, 福建 厦门 361021 4.安徽师范大学化学与材料科学学院, 安徽 芜湖 241000
O3是影响大气氧化性最重要的物种之一,可以与大气中多种痕量气体发生反应,促进大气中新颗粒物的生成,严重影响空气质量、太阳辐射、气候变化、生态平衡和人体健康等[1-4]. O3来源广泛,近年来呈现出O3浓度逐年升高的趋势,O3污染成为灰霾问题改善之后的又一大气环境问题,在人类聚集地区其浓度增加明显,模型预测发现,在未来相当长的一段时间内O3浓度均未出现下降趋势[5-6]. 因此,O3参与的反应将越发重要起来,其中O3与挥发性不饱和有机物的反应是其损耗的重要途径之一,如烯烃、卤代烯烃、生物挥发性有机物(Biogenic Volatile Organic Compounds,BVOCs)等[7-10]. BVOCs来源也十分广泛,种类繁多,除已知的单萜烯类和倍半萜烯类等物质外,还有一些树木、蔬果、花草等植物释放出来带有清香气味的有机物,如各种含氧生物挥发性有机物(含有多碳的醇、醛、酮和脂类). 这些含氧挥发性有机物对大气中挥发性有机物(Volatile Organic Compounds,VOCs)含量的贡献很大,在城市地区甚至超过人为源排放的VOCs含量[9,11]. 已有报道[9,11-13]发现,己烯醇等由绿叶植物释放的挥发性有机物在城区大量存在;随着各种外部机械损伤、温度剧烈变化、干旱、虫害、高浓度O3等刺激,植物的应激反应会排放大量的己烯醇以应对环境变化. 大部分己烯醇分为顺反两种构型,植物会同时释放两种构型的己烯醇,但通常顺式结构的己烯醇会在植物受到损伤性刺激时释放得更多. Z-2-己烯-1-醇、E-2-己烯-1-醇、Z-4-己烯-1-醇和E-4-己烯-1-醇已经被证实在蔬果和绿叶植物排放的挥发性有机物中是重要的生物挥发性有机物[14]. 随着近年来提倡退耕还林以及增加城市绿化面积政策的实施,这些由植物排放出来的环绕在人们身边的己烯醇也在悄然增长[9,11,15]. 同时,由于己烯醇还具有清香气味[16],常作为化工溶剂或原料参与化工生产,从而由人为源途径进入到大气中[17]. 5-己烯-1-醇因其特殊的结构而被用到高分子材料的制备当中,常以人为源方式进入到大气中[17-18].

所以,为了能更好地理解己烯醇与O3的反应活性,笔者拟采用烟雾箱系统和准一级反应速率法获得O3与Z-2-己烯-1-醇、E-2-己烯-1-醇、Z-4-己烯-1-醇、E-4-己烯-1-醇、5-己烯-1-醇的动力学常数,并通过试验结果和理论计算对其进行分析,通过大气O3平均浓度计算各种己烯醇的大气寿命. 理论计算基于反应涉及的相关结构计算热力学量,通过对比不同反应的热力学量推测试验速率常数的相对大小关系,不仅验证了试验结果,而且对其他试验数据的预测具有指导意义.
1 材料与方法
1.1 试验条件
动力学试验是在烟雾箱中,以100 L的特氟龙薄膜袋作为反应器,在室温〔(298±1)K〕、常压(101 325 Pa)条件下进行反应. 烟雾箱系统已经发展较为成熟,在此系统中已进行大量试验研究[28-30],且该试验仅使用其简单功能,因此不再赘述. 在进行试验之前,特氟龙薄膜袋使用高浓度O3钝化24 h. 零空气的生成是通过零空气发生器(AADCO 737 series, 美国)处理室外空气产生. 试验过程中的气体体积全程由质量流量控制器(D08-8CZM, 北京七星华创流量计有限公司)所控制. 不饱和己烯醇与环己烷的注入,是将有机物注入到一个U型玻璃三通管中,通过注入零空气时带入反应器中,必要时可以加热U型玻璃三通管. 反应器中环己烷(cyclohexane)的注入是为了消除因CC 与O3反应产生的OH自由基,避免影响试验精度[31-33].
1.2 动力学试验
使用绝对速率法来获得O3与Z-2-己烯-1-醇、E-2-己烯-1-醇、Z-4-己烯-1-醇、E-4-己烯-1-醇、5-己烯-1-醇的动力学参数. 绝对速率法详见文献[28,30],在此仅做简短介绍. 全部试验均在100 L的特氟龙薄膜袋中进行. 反应过程中由于初始己烯醇浓度较高,所以O3与己烯醇的反应可以近似遵循准一级反应.
(1)
(2)
(3)
式中,M为反应器壁,t为反应时间,kwall为O3壁损失的反应速率常数,Pr为产物,A为己烯醇,k1为O3与己烯醇的反应速率常数,[O3]为O3浓度,[A]0为己烯醇初始浓度.
在反应过程中,O3除了与己烯醇反应之外,还有一部分因吸附在反应器壁上造成损失,其反应速率常数分别为k1和kwall,如式(1)(2)所示. 若在固定己烯醇浓度条件下,O3的损失速率k1[A]0远大于O3壁损失的反应速率kwall,则可以忽略反应过程中由于壁吸附带来的O3浓度损失. 当己烯醇初始浓度远大于O3初始浓度时,如[A]0[O3]=20∶1,则即使O3反应完全,也会有95%的己烯醇留存在体系当中,因此,在这种条件下,反应动力学过程可以作为准一级反应动力学研究,即式(3)可以简化为
(4)
式中,-d ln[O3]dt为O3浓度的时间变化率.
在己烯醇与O3反应过程中,只需要对O3浓度进行检测,通过式(4)得到O3浓度随时间变化的函数图,拟合直线的斜率即为k1与己烯醇初始浓度的乘积;然后选定数个不同初始浓度,在各初始浓度条件下得到准一级反应速率常数,通过准一级反应速率常数与各初始浓度的函数拟合,即可得到各种己烯醇与O3的反应速率常数.
试验过程中Z-2-己烯-1-醇、E-2-己烯-1-醇、Z-4-己烯-1-醇、E-4-己烯-1-醇、5-己烯-1-醇的初始浓度分别为3.83×1013~7.66×1013、3.97×1013~7.94×1013、4.00×1013~8.00×1013、3.97×1013~7.94×1013、4.15×1013~10.38×1013moleculecm3. O3浓度为2.7×1012~5.3×1012moleculecm3. 环己烷的浓度为1.39×1015moleculecm3.
1.3 理论计算
1.4 药品
E-2-己烯-1-醇(trans-2-hexen-1-ol, 97%, Alfa Aesar)、Z-2-己烯-1-醇(cis-2-hexen-1-ol, 94%, Alfa Aesar)、E-4-己烯-1-醇(trans-4-hexen-1-ol, 97%, Alfa Aesar)、Z-4-己烯-1-醇(cis-2-hexen-1-ol, 94%, Alfa Aesar)、5-己烯-1-醇(5-hexen-1-ol, 99%, Acros)和环己烷(cyclohexane, 99.5%, Acros)均购自商业试剂公司,使用前未经过再次纯化.
高纯O2(浓度>99.995%,北京泰龙电子技术有限公司)通过特斯拉线圈放电流动产生O3,试验中取适量的O3注入到反应容器中混匀,通过O3分析仪(Model 49i, Thermo Electron Corporation, UV Photometric Technology,美国)持续检测O3浓度.
2 结果与讨论
2.1 O3的壁损失
该试验是向特氟龙反应器中充入与试验条件相似的O3浓度,然后记录10 h内O3浓度的变化. O3的壁损失反应速率曲线(见图1)显示,O3壁损失浓度与时间呈一次函数关系,可以得到O3的壁损失是一级反应,壁损失速率为2.36×10-6s-1,该数值与文献[30]报道的结果相吻合,且远小于在固定己烯醇初始浓度条件下O3的消耗速率(见表1). 由此可见,钝化后的反应器内,O3的壁损失与准一级反应速率常数相比可以忽略不计.

注:[O3]0为O3的初始浓度,[O3]t为O3在相应时间的实时浓度. 图1 O3壁损失曲线Fig.1 The wall loss of O3
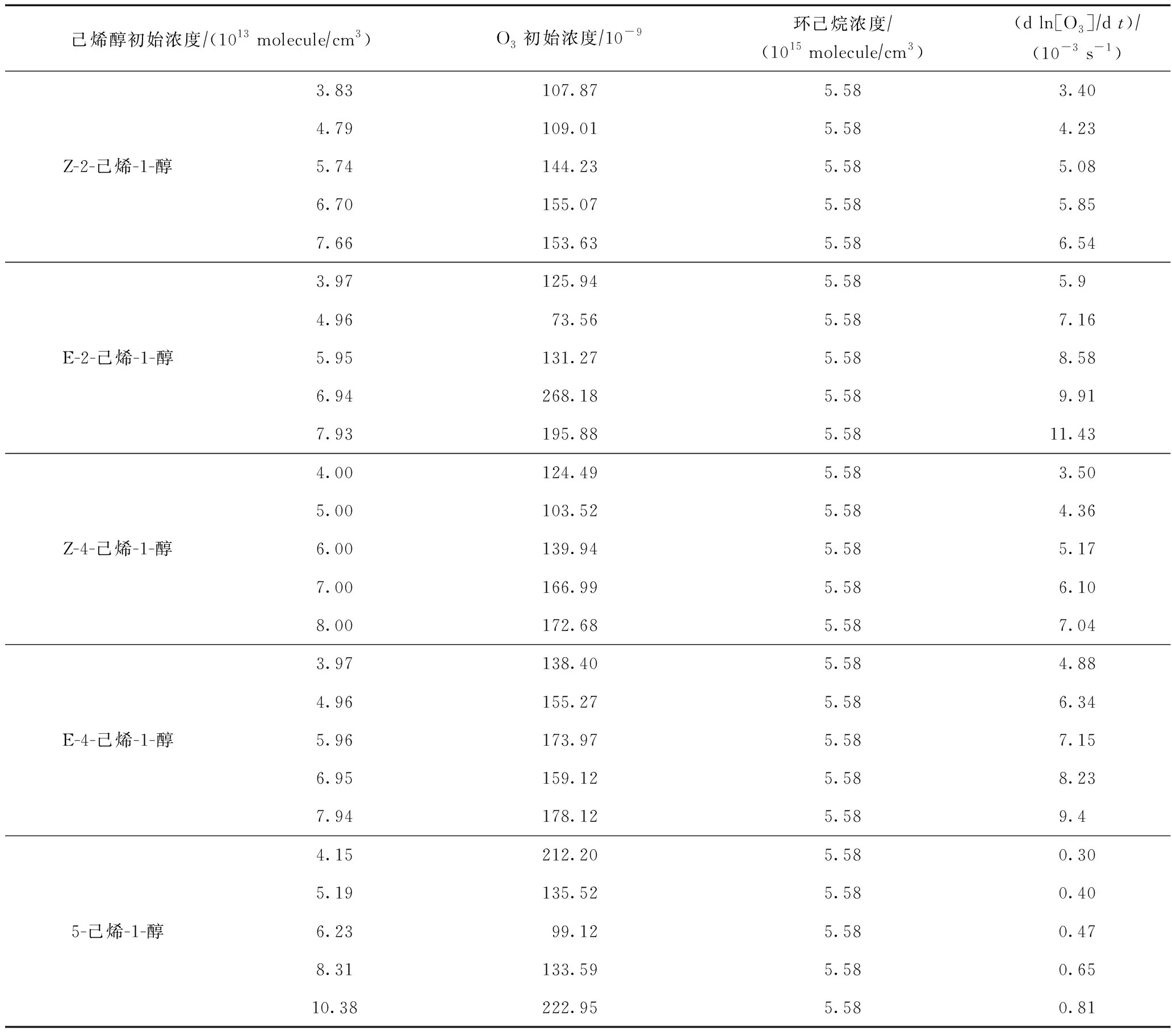
表1 己烯醇与O3反应的试验条件与结果
2.2 己烯醇的反应动力学常数
每种己烯醇均在5种初始浓度条件下进行试验,取得相应的准一级反应速率常数. 每次试验信息见表1. 不同初始浓度条件下,O3浓度的变化与时间均呈函数变化关系,且根据式(4),O3浓度的衰减速率(-d ln[O3]dt)由ln[O3]0[O3]t与时间t的斜率决定,拟合直线斜率值见表1,拟合曲线见图2.
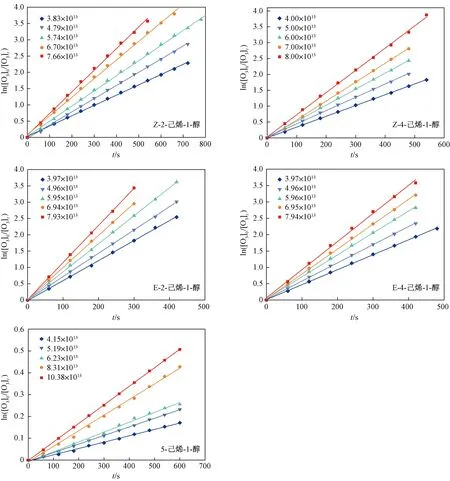
注: [O3]0为O3的初始浓度;[O3]t为O3在相应时间t时的实时浓度;图中各浓度单位均为moleculecm3. 图2 不同浓度条件下5种己烯醇与O3反应的试验结果Fig.2 Results of O3 reaction with 5 hexen-ols at different initial concentrations
由图2可见,Z-2-己烯-1-醇、Z-4-己烯-1-醇、E-2-己烯-1-醇、E-4-己烯-1-醇和5-己烯-1-醇在各浓度下[O3]的衰减(ln[O3]0[O3]t)与时间t的线性函数关系非常好,均可达到R2>0.99,且截距接近于0,说明反应过程中的二次反应可以忽略. 将不同初始浓度己烯醇与O3反应得到的-d ln[O3]dt与初始浓度做衰减函数图像(见图3),其一次拟合斜率即为反应速率常数(k1),各种己烯醇与O3的反应速率常数如下:
kE-2-己烯-1-醇= (13.95×10-17±0.48×10-17)cm3(molecule·s)
kZ-2-己烯-1-醇=(8.94×10-17±0.8×10-17)cm3(molecule·s)
kE-4-己烯-1-醇=(10.01×10-17±1.03×10-17)cm3(molecule·s)
kZ-4-己烯-1-醇=(8.82×10-17±0.31×10-17)cm3(molecule·s)
k5-己烯-1-醇=(0.82×10-17±0.04×10-17)cm3(molecule·s)
反应速率常数的误差为最小二乘法所得标准偏差的2倍.

图3 不同浓度条件下O3的衰减速率(-d ln[O3]d t)与5种己烯醇的衰减函数拟合结果Fig.3 Plots of the decay rate coefficient of O3 (-d ln[O3]/d t) and 5 hexen-ols at different concentrations
在对己烯醇的一系列相关研究中,GAI等[21]使用烟雾箱分析了己烯醇的臭氧化反应速率,得到E-2-己烯-1-醇和E-4-己烯-1-醇的反应速率分别为(16.6×10-17±2.2×10-17)和(10.5×10-17±1.4×10-17)cm3(molecule·s),与笔者得到的结果〔(13.95×10-17±0.48×10-17)和(10.01×10-17±1.03×10-17)cm3(molecule·s)〕十分吻合,说明试验数据可靠.
试验结果表明,E-己烯-1-醇与O3的反应速率高于Z-己烯-1-醇,E-2-己烯-1-醇与O3的反应速率〔(13.95×10-17±0.48×10-17)cm3(molecule·s)〕高于E-4-己烯-1-醇与O3的反应速率常数〔(10.01×10-17±1.03×10-17)cm3(molecule·s)〕;Z-2-己烯-1-醇与O3的反应速率常数〔(8.94×10-17±0.80×10-17)cm3(molecule·s)〕比Z-4-己烯-1-醇的反应速率常数〔(8.82×10-17±0.31×10-17)cm3(molecule·s)〕稍大一些,由此可见,相同的构型中k2-己烯-1-醇>k4-己烯-1-醇. 如表2所示,在结构上,Z-2-己烯-1-醇和Z-4-己烯-1-醇是由母体烯烃Z-2-己烯分别在两端加一个羟基构成的,E-2-己烯-1-醇和E-4-己烯-1-醇则是由母体烯烃E-2-己烯分别在两端加上一个羟基所构成的. 从各己烯醇与O3的反应速率常数上看,E-2-己烯的反应速率常数〔(15.5×10-17±0.06×10-17)cm3(molecule·s)〕高于Z-2-己烯〔(10.9×10-17±0.04×10-17)×10-17cm3(molecule·s)〕,与不同构型己烯醇的反应速率变化趋势保持一致,说明构型是影响己烯醇与O3反应速率常数的重要因素[36]. 在母体烯烃上增加了羟基之后,与顺式己烯醇相比,反式结构己烯醇与O3的反应速率常数所受到的影响相对较小. 已有研究表明,1-己烯与O3的反应速率常数为0.88×10-17~1.21×10-17cm3(molecule·s)[7,36],远小于Z-2-己烯、E-2-己烯与O3的反应速率常数,总体展现出kE-2-己烯>kZ-2-己烯>k1-己烯的趋势,笔者得到的5-己烯-1-醇与O3的反应速率常数为(0.82×10-17±0.04×10-17)cm3(molecule·s),在趋势上同样远小于另外4种由2-己烯衍生出来的己烯醇的反应速率常数,与母体烯烃和O3的反应速率常数相对关系一致. 己烯醇中出现的这种特殊现象,在戊烯醇与O3的反应速率常数测定中也有所发现,如E-2-戊烯-1-醇与O3的反应速率常数高达(169×10-18±25×10-18)cm3(molecule·s)[37]. 然而,对于双键在一端的4-戊烯-1-醇,其与O3的反应速率常数仅为 (7.68×10-18±1.36×10-18)cm3(molecule·s)[29],与该研究体系中的物质在构型及其与O3的反应活性变化趋势是一致的[37]. 己烯醇和O3的反应活性与本体烯烃和O3的反应活性变化趋势一致,但是受羟基的影响,己烯醇与O3的反应速率常数总体上略小于母体烯烃与O3的反应速率常数[28,30].
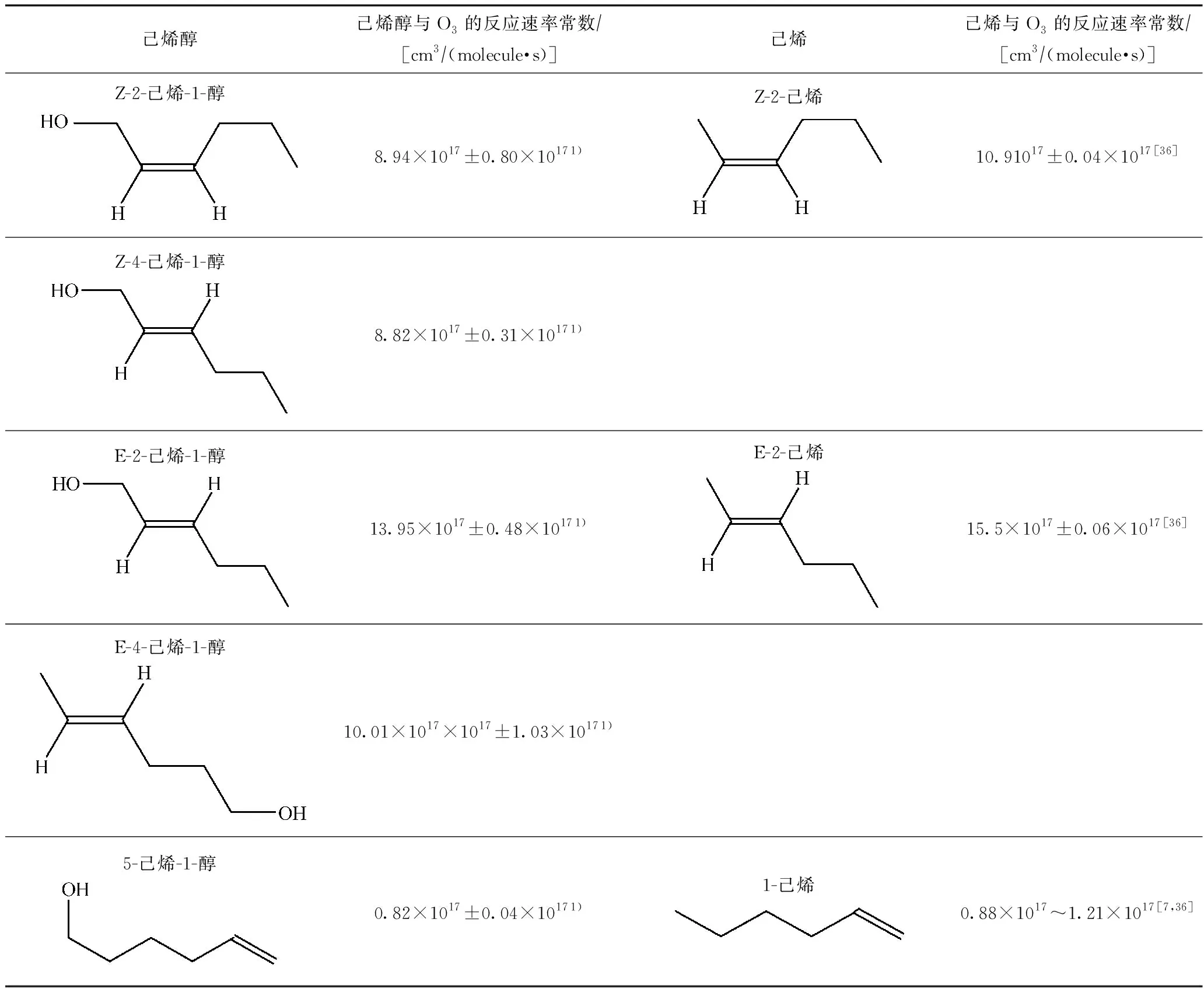
表2 己烯醇和己烯与O3的反应速率常数对比
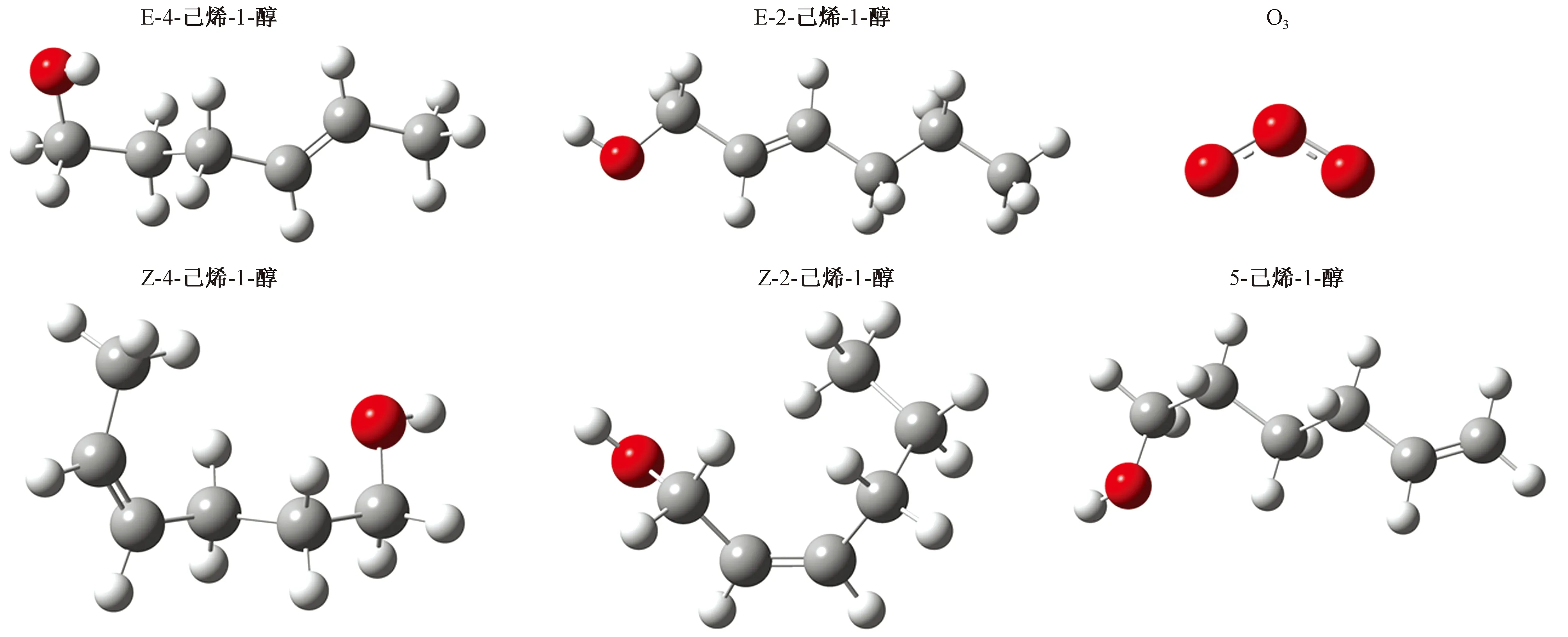
图4 使用M06-2X6-311+G(2d,p)对5种己烯醇和O3进行结构优化的结果Fig.4 The optimization geometries of 5 hexen-ols and O3 with M06-2X/6-311+G(2d,p) level of theory
2.3 热力学理论计算结果

5种己烯醇与O3的构型优化结果见图4. 由于O3可以从两个方向进攻己烯醇,所以每种己烯醇与O3形成的预反应复合物(Prereactive-Complexes,PCs)——过渡态(Transition States, TSs)和POZs均有两种构型[42],分别在M06-2X6-311+G(2d,p)基组上进行结构优化,优化结果见图5~7. 对优化后的结构在M06-2Xdef2-TZVP基组上进行单点能计算,得到各分子的能量,过渡态和反应物之间的能量差即为该反应步的能垒. 由图8可见,每种己烯醇被O3从不同方向进攻形成的各种反应物(例如:预反应复合物、反应中间体和POZs等)的能量相差极小,因此只取O3从正面进攻己烯醇过程中的分子构型进行讨论.

图5 使用M06-2X6-311+G(2d,p)对5种己烯醇和O3形成的10种预反应复合物进行结构优化结果Fig.5 The optimization geometries of 10 pre-reaction complexes from 5 hexen-ols and O3 with M06-2X/6-311+G(2d,p) level of theory
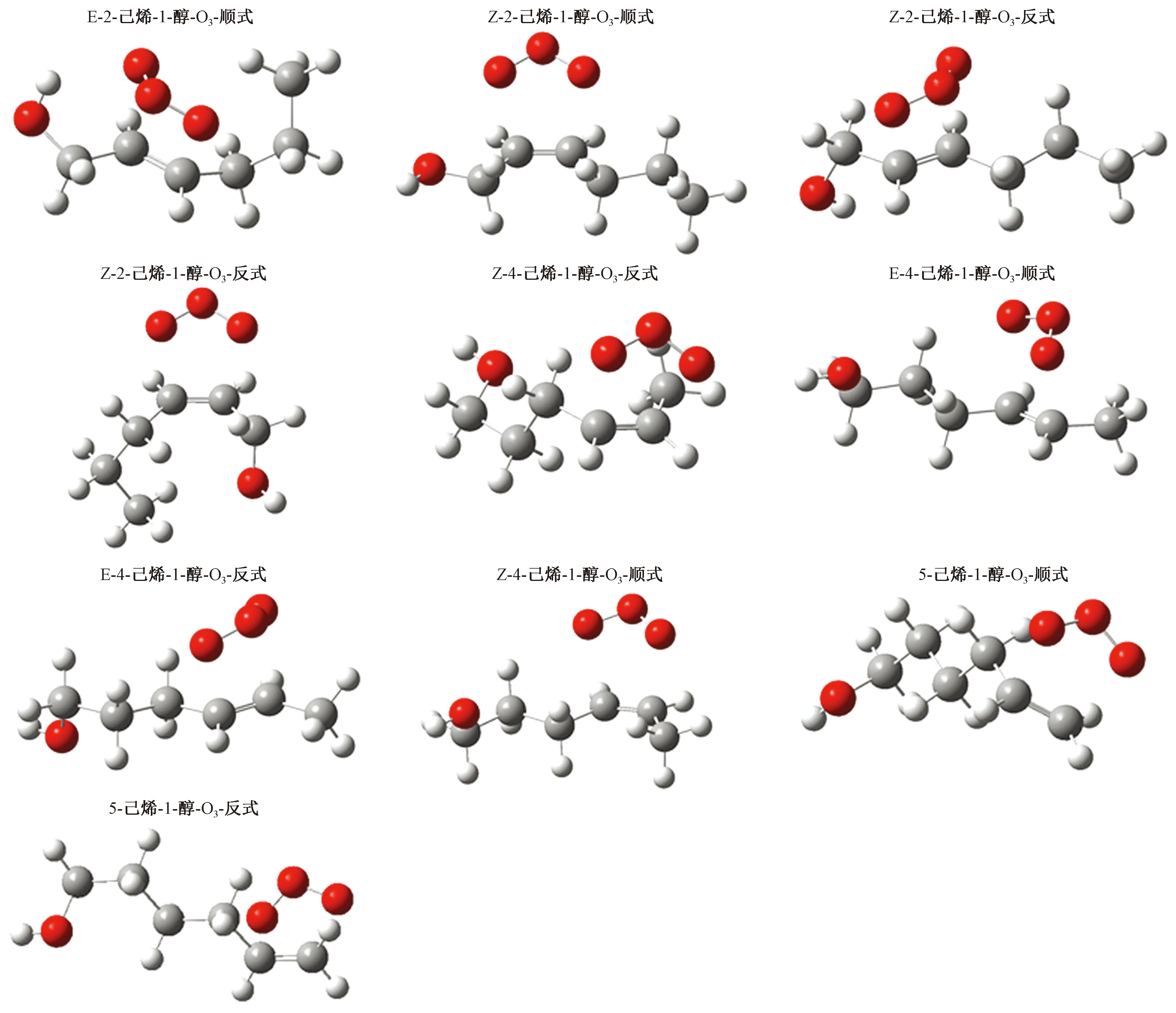
图6 使用M06-2X6-311+G(2d,p)对5种己烯醇和O3反应形成的10种过渡态分子进行结构优化结果Fig.6 The optimization geometries of 10 TSs from 5 hexen-ols and O3 with M06-2X/6-311+G(2d,p) level of theory
图7 使用M06-2X6-311+G(2d,p)对5种己烯醇和O3反应形成的10种POZ进行结构优化结果Fig.7 The optimization geometries of 10 POZs from 5 hexen-ols and O3 with M06-2X/6-311+G(2d,p) level of theory

注: R、CP、TS、P分别代表反应过程中的反应物、预反应复合物、过渡态、POZ;ΔE为不同状态间的能垒变化;红色折线代表O3从己烯醇正面进攻的反应路径,黑色折线代表O3从己烯醇背面进攻的反应路径.图8 五种己烯醇和O3反应决速步的势能折线图(在M06-2Xdef2-TZVP水平条件下计算)Fig.8 Schematic potential energy surface for the reactions of 5 hexen-ols with O3 with M06-2X/def2-TZVP level of theory
图8展示了5种己烯醇与O3反应的反应势能面,从数值上可以看出,E-2-己烯-1-醇与O3的反应能垒最低,与其反应速率常数最大的结果相一致. 5-己烯-1-醇与O3的反应能垒最高,也对应了其与O3的反应速率在5种己烯醇中为最小的试验结果. Z-2-己烯-1-醇、Z-4-己烯-1-醇、E-4-己烯-1-醇与O3的反应能垒则十分相近,难以明显地分辨出哪种己烯醇与O3的反应活性较高,与试验结果的变化趋势相一致. 由此可见,理论计算能较为准确地预测和判断己烯醇与O3的反应速率变化趋势,但是并不能明显分辨出热力学数据差异较小反应的反应速率常数. 从反应物到POZ的形成过程中,E-2-己烯-1-醇与O3反应放出的能量高达80.3 kcalmol,远高于其他4种己烯醇,表明产物POZ更加稳定,也更利于反应的进行;其他4种己烯醇与O3反应生成POZ的过程中也会放出超过70 kcalmol的能量,足以支持后续反应的顺利进行.

2.4 大气意义
在大气中烯醇的主要去除途径是与对流层中的氧化剂(如O3、OH自由基、NO3自由基等)发生反应. 大气寿命可以较好地评估各种大气氧化剂对烯醇的去除效果,在动力学试验基础之上,可以通过各种己烯醇与O3的反应速率常数和式(5)得到相应己烯醇的大气寿命.
τ=1k[X]
(5)
式中:τ为己烯醇的大气寿命,s;k为己烯醇的反应速率常数,cm3(molecule·s);[X]为典型大气氧化剂的浓度,moleculecm3.
已有研究中关于己烯醇与OH自由基、NO3自由基的反应速率常数以及各种己烯醇相应的大气寿命如表4所示. 由表4可见,除5-己烯-1-醇之外,其余几种己烯醇与O3反应的大气寿命均在2~3 h之间,OH自由基与各种己烯醇反应的大气寿命也为2 h左右,二者不相上下;相比于NO3降解各种己烯醇的反应而言,O3对己烯醇的清除效果稍强一些. 在一些光化学污染区域,由于O3的浓度能够达到4.75×1012moleculecm3,导致各种己烯醇的大气寿命大幅缩短,其去除己烯醇的效果甚至远超过强氧化剂OH自由基[45]. 因此,在大部分地区,己烯醇的去除途径可能是OH自由基、NO3自由基、O3氧化的竞争反应,但是在光化学污染严重的地区,则由O3反应所主导.
与不饱和有机物类似,不饱和醇与O3反应时会产生羰基化合物和Criegee自由基,Criegee自由基可以通过自分解反应产生OH自由基,或与其他无机痕量气体VOC反应形成有机大分子,有机大分子挥发性较低,易凝聚成核形成新的颗粒物. 同时,近年来由于颗粒物治理方案显示出了卓著成效,颗粒物浓度逐年下降,但是O3浓度逐年升高,且与有机物反应形成大分子氧化产物后,会促进有机物从气相向颗粒相转化,所以大气中O3和颗粒物污染并不是一个能够简单解决的问题,对于O3和颗粒物的协同控制研究还需要广大科研人员的共同努力.

表4 己烯醇与OH自由基、NO3自由基和O3的反应速率常数及其大气寿命
3 结论
a) 在烟雾箱中,使用绝对速率法测定得到5种己烯醇与O3的反应速率常数(298 K,101 325 Pa):kE-2-己烯-1-醇=(13.95×10-17±0.48×10-17)cm3(molecule·s),kZ-2-己烯-1-醇=(8.94×10-17±0.8×10-17)cm3(molecule·s),kE-4-己烯-1-醇=(10.01×10-17±1.03×10-17)cm3(molecule·s),kZ-4-己烯-1-醇=(8.82×10-17±0.31×10-17)cm3(molecule·s); 并首次得到了5-己烯-1-醇与O3的反应动力学常数,k5-己烯-1-醇=(0.82×10-17±0.04×10-17)cm3(molecule·s).

c) 反应动力学研究发现,试验结果符合反应热力学理论计算结果的趋势,因此在实际应用过程中,反应热力学理论的计算结果可以指导试验动力学数据的研究.
d) O3对5种己烯醇(Z-2-己烯-1-醇、E-2-己烯-1-醇、Z-4-己烯-1-醇、E-4-己烯-1-醇和5-己烯-1-醇)的清除具有重要意义,在光化学污染严重的地区可以主导5种烯烃的去除.
