星状神经节阻滞联合芬太尼对妇科恶性肿瘤患者术后镇痛及免疫应激反应的影响
2021-01-22唐作垒高志勇罗红李雨纱唐莉杨涛
唐作垒 高志勇 罗红 李雨纱 唐莉 杨涛
恶性肿瘤手术治疗所带来的创伤会引发患者不同程度的应激反应。过度的应激反应会使患者发生内环境及机体代谢紊乱,严重者甚至导致机体产生免疫抑制,增加术后肿瘤复发、扩散及发生并发症的风险[1-3]。故围术期应激反应的适度调控有利于恶性肿瘤患者的术后康复。目前研究较多的是应用不同的镇痛药物控制术后疼痛来减少应激反应。但术后应激反应不单单是疼痛所导致的,因此既往仅依靠控制疼痛来调控免疫功能,其结果不尽如人意。研究发现,星状神经节阻滞可调节免疫应激反应[4-6]。本研究旨在观察超声引导下星状神经节阻滞联合芬太尼对妇科恶性肿瘤患者术后镇痛及免疫应激反应的影响,探讨其可行性及安全性,现报道如下。
1 对象和方法
1.1 对象 选取2018年6月至2019年12月在本院行手术治疗的妇科恶性肿瘤患者60例,纳入标准:(1)符合妇科恶性肿瘤根治术手术适应证的患者;(2)年龄 18~75岁,ASA 分级Ⅱ~Ⅲ级。排除标准:(1)合并严重的心血管、脑血管、肝、肾、造血系统等原发性疾病或全身衰竭者,糖尿病、精神病、结缔组织病、血友病有出血倾向等患者;(2)过敏体质及对多种药物过敏者;(3)病情危重,难以对治疗的有效性和安全性作出确切评价者;(4)吸毒患者或3个月内接受过麻醉性镇痛药以及其它镇痛方式治疗的患者;(5)1个月内应用过皮质类固醇激素或免疫抑制剂者;(6)穿刺部位有感染等穿刺禁忌者。其中使用芬太尼术后静脉镇痛20例(F组),使用羟考酮术后静脉镇痛20例(O组),使用星状神经节阻滞联合芬太尼术后静脉镇痛20例(SGB组)。3组患者性别、年龄、体重、ASA分级、手术时间及术中出血量比较差异均无统计学意义(均P>0.05),见表1。本研究经医院医学伦理委员会批准。
1.2 方法 患者均行经腹肿瘤根治切除手术。3组患者麻醉诱导及麻醉维持方案相同。麻醉诱导为丙泊酚2~3 mg/kg,芬太尼 4 μg/kg,顺阿曲库铵 0.15 mg/kg。麻醉维持:持续静脉泵注丙泊酚2~6 mg/(kg·h)、瑞芬太尼0.1~0.2 μg/(kg·min)维持麻醉深度。F组、O组患者术后分别使用芬太尼、羟考酮术后自控镇痛,按照芬太尼 15 μg/kg或羟考酮1.5 mg/kg,配入0.9%氯化钠注射液中,总计100 ml,背景输注剂量为2 ml/h,患者自控镇痛(patient-controlled-analgesia,PCA)设定为1 ml/15 min。如果镇痛泵内药物不足用至48 h,可重复配置。SGB组患者则在芬太尼术后静脉镇痛的基础上,在气管插管前给予超声引导下星状神经节阻滞(采用超声引导下显示第7颈椎平面,采用穿刺针穿刺颈长肌表面,注射器回抽无血、无液后在该靶点注射1%利多卡因注射液5 ml)。
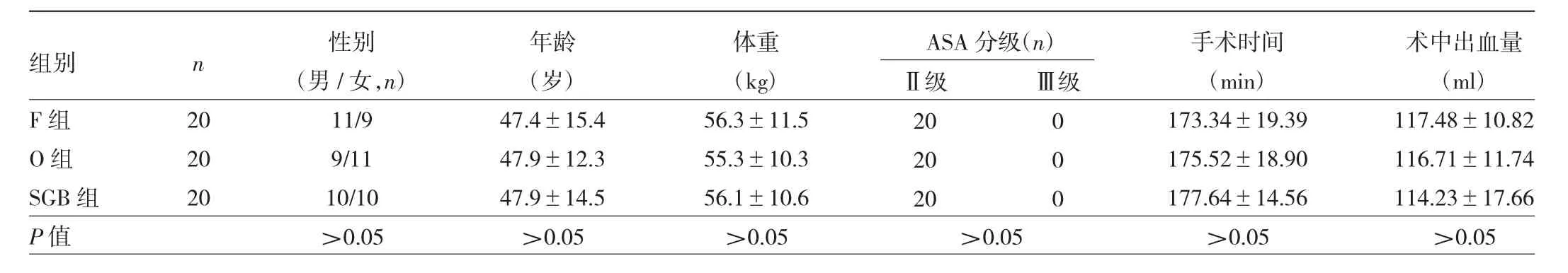
表1 3组患者性别、年龄、体重、ASA分级比较
1.3 观察指标 观察并记录患者麻醉诱导前(T0)、拔除气管插管即刻(T1)、术后镇痛 3 h(T2)、术后镇痛 6 h(T3)、术后镇痛 12 h(T4)、术后镇痛 24 h(T5)、术后镇痛 48 h(T6)等各时点的疼痛评分[视觉模拟评分(visual analogu scale,VAS)]以及不良反应(恶心、呕吐、呼吸抑制、头晕、皮肤瘙痒等)发生情况;采集各时点的血液标本测定TNF-α和IL-6水平。
1.4 统计学处理 采用SPSS 21.0统计软件。计量资料以表示,多组比较采用单因素方差分析,组间两两比较采用LSD-t检验。计数资料以频数和构成比表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 3组患者术后各时点疼痛评分比较 3组患者术后各时点VAS评分比较差异均无统计学意义(均P >0.05),见表 2。

表2 3组患者术后各时点VAS评分比较(分)
2.2 3组患者不同时点血清TNF-α、IL-6水平比较 F组和 O 组患者 T1、T2、T3、T4、T5、T6的血清 TNF-α、IL-6水平均较T0明显升高(均P<0.05),但O组患者均低于F组(均P<0.05)。SGB组患者除T1血清TNF-α、IL-6水平较T0时点升高(P<0.05)以外,其余时点与T0比较差异均无统计学意义(均P>0.05),见表3、4。
2.3 3组患者术后不良反应发生情况比较 3组患者术后恶心、呕吐、呼吸抑制、头晕、皮肤瘙痒发生率比较差异均无统计学意义(均P>0.05),见表5。
3 讨论
肿瘤患者术后免疫功能受疾病本身、疼痛、手术刺激等应激多方面因素影响,手术及放化疗虽能有效提高肿瘤患者的生存率,但会让患者的免疫功能受到不同程度的影响,一旦发生细胞免疫抑制,可能导致肿瘤扩散、复发或并发其他系统性疾病,严重影响预后[7-8]。目前围术期免疫功能研究的热点主要是两个方面:其一是通过控制术后疼痛,降低疼痛导致的应激反应;其二是选择免疫抑制作用更小的镇痛药物,保护肿瘤患者的免疫功能。研究认为,羟考酮具备阿片u受体和k受体双重激动作用,k受体与内脏疼痛关系密切;羟考酮可通过该受体有效降低内脏疼痛而起到更好的镇静、镇痛作用[9-10]。另外有研究表明,羟考酮能降低细胞因子对机体的损伤,其原因可能与其对患者免疫功能影响更小有关[11]。本研究结果亦验证了羟考酮对患者的免疫功能影响较小。
因羟考酮不仅镇痛作用强,对患者免疫功能影响小,所以被推荐应用于肿瘤患者围术期的镇痛。但是羟考酮价格较昂贵、未进入医保,该药在临床应用普及率较低。因此若能找到作用上同等替代甚至优于羟考酮且更容易普及推广的方法具有重要的临床意义。
星状神经节阻滞又称为颈胸交感神经节阻滞。研究发现,超声引导下星状神经节阻滞对全麻期间刺激性操作所引起的心血管反应有一定的抑制作用,可有效减少血流动力学波动,降低应激反应所带来的的危害[12]。还有研究发现,星状神经节阻滞联合羟考酮可提高肿瘤患者的免疫功能,减轻疼痛,提高生活质量[4];星状神经节阻滞可调节免疫细胞的活性和细胞因子的释放,调整淋巴细胞的分布和自然杀伤细胞的活性,从而起到免疫调节的作用[5];星状神经节阻滞还能通过神经-免疫-内分泌系统调节红细胞免疫调控系统中促炎因子及抑炎因子释放的平衡[13]。

表3 3组患者不同时点血清TNF-α水平比较(ng/ml)
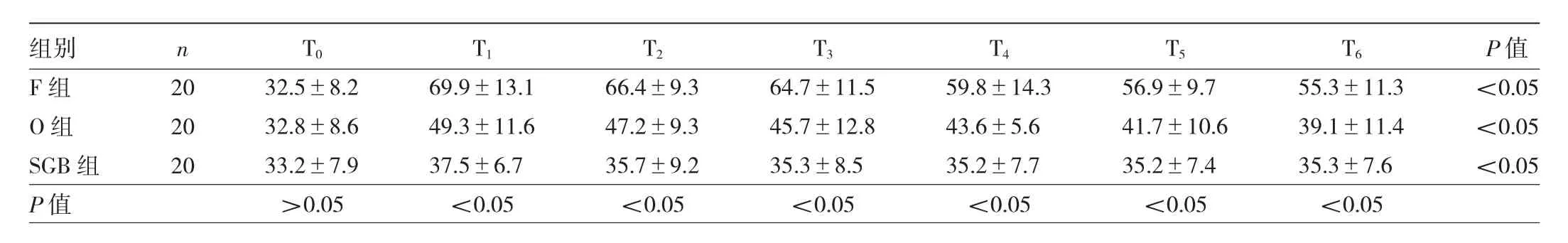
表4 3组患者不同时点血清IL-6水平比较(pg/ml)
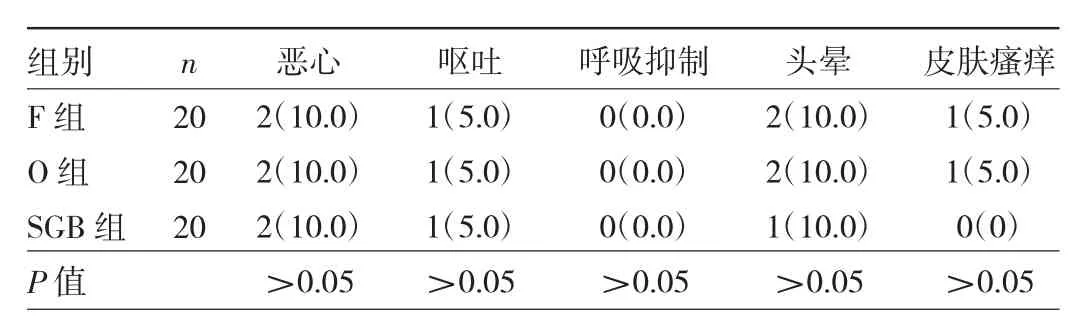
表5 3组患者术后不良反应发生情况比较[例(%)]
综上所述,本研究结果显示,星状神经节阻滞联合芬太尼对妇科恶性肿瘤患者术后镇痛效果好,对免疫功能影响小,可安全有效地调控免疫应激反应,值得临床推广。而星状神经节阻滞联合羟考酮是否能达到更好的效果,尚需临床进一步研究。
