环氧乙烷吸收和转化合成碳酸酯工艺研究进展
2021-01-18褚俊杰常洁罗志斌侯明明李谦
褚俊杰,常洁,罗志斌,侯明明,李谦
(河南大学化学化工学院,河南开封475004)
碳酸乙烯酯(ethylene carbonate,EC)是一种杂环酮化合物,常温下为无色无味晶体,具有介电常数高、挥发性小、热稳定性高、吸湿能力强、溶解性能好等优点[1−2],在石油化工、医药、印染、新能源等行业广泛应用。目前EC 的生产主要有尿素醇解法、酯交换法和环氧乙烷(EO)与CO2的酯化法。其中,EO 的酯化法因其符合“原子经济”和“绿色化学”的科学理念,能够有效利用CO2合成精细化学品,得到了广泛的推广和应用,其生产工艺如图1 所示[3]。本文从EO 生产EC 工艺出发,对吸收剂、催化剂在EO 吸收纯化单元和羰基化反应单元中的作用及其催化机理进行评述,并对生产工艺进行探讨。最后,展望了碳酸乙烯酯工业未来的发展趋势。

图1 EC工艺流程
1 EO的吸收纯化工艺
目前,工业上主要通过乙烯和氧气(空气)在含银催化剂下反应生产EO[4],由于EO的安全性、催化剂的转化率和选择性等多因素的影响,在生成EO的同时会形成含有一定量甲烷、乙烷和乙烯的混合气[5],因此生产EC 之前需要对EO 进行额外的纯化处理。目前纯化EO 的方法主要有吸收法和超临界萃取法,吸收法是依靠溶剂与被吸收气体之间的相互作用力实现EO 纯化,凭借其吸收率高、工艺流程简单等特点而被广泛应用[6−7]。EO的吸收纯化主要由吸收塔、解吸塔和精制塔三单元组成,其工艺流程如图2所示,吸收剂与EO的混合气在吸收塔内逆流接触,塔顶脱EO 后的贫混合气返回乙烯氧化阶段重复利用,塔釜富EO 吸收液经换热后进入解吸塔,解吸后气相塔顶采出,得到环氧乙烷,解吸后液相的解吸贫液从塔釜经过换热后返回吸收塔,解吸后的EO进入精制塔,塔底获得高品质的EO。整个工艺过程中,吸收剂的选择尤为关键,它不仅影响气体的品质,也决定了解吸和精制过程的能耗,因此本节重点对吸收剂的类型和发展进行综述。
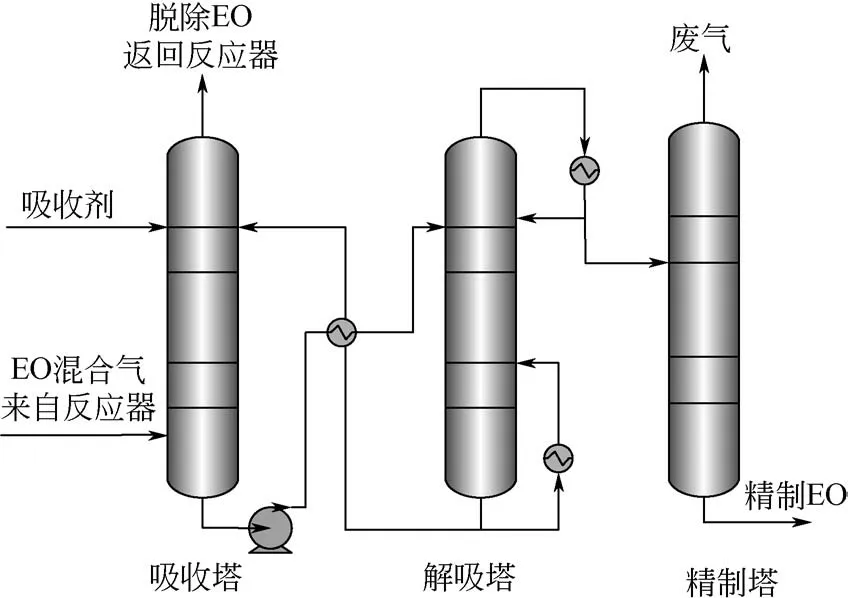
图2 环氧乙烷吸收纯化工艺流程
1.1 单一吸收剂
吸收剂的吸收能力、选择性、价格和物性是影响吸收剂选择的关键因素。由于水具有黏度低、腐蚀小、成本低等优点,在工业上作为吸收剂得到了广泛使用。但是传统工业在利用水为吸收剂吸收EO的过程中,为了保证反应器出口的低浓度EO被充分吸收,通常需要控制吸收剂温度在40℃以下,而汽提和纯化过程需要加热、冷凝和再加热步骤,从而导致了较高的工艺能耗。因此利用水为吸收剂需要对工艺不断改进以降低能耗。
Ozero[8]对传统的汽提器−再吸收器系统进行改进,使汽提塔塔顶蒸气进行部分冷凝,冷凝物作为回流返回汽提塔,在吸收器内汽提塔塔顶蒸气和水逆向接触,以实现EO的优先再吸收,从而增加EO的吸收能力。奥佐罗[9]进一步改进了此工艺,利用水将EO吸收下来,产生稀的EO−水混合物后,将其送至再吸收塔中,减少汽提部分,从而简化工艺流程,降低其能耗。巴斯夫公司[10]提出一种通过蒸馏方法提纯环氧乙烷,操作简单,但该方法只能简单分离醛类,对于不凝气无法达到分离要求。因此陶氏公司[11]对该蒸馏设备进行改进,利用环氧乙烷混合气富足的热量对蒸馏塔提供热量,有效降低高压蒸汽的使用,增加含环氧乙烷进料物流的安全性。张军等[12]发明了一种环氧乙烷吸收装置,如图3所示,该装置由富循环水闪蒸罐、再吸收塔和汽提精馏塔三部分组成,其中汽提精馏塔上部为精馏段,下部为提馏段,EO经过吸收后的富循环水与贫循环水热交换后进入汽提精馏塔汽提,然后进入精馏段纯化。该装置增加了气液相接触面,解决了吸收过程中压力波动大、容易发泡和不凝气积累等问题。兴鲁生物科技公司[13]也提出了一种新型EO回收装置,避免了原料浪费,减轻了生化处理的负担。

图3 环氧乙烷吸收装置[12]
虽然装置和工艺不断改进,但是以水为吸收剂仍存在一些弊端,主要体现为以下两个方面:一是副产物乙二醇[14]的生成,当以水为吸收剂时,汽提塔内的温度高到足以使一部分EO 水合成乙二醇,不仅增加了分离难度,而且会影响后续产品的应用;二是在EO 的解吸过程,整个过程除了水的显热消耗外,在一定的条件下水产蒸汽潜热也会造成能耗大幅增加。为了改善此问题,Gioacchino 等[15]以甲醇为吸收剂吸收EO,不仅避免了副产物乙二醇的生成,而且甲醇的比热容小于水,能够有效降低汽提过程中的能耗。但是吸收剂甲醇的吸收温度必须控制在−50~15℃之间,吸收条件苛刻,不利于工业化的应用。基于此,Dow 公司[16]以EC 为吸收剂吸收EO,具有吸收性能好、副产物少、能耗低等优点,然而由于EC 凝固点较高,吸收温度必须控制在40℃以上,加热系统将导致更高的运营成本。对此,日本三菱[17]利用碳酸丙烯酯作为吸收剂,与其他吸收剂相比具有以下优点:①碳酸丙烯酯对EO的单位质量吸收率比水高50%左右,比碳酸乙烯高40%左右;②碳酸丙烯酯性质稳定,与EO 没有直接反应,而且碳酸丙烯酯对乙烯氧化过程中产生的醛和酸等副产物也非常稳定,甚至比碳酸乙烯酯更稳定。但是碳酸丙烯酯价格昂贵,而且与碳酸乙烯酯性质相似,为后期产物分离带来一定的难度。因此,为了更好地实现乙烯氧化后的混合气中环氧乙烷的吸收和碳酸乙烯酯的生产,仍需要新型吸收剂开发,使之既能够高效吸收环氧乙烷,又能够解决吸收剂成本高、能耗大等问题。
1.2 复合吸收剂
采用两种或两种以上的吸收剂吸收EO,不仅能够弥补单一吸收剂的缺陷,使各个吸收剂之间互补,而且也能有效降低工艺的能耗。
陈玮娜[18]以EC和水的复合吸收剂吸收EO,分别探究塔顶压力、吸收温度、液气质量比对吸收剂的吸收效果的影响,其EC和水的比例对塔顶EO的影响如图4所示。由图可以看出,随着EC的增加,塔顶EO的含量先增加后减少,当EC质量分数达到70%时,吸收效果最好。分析结果为EC对EO的吸收能力比H2O 好,但是随着EC 的量继续增加,受EC 的黏度影响,与水混合不彻底,在吸收塔里分布不均匀,降低了其对EO的吸收能力。
中国石油化工股份有限公司[19]通过采用阴离子为六氟磷酸根的离子液体和三乙二醇二甲醚的混合吸收剂对低浓度EO 进行分离和富集。工艺流程如图5 所示,相较于采用水或者EC 单一吸收剂的传统工艺,其工艺流程得到简化,分离效率更高,具有工业应用潜力。

图4 不同的吸收剂配比对EO的吸收效果比较[18]

图5 改进吸收解吸装置[19]
成卫国等[20]提出以含有EC 和离子液体为吸收剂,吸收液吸收EO 后直接进入反应器中,以离子液体为催化剂将吸收的EO 与CO2反应生成EC。反应后得到一部分EC,另一部分继续充当吸收液循环使用。该过程不仅解决传统生产EC 过程中吸收剂吸收率低的问题,而且简化工艺流程,大大降低了能耗。因此,选择合适的吸收剂对EO 纯化以及产品化利用十分重要,尽量不引入第三组分的情况下选择合适的吸收剂实现EO 的高效吸收,为后续的EO转化奠定了基础。
2 EO的转化工艺

图6 环氧化物和CO2生产EC
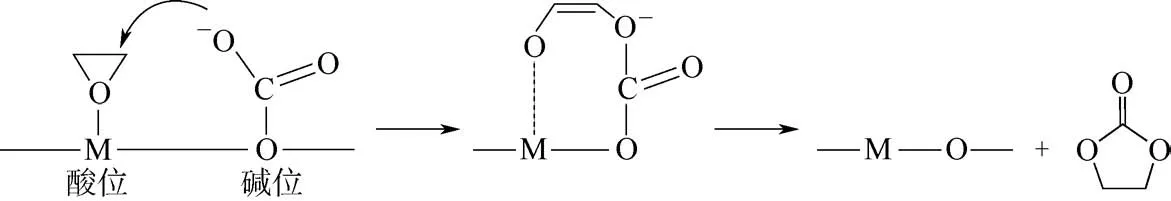
图7 金属氧化物催化合成EC机理
选择性耦合CO2和环氧化合物生产环碳酸酯如图6所示,这不仅是一种原子经济反应,符合“绿色化学”的概念,而且在反应过程中不存在其他副产品[21−22]。但是CO2是作为碳的最高氧化态惰性气体,在该反应过程中催化剂的选择是关键。目前该体系催化剂主要有金属氧化物、金属配合物、碱金属、季铵盐和季盐以及离子液体等催化剂。
2.1 金属氧化物催化剂
金属氧化物因其廉价易得、稳定性强和制备工艺简单而被早期应用于该催化体系,其独特的酸碱位能够同时活化CO2和EO两种反应物,机理如图7所示。
酸碱位对该催化剂的催化效率以及机理研究有着重要意义。Yamaguchi 等[23]利用水滑石焙烧得到Mg−Al 复合氧化物催化剂,研究发现催化剂表面的弱酸与强碱位共同参与催化作用能够有效促进转化率。Dai 等[24]通过煅烧相应的水滑石前体,制备了一系列用碱土金属Zn−M−Al−O(M=Mg、Ca、Sr和Ba)改性的Zn−Al复合氧化物,结果发现Zn−Mg−Al−O (Zn/Mg=4.0,pH=10,不 经 水 热 处理)的性能最好,反应后产物的选择性为99.2%,产率为88.8%,进一步提出了反应可能的机理。Wang 等[25]首次合成一种新颖的多位点完全非均相催化剂Br−LDH,如图8所示,该材料将溴与羟基结合,有利于溴与羟基协同催化环加成反应。Br−LDH具有制备简单、经济可行、环境友好等特点,显现出良好的工业化应用前景。
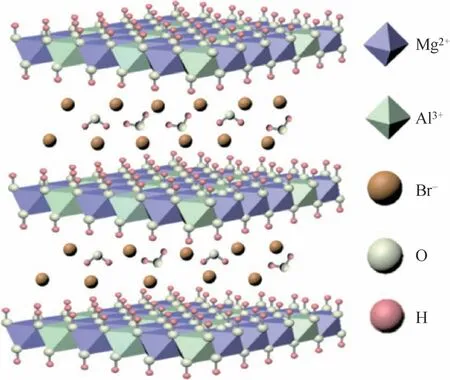
图8 Br−LDH催化剂[25]
2.2 季铵盐/季盐、碱金属催化剂
2002年,Calo等[26]简单地将底物溶解在熔融的四丁基溴化铵(TBAB)或四丁基碘化铵中,即可实现化学固定大气压力下的CO2,而且产品提纯通过真空蒸馏或乙酸乙酯萃取分离就能达到要求。这类催化剂主要反应过程为阴离子(卤素)在空间位阻较小的方向对EO 进攻,致使其开环,然后CO2从另一方向进行环加成反应,最后发生消去反应生成环状碳酸酯,其机理如图9所示。

图9 TBAB合成碳酸酯的催化机理[26]
工业化应用中,在高效的转化率和选择性的前提下,低温低压也是所追求的条件之一。Kumatabara 等[29]利用三乙胺碘化氢作为简单而有效的双官能催化剂,在温和的反应条件下(0.1MPa,40℃,24h)实现高效环状碳酸酯的生成。Zhou等[30]合成了一系列的无金属和无卤素的有机催化剂磷内酯(P−ylide)CO2加合物催化剂,可在环境条件(25℃,0.1MPa CO2)下发生反应,转化率可达到99%。Song 等[31]研究表明,MOF−5(图10)与 季 铵 盐Me4NCl、Me4NBr、Et4NBr、n−Pr4NBr、n−Bu4NBr 有良好的协同催化作用,反应在50℃和6MPa的条件下转化率能达到97%。

图10 MOF−5框架的结构[31]
碱金属盐对合成碳酸酯也有较好的活性,但是单独的碱金属盐的催化活性较低。Rokichi 等[32]研究在冠醚存在下的碱金属的催化活性,取得较好的效果,但是冠醚具有毒性大和价格昂贵等问题使该催化剂生产受限。因此,Ghosh等[33]以Co(Ⅲ)−四酰胺环丙烯醛络合物为催化剂,在4−二甲氨基吡啶存在的情况下,环碳酸酯产率可高达100%。更进一步,Ramidi 等[34]研究碱金属卤化物和Lewis 碱之间具有独特的协同作用,与仅使用碱金属卤化物进行的反应相比,反应效率能够提高40 倍。因此,良好的催化剂不仅需要高活性和稳定性,还需要具有环境友好和易回收等优点。
2.3 金属配合物催化剂
近年来,金属配合物因具有活性高和周期短等优点,逐渐引起科研人员的注意,其作用机理如图11 所示,路易斯酸性金属中心与环氧乙烷配合,然后辅催化剂开环生成醇氧基离子,最后在二氧化碳的基础上进行环合,形成五元环碳酸酯,从而完成催化剂和助催化剂的再生。在金属配合物中,过渡金属离子如铬、钴和镁、锌在环碳酸酯的合成中显示出其价值。表1所示为近些年常见金属配合物催化剂。

图11 金属配合物催化机理

表1 环碳酸酯合成以金属配合物为催化剂
铬和钴为常见的过渡金属,在合成碳酸酯中具有较高的催化活性和较宽的温度活性范围[35−36]。但是在催化剂研发过程中,由于铬钴的毒性和价格昂贵等问题,所以不适合大规模工业化生产,因此需开发无毒便宜的新型催化剂。
铝、铁作为常见的金属,具有比能量高、无毒无害、资源丰富、环境友好等优点,能够替代铬和钴过渡金属[38−47]。前期Taherimehr 等[48]以吡啶基氨基双(酚类)铁配合物为双功能催化剂,在85℃和8MPa 的条件下反应3h,CO2与多种环氧化合物的转化率为99%。但其催化剂用量大而且反应中所需CO2的压力较高,因此Monica 等[49]以硫醚−三酚酸配体负载的双核铁(Ⅲ)和四丁基溴化铵配合物为最佳的催化剂/助催化剂,在120℃和2MPa 条件下反应1h,环氧化合物的转化率大于99%。此外,铝和三酚酸盐的复配物[37]、脒酸铝配合物[47],硫醚−三酚铁(Ⅲ)配合物[52]、双(苯氧基亚氨基)铁(Ⅲ)−氯复合体配合物[53]等催化剂均取得较好的效果。在此基础上Peng等[54]设计合成了一系列新颖的锌、铜、铁超分子配合物(图12)。该类多相、环保、活性高的催化剂体系适用于环氧化合物生产环碳酸酯,使工业化应用更具可行性。

图12 新型的双核超分子Zn、Cu、Fe配合物和二聚体锌催化剂[54]
2.4 离子液体催化剂
离子液体作为“清洁”新型溶剂和新催化体系,具有蒸气压低、热稳定性好、独特氢键和静电作用力、反应产物分离简单等优点,被广泛关注[55−56]。离子液体的催化步骤[57]:①阴离子亲核攻击环氧乙烷开环;②依次向形成的醇氧基中加入CO2;③阳离子稳定,五元环碳酸酯形成,阴离子由分子内SN2反应排出,机理如图13所示。

图13 离子液体催化反应的机理
Peng和Deng[58]首次合成1−丁基−3−甲基咪唑四氟硼酸盐([BMIm][BF4]),在2.5MPa CO2压力和110℃条件下进行6h,飞行时间(TOF)为6.6h−1。随后探究发现,离子液体的氢键基团和Lewis 碱性位点溴化物阴离子能够同时攻击环氧化物的不同部分,使环氧化合物的C—O 键极化开环[59]。基于此理论基础,Sun 等[60]将离子液体与壳聚糖结合开发了一种绿色反应条件下高效、廉价、可回收的壳聚糖功能化1−乙基−3−甲基咪唑卤代烷(CS−EMImX,X=Cl、Br)催化剂,合成步骤如图14 所示,在不添加溶剂和金属辅助催化剂的情况下,通过与各种环氧化合物进行环加成反应,得到了高收率、高选择性的五元环碳酸酯。

图14 合成的CS−EMImX(X=Cl、Br)催化剂[60]
甲酸、乙酸等有机酸也具有较强的氢键,而且廉价易得。Zhou等[61]合成了一系列包含季铵离子和羧酸基团的甜菜碱基盐。研究表明在8MPa CO2压力、140℃、8h的条件下,催化剂(HBetI)负载为2.5%(摩尔分数),碳酸酯的收率为98%。同时研究表明羧基化咪唑啉盐基离子液体接枝到不同的聚合物,也能够取得较好的结果,而且这些多相催化剂可以较容易地从产物中分离出来并重复使用[62−63]。
通过前期研究发现,离子液体在催化过程中存在活性低、制备工艺复杂、反应条件苛刻等缺点。因此,在温和的反应条件下,探索高效、绿色、稳定、易于制备的多位点离子液体是走向工业化应用的必要因素。Rajendra[64]利用二元([EvimOH][Cl]/base)催化体系增加活性位点以提高活性,研究结果表明,在温和的反应条件下,不需要溶剂和金属辅助催化剂,具有99.8%的转化率和99%的选择性。二元催化剂虽然获得较好的效果,但是催化剂研发和生产工艺复杂。Liu 等[65]合成了一系列具有N杂环卡宾前体和羧基作为质子转移剂的钳型化合物(图15),该化合物具有多个CO2吸收活化位点,在环境条件下(25℃,0.1MPa)碳酸酯化合物的收率达96%。Hu等[66]合成了一种结构新颖、多位点、高效催化剂[TMGH+][−O2MMIm+][Br−],用于促进CO2和环氧化物的反应。研究结果表明,在常压无溶剂、低温(30~60℃)的条件下,碳酸酯的收率为89%。同时Liu 等[67]在其基础上开发了一系列新型无金属双离子铵盐催化介质,在室温条件下其产品收率和选择性高达98%和99%。

图15 多活性位点催化剂设计与反应过程[66]
Shi 等[68]将氨基功能化的咪唑离子液体(Si−IMNH2)和季铵盐(Si−TBAI)接枝在介孔笼状二氧化硅SBA−16上,形成了具有多官能团的多相催化体系(图16)。该催化剂具有良好的CO2富集能力、多个活性位点(I−、Cl−、-NH2基团和咪唑环)和开放的介孔通道的协同作用,在无任何助催化剂的情况下,低温、低压(50℃、0.5MPa)条件下,具有优异的产率(98.5%)和选择性(99%)。催化剂易回收、多位点、高活性是目前催化剂研究的热点,有较好的工业应用前景。

图16 固载离子液体的结构[68]
3 EO吸收−转化一体化工艺
目前工业上EO 和CO2合成碳酸乙烯酯的工艺主要分为EO 吸收精制单元和羰基化单元两部分(图1),其中EO 的吸收精制单元决定了整个工艺的能耗,所以前期人们探索不同的吸收剂,逐渐由水转向高沸点、低热容吸收剂,由单一吸收剂向复合吸收剂转变,提高吸收剂对环氧乙烷的吸收能力和选择性,但是在整个工艺流程中,汽提环氧乙烷的过程仍然消耗大量能量,而且工艺流程复杂、设备造价高、一次性投资大。因此,对于该工艺的能耗问题不仅需要高效吸收剂,而且也需要解决汽提过程中能耗大的问题。
刘雪静等[69]提出了一种环氧乙烷装置联产碳酸乙烯酯的方法,利用碳酸乙烯酯和乙二醇作为复合剂吸收EO和CO2混合气,同时将含有EO的混合吸收液直接进入羰基化反应器中,在酯化催化剂作用下将含有EO 和CO2的吸收液催化反应生成碳酸乙烯酯,然后将反应后的混合液体利用常规方法脱除未反应的CO2气体,反应液用常规方法收集乙二醇和碳酸乙烯酯。该工艺过程流程较短,降低了设备成本,不仅解决了吸收剂能耗大等系列问题,同时整个工艺过程在加压下完成,整个流程压力波动较小,能耗较低。
成卫国等[70]提出了一种复合吸收剂及其用于环氧乙烷吸收转化耦合联产碳酸乙烯酯的方法。该方法利用离子液体和碳酸乙烯酯复合吸收剂吸收环氧乙烷和二氧化碳,同时在吸收的过程中离子液体不仅作为吸收剂,而且还作为催化剂,将吸收下来的环氧乙烷和二氧化碳原位反应生产碳酸乙烯酯,吸收的同时实现预转。通过与水和碳酸乙烯酯的吸收过程相比可以看出,在吸收过程环氧乙烷的吸收率低于使用含离子液体的复合吸收剂对环氧乙烷的吸收效率,而在反应过程,环氧乙烷的转化率也有所提高。所以对于该工艺环氧乙烷吸收转化耦合联产碳酸乙烯酯不仅能增强对环氧乙烷的选择吸收性,还对环氧乙烷和二氧化碳的酯化反应有较高的催化效率,从而大大降低了能耗,具有较大的工业化实施前景。
4 发展前景和展望
以EO和CO2为原料合成EC不仅工艺简单,而且能够有效利用CO2以缓解温室效应。该工艺中吸收剂的种类选择和催化剂研发至关重要,吸收剂决定了整个工艺的能耗,催化剂决定产品的品质。对于吸收剂部分,单一的吸收剂无论是水还是碳酸酯类,由于无法同时满足吸收能力强、选择性高等特点,逐渐被复合吸收剂所取代,其中以离子液体复合最为突出。在催化部分,多位点催化剂因其反应条件温和,收率和转化率较高,将会逐步取代单一位点催化剂,但是由于多位点催化制造工艺较复杂,给工业化带来不便,因此,利用简单工业研制多位点催化剂有较好的前景。对于整个工艺,EO吸收转化耦合生产碳酸乙烯酯工艺简单、设备造价低,具有良好的工业应用前景。
