HPLC法检测膏药中硫酸阿托品含量方法的建立
2021-01-06吴春燕张立军张新玥张转平
吴春燕 张立军 张新玥 张转平




【摘 要】 目的:建立高效液相色谱法检测膏药中硫酸阿托品的含量测定方法,用于市售止痛膏药的药品质量控制。方法:采用萃取技术处理不同膏药样品,得含量测定分析提取物。采用HPLC技术,以ODS C18色谱柱(250 mm×4.6 mm, 5 μm),乙腈-磷酸盐缓冲液(取6.8 g磷酸二氢钾溶于1000 mL水中,加入10 mL三乙胺,用磷酸调节pH值至2.8)(7∶93)为流动相,流速为1 mL·min-1,检测波长为210 nm,进样体积10 μL,测定不同厂家止痛膏药中硫酸阿托品含量。结果:建立了止痛膏药中硫酸阿托品含量测定方法,其在0.088 2~0.882 0 μg具有良好的线性,平均回收率为95.73%,不同厂家止痛膏药中硫酸阿托品含量范围为0.06~0.39 mg/100cm2,含量差异很大。结论:该法简便、准确、灵敏度高,重现性好,可以用于止痛膏药中硫酸阿托品含量测定及质量控制。
【关键词】 止痛膏药;质量控制;硫酸阿托品;高效液相色谱法;含量测定
【中图分类号】R284 【文献标志码】 A 【文章编号】1007-8517(2021)22-0029-05
Establishment for Methods of Atropine Sulfate in Acesodyne Plaster by HPLC
WU Chunyan1 ZHANG Lijun1 ZHANG Xinyue2 ZHANG Zhuanping1*
1. Ankang Inspection and Detection Center of Food and Drug Control, Ankang 725000,China;
2.Beijing University of Traditional Chinese Medicine, Beijing 100029,China
Abstract:Objective To establish a method for the determination of atropine sulfate in acesodyne plaster by high performance liquid chromatography (HPLC). Used for quality control of acesodyne plaster.Method Extraction technology was used to extract the atropine sulfate in acesodyne plaster from different production enterprises, HPLC method was developed to determination of atropine sulfate in acesodyne plaster from different production enterprises, and the contents were determined by Phenomenex ODS C18 (4.6 mm×250 mm, 5 μm), with acetonitrile-phosphate buffered salt solution as the mobile phase for isocratic elution (7∶93), the flow rate was 1 mL.min-1, the detection wavelength was 210 nm, injection volume was 10 μL. Result The common mode for the determination of atropine sulfate in acesodyne plaster was established. A linear range of 0.088 2~0.882 0 μg, the mean recovery 95.73%. The content of atropine sulfate in analgesic plasters from different production enterprises varies greatly, the range of 0.06~0.39 mg/100cm2. Conclusion The method showed to be simple, quick, sensitive, accurate, reproducible and can be used to content determination and control quality of acesodyne plaster from different production enterprises.
Keywords:Acesodyne Plaster; Quality Control; Atropine Sulfate; HPLC; Content Determination
止痛膏為《中华人民共和国药典》2010、2015、2020年版收载的制剂,主要以止痛流浸膏、水杨酸甲酯、薄荷脑、冰片、芸香浸膏、颠茄浸膏等七味药为原料,另加基质制成膏药。具有祛风湿、活血止痛等功效。用于风湿性关节炎、肌肉疼痛、关节肿痛等病症[1-3],是国家基本用药目录收载品种[3- 4]。颠茄浸膏为止痛膏的重要组成部分,具有抗胆碱、解除平滑肌痉挛、抑制腺体分泌的作用,可用于胃及十二指肠溃疡,胃肠道、肾、胆绞痛等,外用可解除肌肉痉挛,从而达到止痛的效果,是止痛外用膏药的主要成分。而硫酸阿托品是颠茄浸膏指标性成分和功效成分[5-7]。《中华人民共和国药典》(2015年版及2020年版)收载止痛膏药品中只见硫酸阿托品薄层鉴别,不能很好控制企业生产的膏药质量[3, 8-10]。颠茄浸膏药性俊烈,具有一定的毒性,与诸多药品具有使用配伍禁忌,有必要对其进行质量控制[11]。市场膏药质量参差不齐,不同生产厂家的止痛膏药样品中硫酸阿托品含量差异较大,存在非法或超剂量添加等情况,有必要提升控制标准,建立其含量测定控制线,保证膏药质量与患者用药安全。《中华人民共和国药典》(2015年版和2020年版)中仅对膏药进行了薄层色谱鉴别,难以控制其质量。本次研究,对止痛膏中硫酸阿托品进行了提取分离、含量测定,以期对市售止痛膏药品进行质量控制。该方法操作简便,结果准确,可为市售膏药质量控制提供思路。
1 仪器与试药
岛津LC-20AT型高效液相色谱仪,LC Solution色谱工作站;Phenomenex ODS C18色谱柱(250 mm×4.6 mm, 5 μm);硫酸阿托品购自中国药品生物制品检定所(供含量测定用,批号100040-201312),乙腈为色谱纯,水为超纯水,三氯甲烷、磷酸二氢钾、三乙胺、磷酸、氨水均为分析纯。
2 方法与结果
2.1 色谱条件 Phenomenex ODS C18色谱柱(250 mm×4.6 mm, 5 μm),流动相为乙腈-磷酸盐缓冲液(取6.8 g磷酸二氢钾溶于1000 mL水中,加入10 mL三乙胺,用磷酸调节pH值至2.8)(7∶93)为流动相等度洗脱,流速为1 mL·min-1,检测波长为210 nm,柱温40 ℃,进样体积10 μL。在上述色谱条件下样品中硫酸阿托品与其它组分分离较好,结果如图1所示。
2.2 对照品溶液的制备 取硫酸阿托品对照品约20 mg,精密称定,置20 mL量瓶中,用甲醇溶解并稀释至刻度,摇匀,浓度为0.882 0 mg/mL备用,存贮于4 ℃冰箱中备用。
2.3 供试品溶液的制备
2.3.1 提取溶剂的选择 止痛膏中膏药一般用三氯甲烷或乙醚提取[3,12-13]。取样品(陕西东科,批号:150708)适量,2份(片),分别加入三氯甲烷、乙醚洗尽布衬膏药,再用0.5%硫酸溶液提取4次,合并酸液,再用氨水调至PH为10~11,再分别用三氯甲烷、乙醚萃取4次,水浴蒸干,用流动相定容,过滤,按“2.1”色谱条件进行分析,测定峰面积,结果显示,相比于三氯甲烷处理,乙醚萃取转移率较低,故选用三氯甲烷处理,见表1。
2.3.2 酸提与碱沉次数的选择[14-17] 取样品(陕西东科,批号:150708)适量,分成8份(片),加入三氯甲烷洗尽布衬膏药,分别置分液漏斗中。用0.5%硫酸溶液振摇提取,每次40 mL,考察提取次数(2、3、4次),合并提取液,置分液漏斗中(酸提)。再用氨水调至PH为10~11,分别用三氯甲烷振摇萃取,每次40 mL,考察萃取次数(2、3、4次),合并萃取液,分别置于蒸发皿中水浴蒸干(碱萃)。残渣加流动相溶液定容10 mL容量瓶中,按“2.1”色谱条件进样分析,分别测定峰面积。结果显示,0.5%硫酸溶液提取3次調碱后三氯甲烷萃取4次,样品中硫酸阿托品转移率为98.00%(631871/644767);0.5%硫酸溶液提取3次调碱后三氯甲烷萃取3次,样品中硫酸阿托品转移率为97.84%(618212/631871),见表2。故选择用0.5%硫酸溶液提取3次,调碱后三氯甲烷萃取3次即可。
2.3.3 供试品溶液的制备 综上分析,收集不同厂家生产的膏药,做好标记,剪去适量面积(cm2),平行2份。加入三氯甲烷洗尽布衬膏药,置分液漏斗中,分别用0.5%硫酸溶液提取3次,每次40 mL,合并酸溶液,用氨水调至PH为10~11,置分液漏斗中,再用三氯甲烷萃取3次,每次40 mL,合并三氯甲烷萃取液,水浴蒸干,用流动相定容至10 mL量瓶中,滤过,取续滤液,即得。
2.4 线性关系考察 精密吸取硫酸阿托品对照品储备溶液(0.882 0 mg/mL)0.5、1.0、1.5、2.0、2.5、5.0 mL,用甲醇溶解定容至5 mL,摇匀。按“2.1”项下色谱条件进样分析,测定峰面积,以峰面积Y对进样量X作标准曲线,计算回归线方程为Y=1×107X+5357.9,r=0.9991,结果表明硫酸阿托品在0.088 2 ~0.882 0 μg范围内具有良好的线性。
2.5 精密度试验 精密吸取同一供试品溶液(陕西东科,批号150708),按“2.1”项下色谱条件下连续进样6次,测定硫酸阿托品的峰面积,计算其RSD为1.07%(n=6),表明仪器的精密度良好。
2.6 稳定试验 精密吸取同一供试品溶液(陕西东科,批号150708),按“2.1”项下色谱条件,分别于0、3、6、9、12、24 h进样分析,测定峰面积,计算含量。结果表明供试品溶液在24 h内稳定,样品中硫酸阿托品含量的RSD为1.75%(n=6)。
2.7 重复性试验 取同一批样品6份(陕西东科,批号150708),按“2.3.3”项下供试品溶液的制备方法和“2.1”项下色谱条件进样分析,测定峰面积,计算含量。结果表明,本法有良好的重复性,样品中硫酸阿托品含量的RSD为1.45%(n=6)。
2.8 回收率试验 取已知含量的同一批(陕西东科,批号:150708,含量为0.38 mg/100 cm2)样品适量,平行6份,分别加入硫酸阿托品对照品约0.50 mg(对照品储备液500 μL),按“2.3.3”项下供试品溶液的制备方法和“2.1”项下色谱条件进样分析,测定峰面积,计算回收率(%),平均回收率为95.73%,RSD为0.39%,结果见表3。
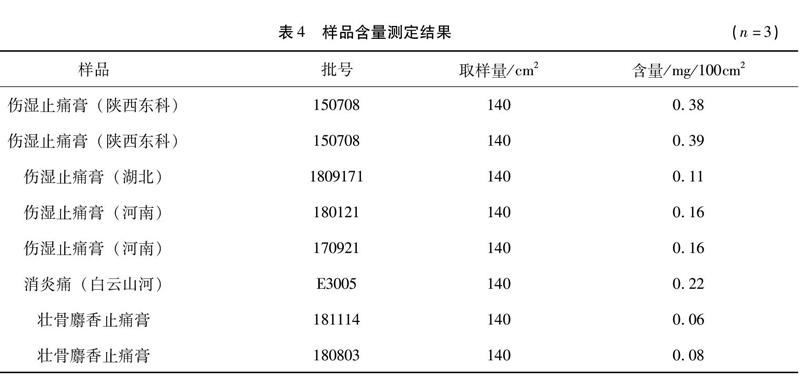
2.9 不同厂家膏药中硫酸阿托品含量测定 取不同厂家止痛膏供试品溶液,按“2.1”项下色谱条件进样分析,计算不同厂家止痛膏药中硫酸阿托品的含量。结果显示,不同厂家生产止痛膏样品中硫酸阿托品含量差异较大,含量范围在0.06~0.39/100 cm2,结果见表4。
3 讨论
3.1 样品处理考察 本次研究分别考察了不同提取溶剂、萃取次数及溶剂用量对止痛膏中硫酸阿托品提取结果的影响。结果发现采用三氯甲烷萃取转移率优于乙醚,可能是因为乙醚萃取时容易产生乳化现象,造成成分萃取不完全;乙醚容易挥发、易爆及危险系数高,最终决定采用三氯甲烷作为提取和萃取溶剂[13, 17]。同时也考察了提取与萃取溶剂用量、萃取次数及PH对样品中硫酸阿托品转移的影响,最终优选出上述样品处理方法。
3.2 色谱条件考察 实验分别考察了甲醇-水溶液、乙腈-水溶液、甲醇-磷酸缓冲盐溶液、乙腈-磷酸缓冲盐溶液,柱温分别考察了30、 40 ℃对分离效果的影响,最终优选出色谱条件为乙腈-磷酸缓冲盐溶液等度洗脱(7∶93),流速为1 mL·min-1,检测波长为210 nm,柱温40 ℃,分析时间50 min。
3.3 耐用性与重现性考察 在上述优选的条件下,分别考察了不同品牌的C18色谱柱(Phenomenex ODS C18、DiKMA spursil C18及Agilent ZORBAX SB-C18)、高效液相色谱仪(安捷伦与岛津)及更换不同的分析人员在不同的实验室(化学室与中药室)对含量测定结果的影响,结果显示新建立的止痛膏中硫酸阿托品含量测定方法耐用性及重现性均很好,RSD均小于3%。
3.3 回收率实验结果分析 通过加入对照品回收实验分析,平均回收率为95.7%,RSD为0.39%,结果显示优选的方法具有很好的回收效果。
3.4 膏药中硫酸阿托品含量测定方法小结 本研究采用溶剂萃取技术处理不同膏药样品,得含量测定分析提取物,通过对提取溶剂选择、酸提碱沉次数及溶剂用量等进行考察,结果显示,该方法被测成分硫酸阿托品转移率高,转移率为97.84%(618212/631871)建立了膏药样品处理方法。采用HPLC法建立膏药中硫酸阿托品含量测定方法,通过专属性、精密度、稳定性、重复性实验以及耐用性与重现性考察,该法简便、准确、灵敏度高,重现性好,可以用于止痛膏药中硫酸阿托品含量测定及质量控制。本次实验测定数据显示,不同生产厂家的止痛膏药样品中硫酸阿托品含量差异较大,颠茄浸膏/流浸膏作为止痛膏重要组成部分,其硫酸阿托品为颠茄浸膏/流浸膏主要指标和功效成分,建立膏药中硫酸阿托品含量测定方法可以很好的用于膏药质量控制。
参考文献
[1]国家药典委员会.中华人民共和国药典一部[M].北京:中国医药科技出版社,2010:767-768.
[2]国家药典委员会.中华人民共和国药典一部[M].北京:中国医药科技出版社,2015:847-848.
[3]国家药典委员会.中华人民共和国药典一部[M].北京:中国医药科技出版社,2020:893-894.
[4]王莉,袁强,成岚,等.我国基本药物目录遴选与评价方法的问题与反思[J].中国药房,2010,10(16):1453-1456.
[5]孙凯,杨丽敏.山莨菪碱的药理和临床研究进展[J].世界临床药物,2010,31(3):182-186.
[6]周华成,董燕斐,代小奇,等.东莨菪碱对骨癌痛鼠吗啡镇痛效果的影响[J].中国疼痛医学杂志,2011,17(11):682-685.
[7]王宇卿,庄果,王晓瑜,等.基于UPLC-ESI-Q-TOF-MS~E技术分析颠茄草化学成分[J].药物分析杂志,2019,39(6):1063-1068.
[8]张文婷,马临科,黄琴伟,等.中国药典2015年版颠茄草类制剂修订情况及操作要点[J].中国现代应用药学,2016,33(5):623-625.
[9]张小山.对维U颠茄铝制剂中不同颠茄料源性质的分析判定与监管[J].中国药物与临床,2013,13(3):132-134.
[10]苏晓红,林华明.测定颠茄流浸膏含量的几点体会[J].基层中药杂志,1999,10(1):3-5.
[11]严玮.含颠茄生物碱中药及其制剂与西药的配伍禁忌[J].实用中医药杂志,2011,27(12):874.
[12]吴玉婷,吕伟旗,汤晟凌.6省13个产地颠茄草中2种成分测定及相关性分析[J].中成药,2019,41(7):1618-1623.
[13]彭拓华,钟世顺,张少俊,等.三种提取方法提取洋金花生物碱的比较研究[J].中成药,2012,34(5):832-835.
[14]黄伟,张文婷,赵维良,等.颠茄流浸膏真伪鉴别及含量测定方法研究[J].药物分析杂志,2012,32(1):151-154.
[15]庄果,王宇卿,熊伟,等.RP-HPLC法同时测定颠茄草5个部位中2种成分[J].中成药,2017,39(12):2560-2563.
[16]张文婷,张春阳,黄伟,等.湖南产颠茄草不同生长期8个成分的动态变化及不同部位分布特征[J].中草藥,2016,47(22):4072-4075.
[17]张立军,戴海蓉,杨志军,等.高乌头炮制前后镇痛抗炎活性部位HPLC指纹图谱建立及质量研究[J].中草药,2017,48(12):2442-2447.
(收稿日期:2021-03-20 编辑:刘 斌)
基金项目:陕西省社会发展科技攻关项目(2015SF286)。
作者简介:吴春燕(1976-),女,汉族,本科,副主任药师,研究方向为药物分析与质量标准研究。E-mail:554633883@qq.com
通信作者:张转平(1966-),男,汉族,本科,主任药师,研究方向为药物分析与质量准研究。E-mail:715401074@qq.com
