颅内动脉瘤栓塞术中及术后出血原因分析
2021-01-04周雷王中李吻朱巍巍
周雷 王中 李吻 朱巍巍
自1995年美国食品与药品管理局(FDA)批准电解脱弹簧圈用于治疗颅内血管性疾病以来,颅内动脉瘤弹簧圈栓塞术即被认为是一种安全、有效的介入治疗方式。根据流行病学调查显示,完全性颅内动脉瘤致密栓塞术后发生再次破裂出血的概率极低,而动脉瘤栓塞术中或术后再次出血事件则更为常见,术中出血或栓塞术后1年内再出血发生率分别为1%和0.90%~2.70%,死亡率可高达80%,患者预后不良[1⁃5]。因此,探询并分析动脉瘤栓塞术中或术后出血机制,对提高手术安全、降低死亡率和病残率具有重要意义。本研究拟对苏州大学附属第一医院神经外科近年采用栓塞术治疗的颅内动脉瘤患者的临床资料进行回顾,并对术中及术后再出血发生率和出血原因进行分析,以为降低术中及术后再出血发生率、提高手术成功率提供参考。
对象与方法
一、观察对象
1.纳入标准 (1)术前经头部CT或腰椎穿刺脑脊液检查证实为自发性蛛网膜下腔出血,且经全脑血管造影明确出血原因为颅内动脉瘤破裂所致。(2)术前CTA、MRA或全脑血管造影发现未破裂动脉瘤,术中经全脑血管造影明确诊断。(3)确诊后行颅内动脉瘤栓塞术。(4)术中动脉瘤破裂出血或于首次栓塞术后3个月内症状加重,并经头部CT证实栓塞的动脉瘤相邻区域出血量较术后即刻增多或可见新发出血灶。(5)患者及其家属对动脉瘤栓塞术可能发生的风险知情并签署知情同意书。
2.排除标准 (1)头部CT和CTA提示蛛网膜下腔出血,但全脑血管造影呈阴性。(2)虽经各项检查确诊为颅内动脉瘤,但未行血管内介入治疗。(3)术前发生再次出血。(4)首次栓塞术后因脑梗死、高血压、脑室外引流术穿刺引起出血。
3.一般资料 选择2015年1月至2017年4月在我院行颅内动脉瘤栓塞术患者共153例,其中男性56例,女性 97例;年龄 24~80岁,平均(56.64±13.39)岁。既往史包括高血压病史者66例(43.14%),伴有颅内出血9例(5.88%)、脑室内出血12例(7.84%)。(1)动脉瘤部位:前交通动脉瘤20例(13.07%)、后交通动脉瘤27例(17.65%)、颈内动脉海绵窦段动脉瘤7例(4.58%)、颈内床突旁动脉瘤35例(22.88%)、颈内分叉部动脉瘤4例(2.61%)、大脑中动脉动脉瘤4例(2.61%)、椎基底动脉动脉瘤37例(24.18%)、大脑前动脉动脉瘤2例(1.31%),以及多发性动脉瘤17例[共35个动脉瘤(11.11%)]。(2)神经功能分级:采用Hunt⁃Hess分级进行神经功能状态评价,1级 119例(77.78%)、2级 23例(15.03%)、3级9例(5.88%)、4级2例(1.31%),以及5级 0例。(3)动 脉瘤体积:<5 mm 者 102例(66.67%)、5~10 mm者37例(24.18%)、>10 mm者14例(9.15%)。
二、研究方法
1.围手术期处理 患者入院后即行体格检查和神经功能评价,对于术中需支架辅助的患者,术前予以负荷剂量阿司匹林300 mg+氯吡格雷300 mg口服或鼻饲,所有患者栓塞术前均须达到全身肝素化。术后穿刺部位局部压迫、加压包扎,下肢制动24 h,根据植入支架种类,继续予以口服阿司匹林100 mg/d和氯吡格雷75 mg/d,持续治疗3~6个月或终身服药,手术前后根据血栓弹性描记图指示和患者具体情况调整药物种类和剂量。
2.颅内动脉瘤栓塞术 (1)设备与仪器:Philips Integris V3000型全脑血管造影仪购自荷兰Philips公司。其他术中所用材料包括6F鞘管、6F Chaperon或Navien导引导管,Headway 21或17微导管,Enchlon 10、Rebar 27和 SL⁃10微导管,Transend PLATINUM、Transend Floppy、Transend SOFTTIP 和0.010X⁃pedion微导丝,LVIS和 Solitaire支架,以及Hyperform球囊分别购自美国Cordis、Microvention、Medtronic、Boston Scientific、EV3、Stryker和 MTI公司;750型动脉瘤夹购自德国Aesculap公司。(2)手术过程:患者平卧位,全身麻醉,经单侧或双侧股动脉Seldinger穿刺,置入6F鞘管,DSA进一步明确诊断,并根据3D成像明确动脉瘤位置、大小、形状,以及与载瘤动脉之间的关系,确定支架释放及弹簧圈填塞角度。将6F Chaperon或Navien导引导管送至距动脉瘤最近的位置(颈内系统动脉瘤置于颈内动脉岩骨段水平),以Transend PLATINUM微导丝将支架Headway 21或17微导管送至动脉瘤远端备用。另外选择SL⁃10微导管于Transend PLATINUM微导丝导引下置于动脉瘤并调整至最佳位置。然后后撤支架微导管并缓慢半释放支架,使其完全覆盖动脉瘤颈部,再依据动脉瘤形状、大小首选3D弹簧圈成篮、再以2D弹簧圈致密栓塞,全脑血管造影或3D成像判断栓塞效果,最后完全释放支架解脱。对于支架打开不完全或贴壁不良者,可选择微导丝按摩支架或Hyperform球囊扩张,DSA评价血管通畅与否,以及动脉瘤栓塞程度。
3.疗效评价 (1)术中出血:定义为动脉瘤栓塞治疗过程中对比剂外渗于动脉瘤壁之外。(2)栓塞率 :根 据 Raymond分 级 标 准(Raymond Classification)[6],术后即刻 DSA 显示弹簧圈栓塞致密、动脉瘤达100%栓塞为Ⅰ级;瘤颈残留、动脉瘤95%栓塞为Ⅱ级;部分瘤体残留、动脉瘤栓塞<90%为Ⅲ级。(3)术后出血:系指动脉瘤栓塞术后即刻至3个月内出现蛛网膜下腔、脑实质或脑室内出血,经CT或MRI证实栓塞动脉瘤相邻区域出血量较术前增加或可见新发出血灶,或腰椎穿刺呈新鲜血性脑脊液,满足以上任何一项即可确诊为术后出血。
4.统计分析方法 采用SPSS 17.0统计软件进行数据处理与分析。采用单因素Logistic回归模型评价各种因素对再出血的影响,以P≤0.05为差异具有统计学意义。

图1 例1患者手术前后头部影像学所见 1a 入院时头部CTA三维重建提示左侧鞍旁占位性病变(箭头所示),拟诊左颈内动脉床突旁动脉瘤 1b CTA三维重建图显示,动脉瘤呈类圆形(箭头所示) 1c 骨窗三维重建提示动脉瘤位于前床突内侧(箭头所示) 1d CT薄层扫描显示动脉瘤指向前上方(箭头所示)1e 术后横断面CT可见广泛性蛛网膜下腔出血,出血量较大,双侧侧脑室枕角积血 1f 环池、小脑上沟及后纵裂血性信号Figure 1 Preoperative and postoperative head imaging findings of Case 1 At the time of admission,the head 3D reconstruction CTA suggested a leftparasellarspace⁃occupying (arrow indicates),suspected of paraclinoid aneurysm of the internal carotid artery(Panel 1a). 3D reconstruction CTA showed the aneurysm was 1fround (arrow indicates,Panel1b). 3D reconstruction ofbone window suggested aneurysm was on the medial side of the anterior process(arrow indicates,Panel 1c).CT thin⁃layer scan suggested thatthe aneurysm point anteriorly and upward(arrow indicates,Panel 1d). The postoperative axial CT showed a wide range of subarachnoid hemorrhage,and hemorrhage amount was large,hematocele was seen in occipital angle of bilateral lateral ventricle(Panel 1e).Hemorrhagic signals were seen in ambient listern,cerebellum on groove,and back interhemispheric fissure(Panel 1f).
结 果
依据Raymond分级标准,术后即刻DSA显示栓塞率呈Ⅰ级者91例(59.48%)、Ⅱ级25例(16.34%)、Ⅲ级37例(24.18%)。其中,瘤颈>4 mm或瘤颈/瘤体≥0.50的宽颈动脉瘤73例(47.71%),支架辅助栓塞63例(41.18%)。栓塞术中出血2例,占1.31%(2/153),1例术后第4天自动出院,出院时Glasgow昏迷量表(GCS)评分4分,出院4 h死亡(图1);1例术后第6天死亡(图2)。栓塞术后再出血2例占1.31%(2/153),1例再出血发生于术后2周,气管插管呼吸机辅助呼吸,升压药维持血压,术后第22天死亡(图3);1例术后第22天发生再出血,急诊行动脉瘤夹闭术并清除血肿,术后第20天出院,出院时GCS评分13分,1个月后随访时GCS评分15分,6个月后生活自理,12个月随访时病情稳定(图4)。单因素Logistic回归分析显示,高血压病史、多发性动脉瘤、肿瘤位置、脑实质出血、脑室内出血,术前脑室外引流,瘤体最大径>5 mm、宽瘤颈、致密栓塞、瘤颈残留、部分瘤体残留、支架应用等均非栓塞后再出血的危险因素(均P>0.05;表1,2)。
典型病例
例1女性,34岁。主因突发头晕伴恶心、呕吐10余天,于2015年10月28日入院。患者10余天前无明显诱因突发头晕,不能直立,伴恶心、呕吐,呕吐物为胃内容物,外院MRA提示左侧鞍旁类圆形流空信号,约2.50 mm×2.10 mm,诊断为“左颈内动脉床突旁动脉瘤”,为求进一步治疗转入我院,门诊以“左颈内动脉床突旁动脉瘤”收入院。既往史、个人史及家族史无可述及。体格检查神志清楚,双侧瞳孔等大、等圆,直径约3 mm,四肢活动自如;实验室检查无特殊。入院后第3天(10月30日)头部CTA及三维重建提示左颈内动脉床突旁动脉瘤(图1a~1d)。全身麻醉下行左颈内动脉床突旁动脉瘤栓塞术(11月12日),Transend SOFTTIP微导丝导引将Enchlon 10微导管推送至床突旁动脉瘤远端的颈内动脉,后更换为Transend Floppy微导丝及Rebar 27微导管,当微导管上行经过动脉瘤至远端时患者血压骤然升高,收缩压高达215 mm Hg(1 mm Hg=0.133 kPa),导引图下可见对比剂外溢,提示动脉瘤破裂,即刻以0.010X⁃pedion微导丝将4 mm×15 mm Hyperform球囊置于动脉瘤近端,支起球囊,临时阻断左颈内动脉,5分钟后血压降至130 mm Hg,提示出血停止,结束手术。术后对症支持治疗,患者呈深昏迷状态,无自主呼吸,气管插管呼吸机辅助通气,双侧瞳孔等大、等圆,直径7 mm,对光反射消失。术后即刻头部CT提示弥漫性蛛网膜下腔出血(图1e,1f),术后4天(11月16日)自行出院,4小时后死亡。
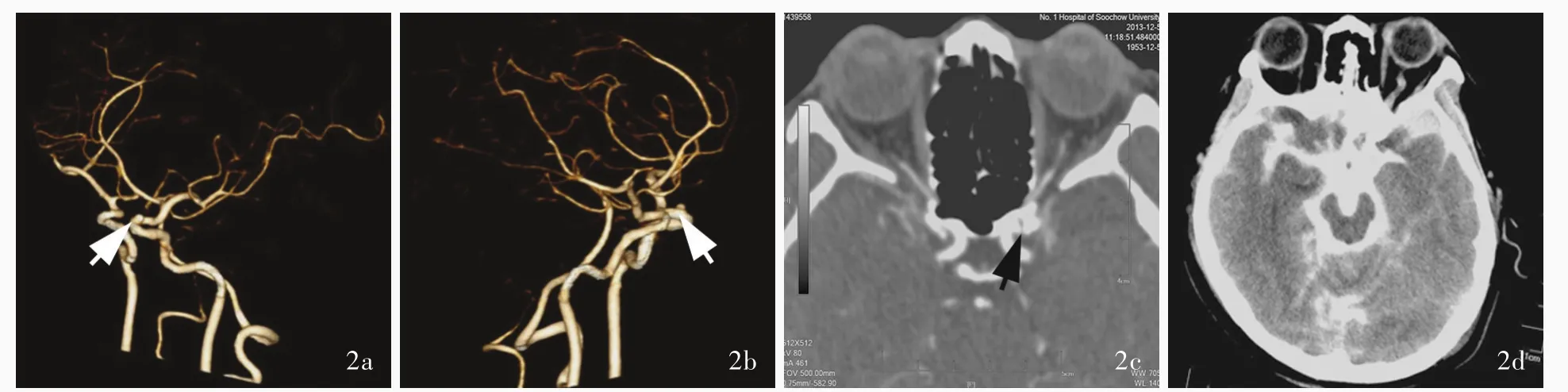
图2 例2患者手术前后头部影像学所见 2a 入院时头部CTA三维重建提示左侧鞍旁占位性病变(箭头所示),怀疑左颈内动脉床突旁动脉瘤 2b CTA三维重建显示动脉瘤呈类圆形,指向后上方(箭头所示) 2c CT薄层扫描提示左侧床突旁动脉瘤(箭头所示) 2d 术后复查头部横断面CT可见广泛性蛛网膜下腔出血Figure 2 Preoperative and postoperative head imaging findings of Case 2 At the time of admission,the head 3D reconstruction CTA suggested a left parasellar space⁃occupying,suspected of paraclinoid aneurysm of the internal carotid artery(arrow indicates,Panel 2a).3D reconstruction CTA showed aneurysm was round,pointing to the upper posterior(arrow indicates,Panel 2b).CT thin⁃layer scan suggested a left paraclinoid aneurysm of the internal carotid artery(arrow indicates,Panel 2c).The postoperative axial head CT showed a wide range of subarachnoid hemorrhage(Panel 2d).
例2女性,49岁。主诉间断性头痛2年、加重6个月,于2015年11月26日入院。患者2年前无明显诱因出现额部胀痛,无明显规律性,自行服用止痛药(药物名称与剂量不详),近6个月以来症状加剧难以忍受,2013年12月5日外院头部CTA三维重建提示“左颈内动脉床突旁动脉瘤”;为求进一步治疗,至我院就医,门诊以“左颈内动脉床突旁动脉瘤”收入院。既往史、个人史及家族史无可述及。入院后体格检查、实验室检查均未见特殊。2015年9月16日头部CTA三维重建提示左颈内动脉床突旁动脉瘤(图2a~2c),2015年11月27日于全身麻醉下行脑血管造影术并左颈内动脉床突旁动脉瘤栓塞术。术前脑血管造影提示瘤体位于眼动脉段,呈囊状、宽颈,大小3.50 mm×3.00 mm、瘤颈3 mm;6F长鞘和6F Chaperon导引导管置入左颈内动脉岩骨段,分别采用Transend SOFTTIP和Transend Platinum微导丝,将Rebar 18和SL⁃10微导管分送至左颈内动脉后交通段和动脉瘤体,释放1枚4 mm×20 mm Solitaire支架并覆盖瘤颈,未解脱支架,当缓慢填塞首枚3 mm×4 cm Axium弹簧圈时患者血压突然升高,收缩压达150 mm Hg,于导引图下可见对比剂外溢,考虑动脉瘤发生破裂,稍撤出微导管,继续填塞2枚Axium 3D弹簧圈(6 mm×20 cm、7 mm×30 cm),另选1枚Enchlon微导管进入左颈内动脉眼动脉段,填塞2枚Axium 3D弹簧圈(6 mm×20 cm),经DSA证实栓塞率达RaymondⅠ级,结束手术。患者术后昏迷,双侧瞳孔不等大,左侧直径6 mm、右侧2 mm,对光反射消失,四肢刺痛无反应,术后即刻头部CT检查提示弥漫性蛛网膜下腔出血(图2d)。术后5天(2015年12月2日)血压逐渐下降,最低降至65/44 mm Hg,心率缓慢,虽经去甲肾上腺素10 mg/h维持血压,终因心跳骤停,抢救无效死亡。
例3女性,40岁。主诉头痛3天伴呕吐10余次,于2016年1月26日入院。患者3天前突发剧烈头痛伴呕吐,呕吐物为胃内容物,发作时不能直立;发病前2天出现视物模糊、视力减退,外院头部CT和CTA三维重建提示“蛛网膜下腔出血,左椎动脉动脉瘤”,予对症治疗(具体方案不详)。为求进一步治疗至我院就诊,门诊以“蛛网膜下腔出血,左椎动脉动脉瘤”收入院。既往史、个人史及家族史无可述及。入院后体格检查无特殊,实验室检查血白细胞计数26×109/L[(3.50~9.50)×109/L]、中性粒细胞24×109/L[(1.80~6.30)×109/L],血清钠离子124 mmol/L(137~145 mmol/L),其余各项指标均于正常参考值范围。1月26日头部CT提示蛛网膜下腔出血(图3a),头部CTA三维重建可见左椎动脉夹层动脉瘤形成(图3b)。1月28日于全身麻醉下行左椎动脉夹层动脉瘤栓塞术,术前DSA造影于左椎动脉V4段可见一囊性突起,大小约为5.75 mm×7.50 mm,小脑后下动脉自瘤体发出(图3c,3d)。Rebar微导管在Transend PLATINUM 0.014微导丝导引下超选择送至椎动脉远端,再以SL⁃10微导管送至动脉瘤体深部约2/3处。首先以3D Axium弹簧圈(4 mm×8 cm)于瘤内成篮,然后选用1枚4 mm×20 mm Solitaire支架覆盖动脉瘤颈部,后再依次填入3 mm×6 cm(1枚)、2 mm×6 cm(3枚)和2 mm×4 cm(1枚)共6枚Axium弹簧圈,术后DSA提示栓塞率达RaymondⅢ级,小脑后下动脉血流通畅(图3e,3f)。术后第2天行腰大池引流并复查头部CT提示蛛网膜下腔出血较前减少(图3g),可见淡红色脑脊液流出,引流量控制在100 ml/d。2月11日患者突然昏迷、呼之不应,脑脊液引流呈新鲜血性液体,考虑动脉瘤再次破裂出血。体格检查呈浅昏迷状态,双侧瞳孔等大、等圆,直径2 mm,对光反射消失;双上肢刺痛无反应、双下肢屈曲;10分钟后转为中度昏迷,血氧饱和度<50%、血压70/40 mm Hg。采取面罩人工辅助呼吸,去甲肾上腺素10 mg/h静脉持续泵入以维持血压,经气管插管呼吸机辅助通气后生命体征平稳,继续对症支持治疗,偶有癫发作,2月20日突发心跳骤停,呼吸、循环衰竭死亡。

图3 例3患者手术前后头部影像学所见 3a 术前横断面CT扫描显示,蛛网膜下腔出血,以四叠体池、双侧小脑上沟出血为主(箭头所示)3b 术前三维重建CTA提示左椎动脉动脉瘤(箭头所示) 3c 正位DSA显示左椎动脉夹层动脉瘤形成(箭头所示) 3d 侧位DSA可见小脑后下动脉由瘤体穿出(箭头所示) 3e 术后即刻左椎动脉DSA显示栓塞率达RaymondⅢ级(箭头所示) 3f DSA显示小脑后下动脉血流通畅(箭头所示) 3g 术后第2天横断面CT提示蛛网膜下腔出血较术前明显减少Figure 3 Preoperative and postoperative head imaging findings of Case 3 Axial CT of preoperation showed subarachnoid hemorrhage,mainly at bilateral superior sulcus cerebellum and quadruple cistern(arrow indicates,Panel 3a).3D reconstruction CTA of preoperation suggested left vertebral aneurysm(arrow indicates,Panel 3b).Orthotopic DSA showed that the left vertebral artery dissecting aneurysm(arrow indicates,Panel 3c).Lateral DSA showed the posterior inferior cerebellar artery originated from the aneurysm(arrow indicates,Panel 3d).Raymond gradeⅢembolism was performed immediately after operation(arrow indicates,Panel 3e).DSA showed that the posterior inferior cerebellar artery remained unobstructed(arrow indicates,Panel 3f). On the second day after operation,axial CT showed that subarachnoid hemorrhage was significantly decreased than that before operation(Panel 3g).
例4男性,51岁。主因突发头痛伴恶心、呕吐5小时,于2014年6月3日入院。患者入院前一天(6月2日)夜间如厕时因突发剧烈头痛伴眩晕、黑蒙摔倒,随即出现左下肢抽搐,发作过程中意识清楚,伴大小便失禁。6月2日外院头部CT提示环池、鞍上池、纵裂池、外侧裂池及部分脑沟高密度影,诊断为“自发性蛛网膜下腔出血”。为求进一步治疗转至我院,门诊以“蛛网膜下腔出血”收入院。既往高血压病史10余年,个人史及家族史无可述及,入院后体格检查及实验室检查无特殊。6月3日头部CTA三维重建提示右前交通动脉动脉瘤,次日(6月4日)于全身麻醉下行前交通动脉动脉瘤栓塞术,术前DSA提示右前交通动脉处有一囊性凸起(图4a),大小约4.10 mm×4.00 mm。于Transend PLATINUM 0.014微导丝导引下,将 Echerlon⁃10微导管超选送至动脉瘤体深部约2/3处,首先采用1枚3 mm×6 cm 3D Axium弹簧圈瘤内成篮,然后依次填入2 mm×4 cm(1枚)、2 mm×2 cm(3枚)、2 mm×2 cm(1枚)共5枚2D Axium弹簧圈,单纯弹簧圈栓塞未使用支架,术后右颈内动脉正位DSA提示栓塞率达RaymondⅢ级(图4b)。术后1小时清醒后拔除气管插管返回病房,予丙戊酸钠500 mg/d口服、20%甘露醇注射液250 ml/次(2次/d)静脉滴注、尼莫地平10 mg/次(2次/d)静脉泵入,以及埃索美拉唑40 mg/d静脉注射,疗程3至7天。术后1周出院,神志清楚,头痛症状明显改善,四肢活动自如,出院前(6月10日)复查头部CT未见明显异常(图4c)。出院后2周(7月1日)因突发意识障碍伴右侧肢体活动障碍10小时再次入院,头部CT检查提示蛛网膜下腔出血,胼胝体区出血。体格检查:神志蒙眬、Hunt⁃Hess分级3级;双侧瞳孔等大、等圆,直径约2.50 mm,对光反射灵敏;左侧肢体肌力5级、右侧为3级,肌张力正常。7月2日于全身麻醉下行血肿清除术并颅内动脉瘤夹闭术。术中可见一囊性凸起指向左侧前下方,周围组织被血肿包裹,考虑动脉瘤复发再次破裂所致;采用Aesculap750型动脉瘤夹夹闭动脉瘤颈,载瘤动脉通畅,手术顺利,术后即刻复查头部CT未见再出血(图4d)。术后继续对症支持治疗,病情好转于7月21日出院,呈嗜睡状态,四肢活动自如,GCS评分13分;头部CT提示病情稳定(图4e)。出院后于外院接受康复治疗,出院1个月后随访,GCS评分15分;6个月时生活能自理;12个月随访时,病情稳定。
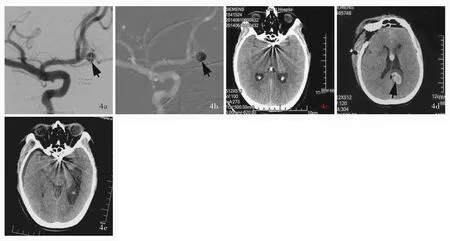
图4 例4患者手术前后头部影像学所见 4a 正位DSA提示前交通动脉动脉瘤,其大小约为4.10 mm×4.00 mm(箭头所示) 4b 术后即刻右颈内动脉正位DSA提示Axium弹簧圈栓塞率达RaymondⅢ级(箭头所示) 4c 出院前(2014年6月10日)横断面CT扫描未见明显蛛网膜下腔出血 4d 动脉瘤复发夹闭术后(2014年7月2日)横断面CT扫描提示蛛网膜下腔出血,脑室内积血(箭头所示) 4e 出院前(2014年7月21日)横断面CT提示脑室内血液基本吸收Figure 4 Preoperative and postoperative head imaging findings of Case 4 Orthotopic DSA showed the diameter of anterior communicating artery aneurysm was 4.10 mm×4.00 mm(arrow indicates,Panel 4a).Postoperative orthotopic DSA angiography showed Raymond gradeⅢembolism(arrow indicates,Panel 4b). Axial CT before discharge(June 10,2014)showed there was no obvious subarachnoid hemorrhage(Panel 4c).After the clipping operation of aneurysm recurrence axial CT showed that subarachnoid hemorrhage and intraventricular hemorrhage(arrow indicates,Panel 4d).Axial CT before discharge(July 21,2014)showed intraventricular hemorrhage disappeared(Panel 4e).
讨 论
颅内动脉瘤于栓塞术中破裂出血是最为严重的并发症,病死率及病残率极高,文献报道的发病率为2%~5%[6]。本文2例术中出血患者均发生于动脉瘤栓塞过程中的“早期”,例1动脉瘤体积为2.50 mm×2.10 mm,微导管置入动脉瘤体时发生破裂出血,考虑与微导管推送操作不当有关;例2为小体积动脉瘤,大小约为3.50 mm×3.00 mm,支架释放后填塞第1枚弹簧圈时动脉瘤破裂出血,术后总结出血原因,可能与支架释放后使动脉瘤腔内的操作空间更为狭小,而且所选用的弹簧圈较大填塞时致动脉瘤破裂出血。对于小体积的动脉瘤,应避免微导丝和微导管直接接触动脉瘤顶端,使其受力;对于支架释放后操作空间的缩小,可以选择较小且韧性良好的弹簧圈,提高安全系数。术中动脉破裂出血患者,应即刻以肝素中和并迅速完成动脉瘤栓塞,出血严重者可于术后施行脑室外引流。有研究显示,急性蛛网膜下腔出血或操作空间狭小的小体积动脉瘤是颅内动脉瘤栓塞术中出血相关危险因素[7],究其原因可能与操作或选材失当有关,诸如微导丝、微导管推送操作不当或所用材料质地较硬致瘤体破裂,以及弹簧圈过度填塞,或所用弹簧圈为体积较大、质地较韧的3D弹簧圈[8]。若术中动脉瘤破裂出血后微导管尖端依然位于瘤体内,一般继续填塞即可达到止血目的,甚至部分弹簧圈可留在瘤体外、蛛网膜下腔内;也可另选一支微导管推送至瘤体内,然后继续填塞,仍可取得较好疗效[9⁃10]。有学者指出,动脉瘤破裂的时期对患者预后极为关键,于栓塞术早期发生的动脉瘤破裂出血致死性更高[11];而栓塞术后期出现的出血,目前认为不必追求完全致密填塞,瘤颈残留更为安全,可通过二期手术再行致密栓塞[12]。栓塞术中动脉瘤破裂出血后,首先须明确诊断,然后即刻予肝素中和出血,并继续快速完成填塞,同时监测颅内压、血压变化,术后行脑室外引流[13]。

表1 栓塞后再出血影响因素变量赋值表Table 1. Variable assignmentoffactors associated with bleeding after embolization

表2 栓塞后再出血影响因素的单因素Logistic回归分析Table 2. Univariate Logistic regression analysis of factors associated with bleeding after embolization
颅内动脉瘤栓塞术后再出血率为0.90%~2.70%,导致栓塞术后再出血的原因包括动脉瘤栓塞不完全、小体积动脉瘤(<6 mm)、前交通动脉瘤、入院时Hunt⁃Hess分级、宽颈动脉瘤术中是否使用支架、术后是否应用抗血小板药、循环血压控制不良等[14]。本组153例患者栓塞术后再出血率为1.31%(2/153),与既往研究结果基本相一致[15]。我们尝试对患者年龄、性别、既往高血压病史、是否伴有颅内出血或脑室内出血,动脉瘤体积、瘤颈大小、位置、栓塞程度,以及是否使用支架等因素对颅内动脉瘤栓塞术后再出血危险因素进行分析,但经统计分析未筛查出危险因素,精简上述因素进一步代入Logistic回归方程仍未显示出统计学意义,今后我们将进一步扩大样本量继续开展此方面的研究。既往文献提示,栓塞程度(Raymond分级)与栓塞后再出血存在一定关联性[16],本组2例术后出血患者Raymond分级均为Ⅲ级,因此我们高度怀疑栓塞不完全是术后再出血的重要危险因素,根据流行病学调查显示,约有50%行动脉瘤栓塞术的患者于术后3天内出现动脉瘤再出血。
目前关于动脉瘤是否必须进行致密栓塞仍存争议[17],虽然大部分颅内动脉瘤再出血病例中以不完全性栓塞者居多,然而致密栓塞即达到RaymondⅠ级者亦仍有再次出血发生。本文2例栓塞后再出血患者均与动脉瘤栓塞不完全有关,其中1例(例3)术前CTA和术中DSA均显示为左椎动脉夹层动脉瘤,“酒窝征”十分明显,提示动脉瘤体内有血栓形成,经支架辅助栓塞后,DSA显示栓塞率为RaymondⅢ级,瘤体内部分显影,导致该患者栓塞术后再出血原因主要为动脉瘤内血栓形成,无法达到致密栓塞,术后14天再出血。另1例患者(例4)术前CTA提示右前交通动脉动脉瘤,术中未选择支架辅助治疗,仅以6枚弹簧圈对动脉瘤进行栓塞,术后即刻DSA提示栓塞率为RaymondⅢ级,瘤颈及部分瘤体显影,提示非致密栓塞;患者住院6天出院,于术后25天发生再出血。在有些情况下,尽管影像学上达到致密栓塞即RaymondⅠ级,但仍不能完全避免动脉瘤再次出血,这是由于弹簧圈分布不均匀使瘤腔内形成许多小通道,导致血流重新进入瘤体,或瘤腔内血栓溶解而诱发再出血[18]。动脉瘤破裂后瘤腔内血栓形成,此时影像学检查所显示的动脉瘤体积小于其实际体积,这种小体积动脉瘤是栓塞术后再出血的重要危险因素之一[19],本文例1患者术后动脉瘤再次破裂出血即是由于瘤腔内血栓形成而无法致密栓塞所致。但也有学者认为,即使术后即刻DSA显示栓塞率达到RaymondⅠ级,然而栓塞后弹簧圈持续压迫动脉瘤壁出血部位,导致其内膜营养供应减少、瘤壁变薄,最终破裂出血处瘤壁再破裂、弹簧圈脱出,发生再出血[20]。因此,对于非致密栓塞的患者术后应早期行DSA复查,及时发现危险、及时处理,改善患者预后。
利益冲突 无
