2013—2020年7次实验动物病原菌项目国际比对结果分析
2021-01-02冯育芳张雪青岳秉飞
邢 进, 冯育芳,王 洪,张雪青,高 强,岳秉飞,付 瑞
(中国食品药品检定研究院实验动物资源研究所,北京102629)
国际实验动物科学理事会(International Council for Laboratory Animal Science,ICLAS)在2007 年建立了诊断实验室性能评估程序(Performance Evaluation Program for Diagnostic Laboratories,PEP)(简称“国际比对”)。通过ICLAS提供的PEP标准样品,各参加实验室能够评估自身的检测水平和能力[1]。参加PEP活动有助于检测实验室使用科学可靠的程序来监督检测质量,同时可获得国际同行专家的帮助和建议,促进实验室实施质量保证措施,有助于提高动物质量检测技术、水平和能力,确保实验动物的质量[2]。样品由经国际认可的实验室制备和确认后,发送给世界各地想要参加PEP活动的实验室进行比对检测。样品均为盲样,当前的PEP样品库包括可以感染大鼠和小鼠的常见病原体,涉及病毒、病原菌和寄生虫。每次PEP活动需要检测10 个或20 个样品,可能是病毒、细菌、真菌、寄生虫等病原样品和微生物抗体血清样品的不同组合。PEP对检测方法没有限制,参加实验室依据自身检测体系和能力开展检测,所得结果与ICLAS反馈的预期结果相比较,对检测方法的特异性和敏感性进行监测和评估[3]。2020年的PEP活动共有21个实验室参与,其中亚洲6个、大洋洲2个、欧洲9个和北美洲4个[4]。
2013—2020 年,本实验室共参与了7 次ICLAS 的PEP 活动(2015 年未参加),是参加次数最多的国内实验室。病原菌项目在PEP中占有很大比例,本文针对病原菌部分进行总结,对国内实验动物的病原菌检测项目和方法起到查漏补缺的作用,以促进我国实验动物质量控制的发展。
1 材料与方法
1.1 培养基和试剂
哥伦比亚血琼脂培养基为英国Oxiod 公司产品;无菌脱纤维羊血为北京陆桥技术股份有限公司产品;DHL琼脂培养基、高盐甘露醇琼脂培养基为北京三药科技开发公司产品;革兰染色液为法国生物梅里埃公司产品,细菌鉴定板为美国BD公司和法国生物梅里埃公司产品;DNA提取试剂盒为德国Qiagen公司产品;PCR试剂为日本TaKaRa 公司产品;荧光定量反应预混液为美国Applied Biosystems 公司产品;普通PCR 引物由生工生物工程(上海)股份有限公司合成;荧光定量PCR引物和探针由美国Invitrogen公司合成;羊抗小鼠、大鼠辣根过氧化物酶为美国KPL公司产品;支原体的酶联免疫吸附测定(enzymelinked immunosorbent assay,ELISA)试剂和泰泽病原体的间接免疫荧光法(indirect immunofluorescence assay,IFA)检测试剂均由本实验室自制;泰泽病原体ELISA和CAR杆菌、肺孢子菌ELISA检测试剂盒购自苏州西山生物技术有限公司。
1.2 仪器设备
生物安全柜购自美国Nuaire公司(型号NU-437-400S);恒温培养箱购自美国Thermo 公司(型号IGS180);细菌鉴定仪购自美国BD 公司(型号Phoenix100)和法国梅里埃公司(型号Vitek2 Compact);酶标仪购自美国Thermo 公司(型号MK3);冷冻离心机购自德国Hettich 公司(型号22R);PCR 仪购自美国ABI 公司(型号Verit96);荧光定量PCR 仪购自美国ABI 公司(型号7500Fast);电泳仪购自美国Bio-rad 公司(型号Powerpac HC);紫外凝胶成像系统购自美国Kodak公司(型号GL212pro)。
1.3 PEP样品
7次PEP样品共90份,包含病毒、细菌、真菌、寄生虫和微生物抗体5 个种类,见表1。样品经冷链干冰运输,到达本实验室后,保持内包装完整,置于-80 ℃冻存。经海关监管检查后方开展实验。PEP 样品的最小包装为螺口1.5~2.0 mL 冻存管。根据ICLAS 提供的样品清单,含细菌样品32 份、真菌样品1 份、寄生虫样品2份、病毒样品15 份和40 份微生物抗体样品。在抗体样品中也包含病原菌检测项目。细菌培养或抗体检测样品体积均0.5 mL,真菌DNA 样品体积0.1 mL。

表1 7次PEP样品的病原种类Table 1 Pathogeny types of seven batches of PEP samples
1.4 样品培养
依据国家标准[5],先对细菌样品进行培养和生化鉴定。用接种环蘸取样品液接种于5%血琼脂培养基、DHL 琼脂和高盐甘露醇琼脂培养基,36 ℃需氧培养24~48 h,记录菌落形态。挑取典型单个菌落,相同条件次代培养后,用自动细菌鉴定仪鉴定。
1.5 抗体检测
依据国家标准[6-7]或试剂盒说明检测微生物抗体样品。将5倍PBS稀释的待检样品用PBS再稀释10 倍或2 倍,至体积比为1∶50 或1∶10,然后分别用于ELISA和IFA检测。
1.6 核酸检测
通过前期的样品培养,对已分离到病原菌的样品,提取目标菌基因组DNA,扩增16S rDNA,将序列比对结果与生化鉴定结果相互验证。当采用培养法未见病原菌生长时,吸取20 μL样品原液,提取DNA,扩增其16S rDNA。同时采用特异引物(表2)扩增可疑病原。对细菌DNA样品则直接扩增16S rDNA,对真菌DNA的样品扩增ITS 序列。目的片段送生工生物工程(上海)股份有限公司测序,所得序列在Genbank (https://blast. ncbi. nlm. nih. gov/Blast.cgi)中进行序列比对。
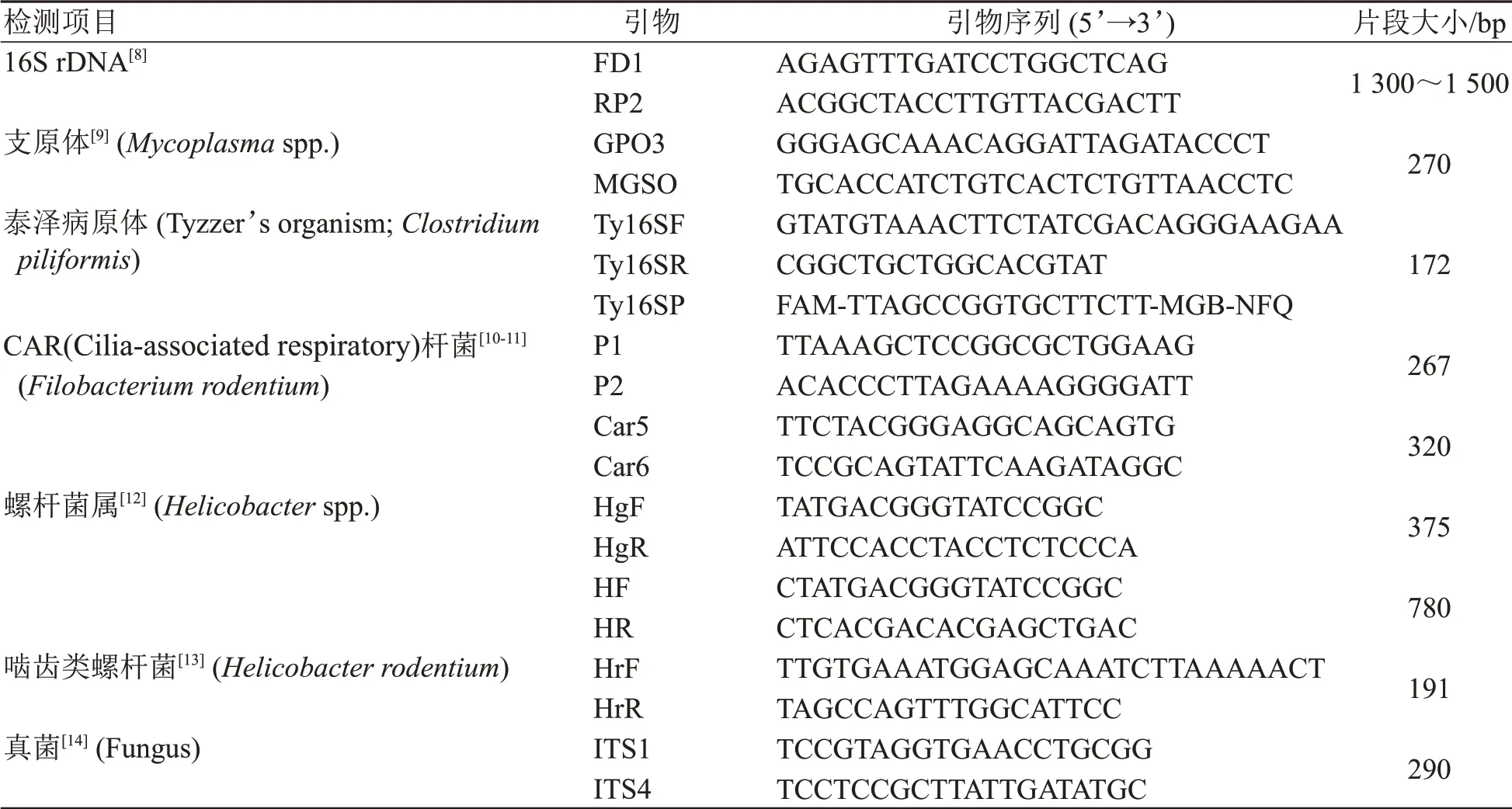
表2 7次PEP项目中所用PCR引物和探针Table 2 Primers and probe used in seven PEP projects
2 结果
2.1 预期结果
向ICLAS提交检测结果后,即获得当次PEP样品的预期结果,见表3。

表3 7次PEP病原菌项目汇总Table 3 Summaries of pathogenic bacteria in seven PEP projects
7次PEP病原菌项目共40份样品,涉及27种病原菌;其中,病原检测33 项(含活菌样品29份、核酸样品4 份),抗体检测7 项(抗体样品7份)。与预期结果相比较,本实验室7 次PEP 检测结果的符合率分别为8/8、2/2、5/8、9/9、5/5、6/7和1/1,见表4。

表4 检测方法和结果符合率Table 4 Test methods and coincidence rates of results in seven PEP projects

续表
2.2 不符合项目
全部40份病原菌样品中,有以下4个项目的检测结果出现偏差:(1)2016 年的41-7 CAR 杆菌血清样品检出腺病毒(Adenovirus)抗体阳性,未检出目标抗体CAR 杆菌抗体;(2)41-8大鼠血清中检出淋巴细胞脉络丛脑膜炎病毒(lymphocytic choriomeningitis virus,LCMV)抗体阳性,未检出泰泽病原体抗体;(3)将41-15乳腺炎棒状杆菌(Corynebacterium mastitidis)误鉴定为眼棒状杆菌(Corynebacterium oculi);(4)在52-5 小鼠粪便中检出泰泽病原体核酸阳性,漏检啮齿类螺杆菌。
3 讨论
PEP 网站公布的现行样品库为2012 版[15],包括小鼠和大鼠两种动物的样品。其中,小鼠样品35项,病原菌和病毒分别为21项和14项;大鼠19 项,病原菌11 项,病毒7 项,寄生虫1 项。本实验室参与的7次PEP活动中,共40份病原菌样品,涉及27 种病原,样品全部为液体,分为病原检测和抗体检测两种类型。样品形式涵盖菌液、水、气管冲洗物、血清、核酸等,采用病原菌培养、抗体检测和核酸检测3种方法。在27种病原菌中,绿脓杆菌、肺炎链球菌、辛氏鲍特菌、假结核耶尔森菌、乳腺炎棒状杆菌、肺炎克雷伯杆菌、大肠埃希菌和念珠状链杆菌这8种细菌超出了PEP样品库的范围,说明样品库仅为基础项目,实际检测项目仍在不断更新。相比而言,我国实验动物质量检测标准涉及的病原菌种类尚有欠缺,一些检测项目在我国缺少相应标准,比如PEP样品中出现的辛氏鲍特菌、黏质沙雷菌、乳腺炎棒状杆菌、CAR杆菌、小鼠放线杆菌、弗劳地枸橼酸杆菌、产酸克雷伯杆菌、无乳链球菌和致病性大肠埃希菌这9个项目,以及尚未出现的嗜麦芽假单胞菌(Stenotrophomonas maltophila)、兽 疫 链 球 菌(Streptococcus zooepidemicus)和弯曲菌属(Campylobacterspp.)等(后两项为Charles river检测项目)。在检测工作中,以上病原菌偶有检出,应引起重视,并尽快制定相应的检测标准。
我国实验动物质量检测标准中的检测技术和方法亟待补充和更新。PEP的微生物样品均为盲样,对检测方法不做要求。采用分离培养方法时,需要考虑到培养的温度、气体环境、时间等条件,检测过程复杂。根据ICLAS网站公布的检测项目,血琼脂平板可以满足绝大部分采用培养法检测病原菌的生长需要。根据在血琼脂平皿上的生长特性,并参考在DHL 和高盐甘露醇等选择性培养基上的生长状态,可直接缩小检测范围。对于单一病原的样品,检测过程相对简单,同时采用16S rDNA 测序的方式则更为简便。如根据样品信息缩小检测范围,采用特异的PCR方法会事半功倍。34-9、44-13 和52-5 样品在血琼脂中未见菌落生长,直接对样品提取DNA,通过特异性PCR 检测,以及16S rDNA 测序验证,得到啮齿类螺杆菌和肺支原体的结果。因培养法较为费时,对44-13 肺支原体样品直接按核酸样品检测。肺孢子菌(Pneumocystisspp.)是一类条件致病真菌,国际上将其列为真菌检测项目。现行的国家标准GB/T 18448.4—2001规定了卡氏肺孢菌(Pneumocystis carinii)的染色镜检方法仍作为寄生虫检测项目,对检测人员水平和样品要求较高[16]。44-19 小鼠肺孢子菌为真菌DNA样品,本研究中使用真菌通用引物ITS1/ITS4 扩增和测序获得了结果。此外,病原菌名称也在不断更新变化。大肠埃希菌O115a,c:K(B)更新为啮齿类枸橼酸杆菌[17],CAR 杆菌的拉丁名称更新为Filobacterium rodentium[18],嗜肺巴斯德杆菌Heyl 生物型更新为Rodentibacter heylii[19]。建议尽快修订相关标准,与国际标准名称一致。2017年中国实验动物学会颁布了首批团体标准,其中涉及牛棒状杆菌的实时荧光PCR检测方法,以及螺杆菌的普通PCR 和实时荧光PCR检测方法;针对其他不易培养的病原菌,如泰泽病原体、CAR杆菌、支原体等,也应尽快制定相应的分子生物学检测标准,助力实验动物质量检测。
检测试剂与菌种资源的缺乏亟需解决。血清样品可能存在多种病原抗体的情况,如41-7 和41-8样品同时检出腺病毒和LCMV抗体,44-6样品(鼠腺病毒2 型血清样品,表3 中未列出)检出泰泽病原体抗体;这可能与制备时的动物血清本底有关,更要求检测试剂具有良好的特异性和敏感性。CAR 杆菌、兔脑原虫等ELISA 检测试剂盒仍然需要进口,国内缺少自主知识产权的检测试剂,限制了检测工作的开展。例如,41-15样品的生化鉴定结果是眼棒状杆菌,16S rDNA序列与乳腺炎棒状杆菌(Genbank AY834747.1)和眼棒状杆菌(Genbank KJ938710.1)符合度分别为99.09%和97.00%,结合眼部病灶分离菌的备注提示,判定为眼棒状杆菌(系错误结果)。可见在实际检测中遇到新发病原菌时,设置阳性菌株对照很重要,而且应对生化结果进行验证,须结合测序结果和文献报道来慎重判定。再如,52-5 的小鼠粪便样品检测结果是啮齿类螺杆菌,核酸检测结果却是泰泽病原体,对粪便革兰染色也同样提示梭菌,最终导致螺杆菌漏检。因此,如能建立同时检测多种病原的高通量抗原和抗体芯片检测方法,将会极大地促进实验动物微生物检测水平的提升。
经过连续参加PEP活动,充分评估和验证了本实验室的检测能力。目前我国实验动物质量检测水平仍不均衡,在检测新技术应用、病原检测种类方面与国际水平尚存在差距。我国实验动物质量检测项目的设置有较大局限性,国家标准中的检测方法相对落后,病原名称、检测方法和技术有待更新,检测试剂亟需开发。同时,本实验室作为能力验证提供者,在PEP活动中也获得了丰富的经验,这将有助于国内能力验证活动的改进,以促进国内实验室检测能力进一步提高。
