极谱仪-阳极溶出伏安法测定大米中镉的方法研究
2020-12-30张雷
张 雷
(辽宁省生态环境监测中心,辽宁 沈阳 110000)
前言
随着科技的发展,加上治理方法仍未完善,镉污染在电镀业、冶炼厂、矿石开采等作为副产物出现,以废气粉尘形式沉降于周围土壤,或以污水形式污染周边水体,最后间接污染土壤。据统计,全球每年向环境中排放的镉总量达到3万t左右,其中约85%进入土壤,水稻是对镉吸收最强的谷类作物。医学文献已经证明,镉进入人体,多年后可引起骨痛等症,严重时导致可怕的“痛痛病”[1]。我国现行的《粮食卫生标准》(GB 2175-2016)和《食品安全国家标准 食品中污染物限量》(GB 2762-2017)中规定大米中镉的限量值为0.2mg·kg-1,与欧盟一致,严于CAC、日本和泰国[2]。
目前,大米中镉的测定常采用石墨炉原子吸收法,方法较为成熟,但仪器耗材费用较高,且方法受基体影响较大[3]。本文采用极谱仪-阳极溶出伏安法进行大米中镉的测定,运用标准加入法进行分析测定,仪器操作简便,分析成本低,灵敏度高,选择性好,抗干扰能力强,且废液便于回收处理,环境污染小[4],方法开展了样品的前处理条件的选择及仪器工作条件的优化和确定研究,形成适用于大米中镉的测定方法,对大米镉超标控制具有实际意义。
1 实验原理
大米样品采用干灰化法进行消解,用1%硝酸溶液溶解定容形成溶液,加入到极谱仪的反应槽中,溶液中的金属镉离子在一定电位下,部分还原成金属镉,析出于汞电极表面,然后向电极施加反向电压,使汞电极上的金属镉氧化而产生氧化电流,根据氧化过程的电流—电压曲线进行分析测定。
2 材料与方法
2.1 实验材料
2.2.1 实验仪器
884 Professional VA型极谱仪(瑞士万通),分度值为0.1mg的电子天平(梅特勒-托利多),FO810C型马弗炉(雅马拓),PB-10型pH计(塞多利斯),可调式电炉,一般实验室常用仪器和设备,本方法所用玻璃量器除非另有说明,分析时均使用符合国家标准的A级玻璃量器。
2.2.2 实验试剂
浓硝酸(HNO3),氯化钾(KCl),汞(>99.999%),乙酸,氨水,镉标准贮备溶液(ρ=100mg·L-1),氮气(纯度大于99.99%),非另有说明,分析时均使用符合国家标准的分析纯化学试剂,实验用水为新制备的去离子水。
3 结果与讨论
3.1 仪器工作条件的优化和确定
3.1.1 预电解电位的确定
在相同的仪器条件下,分别对1%硝酸介质中含镉浓度为4μg·L-1的样品进行6次测定,溶出峰电位在-0.552~-0.553V变动,6次平值均为-0.553V。参考《化学试剂 阳极溶出伏安法通则》(GB/T 3914-2008)的规定,选定预电解电位应比待测物在该测定条件下的溶出峰电位-0.2V以上[5],确定-0.75V为本实验的预电解电位。
3.1.2 预富集时间的选择
参考《化学试剂 阳极溶出伏安法通则》(GB/T 3914-2008)的规定,预电解富集时间不少于1min,不多于10min,在测定过程中此值应保持恒定[5]。分别对含镉浓度为4μg·L-1的样品进行不同富集时间的6次测定,由图1可知,在其他条件相同的情况下,采用富集时间为120s峰电流灵敏度高、RSD较小,因此,本方法选择的预富集时间为120s。
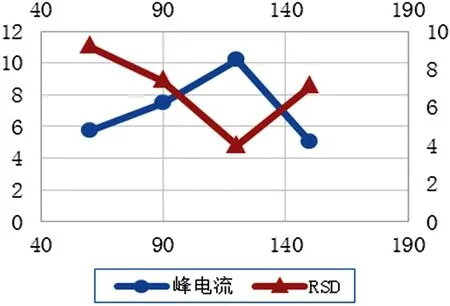
图1 预富集时间与峰电流及其稳定性的关系
3.1.3 扫描电位范围的选择
扫描电位范围应包括待测物的溶出峰。综合多次实验数据可以得出,扫描电位在-0.75~0.00v时,可保证Cd能完整出峰,故选择此电位范围。
3.1.4 搅拌速度的选择
根据电化学原理,极限扩散电流与搅拌转速有关。实验选择了0rpm、1000rpm、2000rpm、3000rpm,通过对Cd含量分别为4.0μg·L-1的溶液进行平行6次扫描,确定最佳搅拌速度。实验结果如图2所示。
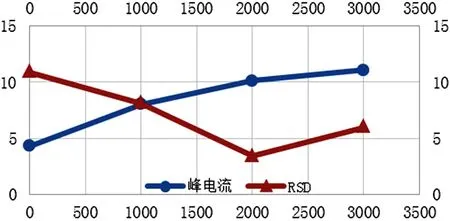
图2 搅拌速度与峰电流及其稳定性的关系
实验结果表明,搅拌速度增大时,Cd的电流强度增大;不搅拌时,Cd出峰稳定性差且电流强度低;搅拌达到3000rpm时,虽然电流强度最大但稳定性降低。因此本方法选择2000rpm为最佳搅拌速度。
3.2 前处理方法的确定
3.2.1 灰化条件的选择
3.2.1.1 国家标准方法《食品安全国家标准 食品中镉的测定》(GB 5009.15-2014)
前处理部分中的干灰化法进行样品消解:称取0.3~0.5g干试样(精确至0.0001g)于石英干锅中,先小火在可调式电炉上碳化至无烟,移入马弗炉500℃灰化6~8h,冷却。若个别试样灰化不彻底,加1mL混合酸在可调式电炉上小火加热,将混合酸蒸干后,再转入马弗炉中500℃继续灰化1~2h,直至试样消化完全,呈灰白色或浅灰色。放冷,用硝酸溶液(1%)将灰分溶解,将试样消化液移入10mL或25mL容量瓶中,用少量硝酸溶液(1%)洗涤坩埚3次,洗液合并于容量瓶中并用硝酸溶液(1%)定容至刻度,混匀备用[6]。
3.2.1.2 本研究采用方法
称取0.3~0.5g干试样(精确至0.0001g)于石英干锅中,先小火在可调式电炉上碳化至无烟,移入马弗炉600℃灰化6h,直至试样消化完全,呈灰白色或浅灰色;放冷,用硝酸溶液(1%)将灰分溶解,将试样消化液移入25mL或50mL容量瓶中,用少量硝酸溶液(1%)洗涤坩埚3次,洗液合并于容量瓶中并用硝酸溶液(1%)定容至刻度,混匀备用。

图3 国标方法条件试验 图4 本研究方法条件试验
分别采用上述2种方法进行灰化实验,图3为采用国家标准方法,500℃灰化6h后结果,图4为600℃灰化6h后结果。可以看出,采用国标方法灰化后的部分样品仍存在黑色,灰化不彻底,需要加混合酸进行进一步灰化;而在采用600℃灰化6h的条件下,样品能够灰化完全。因此,本实验选择采用的灰化条件为600℃灰化6h,不仅节省大量的时间,还避免了硝酸、高氯酸的使用。
3.2.2 定容介质的选择
按照3.2.1中确定的条件对大米样品进行前处理,分别以纯水和1%硝酸溶液进行灰分的溶解和定容,在相同极谱仪器条件下测定,结果如表1。

表1 不同定容介质测定结果比对表
结果表明,2种定容介质下,仪器测定结果的RSD并无明显变化,但采用酸定容的样品峰电流响应值要比水定容的更加灵敏,且灰化后的样品能够在1%硝酸介质中完全溶解,而在纯水介质中可见明显沉淀物。因此,选择1%硝酸介质来进行样品的溶解与定容。
3.2.3 缓冲溶液的选择
选取镉含量为4μg·L-1的样品,验证其在不同pH值下的峰电流。根据本实验室的数据,发现pH的改变影响金属离子的活性,pH值过高,样品中的金属离子易被生成的胶体所吸附,从而降低被测金属离子的活性;pH过低,受氢波的干扰。最终确定采用55.5mL 100%乙酸加37mL 25%氨水,定容至500mL(此溶液pH约为4.6),作为本研究的缓冲溶液,结果如图5。

图5 不同pH值下镉峰电流
4 结论
综上所述,本研究采用600℃灰化6h的消解条件,消解后样品用1%硝酸溶液溶解,选用乙酸-氨水(pH约为4.6)作为缓冲溶液上机测试;确定仪器工作条件为:扫描电位范围-0.75~0.00V,预富集电位-0.75V,预富集时间120s,搅拌速度2000rpm。
