小麦苗期氮素响应的生理及分子差异研究
2020-12-21徐晴许甫超秦丹丹刘小强袁旭葛双桃董静
徐晴 许甫超 秦丹丹 刘小强 袁旭 葛双桃 董静
摘要:为探明小麦幼苗对不同氮素浓度的响应差异,设置高、低2种氮素浓度对12个不同基因型小麦进行营养液沙培,研究不同处理间小麦幼苗植株鲜重、叶片叶绿素含量、根系形态等的差异,并对植株谷氨酰胺合成酶(GS)活性以及氮素吸收利用相关基因表达差异进行分析;同时,根据不同基因型小麦材料的植株鲜重对其氮素利用效率进行评价。结果表明,氮素充分供应可显著提高植株鲜重;低氮条件下植株根冠比显著大于高氮水平下数值;氮素缺乏可以促进主根伸长、总根长和总根表面积的扩大,且不同基因型间主根长度差异显著。幼苗的叶绿素含量随着氮素浓度升高而增加。不同氮素浓度处理下小麦幼苗叶片的谷氨酰胺合成酶活性在小麦各基因型间表现不同。小麦TaNRT1.1和TaNRT2.1基因在低氮处理下表达量较高,且高氮效材料郑麦9023和“410187”中2个基因的转录量高于低氮效材料南农08Y611中的转录量。氮素浓度正向调控氮素同化基因TaGS2的表达,而TaGS1表达量则在基因型间和氮素处理间差异不大。
关键词:小麦;苗期;氮素响应
中图分类号:S512
文献标识码:A
文章编号:0439-8114( 2020) 20-0039-07;
DOI:10.1408 8/j .cnki.issn0439-8114.2020.20.009
氮素是小麦产量形成的关键因子,它参与植物体内核酸、蛋白质和氨基酸合成,调控植株生长发育的多个进程,对植物生长发育起重要的作用[1]。然而,目前土壤当季氮肥利用率仅有30%-50%,其余均以淋溶、挥发的形式流失,对农业经济和环境造成了很大损失和破坏[2]。小麦作为中国第二大粮食作物,氮肥需求量大,因此,采取栽培和遗传措施提高小麦新品种的氮素利用效率至关重要。
苗期是小麦生长发育的重要时期,它形成小麦植株最初的生物量,以对抗苗期胁迫和奠定后期生长基础。苗期氮素吸收主要由根系完成,且根系吸收氮素受周围氮素浓度调控[3]。低氮条件下,根系体积扩大以增加对氮素的吸收量满足植物体的营养需求,高氮条件下则反之[4]。氮素水平还影响植株叶绿素的合成和光合作用,从而影响植株生物量的形成[5]。王平[6]采用水培的方式对128份小麦材料苗期氮素利用效率进行研究,发现随着氮素浓度的升高,小麦植株干重、鲜重等随之增加,且不同供氮水平对根系形态有显著影响。汪晓丽等[7]对小麦苗期根系的研究认为,植株地上部和根系生物量随着氮素浓度提高而增加,高氮浓度可抑制总根长和根表面积。此外,氮素代谢途径中的关键酶,特别是硝酸还原酶(NR.nitrate reductase)和谷氨酰胺合成酶(GS,Clutamine synthase)活性也存在不同氮素供应间的差异。王琳琳等[8]对小麦苗期氮代谢相关指标研究表明,NR和GS活性均随着氮素浓度升高而升高。不同氮素浓度下,植株氮素吸收调控分子机制也有不同[9]。NRT1(Nitrate transporter 1)和NRT2(Nitrate transporter 2)基因家族分别负责高浓度和低浓度下氮离子的转运[10]。拟南芥AtNRT2.1基因在氮素胁迫条件下上调表达[11]。GS1(glutamine syn-thase 1)和GS2 (glutamine synthase 2)基因作为铵根离子同化过程中的关键基因,已经被证明对作物氮素利用效率的提高和产量形成具有重要作用[12]。小麦苗期氮素胁迫可造成约4 000多基因表达的变化,且根系基因变化数目大于叶部[13]。
鉴于低氮胁迫处理下小麦幼苗根系形态不同研究结果存在差异[ 13.14],且相关研究多采用水培和土壤盆栽[6-8],盆栽种植受种质研究份数限制;而水培若条件控制不好(黑暗环境和持续的氧气供应),易造成苗期根系胁迫,影响试验数据准确性。因此,本研究采用沙培的方式,模拟根系正常生长环境,设置不同氮素水平,以12份湖北省不同时期审定的主要小麦品种和外引骨干亲本为材料,比较小麦植株苗期不同氮素浓度响应的生理形态和分子变化;同时,鉴定与小麦氮素利用效率密切相关的苗期性状,筛选苗期氮素高效小麦材料,为进一步明确小麦苗期氮素响应机制和培育氮素高效的小麦品种提供依据。
1 材料与方法
1.1 试验材料
供试材料为12个湖北省不同时期审定小麦品种和骨干亲本材料:郑麦9023、鄂麦006、鄂麦398、鄂麦251、“410187”、襄麦35、荆麦66、华1223、“1168”、百农矮抗58、南农08Y611、“366”。
1.2试验方法
1.2.1 种子处理小麦材料于2018年12月在湖北省农业科学院洪山區南湖试验基地温室种植。种植前,每株系挑选30颗饱满、大小均匀一致的种子,用10%双氧水处理5 min,然后用去离子水冲洗干净置于垫有3层湿润的吸水滤纸的培养皿中,22 qC培养箱中保持3d,促进发芽。发芽后每株系每处理挑选10棵生长一致的幼苗转入提前用营养液浸湿装有黄沙的96孔穴盘中,每穴一株。
1.2.2 营养液沙培处理前,选取黄沙,用流水淘洗干净直到水清澈为止(沙里不含任何土和腐殖质)。用不同氮素浓度的营养液浇灌,对小麦幼苗进行培养。营养液配方参考He等[15],略有修改,具体如下:Ca(NO3)2(0.2 mmol/L或2mmol/L), 0.2 mmol/LKH2PO4, 1.0 mmol/L MgSO4, 1.5 mmol/L KCI, 1.5 mmol/LCaC12,1×10-3mmol/L H3803,5×10-5mmol/L (NH4)6MO7O24,5×10-4mmoI/LC uSO4,1×10-3mmioI/L ZnSO4,1×10-3mmol/LMnSO4, 0.1 mmol/L Fe(lll) -EDTAn
1.2.3 氮素处理上述营养液中以Ca(NO3)2为氮源,设置低氮(0.2 mmol/L)和高氮(2.0 mmol/L)2个浓度,每个培养箱的营养液为2L,每3d更换一次营养液。培养21d后,测定不同品种(系)植株总鲜重、地上部和根系鲜重、叶绿素含量(SPAD值)、主根长、总根长、总根表面积和植株地上部GS酶活性,并采用液氮速冻部分材料用作基因表达分析。
1.3 性状测定指标及方法
苗期地上部、根系鲜重:从根基部起分成地上部和根系,分别测定重量。
根系性状测定:采用RhizoScan扫描仪对主根长、总根长和总根表面积进行测定。
叶绿素含量测定:采用SPAD-502 Plus叶绿素测定仪对生长3周的小麦植株最上部完全展开叶的叶片中部叶绿素含量进行测定,测定3次,取平均值进行计算。
CS酶活性测定:对植株地上部分混合取样(新鲜材料)0.1 g,采用谷氨酰胺合成酶(GS)活性检测试剂盒(北京索莱宝科技有限公司)进行检测。
1.4 基因表达分析
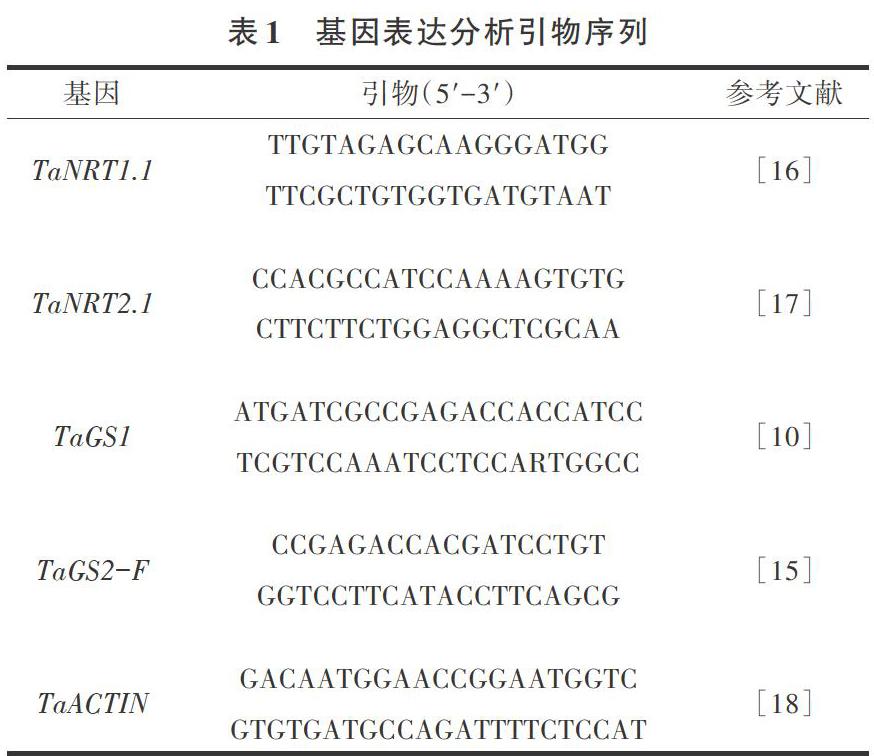
采集不同处理下生长3周的小麦植株,液氮速冻,-80℃保存备用。RNA提取采用OMEGA植物提取试剂盒进行,操作按照试剂说明书进行。cDNA合成按照Primerscript RT reagent kit进行操作。氮素吸收利用相关基因引物序列根据前人研究合成[10,15-18],并在网站( http://202. 194. 139.3 2/blast/viro-blast.php和Enzemble plants)上进行序列确认,引物具体序列见表1。qRT-PCR采用QuantStudi0 6 Flex实时荧光定量PCR系统(美国ABI公司),以TaAc-tin基因为内参基因,检测基因的表达量变化。反应体系为:cDNA 1 μL,Mix 5 μL,primer各0.25 μL,H2O3.5 μL。每反应设置3次机械性重复和生物学重复,根据Ct值,利用公式2-△△Ct,计算基因的相对表达量。
1.5 数据分析
采用Excel软件进行平均值、变异系数的计算;采用SPSS软件进行性状相关性分析和方差分析。
2 结果与分析
2.1 不同氮素水平下小麦植株生物积累量的差异
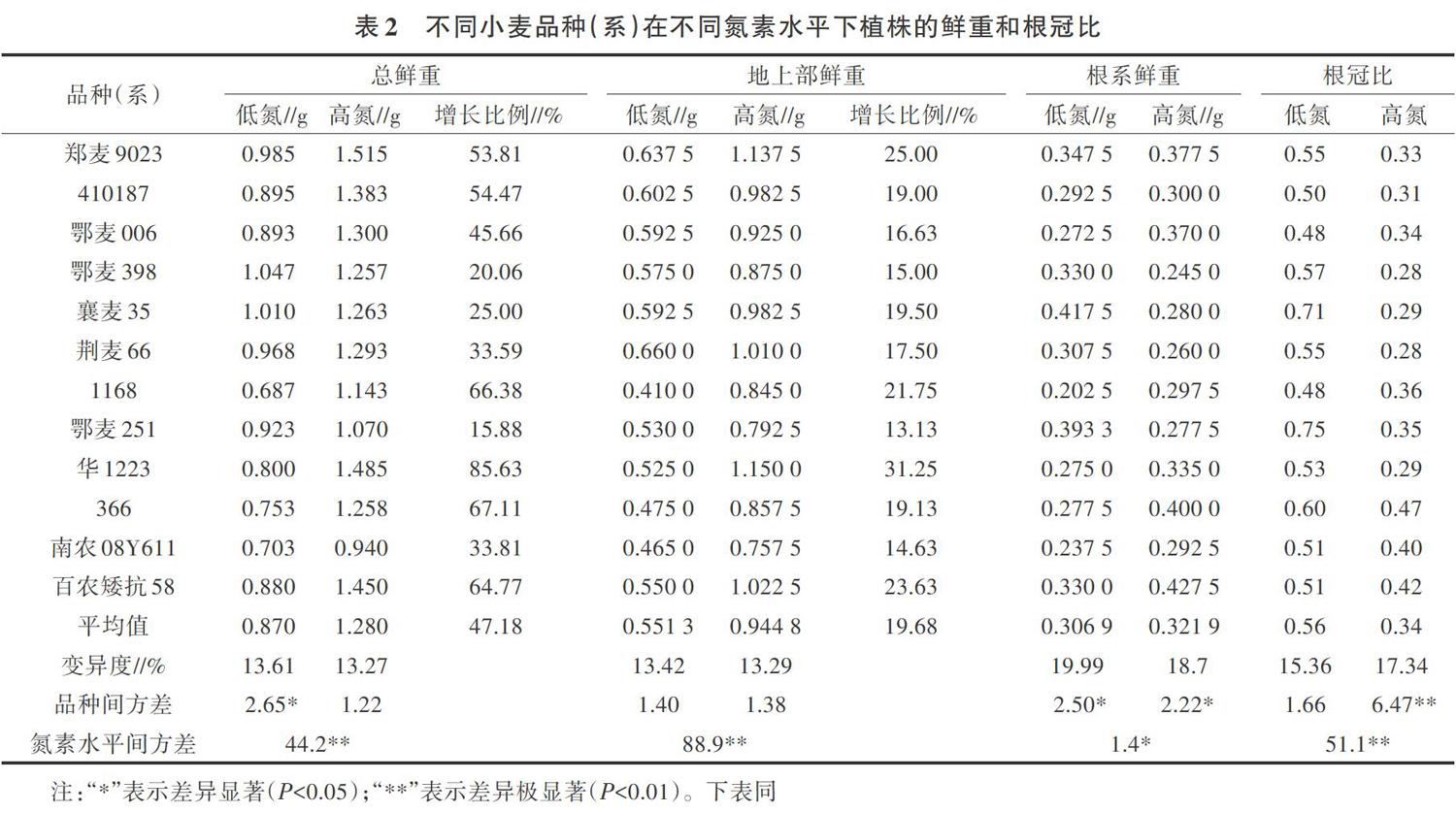
由表2所示,在0.2 mmol/L( LN)和2.0 mmol/L(HN)氮素水平下,12个不同基因型小麦材料植株总鲜重、地上部鲜重均表现出随着氮素浓度提高而升高的趋势。低氮条件下,植株平均总鲜重为0.870 g,而高氮条件下植株总鲜重可达1.280 g。同时,不同基因型小麦对氮素浓度提高的敏感程度也存在较大差异,华1223、“1168”、百农矮抗58、“366”、郑麦9023和“410187”6个小麦材料的植株总鲜重均增加50%以上;鄂麦251、襄麦35、荆麦66等品种则对氮素浓度提高反应敏感度较低。此外,地上部鲜重的增幅(全部品种平均增幅为19.68%)低于植株总鲜重增幅(全部品种平均增幅为47.18%)。根系鲜重对氮素浓度的反应则不同品种(系)间表现不一致。不同供氮水平下植株根冠比分析结果显示,低氮条件下植株根冠比大于高氮浓度下数值。
方差分析结果表明(表2),不同参试小麦品种的总鲜重、根系鲜重在低氮条件下存在显著差异。高氮条件下,根系鲜重和植株根冠比在不同品种(系)间存在显著和极显著差异。植株总鲜重、地上部鲜重和根冠比3个性状在不同氮素水平间存在显著或极显著差异。
2.2不同氮素水平下小麦植株根系特征的差异
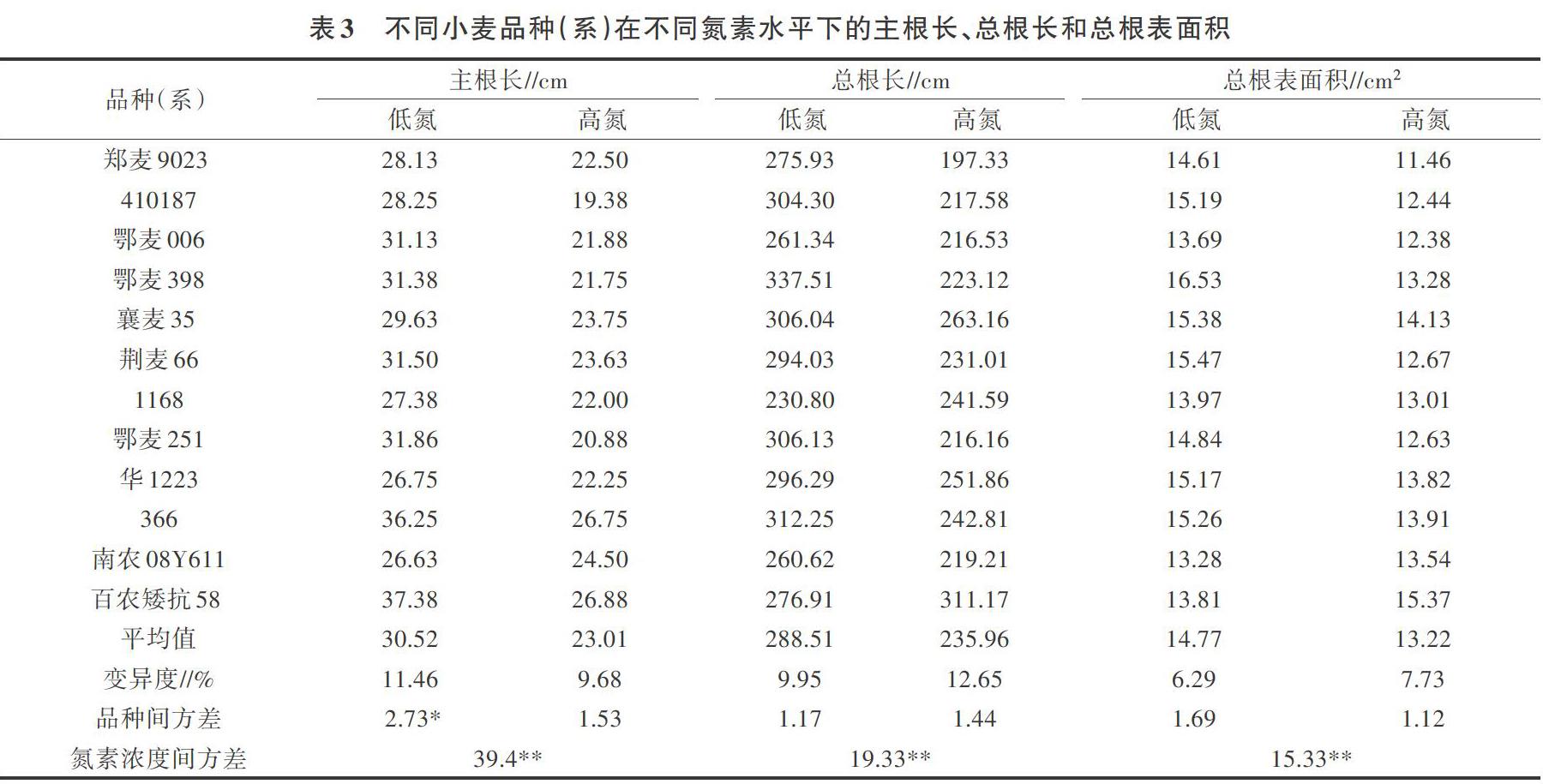
对不同氮素浓度下小麦幼苗根系特征分析可见(表3),低氮条件下主根长、总根长和总根表面积大部分大于高氮条件下数值,且各指标平均值在不同氮素浓度处理间差异极显著。不同氮素浓度处理基因型间变异系数相差不大。主根长、总根长和总根表面积3个性状品种间方差分析显示,仅低氮条件下主根长在不同基因型间差异显著。
2.3 不同氮素浓度处理下小麦植株叶绿素含量的差异
不同氮素浓度处理下小麦幼苗叶片叶绿素含量分析表明(图1),氮素浓度升高促进小麦叶绿素含量的提高,且不同氮素浓度间小麦叶片叶绿素含量差异均达极显著水平。参试小麦材料在同一氮素浓度下,叶绿素含量总体相差不大,仅荆麦66、鄂麦251和“1168”3个小麦材料的叶绿素含量低于其他品种(系),可能与品种特性有关。
2.4 不同氮素处理下植株体内谷氨酰胺还原酶(GS)活性的差异
对12个小麦材料2种氮素处理的地上部GS活性测定结果显示(图2),不同氮素浓度下不同品种(系)间CS活性差异较大。不同氮素水平下,8个小麦品种(系)CS活性存在显著差异,分别为鄂麦006、襄麦35、荆麦66、南农08Y611、鄂麦251、华1223.“366”和“1168”,而郑麦9023、百农矮抗58、鄂麦398和“410187”4个品种CS活性差异不显著。其中,鄂麦006、襄麦35、荆麦66、华1223和“1168”表现为低氮浓度下植株CS活性大于高氮浓度下数值;鄂麦251、南农08Y611和“366”则表现相反。
2.5 氮素吸收同化及信号转导相关基因表达分析
为了研究氮素吸收同化相关基因TaNRT1.1、TaNRT2.1、TaGS1和TaGS2在不同氮素浓度下和品种中的表达差异,以生物积累量显著差异的郑麦9023、“410187”(高积累量)和南农08Y611(低积累量)为材料进行表达分析。结果表明(图3),高氮条件下,TaNRT1.1和TaNR T2.1表达量均随着氮素浓度提高而降低,且2个基因表达量在高生物積累量小麦材料(郑麦9023和“410187”)中明显高于低生物积累量材料南农08Y611。氮素同化基因TaCS2表达量与氮素浓度呈正相关,高氮浓度下的表达量大于低氮浓度下表达量,而TaGS1的表达量在不同氮素浓度和基因型间变化不大。
[2] FRINK CR,WAGGONER PE,AUSUBEL JH Nitrogen fertilizer:ReLrospect and prospect[J]. Proc Natl Acad Sci U S A,1999. 96:1175-80.
[3] MILLER A J,FAN X,SHEN Q,et al Amino acids and nitrate as signals for che regulaLion of nitrogen acquisition [J].J Exp BoL,2008. 59: 111-119
[4]任书杰,张雷明,张岁岐,等氮素营养对小麦根冠协调生长的调控[J].西北植物学报,2003,23(3):395-400.
[5] BASCUNAN-CODOY L, SANHUEZA C,PINTO K, et al. Nitrogenphysiology of contrasting genotypes of Chenopodium quinoa Willd (Amaranthaceae) [Jl. Sci Rep, 2018,8: 17524.
[6]王平,不同氮效率类型小麦氮代谢差异及其机理分析[D]山东秦安:山东农业大学,2011.
[7]汪晓丽,陶玥玥,盛海君,等.硝态氮供应对小麦根系形态发育和氮吸收动力学的影响[J].麦类作物学报,2010,30(1):129- 134.
[8]王琳琳,王平,王振林,等.小麦亲本及其杂交后代苗期氮代谢相关指标的遗传与表达差异[J]中国农业科学,2014.47( 12):2300-2312.
[9] KANT S,BIY M. ROTHSTEIN S J.Understanding planL responseto nitrogen limitation for the improvement of crop nitrogen use effi-ciency[J].J Exp Bot, 2011, 62: 1499-1509.
[10] BUCHER P,HAWKESFORD M J Complex phylogeny and geneexpression patterns of memhers of the NITRATE TRANSPORTER1/PEPTIDE TRANSPORTER familY (NPF) in wheat [Jl. Journalof experimental botanY .2014. 65: 5697-5710.
[11] OKAMOTO M. VIDMAR J J,GLASS A D.Regulation of NRTIand NRT2 gene families of Arabidopsis thaliana: Responses to ni-trate provision [J] Plant Cell Physiol.2003, 44: 304-317.
[12] HU M,ZHAO X, LIU Q,et al. Transgenic expression of plastidic glu-tamine synthetase inc:reases nitrogen uptake and yield in wheat [J]Plant Biotechnol J, 2018, 16: 1858-1867.
[13] WANC J,SONC K,SUN L,eI al.Morphological and transcrip- tome analvsis of wheat seedlings response to low nitrogen stress LJlPlants (Basel) .2018.8: 1-8.
[14]張定一,张永清,杨武德,等不同基因型小麦对低氮胁迫的生物学响应[J].小麦研究,2006.27(1):1-9.
[15] HE X. QU B,LI W,et al.The nitrate-inducible NAC transcrip-tion factor TaNAC2-5A controls nitrate response and increaseswheat yield[J]. Plant physiology, 2015, 169: 1991-2005.
[16] DUAN J,TIAN H. DRIJBER R A,el al.SVstemic and local regu- lacion of phosphate and nitrogen transporter genes by arbuscular my-corrhizal fungi in roots of winter wheat( Triticum aestivum L.)[J]Planl PhVsiol Biochem, 2015, 96: 199-208.
[17] YANC J,WANG M, LI W. et al Reducing expression of a ni-trate-responsive bZIP transcription factor increases grain yieldand N use in wheat [Jl. Planl Biotechnol J, 2019. 17(9):1823- 1833.
[18] MELINO V M. FIENE G, ENJV A.et al. Genetic diversitv for rootplasticity and nitrogen uptake in wheat seedlings [J]. Functionalplant biology, 2015, 42: 942-956.
[19]李双双,李晶,陈龙涛,等施氮量对春小麦根系生长及产量的影响[J].麦类作物学报,2013.33(1):141-145
[20]盛海君,董召娣,张明伟,等春性和半冬性小麦苗期氮肥吸收效率的差异及其与根系性状的关系[J]麦类作物学报,2016,36(8):1-6.
[21]徐晴,许甫超,董静,等.小麦氮素利用效率的基因型差异及相关特性分析[J].中国农业科学,2017.50( 14):2647-2657.
[22] NAWAZ M A. CHEN C, SHIREEN F, et al. Cenome-wide expres-sion profiling of leaves and roots of watermelon in response to lownitrogen[Jl. BMC Genomics. 2018( 19):456
[23] ZHANG C,HOU Y. HAO Q. et al.Cenome-wide survev of thesoybean CATA transcription factor gene family and expressionanalysis under low nitrogen stress [J]. PLoS One, 2015, 10 (4):e0125174
[24] HABASH D Z,MASSIAHA J,RONGH L,et al The role of cy一tosolic glutamine synthetase in wheat [Jl. Ann Appl Biol. 2001,138:83-89.
[25] KICHEY T,HEUMEZ E,POCHOLLE D. et al Combined agro-nomic and physiological aspects of nitrogen management in wheathighlight a central role for glutamine synthetase[J]. New Phytol,2006. 169:265-78.
[26] WANC P, WANC Z L,CAI R G,et al. Physiological and molecu-lar response of wheat roots to nitrate supply in seedling stage LJ]Agricultural sciences in China, 2011, 10(5):695-704.
[27]軒红梅,王永华,魏利婷,等.小麦幼苗叶片中硝酸盐转运蛋白NRTI和NRT2家族基因对氮饥饿胁迫响应的表达分析[J].麦类作物学报,2014.34(8):1019-1028.
作者简介:徐晴(1983-),女,河南平顶山人,助理研究员,博士,主要从事麦类遗传改良与抗逆遗传机制研究,(电话)18571550899(电子信箱)395045924@qq.com;通信作者,董静,副研究员,主要从事麦类遗传改良与抗逆遗传机制研究,(电子信箱)dongjingsir061@163.c:om。
