12例原发性骨髓纤维化合并肝硬化患者的临床特征分析
2020-11-25何婷婷白云峰张晶晶付双楠梁肖肖
王 宣, 何婷婷, 张 宁, 周 超, 王 葽, 白云峰, 张晶晶, 付双楠, 梁肖肖, 李 昕, 宫 嫚
解放军总医院第五医学中心 中西医结合科, 北京 100039
原发性骨髓纤维化(primary myelofibrosis, PMF)是由异常造血干细胞的克隆性增殖,导致进行性骨髓纤维化的一种骨髓增殖性肿瘤[1]。有研究[2]发现部分骨髓纤维化患者可出现肝脏硬度值升高。近年来,亦有研究者对PMF合并肝硬化、门静脉高压、消化道出血等进行过临床报道[3-4],但病例数较少。此外,PMF作为一种罕见病,常伴有脾大、门静脉高压、进行性血细胞减少及消化道出血等,与肝硬化表现较为相似,当该病合并肝硬化时,易出现漏诊、误诊。PMF可导致肝硬化,但其进展至肝硬化的间隔时间不详,且无相关临床报道。因此,通过对本院PMF合并肝硬化病例的总结,并结合文献复习,有助于更好地认识PMF与肝硬化之间的关系,对临床早期诊断,减少漏诊、误诊十分重要。
1 资料与方法
1.1 研究对象 收集2011年1月-2020年4月本院收治住院的PMF合并肝硬化患者临床资料,包括患者的一般资料、临床症状、合并症、实验室及影像学检查等。纳入标准:经骨髓病理检查明确诊断为PMF,且符合2016年世界卫生组织制定的PMF诊断标准[5];同时合并肝硬化,诊断符合《肝硬化诊治指南》[6]中的肝硬化诊断标准。排除标准:排除病毒性、酒精性、药物性、代谢性、自身免疫性、血管因素等其他明确病因导致的肝硬化,排除寄生虫如血吸虫、肝吸虫病。
1.2 其他诊断标准 (1)巨脾判定标准[7]:脾缘超过脐水平线或前正中线为巨脾。(2)贫血分级标准[8]:重度贫血,血红蛋白为31~60 g/L;中度贫血,血红蛋白为61~90 g/L;轻度贫血,血红蛋白大于90 g/L且低于正常值下限(男性120 g/L;女性110 g/L)。(3)腹水分级标准[9]:1级或少量腹水为超声下腹水位于各个间隙,深度<3 cm;2级或中量腹水为超声下腹水淹没肠管,但尚未跨过中腹,深度3~10 cm;3级或大量腹水为超声下腹水占据全腹腔,中腹部填满,深度>10 cm。
1.6 伦理学审查 本研究方案经由中国人民解放军总医院第五医学中心伦理委员会审批(批号:R2018007DC010)。
2 结果
2.1 一般资料及临床症状 共纳入12例患者,其中男6例(50%),女6例(50%)。年龄38~79岁,平均(60.08±11.53)岁,其中<45岁2例(16.67%), 45~59岁3例(25%), ≥60岁7例(58.33%)。详细查阅所有患者现病史及既往病史,7例患者在确诊肝硬化前已确诊PMF,其中1例患者从确诊PMF至确诊肝硬化的间隔时间不详,余患者间隔时间分别为8.7、24、31、40、72、156个月。3例患者在确诊PMF前已确诊肝硬化,间隔时间分别为2.5、48、324个月。2例患者同时确诊PMF及肝硬化。纳入病例中临床症状以黑便、呕血最常见,为8例(66.67%),其次为腹胀7例(58.33%),乏力6例(50%),双下肢水肿、鼻衄或齿衄各2例(16.67%),发热、纳差、腹痛各1例(8.33%)。
2.2 并发症 所有病例中,11例(91.67%)患者伴不同程度腹水:1级腹水4例(33.33%)、2级腹水6例(50%)、3级腹水1例(8.33%)。11例(91.67%)患者疾病过程中存在不同程度贫血:轻度2例(16.67%)、中度4例(33.33%)、重度5例(41.67%)。伴低蛋白血症8例(66.67%)。伴消化道出血8例(66.67%)。伴感染4例(33.33%):自发性细菌性腹膜炎3例(25%)、胆道感染1例(8.33%)。此外,伴肾功能不全2例(16.67%)、胸腔积液2例(16.67%)、心律失常1例(8.33%)。
2.3 实验室检查 血常规、凝血功能方面,所有患者WBC(0.72~36.12)×109/L,异常下降5例(41.67%),异常升高6例(50%);PLT(17~795)×109/L,异常下降5例(41.67%),异常升高3例(25%)。凝血功能方面,凝血酶原活动度(PTA)42.6%~89.2%,异常下降8例(66.67%);国际标准化比值(INR)1.04~1.59,1例(6.25%)INR>1.5(表1)。
生化指标方面,所有患者TBil 6.9~112 μmol/L,异常升高6例(50%);ALT 7~115 U/L,异常升高1例(8.33%);AST 6~193 U/L,异常升高1例(8.33%);ALP 53~718 U/L,异常升高3例(25%);GGT 9~351 U/L,异常升高6例(50%);肌酐(Cr) 47~244 μmol/L,异常升高3例(25%);乳酸脱氢酶(LDH) 122~618 U/L,异常升高8例(66.67%);Alb 23~39 g/L,异常下降8例(66.67%);球蛋白(Glo) 21~45 g/L,异常升高1例(8.33%)(表2)。
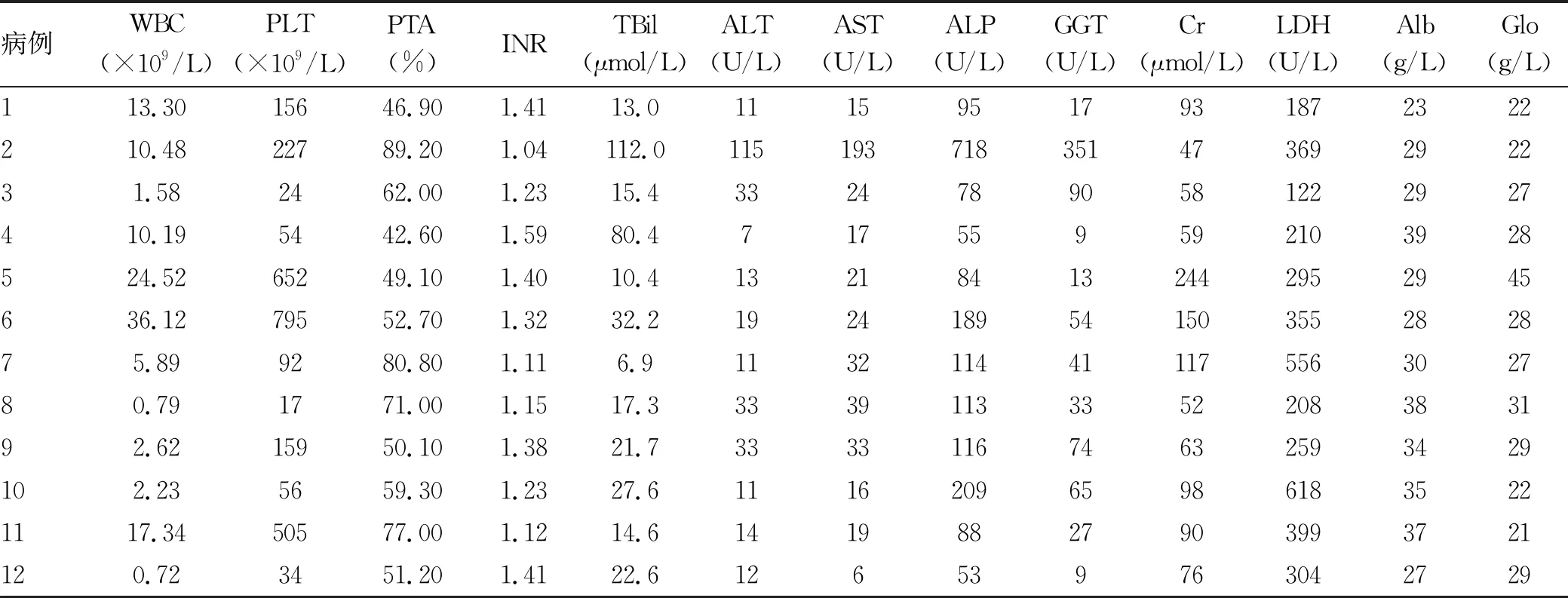
表1 12例PMF合并肝硬化患者实验室检查结果
2.4 影像学和胃镜检查 结合影像学资料,所有患者均有脾大,其中巨脾8例(66.67%)。此外,8例(66.67%)患者脾静脉内径>10 mm或增粗。9例(75%)患者门静脉内径≥13 mm。6例(50%)患者肝脏影像学检查提示门静脉血栓、栓子形成,2例(16.67%)患者肝脏影像学检查虽未提示门静脉栓子形成,但提示门静脉海绵样变,而门静脉海绵样变与门静脉栓塞所致的门静脉高压密切相关。纳入病例中6例患者行胃镜检查,且均有食管静脉曲张(5例伴胃静脉曲张):轻度曲张2例、中度曲张1例、重度曲张3例;余患者虽未行胃镜检查,但腹部增强CT或增强MRI均提示食管胃静脉曲张。所纳入病例中仅2例患者行B超肝脏无创纤维化评分检测,肝脏硬度值分别为15.6、15.1 kPa,相当于肝组织病理纤维化F3~F4,提示肝纤维化程度较重。
2.5 治疗及预后 所有病例结合其主要症状及并发症分别或联合给予保肝、降酶、退黄、利尿、抗感染、止血、经颈静脉肝内门体分流术及腹水回输术等对症治疗,所有患者相关并发症均好转。仅2例患者予对症治疗同时亦对PMF进行相关治疗,其中1例患者应用醋酸泼尼松联合沙利度胺、干扰素治疗,1例患者应用沙利度胺治疗,但由于无随访结果,故无法针对PMF进行疗效判定。
3 讨论
PMF以伴发不同程度骨髓纤维化为其突出特征[10]。而骨髓纤维化是发生在骨髓间质的纤维化过程,包括细胞外基质胶原性成分(网状蛋白)和非胶原性成分(纤黏蛋白)的积累、组装,标志性的血管新生伴胶原沉积[11]。肝脾髓外造血是其主要特征之一,继而引起脾血流增加、肝血窦阻力增大等,导致部分患者继发门静脉高压症,晚期可导致肝硬化[3]。
10%~20%的PMF患者合并肝硬化,是由于肝血窦周围血管阻塞及肝窦髓外造血引起门静脉血流量增加所致[8]。但PMF合并肝硬化相关研究较少,故有关PMF所致肝硬化的病理改变文献较少。笔者考虑,一方面,肝血窦周围血管阻塞可引起肝内淤血,进而导致肝细胞损伤,最终发展为肝硬化;另一方面,肝脾髓外造血,可引起血流速度增加、血管阻塞、静脉回流障碍以及门静脉血栓形成,严重者可损伤肝功能,甚至发展为肝硬化。
本研究发现,PMF合并肝硬化以中老年患者较为多见,男、女所占比例相同,提示男、女发病率相似。PMF患者常伴发热、乏力、盗汗、消瘦等全身症状[12],有研究[13]显示多数PMF患者最终死于合并症,主要包括心血管事件、血细胞减少所致的感染和出血等。而本研究纳入病例中临床表现以黑便、呕血为主,其次为腹胀、乏力,并发症以腹水、贫血、低蛋白血症、消化道出血多见。考虑主要原因为本院属肝脏病专科医院,就诊患者多以肝硬化并发症入院,因此并不能全面概括PMF的临床表现及并发症。可见确诊PMF后,应警惕逐渐进展的肝纤维化乃至肝硬化,故早期诊断、早期干预,积极防治并发症,对提高患者生存质量、延长生存期尤为重要。
PMF可导致肝硬化,有学者[3,14]对PMF合并肝硬化进行过临床报道,但肝硬化能否导致PMF尚不明确,且未查阅到相关文献。本研究中7例患者在确诊肝硬化前已确诊PMF,提示肝硬化原因可能与PMF密切相关,该7例患者从诊断PMF到发现肝硬化的间隔时间为数月至10余年不等,但由于本研究为回顾性研究且样本量少,因此从PMF确诊至出现肝硬化的具体间隔时间有待进一步研究。此外,部分患者在确诊PMF前已确诊不明原因肝硬化,间隔时间短则数月,长则20余年,该部分患者不除外既往漏诊PMF的可能,但肝硬化能否导致造血微环境改变致使骨髓造血功能紊乱进而诱发PMF亦有待进一步研究。
有研究[15]发现炎症是PMF发生骨髓纤维化等骨髓基质改变的基础,炎症可致造血微环境发生改变,使造血细胞更易获得突变。PMF骨髓异常克隆性造血增殖逐渐取代正常多克隆造血,会引起一系或多系造血细胞增多[10],故PMF可伴外周血WBC、PLT的增高,而WBC>11×109/L也是PMF的次要诊断标准[5],但随着疾病进展血细胞会逐渐下降。本研究中患者外周血WBC、PLT变化范围跨度较大,多数患者WBC、PLT未明显下降,该特点与其他明确病因肝硬化伴脾功能亢进所致的WBC、PLT减少有所不同。其他指标方面,所纳入病例中多数患者LDH异常升高,而LDH升高亦是PMF的次要诊断标准[5]。此外,脾大是PMF的突出体征,且常表现为巨脾,本研究中所有患者均伴脾大,其中66.67%伴巨脾,巨脾的比例似乎明显高于其他明确病因所致的肝硬化患者。因此当不明原因肝硬化患者出现巨脾,尤其伴有WBC、PLT未明显下降,且LDH升高时,应考虑有无PMF。另外,本研究还发现半数病例GGT升高,提示当PMF患者出现GGT等肝脏生化指标异常时需警惕有无合并肝实质损伤甚至肝硬化。
目前针对PMF合并肝硬化的研究较少,且多以个案报道及回顾性研究为主,后续研究需进一步扩大样本量,加强前瞻性研究,从细胞、分子甚至基因水平探讨两者的关系,为临床诊治提供科学依据。
利益冲突声明:本研究不存在研究者、伦理委员会成员、受试者监护人以及与公开研究成果有关的利益冲突,特此声明。
作者贡献声明:王宣负责课题设计,资料分析,收集数据,撰写论文;何婷婷等参与课题设计,修改论文;宫嫚负责拟定写作思路,指导撰写文章并最后定稿。
