医用便携式一氧化氮(NO)发生机的设计与性能研究
2020-11-23林涛刘寒春
林涛 刘寒春


摘要:一氧化氮(NO)吸入疗法在临床中用于治疗新生儿肺动脉高压,并被拓展应用到其他多个临床适应证治疗。为解决现有一氧化氮发生机存在的易产生有毒气体NO2及需笨重的高压钢瓶作为气源等问题,设计了一款新型的便携式一氧化氮发生机,详细介绍了该装置的原理、组成结构、性能指标及电磁兼容性。该装置灵巧、便携,同时利用室内空气递送NO,实现了气体发生、流量控制和输气的一体化,对于非使用有创呼吸的重症患者可以实现床旁交互使用。
关键词:一氧化氮发生机;便携式医疗器械;电化学传感器;气体吸入疗法;电磁兼容测试
0 引言
一氧化氮(NO)是一种人体内存在的内源性气体分子,不仅具有控制血压和防止血栓形成的作用,还是人体免疫系统的重要组成部分。自1998年诺贝尔生理学和医学奖被授予关于一氧化氮可以控制血压和血管张力的发现后,更是引发了研究者们对一氧化氮相关研究的关注,这些研究证实了一氧化氮具有防止血小板凝结,促进伤口愈合、血管生成及抑制微生物(包括细菌、真菌和病毒)的功效。
一氧化氮吸入(Inhaled NO,INO)療法是20世界90年代呼吸医学技术理论的重要突破,该疗法是由美国食品药品监督管理局(FDA)批准的,作为原发性和继发性肺动脉高压的治疗手段,INO疗法能够改善机体氧合能力,对重度的甚至发展到呼吸窘迫综合征(ARDS)的患者,可以通过合用呼吸机起到扩张肺部血管、降低肺血管阻力,进而增加氧合、改善肺通气-灌流比例,从而有效地缓解肺水肿和肺损伤。
同时,INO疗法对新生儿重症原发和继发的肺动脉高压也具有非常明显的治疗效果,常被作为各种国内外权威指南推荐使用。在欧美国家,INO疗法是新生儿重症的常用必备治疗方式。近些年,国内外已经开始一氧化氮单独吸入或局部性治疗的新型适应证研究,包括慢性阻塞性肺疾病(COPD)、肺纤维化、囊肿性纤维化、缺氧性肺炎以及糖尿病足等,部分研究已经进入二、三期的临床研究阶段。在成人重症方面,也有探索一氧化氮吸入同体外循环(ECC)和体外膜氧化(ECMO)的合用技术,从而减少ECC和ECMO治疗过程中存在的炎症反应和并发症。
目前用于INO治疗的产品是传统的一氧化氮钢瓶作为气源,钢瓶中含有NO和氮气(N2)的混合物,NO浓度一般为10-4或8×10-4。高浓度NO会和空气中的氧气发生反应,生成对人体有危害的NO2(安全浓度为5×10-6以内),即使在N2保护条件下,长时间保存高浓度的NO也会逐步积累有害的NO2,在纯度和安全性方面有较大风险。同时,气体钢瓶的使用需要配置多重减压阀才能够实现精准控制,操作者需经过专门培训才能正确安全使用钢瓶。此外,气体钢瓶在运输和成本上均有特殊和较高的要求。这些因素限制了NO的进一步临床应用和治疗适应证的扩展应用。
1 便携式一氧化氮发生机的设计原理和结构
本文研发的便携式一氧化氮发生机主要由一氧化氮生发系统、气体输送系统、气体混合装置、气体监控系统、显示系统、电源适配器、呼吸口鼻罩、管路和软件等部分组成。NO发生机整体结构如图1所示。其工作原理:通过电解电流模块控制一定大小的电流,电解特定的化合物溶液产生高纯度NO气体,经气液分离器析出后,再由气体流量控制模块控制与新鲜空气的混合配比,最后经气体监控系统,实现流量与浓度可控的、持续稳定输出的NO混合治疗气体,供病人吸入治疗使用。
(1)一氧化氮生发系统:主要利用电极电解特定的化合物溶液产生的高纯度一氧化氮气体,通过液体循环泵流经气液分离器后析出,同时气液分离器连续通过一定流量的空气后,产生连续的一定浓度的一氧化氮和空气混合气体。
(2)气体输送系统:分为两部分,一部分主要通过气泵输送洁净的空气给一氧化氮生发系统以及供病人呼吸吸入,输送的空气流量可以在一定范围内调节;另一部分主要用于抽取混合后的定量混合气体,输入气体浓度传感器。
(3)气体混合装置:气体混合装置与一氧化氮生发系统和气体输送系统连接,均匀混合输入的空气和一氧化氮气体。
(4)气体监控系统:由气体浓度传感器、气体流量控制模块、电极电解电流控制模块组成,主要检测并控制系统输送的一氧化氮和空气混合气体的流量以及混合气体中一氧化氮的浓度,并实现报警功能。气体浓度传感器由一氧化氮和二氧化氮浓度传感器组成,精准测量气体浓度并显示到显示屏。气体流量控制模块主要控制输入空气的流量,电极电解电流模块主要调节电解电流的大小,两个模块配合共同实现一氧化氮混合气体的一定浓度输出。
(5)显示系统:显示一氧化氮浓度、二氧化氮气体浓度、气体流量、治疗时间、电解池计时、报警提示等。
(6)电源适配器:为整机提供电源。
(7)呼吸口鼻罩:供病人吸入治疗气体使用,带有漏气孔。
(8)管路:用于输送一氧化氮和空气气体。
(9)软件:实现产品功能状态的设定、控制、显示、监控和(或)指示。
2 便携式一氧化氮发生机性能指标
2.1 生成NO气体纯度分析
本文研发的便携式一氧化氮发生机采用高效催化剂在常温常压下将水溶液中的一氧化氮供体还原成气态NO,通过空气或氮气为载气,将NO从气液分离器中萃取,含有不同NO浓度的空气可以用于NO吸入治疗。为了证实该方法所制备NO气体中不含N2O和NO2等有害氮氧化物,对生成气体进行了成分分析。
NO的浓度通过基于金标准的化学发光法的Thermo Fisher一氧化氮检测仪进行测定,该检测仪除可以精准检测NO以外,还可以将其他氮氧化物都转化为NO,得到总氮氧化物的浓度,从差值可以计算出除NO以外的其他氮氧化物浓度。使用化学发光一氧化氮分析仪测定不同电流条件下生成的气体浓度如表1所示,从表1数据可以看出,该一氧化氮发生机可以产生高纯度的NO气体,其他形式的氮氧化物浓度,如NO2等数值在仪器的检测误差范围内(±10-6),远低于NO2 5×10-6的安全浓度。
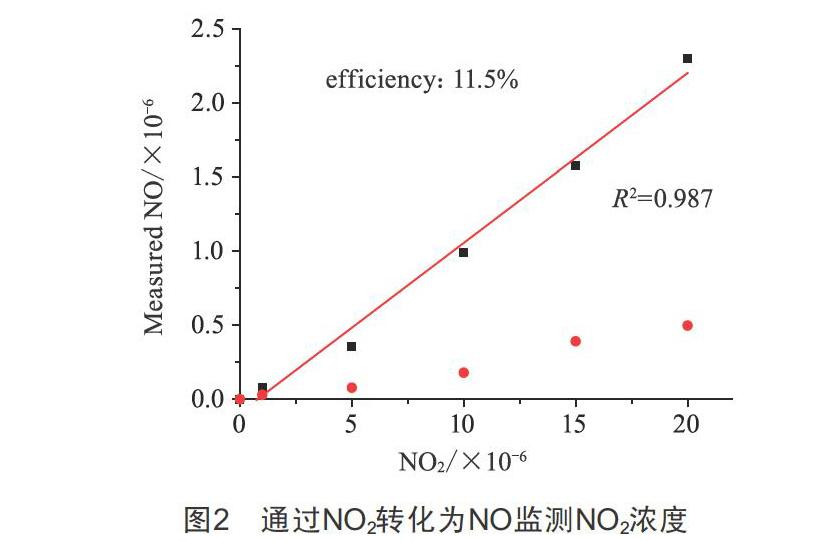
NO2可以通过NO和O2反应得到,是NO临床使用中最容易产生的有毒副产物,因此本文专门针对NO2进行了研究。NO2在紫外光(<400 nm)照射下转变为NO,然后通过一氧化氮分析仪对NO进行监测。图2所示为通过NO2转化为NO监测NO2浓度,首先验证了紫外照射转化二氧化氮的过程,图中红色数据点为NO2标准气体浓度,黑色数据点是紫外转化后测得的NO浓度。从图2可以看出,转化后的NO浓度呈现较好的线性关系(R2=0.987),并能够准确反映NO2的浓度变化。该方法能够准确、灵敏地检测NO2的含量。
在此基础上,本文在对一氧化氮发生器生成的NO浓度进行持续检测的过程中,加上UV光照,观察NO浓度的变化,如图3所示。从图3可以看出,在固定电流大小和吹扫流速的条件下,UV光照对NO浓度没有影响,增大电流可以使NO浓度迅速增高,待浓度稳定后,再次使用UV光照,NO浓度也没有发生变化,说明不同条件下产生的不同浓度的NO气体中均不含有NO2。
2.2 生成NO气体浓度的精準调控
精准控制是检验仪器性能的一个重要指标。当载气流速固定时,通过调节电流大小或电压大小可实现对生成NO浓度的调节。本文研究了电流控制和电压控制两种模式的优缺点。控制电压模式和控制电流模式对NO浓度进行调控如图4所示,在使用氮气为载气的条件下,将气体流速固定在200 mL/min,改变控制电位可以对NO浓度进行精准调控,改变电流同样可以灵敏地改变NO浓度。
比较上述两种调控模式,控制电流模式更具优越性,由于仿生催化反应的速率和电流成正比,控制电流对NO产生的调控更直接,同时,如图5所示,控制电流模式中,温度对NO产生的影响较小。改变温度对恒电流模式下产生NO的影响较小,蓝色为电流曲线(控制在0.5 mA,随后变化至0.8 mA),黑色为在恒流下对应的电压值,红色为NO浓度。在温度从25~37 ℃时,电压值发生较大变化,但NO浓度基本保持不变。
基于上述研究,笔者采用恒流模式用于后续研究。载气流速(0.25 L/min)固定,NO浓度随着电流变化情况如图6所示。在空气流速为0.25 L/min,混合气流速为8.4 L/min时,在100~400 mA内调节电流大小,可实现持续、稳定、台阶式上升的NO气体生成。同时可以看出,在升至某一电流时,NO的浓度可快速达到平稳状态,说明仪器具有较强的NO生成速率控制精准性。
基于图6数据,笔者首先对相关电流强度下生成的NO浓度进行平均,再与电流强度相关联,得到电流强度与生成NO浓度的线性关系,如图7所示,可以看出,随着电流强度的增加,NO生成浓度也持续线性增加,R2=0.993 6,进一步说明了本文设计的便携式一氧化氮发生机可以实现NO气体的持续稳定生成控制。
2.3 输出NO气体浓度的精准调控
在实际临床治疗中,需要把生成高浓度的NO气体与新鲜空气混合稀释,再控制输出。为了验证最终输出气体的浓度及流量可控,在固定工作电流为220 mA的条件下,通过增加一道空气气流和NO进行混合,得到不同NO浓度的气体。通过调节质量流量控制器和混合气流速,实现对NO浓度的快速调控(3 min内)如图8所示,便携式一氧化氮发生机在0~160×10-6和流量3~7 L/min内可实现对NO浓度的快速调控。
2.4 输出NO气体的稳定性测试
在固定工作电流200 mA、载气流速1 L/min、混合气总量5 L/min的条件下,使用化学发光NO检测仪持续监控NO浓度,NO输出长期稳定性如图9所示,在恒定电流和流速的条件下,一氧化氮发生机能够稳定输出一氧化氮8 h以上,变化大小不超过±2×10-6,说明仪器输出的NO气体浓度具有较好的稳定性。
2.5 电解池重复性测试
在工作电流恒定200 mA、载气流速1 L/min和混合气总流量5 L/min条件下,同一批次生产的电解池产生NO的浓度大小和趋势均保持一致,如图10所示,同一批次生产的电解池提供的NO浓度变化范围在10-6以内。
2.6 NO传感器检测性能测试
基于臭氧和NO反应产生化学发光信号的NO检测仪是NO测试的标准方法,但其体积大、需要真空室和臭氧发生器,无法和便携式一氧化氮发生机进行整合。为此,研究了基于电化学检测原理的传感器用于NO的快速实时监测。电化学NO传感器采用Pt镀层的高分子材料薄膜,膜的一面接触内控溶液,NO气体从传感膜的另一表面通过,NO在Pt膜表面发生电化学反应产生可检测的电流信号。一氧化氮分析仪(NOA)和电化学传感器对不同NO的响应曲线如图11所示,电化学传感器对NO浓度的响应性能和一氧化氮检测仪(NOA)相同。
两种检测方式的相关性达到R2=0.995,如图12所示,这些结果证明使用小巧的电化学NO传感器可以替代传统的大型一氧化氮分析仪。
3 电磁兼容性测试
3.1 电磁骚扰测试
作为有源医疗器械,一氧化氮发生装置按照国家医疗器械监督管理条例的要求,根据《医用电气设备 第1~2部分:安全通用要求 并列标准:电磁兼容 要求和试验》(YY 0505—2012)进行了全项目检测,主要从电磁骚扰(EMI)和电磁抗扰(EMS)两方面全面评价其电磁兼容合规性。传导发射(CE)项目主要评价便携式一氧化氮发生机工作时产生的低频电磁波(150 kHz~30 MHz)沿着供电线路对外辐射的能力,传导发射测试环境和测试结果如图13所示,左图为测试现场布置,右图为实测结果,其中红线代表1组A类设备传导发射噪声准峰值限值;粉线代表平均值限值;蓝线、绿线分别代表实测准峰值和平均值,可以看出实测值远远低于限值,符合标准要求,通过测试。
輻射发射(RE)项目主要评价便携式一氧化氮发生机工作时产生的高频电磁波(30 MHz~1 GHz)直接对外辐射的能力,辐射发射测试环境和结果如图14所示,左图是实测现场布置,右图为测试结果,其中红线表示1组A类设备辐射发射噪声准峰值限值,蓝线表示实测值,同样实测值低于限值,通过测试。
3.2 电磁抗扰测试
电磁抗扰方面主要包括静电放电(ESD)、辐射抗扰(RS)、传导抗扰(CS)、电快速瞬变脉冲群(EFT)、浪涌(Surge)、电压暂降和中断、工频磁场测试项目。通过这些测试项目,分别模拟出雷击/静电现象、大功率负载启动、电网电压突降或中断、周边强辐射和磁场等干扰状态下一氧化氮发生机的工作能力,便携式一氧化氮发生机电磁抗扰测试环境和结果如图15所示。现场测试结果表明,在各种干扰状态下,便携式一氧化氮发生机均能满足其基本性能要求。
4 结语
本文介绍了国内首个便携式一氧化氮发生机的设计原理、组织结构、性能指标及电磁兼容性测试。该设备使用仿生催化电解产生高纯度、无杂质的医用一氧化氮气体,装置配有气体传感器和流量控制器,智能精密地输送NO,即时产生按需的NO气体,使用NO固态电化学传感器(0~250×10-6)和NO2固态电化学传感器(0~5×10-6)作为监控装置,保证NO2浓度低于30×10-6。该装置小巧、便携,同时利用室内空气递送NO,不需笨重的高压钢瓶作为气源。和传统使用气体钢瓶的NO吸入装置比较,该装置实现了气体发生、流量控制和输气系统的一体化,是新型的NO发生一体机,有望适应更多的临床应用场景和临床适应证,对于非使用有创呼吸的重症患者也可以实现床旁交互使用。
[参考文献]
[1] WANG T,KEBIR D E,BLAISE G.Inhaled nitric oxide in 2003:A review of its mechanisms of action [J].Canadian Journal of Anaesthesia,2003,50(8):839-846.
[2] XU W M,LIU L Z.Nitric Oxide:from a mysterious labile factor to the molecule of the Nobel Prize Recent progress in nitric oxide research [J].Cell Research,1998,8(4):251-258.
[3] SORELLE R.Nobel Prize Awarded to Scientists for Nitric Oxide Discoveries [J].Circulation,1998,98(22):2365-2366.
[4] MIRANDA M M,PANIS C,CATANEO A H D,et al.Nitric oxide and brazilian propolis combined accelerates tissue repair by modulating cell migration,cytokine production and collagen deposition in experimental leishmaniasis[J].PLoS ONE,2015,14(10):e0125101.
[5] LUO J D,CHEN A F.Nitric oxide:a newly discovered function on wound healing [J].Acta Pharma-cologica Sinica,2005,26(3):259-264.
[6] COLEMAN J W.Nitric oxide in immunity and inflammation[J].International Immunopharma-cology,2001,1(8):1397-
1406.
[7] CHOUDHARI S K,MINAL CHAUDHARY.Nitric oxide and cancer:a review [J].World Journal of Surgical Oncology,2013,11(1):118.
[8] SCHAIRER D O,CHOUAKE J S,NOSANCHUK J D,et al.The potential of nitric oxide releasing therapies as antimicrobial agents [J].Virulence,2012,3(3):271-279.
[9] ANN D G M,FANG F C.NO Inhibitions:Antimicrobial Properties of Nitric Oxide [J].Clinical Infectious Diseases 1995;21(S2):162-165.
[10] SAURA M,ZARAGOZA CMCMILLAN A,QUICK R A,et al.An antiviral mechanism of nitric oxide:inhibition of a viral protease [J].Immunity,1999,10(1):21-28.
[11] ABMAN S H.Inhaled Nitric Oxide for the treatment of Pulmonary Arterial Hypertension [J].Handbook of Experimental Pharmacology,2013,218(218):257-276.
[12] AFSHARI A,BROK J,ANN MERETE,et al.Inhaled nitric oxide for acute respiratory distress syndrome (ARDS) and acute lung injury in children and adults [J]. Cochrane Database of Systematic Reviews,2010,7(7):2787.
[13] CHEN L N,LIU P,GAO H,et al.Inhalation of Nitric Oxide in the Treatment of Severe Acute Respiratory Syndrome:A Rescue Trial in Beijing[J].Clinical Infectious Diseases,2004,39(10):1531-1535.
[14] KINSELLA J P,ABMAN S H.Inhaled Nitric Oxide in the Premature Newborn [J].Journal of Pediatrics,2007,151(1):10-15.
[15] KINSELLA J P.Inhaled nitric oxide in the term newborn [J].Early Human Development,2008,84,709-716.
[16] CATHIE K,HOWLIN R,CARROLL M,et al.G385 RATNO-Reducing Antibiotic Tolerance using Nitric Oxide in Cystic Fibrosis:report of a proof of concept clinical trial[J].Archives of Disease in Childhood,2014,99:159.
[17] SILVA S Y,RUEDA L C,GUSTAVO A MARQUEZ,et al.Double blind,randomized,placebo controlled clinical trial for the treatment of diabetic foot ulcers,using a nitric oxide releasing patch:PATHON[J].Trials,2007,8(1):26.
[18] JAMES C,MILLAR J,HORTON S,et al.Nitric oxide Admini-
stration during paediatric cardiopulmonarybypass:a randomised controlled trial[J].IntensiveCare Medicine,2016,42(11):1744-1752.
[19] CHILETTI R,Horton S,Bednarz A,et al.Safety of nitric oxide added to the ECMO circuit:a pilot study in children [J].Perfusion,2017,33(1):74-76.
[20] MILLER C,MILLER M,MCMULLIN B,et al.A phase I clinical study of inhaled nitric oxide in healthy adults[J].Journal of Cystic Fibrosis,2012(11):324-331.
[21] BENTUR L,GUR M,ASHKENAZI M,et al.Pilot study to test inhaled nitric oxide in cystic fibrosis patients with refractory Mycobacterium abscessus lung infection[J].Journal of Cystic Fibrosis,2020,19(2):225-231.
[22] TSUKAHARA H,ISHIDA T,TODOROKI Y,et al.Gas-phase Disproportionation of Nitric Oxide at Elevated Pressures[J].Free Radical Research,2003,37(2):71-177.
[23] 醫用电气设备 第1~2部分:安全通用要求 并列标准:电磁兼容 要求和试验:YY 0505—2012[S].
[24] 工业、科学和医疗(ISM)射频设备 骚扰特性 限值和测量方法:GB 4824—2013[S].