ELISA检测献血者抗-HCV室内质控异常失控1例报告
2020-11-17贾波
贾波
(济源市中心血站 质控科,河南 济源 459000)
采供血机构对血液的筛查项目主要包括乙型肝炎病毒(hepatitis B virus,HBV)、丙型肝炎病毒(hepatitis C virus,HCV)、人类免疫缺陷病毒(human immunodeficiency virus,HIV)、梅毒螺旋体(treponema pallidum,TP)等感染标志物检测。试验方法可分为血清学检测抗原、抗体的酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA)或化学发光免疫分析(chemiluminescence immunoassay,CLIA),以及用于HBV-DNA、HCV/HIV-RNA的核酸检测。其中,ELISA或CLIA试验的室内质控通常采用试剂盒阴阳性对照、弱阳性质控品实时监控试验的有效性,同时采用弱阳性质控品和Levey-Jennings(L-J)质控图监控试验的稳定性[1]。本文对1例ELISA检测献血者抗-HCV室内质控异常失控结果进行快速分析处置,在明确诱因的基础上进一步提出防范措施,现报告如下。
1 材料与方法
1.1 一般资料2020年4月7日,济源市中心血站在进行献血者血液样本ELISA初、复检过程中,复检组抗-HCV项目室内质控结果异常失控,随即展开调查、分析与处置。
1.2 试剂与仪器抗-HCV ELISA试剂盒(某药业股份有限公司,批号20190701),抗-HCV质控品0.03 Ncu·mL-1(康彻斯坦生物,批号201906001),AE 280、AE 288全自动酶免分析仪(深圳爱康医疗电子),室内质控软件(唐山启奥SHINOW 9.0)。
1.3 方法对试验过程中人、机、料、法、环等关键环节进行追溯分析,并以初检设备(AE 280)、复检设备(AE 288)及手工操作的方法分别对在用试剂、库存试剂进行试验分析,纠正失控诱因后重新比对检测冷藏保存7 d以内的已检合格样本。
2 结果
2.1 试验过程追溯分析结果当日复检组进行ELISA检测抗-HCV两批次,室内质控结果均违背13s规则,同一设备检测其他项目均在控;试验过程追溯分析未见明显异常。见表1。
2.2 在用试剂、库存试剂以不同仪器及手工试验分析结果在用试剂、库存试剂以不同仪器及手工试验分析,在用试剂室内质控结果均失控,库存试剂室内质控结果均在控。见表2。
2.3 比对检测分析结果以库存试剂重新比对检测冷藏保存7 d以内的已检合格样本494份(分6批次完成试验),室内质控结果均在控,样本检测结果均符合。质控图见图1。

表1 试验过程追溯分析结果
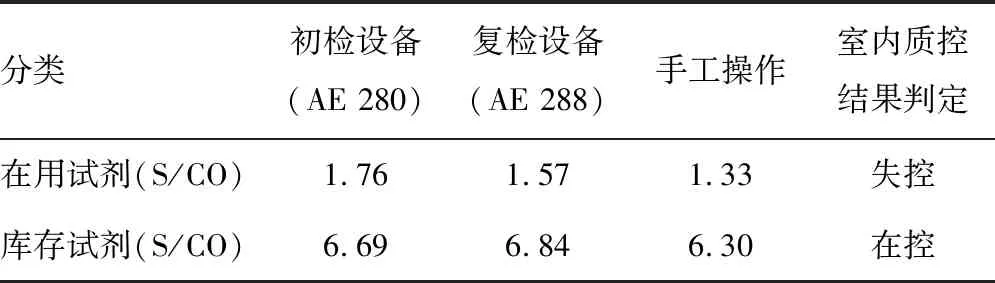
表2 在用试剂、库存试剂以不同仪器及手工试验分析结果
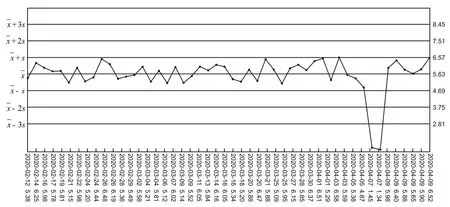
图1 质控图
3 讨论
试验分析结果证实(表2),对在用试剂分别采用初检设备(AE 280)、复检设备(AE 288)、手工操作的方法进行重复试验分析,其室内质控结果均违背13s规则(为不影响整体质控数据计算,仅在表2中列出质控品检测的S/CO结果,未在质控图中标注),采用同样方法对库存试剂进行试验分析,室内质控结果均在控。在以上试验验证抗-HCV项目同时,HBsAg、抗-HIV和TP项目也同步进行了验证,室内质控结果均在控。至此,可基本确定本例ELISA检测抗-HCV室内质控异常失控原因与第2次采购的试剂在使用中检测性能降低有关。再次以库存试剂分6批次比对检测冷藏保存7 d以内的已检合格样本494份,室内质控结果均在控(见图1质控图中4月9日的6个质控点),样本检测结果均符合,进一步佐证了在用试剂在使用中检测性能降低导致失控的诱因分析。
导致试剂性能发生变化的常见因素包括:(1)试剂盒稳定性试验不好,试剂在储存、运输过程中温度发生改变,导致试剂盒内有效成分发生变化[6]。其中尤以冷链控制最为关键,其储存温度要求为2~8 ℃,低温冰冻或超温均可导致酶活性改变,而相对于试剂的运输,现行物流体系大多难以将其控制在一个非常理想的状态,存在季节变化、冷链方式、供货渠道、运输途径以及路途、时间等诸多因素影响。(2)试剂盒临近有效期,试剂检测性能下降,导致室内质控结果逐渐降低,在排除人为原因和设备因素情况下,若失控仍未纠正,则考虑试剂性能发生变化[7]。
本例异常失控给采供血工作带来的风险在于:(1)直接导致血液检测报告不能在预定的时间发放,临床急诊/预约的单采血小板或其他特殊血液制品面临延期发放及过期报废的重大风险,严重影响临床供血及时性、安全性;(2)相同批号试剂存在3次购入过程,不同的发货、运输、交接等环节增加了不可控风险的发生概率;(3)试剂接近效期存在检测性能降低的可能性,本例中,若第3次购入的试剂同样存在检测性能降低并继续导致室内质控结果失控,重新组织新批号试剂或不同厂家试剂的评审、采购、确认、使用等将会是一个漫长的过程,无疑会给采供血机构带来严峻的考验;(4)异常失控导致试剂、耗材等资源浪费,增加了无偿献血工作成本投入。
需要注意的是,室内质控结果失控往往不是某一个独立因素导致。就该例而言,同批号、不同进货时间的试剂发生室内质控结果失控应引起相关人员的高度重视。首先,应注重试剂使用过程中的异常趋势分析,第2批试剂于4月1日投入使用,本例失控前的室内质控结果已出现降低的趋势;其次,应重视试剂正式投入使用前的确认工作,尤其不能因试剂批号完全相同而放松警惕,若该批试剂在正式投入使用前已发现性能减低,至少能为纠正措施的实施提供时间上的保障;最后,应探讨建立行之有效的应急预案,重点包括备用试剂、仪器等管理,必要时参考核酸集中化检测模式建立异地实验室之间的互为备份检测方式,充分保障应急情况下血液检测结果的及时性、有效性。
综上所述,本例中ELISA检测抗-HCV室内质控结果的异常失控,其主要诱因与在用试剂检测性能降低有关,强化试剂库存管理,重视试剂性能监控,创新失控应急预案,可作为今后规避类似失控风险、保障血液检测结果及时有效的参考策略。
