对基于重点监管化工工艺开展反应热安全评价的思考
2020-11-05高建村王胜男任绍梅詹建蒂刘思思
高建村 王胜男 任绍梅,2 詹建蒂 刘思思
(1.北京石油化工学院 安全工程学院,北京102617;2.北京市安全生产工程技术研究院,北京 102617)
0 引言
近年来化工企业危险化学品火灾、爆炸事故,对我国安全生产与化工行业发展产生比较严重的负面影响,特别是精细化工企业反应热失控引发的安全事故受到广泛关注。如:2017年2月内蒙古阿拉善盟立信化工有限公司对硝基苯胺车间发生爆炸事故,事故原因是事故企业在应急电源不完备的情况下擅自复产,遭遇大雪天气致使企业所在工业园区全面停电,未能按照规定启动应急电源导致对硝基苯胺车间反应釜无法冷却降温,引发反应釜超温超压发生爆炸;同年7月江西九江彭泽县矶山工业园区之江化工公司胺化反应(属于重点监管的危险化工工艺)装置生产过程中冷却失效,恰巧该装置安全联锁设备被企业违规停用,大量反应热不能及时通过冷却介质移除,体系温度不断升高超过200℃,反应产物对硝基苯胺发生分解,导致体系温度、压力极速升高造成爆炸。这些事故说明,反应热积累造成反应器内温度超限,是导致化工装置燃烧爆炸事故的重要原因之一。
化学反应过程中的热安全问题表现在2个方面:热安定性与热危险性[1]。热安定性是指参与反应过程的化学物质或者物料体系的热稳定性;热危险性是指化学反应过程当中存在的危险特性,突出表现在反应热失控[2]。其中针对反应热失控的热危险性研究更加引人关注。Ciba.Geigy公司统计分析了1971-1980年10年间的化工厂事故,结果显示56%的事故都是由反应热失控或近于失控所造成;日本对间歇式化学工艺事故进行了统计分析,结果显示有51%~58%的着火源均由反应热失控引起,2者结果近乎相似[1]。目前国际上己将反应失控作为了重要的研究课题开展研究和交流,是安全工程领域研究的一个重要内容[3-4]。然而此课题也具有一定的局限性,如不能制定统一的安全应急措施,需要根据不同的反应,制定不同的安全方案;如实际生产过程中,反应釜容积与工艺原理都不同,需做不同的工艺放大试验,过程中也会遇到其他问题。另外原国家安全监管总局《关于加强精细化工反应安全风险评估工作的指导意见(安监总管三〔2017〕1号)》[5],准确把握精细化工反应安全风险评估范围和内容仍然有许多不好把握之处。针对这些问题,本文在全面论述反应热危险性评价方法的建立、化工工艺热安全评价研究、化工过程热危险性分析应用以及重点监管化工工艺等方面的基础上,总结反应热安全评价研究领域存在的部分问题以及对今后研究方向进行展望。
1 反应热危险性评估方法的建立
1988年Gygax较为详细的阐述了在化工生产工艺中的热危险性,首次提出温度参数—目标反应发生失控时体系所能达到的最高温度(Maximal Temperature Attainable by Runaway of the Desired Synthetic Reaction,MTSR),这一参数很好的表征反应的热积累情况。他认为工艺过程发生热失控的根本原因都是由于反应的放热速率超过了冷却设备的散热能力,冷却失效是其中最为严重的情形,因为此时反应体系处于绝热模式下,目标反应失控导致的热积累引发了二次分解反应,致使反应体系的温度、压力的继续升高[6]。学者Grewer总结出对于聚合、重氮化、加氢等目标反应和二次分解反应的测试评估和实验方法,初步总结出评估流程图[7]。
Stoessel在上述研究的基础上,依据危险度的定义,从风险评价角度出发将反应发生失控的危险分为可能性和严重度2个方面,再将反应的热危险从低到高划分为1-5危险程度级别,最终形成了评估化学反应失控热危险性的系统化流程,对研究化学工艺过程反应热安全评价提供很好的理论基础[8-9],如图1。
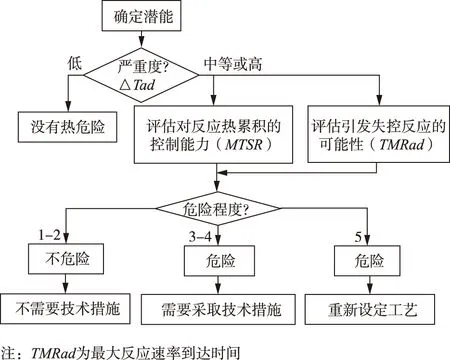
图1 评估化学反应失控热危险性的系统化流程Fig.1 A systematic process for assessing the thermal risk of uncontrolled chemical reactions
还有许多学者研究了间歇与半间歇反应模式下的热危险性,涉及反应条件和参数评估方法等内容,总结反应失控模型、安全操作的临界条件及评价方法,如M.A.Alós等学者基于李亚普诺夫指数的判据,提出将热失控区描述为设计参数的一种新的热稳定性评价方法[10-11]。还推导得出了适用于不同反应模式的反应放热速率、绝热温升等安全性参数的计算公式,如P.Hugo等学者利用达姆科勒数得出反应器温度方程的最优条件为B=2/(1-XS)[12-13],其中,XS为转化率;B为热反应数,这些研究对反应过程安全性和工艺优化具有很大的意义。
Huiping Liu等利用绝热加速量热(Accelerat-ing Rate Calorimeter,ARC)具体研究了氢过氧化叔丁基(Tert-butyl Hydroperoxid,TBHP)的热稳定性,依据实验结果估算绝热条件下TBHP放热反应的动力学参数,并计算了实际绝热条件下的绝热温升130.07℃,最大温升速率165.33℃/min和摩尔反应热184.50kJ/mol等热危害参数,提出温度高于145℃时若不采取措施控制温度,TBPH分解迅速,反应将达到不可控状态。总结出氢过氧化叔丁基在生产、运输和储存过程中的环境温度应控制在55.6℃以下,防止反应变得无法控制,最终导致火灾爆炸事故[14]。
2 化工工艺热安全评价研究
2.1 实验研究
早期国外对化工工艺的热危险性就有较为详细的描述研究,虽未形成完整的评价体系,但无论是对间歇还是半间歇反应其热释放速率、绝热温升等安全参数的计算公式,都可为过程安全和工艺优化提供好的参考,可依据冷却失效情形图及MTSR这一数据总结出失控反应模型及安全操作条件[6,12-13,15],冷却失效情形图,如图2。
国内对反应过程热危险性方面的研究工作开展较晚,故对工艺反应过程的这方面研究内容较窄,学者们主要以反应量热仪为主,DSC、DTA、ARC等仪器为辅进行实验探究,针对各种反应体系进行针对性研究,为工艺安全控制提供理论基础和实验依据。比如周诚等利用反应量热器测定了FOX-7硝化反应加料过程的平均放热速率是保温反应过程的2倍,提出了在规模化试验中降低硝化反应过程中的热危险性措施[16]。庄众利用全自动反应量热仪(RCle)测试了醋酸酐水解反应的热力学数据,建立反应动力学模型,获得不同温度转速条件下的动力学参数,总结出安全界限图从而进行反应过程的热安全性研究[17]。杨庭利用DSC、ARC、反应量热仪得出硝酸异辛酯的反应温度高于25℃,易引发反应失控,最后用风险矩阵法和热失控情形分析方法分析总结出硝酸异辛酯的生产过程只能在20℃以下的温度进行[18]。
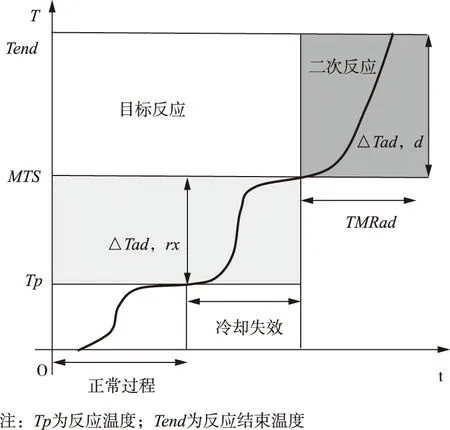
图2 冷却失效情形图Fig.2 Cooling failure scenario diagram
2.2 理论分析
反应热安全评价研究过程,涉及热动力学、热危害分析技术、热失控等多种基本理论。Shang Hao Liu等在2015年利用热危害分析技术理论对工艺过程中偶氮化合物和有机过氧化物的危害行为进行了表征,为热稳定性、不相容性、最低放热温度和危险后果分析等的理论研究提供了基础[19]。2017年Shang Hao Liu等又基于Friedman、Flynn-Wall-Ozawa、ASTME698-11、Kissinger 4种不同的热动力学理论方法结合差示扫描量热的热危害分析技术理论评估了2,2’-偶氮基-(2-甲基丁腈)在生成过程中的基本动力学参数和主要热危害,并提出其周围温度为323.0~333.0K时,工作温度应低于临界温度[20]。Qingsong Wang等总结了热失控理论及相关理论,对未来锂离子电池的安全发展提出展望[21]。
2.3 数值模拟评价
近年随着科学与化工热动力学技术发展,数值模拟技术预测任意温度模式下目标反应的热稳定性及其反应进程成为可能。热动力学分析模拟软件(Advanced Kinetics and Technology Solutions,AKTS)热动力学分析模拟方法在辅助理论及试验研究方面应用广泛,有效实现了工艺放大及热稳定性预测等研究,还可节约实验成本,缩短反应研究周期等[22-23]。由于利用大型反应釜进行试验的不现实性,决定了借助AKTS热动力学分析模拟技术直接分析计算多步反应的动力学参数可能性。有关反应热的数值模拟研究较少,已有少数研究主要借助研究目标反应物的特性理论,利用多种量热仪器,得出目标反应的反应热、热分解特性及反应进程。如俞进阳等借助AKTS模拟研究了绝热与等温条件下绿焰剂的热稳定性能[24]。张巍青等借助AKTS模拟研究了硝酸铵在绝热条件下的TD24(反应体系达到最大反应速率所需要的时间为24h的温度)为137.2℃,根据实验与模拟最终评估硝酸铵的风险等级为Ⅱ级,为有条件可接受风险[25]。Shang Hao Liu等利用AKTS模拟评估研究得到热稳定较为规范的2,2’-偶氮基-(2-甲基丁腈),并得出其放热反应阶段本质上是一个相对简单的模型,但通过对实验结果的模拟得出最佳方法是采用n阶反应模拟[20]。
3 化工过程热危险性分析应用
反应过程热危险性分析评价方法有风险矩阵法[26-27]、失控情形分析方法[7-8]和安全界限图法[28]等,但因安全界限图法的提出是依据反应系统对温度具有敏感性的特点,大部分学者认为对反应失控评估及优化而言较为简单,不能完全反映生产工艺中的热危险特性[29-30],还有学者认为此方法未考虑到产物二次分解的问题[17],故大部分研究主要运用前2种评价方法。如陈利平运用了风险矩阵法和失控情形分析法判断甲苯一段硝化二次反应失控的可能性与严重度,最后得出热危险性为“可接受风险”[31]。杨茜利用风险矩阵法和失控情形分析法对某医药中间体合成的3个反应过程分别进行工艺热危险性分析,得出反应1(二氯甲烷、乙酸酐和原料A与原料B在35~40℃条件下反应)、反应2(反应1所得混合物与原料C在70℃条件下反应)、反应3(反应2所得混合物中加入乙醇、水于室温条件下与原料D反应)的热风险等级分别为三级、一级、三级,均为可接受风险,只需采取适当的措施就可使风险可控[32]。此外鲍士龙、彭浩梁等人在对目标反应进行热安全性研究时,都采用此种方法[33-34],见表1-3,如图3。
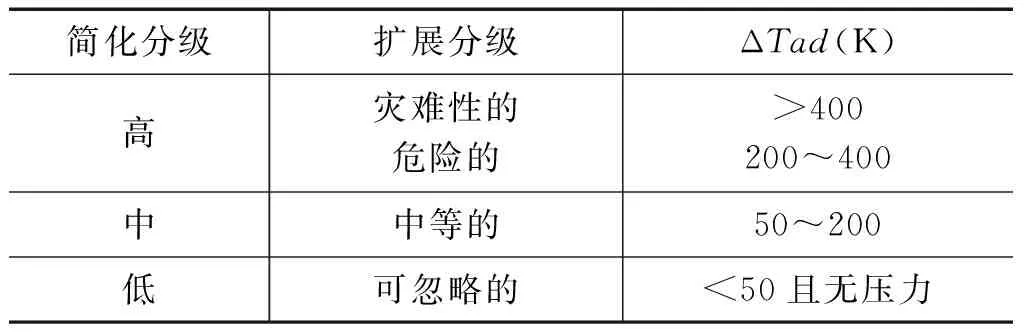
表1 失控反应的严重度等级Tab.1 The severity of the uncontrolled response

表2 失控反应的可能性评估标准Tab.2 Assessmentcriterion on the possibility of an uncontrolled reaction
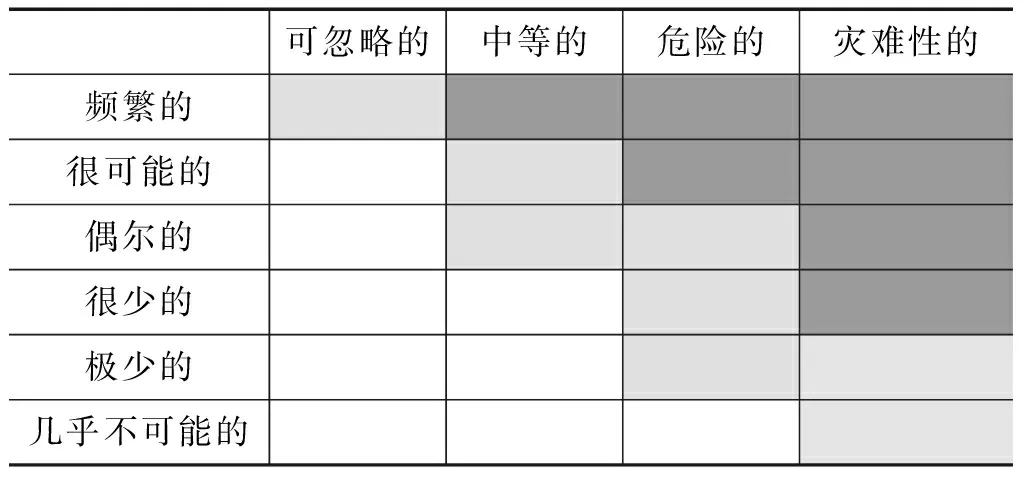
表3 风险评价矩阵Tab.3 The risk evaluation matrix
风险矩阵法是利用绝热情况下的最大反应速率到达时间(TMRad)来评估反应发生风险的可能性,即利用表2判定事故可能行的准则,再结合表1判定失控反应的严重度即可,最后利用表3风险矩阵评估失控反应的风险。
根据参数Tp、MTSR、MTT和TD24数据,利用图3判断4个数据的大小关系,即对反应危险程度进行分级,继而采取相应的技术措施保障安全。其实对于失控反应的可能性而言,目前尚无直接定量分析的方法,但是可依据半定量化方法对反应进行风险分析。
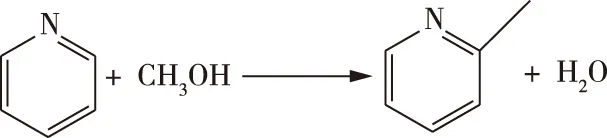
在对醋酐法合成奥克托今工艺加料过程的热危险性研究时通过4次实验得出MTSR为70.55℃,TMRad远远大于100h,对应上表2可能性为“几乎不可能的”;最大绝热温升99.96℃、最小绝热温升63.63℃,对应上表1严重度为“中等的”;最后结合上表3说明加料过程的风险等级为“风险可接受”。又已知加料过程的Tp值为45℃;反应物料醋酸的沸点值MTT值为118℃;在绝热量热实验中,基于修正后的TMRad曲线图利用外推法得出TD24为111.89℃。综上得出Tp 图3 由Tp、MTSR、MTT和TD24判别的危险级别Fig.3 Hazard levels obtained by Tp,MTSR,MTT,and TD24 根据原国家安全监管总局《关于加强精细化工反应安全风险评估工作的指导意见(安监总管三〔2017〕1号)》要求,开展反应安全风险评估的反应应该是涉及重点监管危险化工工艺和金属有机物合成反应(包括格氏反应)的间歇和半间歇反应并且有以下情形之一的:国内首次使用的新工艺、新配方投入工业化生产的以及国外首次引进的新工艺且未进行过反应安全风险评估的;现有的工艺路线、工艺参数或装置能力发生变更,且没有反应安全风险评估报告的;因反应工艺问题,发生过生产安全事故的。在实际应用中,虽然目前国家颁布的18种[35]重点监管的化工工艺有具体列举了典型工艺,但是在准确把握精细化工反应安全风险评估范围和内容方面仍然有许多不好把握之处。 例如:其中第10种重点监管的氧化反应中,常用的氧化剂明确有双氧水;双氧水为氧化剂与甲基吗啉生成氧化甲基吗啉的工艺过程,具体方程式如下: (1) 此反应工艺未列入重点监管的典型工艺,但是反应原料及产品具有燃爆危险性,吗啉的闪点为14℃,反应气相组成容易达到爆炸极限,具有闪爆危险。但是目前研究多以甲基吗啉与氧化甲基吗啉的催化、合成为主[38-41],多在以双氧水为氧化剂、不同催化剂的条件下进行,通过多种表征和实验手段研究反应温度、原料配比等对物质合成产率的影响,得出加催化剂比不加催化剂物质的产率要高30%左右,针对此反应的反应热安全评价研究较少。但与双氧水相关的反应还是存在潜在的危险,如山东国金化工厂2012年8月25日双氧水分解产生的压力和热量无法释放和移走、分解加剧,致氧化塔发生爆炸,造成3人死亡,7人受伤,重视与双氧水相关工艺的危险等级评定必要的。 再如,第15种重点监管的烷基化反应中,列举出典型工艺O-烷基化反应的实例中就有高级脂肪醇或烷基酚与环氧乙烷加成生成聚醚类产物的反应: (2) 以上反应为非离子表活剂壬基酚聚氧乙烯醚的制备反应方程式。但在某些企业以四甲基哌啶醇与环氧乙烷为原料,反应合成N-(2-羟乙基)-2,2,6,6-四甲基哌啶醇,与之有相似之处,具体反应方程式如下: (3) 该反应初步试验放热量较大,3.82mol 4-甲基哌啶醇与3.86mol环氧乙烷反应的单釜放热量达到573 248kJ/h,目前针对4-哌啶醇[36]、N-(2-羟乙基)-2,2,6,6-四甲基哌啶醇[37]等的研究以制备、合成工艺为主,而针对其反应热危险特性及反应安全风险评估的研究极少。环氧乙烷属于易燃易爆的危险化学品,闪点-29℃,爆炸极限(V/V):3%~100%,生产和使用环氧乙烷的化工企业常常发生燃烧爆炸事故,1999年3月30日,湖北荆州石化总厂在未控制进料速度的情况下造成环氧乙烷进料速度过快,反应釜内压力迅速上升,高压气体急剧喷出产生静电引发爆炸,造成4人死亡,直接经济损失45万元。因此,在依据已经颁布的18种重点监管的化工工艺所列举的典型工艺开展热安全评价时,应当全面考虑反应物的热安定性和反应的热危险性,实事求是的根据反应物料、化工工艺和反应热效应进行综合判断;对于类似工艺曾经发生过工艺安全事故的、未列入重点监管化工工艺的典型工艺但是热安全基础数据不全的建议应当进行反应热安全风险评估。 精细化工反应常有高压反应,通常高压反应都具有一定的反应热危险性,现有的反应热测定方法主要适用于常压反应,准确测量高压条件下反应热主要困难有:适用于高压反应热测定仪器设备少、价格昂贵;高压反应的反应热测定基础数据较少,模拟研究难以准确进行;高压条件下化学反应量热标定方法受到考验,对反应热模拟计算结果产生很大影响。 以吡啶选择性催化甲基化生产2-甲基吡啶的为例,生产条件为200℃,3.5MPa,具体反应方程式如下: (4) 目前利用某全自动反应量热仪高压釜进行反应量热实验,通过实验发现标定方式对实验结果影响较大;若先施加反应压力再进行标定,由于反应过程中随着温度升高压力也会不断升高,一定会造成反应压力过高;若先标定再加压,会造成二次标定与一次标定数据波动较大,造成结果误差较大,难以得到良好的实验结果。 图4表明先标定再进行加压会导致原本平稳的反应功率曲线突然下降并出现尖峰,从而导致标定数据出现较大误差。 图4 先标定再加压的数据波动过程Fig.4 The data fluctuation process after calibrating and pressuring 加大力度优化高压模拟软件、探索新标定方法,对精细化工反应热安全评价具有重要意义。 (1)针对反应热失控的热危险性,利用系统化的评估流程有助于正确评估各项工艺反应热安全风险,对精细化工行业具有现实的指导意义。精细化工工艺的热安全评价研究可在实验研究的基础上,结合理论分析和数值模拟等研究手段,准确确定反应热、ΔTad、MTSR,为理论研究或经验模型开发提供依据,为精细化工工艺热安全及其热危险性评价提供更准确的判断及研究依据。 (2)精细化工反应安全风险评估范围和反应工艺在危险定性方面仍然有难以准确界定之处,针对已经颁布的重点监管化工工艺目录进行判断时,应在考虑反应物的热安定性和反应的热危险性的基础上根据反应物料、化工工艺和反应热效应具体情况先进行实验室规模实验,开展反应热安全风险评估等再进行实事求是的判断。 (3)精细化工高压反应较为常见,但针对高压反应的准确测定无论是反应量热仪、模拟计算软件还是标定实验方法等存在标定误差较大、标定过程压力难于精准控制等问题,可尝试优化高压模拟软件、探索新标定方法。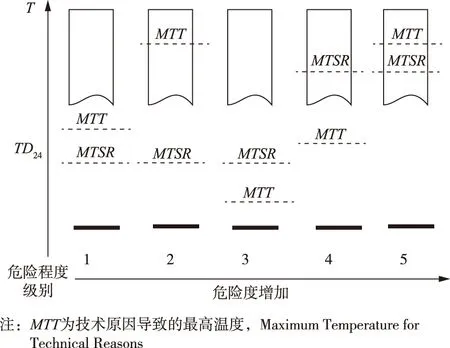
4 对热安全评价个别问题的探讨
4.1 重点监管危险化工工艺的界定
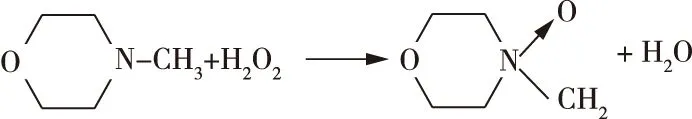
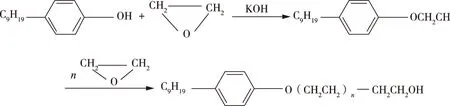
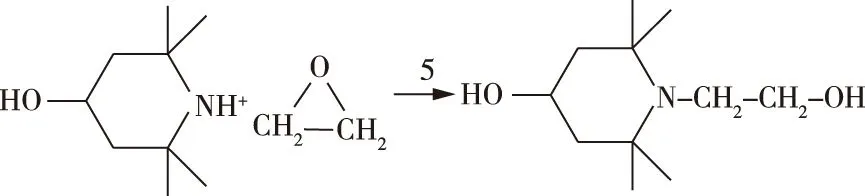
4.2 高压精细化工反应热的精确测定

5 结论
