农田土壤对磺胺甲恶唑和双酚A的吸附
2020-11-02张海洋陈凌源何鸿庆
张海洋 陈凌源 何鸿庆


摘要 为探究磺胺甲恶唑(SMX)和双酚A(BPA)在南充农田土壤中的迁移特性,采用静态批量吸附试验,研究SMX和BPA在黄土(LS)和红土(RC)2种典型农田土壤中的吸附过程,以及土壤有机质(SOM)和水溶性有机质(DOM)对2种有机污染物吸附行为的影响。结果表明,SMX和BPA在2种土壤中的吸附动力学与吸附热力学过程均符合准二级动力学模型和Freundlich模型,属于多层化学吸附。SOM含量是影响SMX和BPA吸附的重要因素,而DOM能增强土壤对SMX吸附。SMX在2种农田土壤中的迁移能力强(KOC=60.04、42.88),BPA在2种农田土壤中迁移能力较弱(KOC=921.52、393.87)。
关键词 磺胺甲恶唑;双酚A;吸附;污染物;迁移
中图分类号 X131.3 文献标识码 A 文章编号 0517-6611(2020)19-0060-05
doi:10.3969/j.issn.0517-6611.2020.19.017
Abstract Adsorption and migration processes were studied for the sulfamethoxazole (SMX) and bisphenol A (BPA) in two cropland soils. Batch experiments were used to conduct kinetic and thermodynamics studies, as well as to evaluate adsorption for SMX and BPA on Loess (LS) and Red Clay (RC).The correlations between soil organic matter (SOM), dissolve organic matter (DOM) and the adsorption of SMX, BPA in soils were also studied. The results showed that the adsorption kinetics and adsorption thermodynamic process of SMX and BPA in the two soils were in accordance with the quasisecondorder kinetic model and the Freundlich model, which belong to multilayer chemical adsorption.SOM content was an important factor affecting the adsorption of SMX and BPA, and DOM could enhance the adsorption of SMX to soil.SMX had strong migration ability in two farmland soils (KOC=60.04,42.88), and BPA had weak migration ability in two farmland soils (KOC=921.52,393.87).
Key words Sulfamethoxazole;Bisphenol A;Adsorption;Pollutant;Migration
基金项目 化学合成与污染控制四川省重点实验室开放基金(CSPC201 902);南充市科技计划研发项目(19YFZJ0112)。
作者简介 张海洋(1996—),男,四川巴中人,硕士研究生,研究方向:有机污染物在土壤中迁移转化。 *通信作者,副教授,博士,硕士生导师,从事污染物在土壤中迁移转化研究。
收稿日期 2020-01-12
磺胺甲恶唑(SMX)作为常见抗生素,常被用来治疗和预防动物疾病[1],研究表明约80%的磺胺类药物会被生物体排入环境中[2]。目前城市污水处理對SMX的去除率较低,因此SMX成为在再生水体中和农田土壤样品中最常检测出的有机污染物之一[2]。有研究表明,抗生素的使用会使多种细菌产生耐药性,形成大量抗药细菌,极大地威胁人们的健康[1]。双酚A(BPA)是类激素物质中极具代表的物质之一,在塑料制品广泛应用的今天,BPA作为塑料的添加剂,已对环境造成了严重的污染[3]。BPA具有很强的生物毒性,即使很少低的浓度也会对生物体造成严重的影响[4],因此研究SMX、BPA等物质的环境行为和风险迫在眉睫。
南充是传统农业型城市,农业发展条件和基础相对较好,一直以来都是国家重要的商品粮和农副产品生产基地[5],因此农业安全对人们健康极为重要。农畜业的迅速发展,使得抗生素被大量使用,牲畜排泄物的堆肥、农家肥的使用、污水灌溉等使得SMX、BPA进入到农田。目前在水体中、土壤中均已经检测到SMX、BPA的存在[4]。SMX在土壤中较稳定,易长期残留在土壤中[6]。长期暴露在这2种有机污染物环境中,即使是mg/L 的浓度级别,也会使生活中该环境中的生物体发生慢性中毒[7]。
目前已有学者对SMX、BPA在高有机质土壤[8]、沉积物[9]、川西贝沙土[4]、滇池泥炭土[2]、西班牙农田土壤[10]等吸附材料中的吸附迁移过程进行了研究。研究表明土壤有机质(SOM)[4]、水溶性有机质(DOM)[11]会影响土壤中污染物的迁移。但对于SMX、BPA在南充农田土壤的吸附特性研究较少,SMX、BPA在该地区农田土壤中的迁移吸附机制尚不清楚。且目前南充农业耕作依然沿用传统方式,农田土壤与人体接触频率高,因此研究SMX、BPA在南充农田土壤中的迁移刻不容缓。
南充农田土壤主要以黄土和红土为主,笔者选取黄土(LS)、红土(RC)2种农田土壤作为试验材料,并以森林土作为对照,探究SMX、BPA在农田土壤中的吸附行为和机制,以期为SMX、BPA在南充农田土壤中的吸附迁移过程和环境风险评估提供科学依据。
1 材料与方法
1.1 吸附剂的制备
供试样品土壤采样深度为0~10 cm,在南充市嘉陵区新收稻田中采集LS,在南充市顺庆区蔬菜种植用地中采集RC。并在森林密集地区采集由多年掉落物覆盖下0~10 cm深度、有机质含量较高的6种土壤,分别命名为FS1、FS2、FS3、FS4、FS5、FS6。采样点选择远离污染地点的山区农田和深山森林。将样品避光条件下风干,过2 mm筛去除土壤中的植物残体及石砾。
1.2 土壤理化性质表征
对土壤样品pH采用《土壤质量pH的测定》(ISO 10390:2005)国际标准测定,SOM含量采用750 ℃热氧化法测定,DOM含量采用水溶液提取法测定[12]。pH、SOM、DOM测定结果如表1所示。
1.3 吸附试验
将一定量的土壤加入到恒定初始浓度的溶液中,添加0.01 mol/L CaCl2使土壤在吸附离子强度相似、添加200 mg/L NaN3抑制微生物的生长,以排除微生物的作用[8]。用上述浓度的无机盐溶液作为土壤吸附背景溶液。由表1可知,土壤的pH均在6左右,在吸附试验中使用1 mol/L HCl、1 mol/L NaOH将吸附溶液的pH调至6,吸附剂与溶液固液比为20∶1(mg∶mL),在298 K、180 r/min的条件下避光恒温振荡,每组试验重复3次确定试验数据的准确性。动力学试验SMX、BPA的初始浓度分别为50、100 μmol/L,动力学测定时间设置为0~480 min,时间梯度为12个。吸附热力学在298 K的恒溫条件下完成[13-14],吸附等温线试验溶液的初始浓度分别为CSMX=2~100 μmol/L,CBPA=10~400 μmol/L,吸附平衡时间设置为480 min。不同有机质含量土壤吸附试验,SMX、BPA浓度分别为50、100 μmol /L,8种吸附剂对污染物进行单点吸附试验,吸附平衡时间为480 min。吸附试验均使用0.45 μm滤膜过滤,取0.5 mL滤液于液相瓶中,使用HPLC检测吸附质的紫外吸收峰。
1.4 吸附质定量分析
采用Agilent 1200 型高效液相色谱仪(HPLC)对SMX、BPA进行定量分析,具体条件设置如表2所示,Agilent C18反相柱(4.6 mm×150 mm,5.0 μm)。
2 结果与分析
2.1 吸附动力学
从图1可以看出,LS、RC对SMX、BPA的吸附都表现出快吸附和慢吸附2个阶段。在吸附的前1 h吸附迅速,这是因为在初始阶段吸附剂表面吸附点位充足,能够为污染物提供充足的吸附点位,在短时间内能够快速地吸附大量的污染物。随着时间的推移,吸附点位逐渐被SMX、BPA占据,吸附过程逐渐转向为扩散作用,使吸附阻力增加[6]。
如图1所示,2种污染物在土壤中的吸附量有着极大的差距,这可能是因为2种污染物的性质不同所表现出的结果。SMX的疏水性大于BPA(表3),但对于2种污染物的吸附容量,2种土壤吸附均表现为BPA大于SMX。造成此现象是因为土壤对SMX的吸附以疏水分配为主[15],而对BPA的吸附不仅仅是简单的疏水分配。
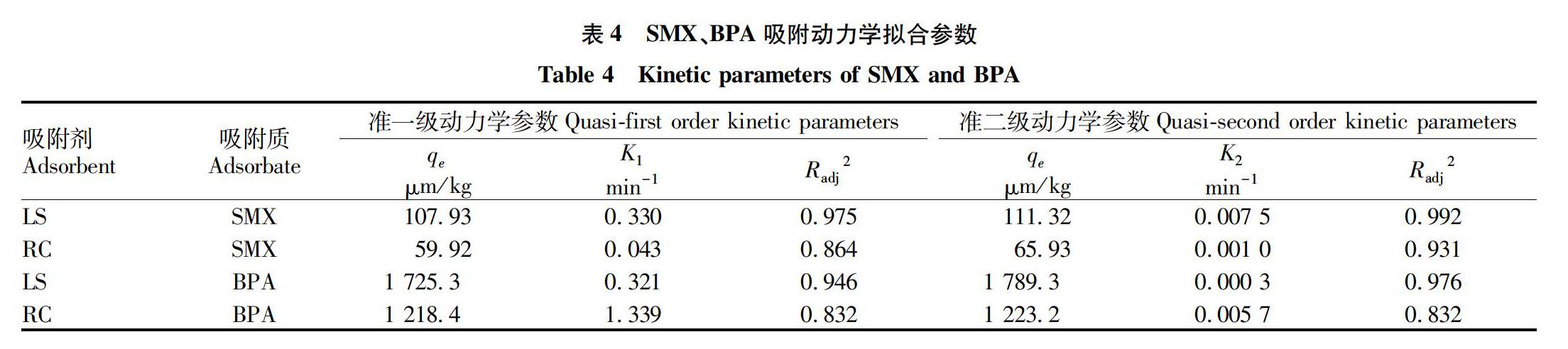
由表4可知,2种土壤对于SMX、BPA的吸附过程均更加符合准二级动力,通过准二级动力学拟合出的吸附最大量与试验所得出的吸附数据更加接近。说明SMX、BPA在吸附过程中均存在化学吸附的参与[16],其吸附过程可能是通过2种不同土壤中的部分组分和吸附质之间的电子共享或交换而发生的化学吸附[4]。
2.2 吸附等温线
从图2可以看出,LS、RC的吸附过程中,吸附质溶液浓度越大,在平衡时吸附剂吸附的有机污染物的量也有一定的增大。根据公式(2)计算得,吸附溶液浓度越大对污染物的去除率越低。2种吸附剂对SMX的吸附表现出更强的线性吸附,说明对SMX的吸附机制主要以疏水分配为主。
LS、RC对SMX、BPA的吸附等温线如图2所示,表5为Langmuir与Freundlich模型拟合数据,根据拟合数据表明Freundlich模型更加符合2种土壤对模拟污染物的吸附。说明在吸附过程中2种土壤对模拟污染物的吸附过程并不是简单的单层表面吸附,而是多层吸附,以及分子间作用力共同作用的吸附过程。此结论与吸附动力学表现出相同结论。
LS对SMX、BPA的吸附亲和力(KF)均大于RC,其表现出与测定值相符。由n值可知,在吸附过程中LS土壤表现出的线性吸附低于RC,土壤中的有机质存在大量的不均一吸附点位,因此有机质含量高的土壤可能会表现出更加强烈的非线性吸附[8]。有报道称土壤吸附的非线性可能与土壤碳含量有关[7]。土壤有机质(SOM)的含量会影响土壤对有机污染物吸附的能力。
2.3 吸附质性质的影响
多种证明有机污染物在土壤中的吸附机制主要有包括电子供受体作用、氢键、阳离子交换、静电作用等。有机物的吸附量会受到有机质的官能团种类及数量的影响,官能团的种类和数量越多越容易与土壤结合[3]。
由表3可知,SMX存在2个pKa值,且BPA的值高于SMX[13]。当pH<1.7时,SMX主要以SMX+形态存在;pH在1.7~5.7时,SMX主要以分子态存在;在pH>5.7时,SMX主要以SMX-形态存在[17]。吸附质溶液初始pH=6,在吸附过程中SMX始终以中性分子及阴离子态2种形态存在,对SMX的吸附中,静电吸引是一种吸附机制[17]。土壤中带电荷粒子众多,带电荷SMX与土壤中带同种电荷微粒相互排斥。SMX分子上较为活跃的胺基易形成氢键,但在pH=6的条件下该胺基处于离子态,不易与吸附剂直接形成分子间作用力[6]。且疏水性SMX>SMX-,分子电离导致SMX疏水分配作用降低。
在pH=6时,BPA在溶液中以分子形式存在,此时氢键、疏水作用力为土壤对BPA吸附的主要作用力,其两侧酚羟基可与吸附剂中的物质形成氢键[18]。且由表3可知BPA的结构式,其2个酚羟基呈现出蝴蝶状,使得土壤对其可能具有特异性吸附。羟基有较强的极性,因此BPA可以与土壤中的极性分子发生相互作用[3]。
2.4 土壤有机质对吸附的影响
SOM种类繁多,能够通过分子间作用力与吸附质分子上活跃的元素结合,为吸附质提供更多的吸附点位,因此SOM的含量可能会影响土壤对SMX、BPA的吸附能力[6]。表6为不同SOM含量土壤对SMX、BPA的吸附量。如图3所示,土壤中有机质的含量与土壤吸附能力呈正相关,且SOM与土壤对SMX的吸附有着极强的线性关系(Radj2=0.919),说明土壤对SMX的主要吸附贡献由SOM提供,作用力主要为疏水分配力。SOM与土壤对BPA吸附的线性关系相对较低(Radj2=0.747),说明土壤对BPA的吸附是多种作用力共同作用的结果[2]。有机质含量高的土壤含有多种官能团,SMX分子中的酰胺基较活跃,可与其他含基团相结合[8],BPA拥有2个活跃的酚羟基,在吸附过程中极易与土壤中的有机质以分子间作用力相结合,从而增加土壤的吸附容量[4]。
FS3有机质含量低于FS2,但对SMX的吸附量更大,这可能因为2种土壤在吸附时溶出的DOM量不同所造成。胡明酸会阻塞土壤微孔,抑制土壤对SMX的吸附[8]。胡明酸在弱酸性或中性条件下溶出量小,水溶性小分子有机物较为容易溶解。水溶性小分子有机质含有较多官能团,能提高土壤对SMX的吸附容量[8],使FS3对SMX的吸附量增加。
KOC为土壤有机质吸附系数,KOC为KF与土壤有机质含量的比值,可用于评估有机污染物在土壤中的迁移性。KOC在150~500表示中等遷移,在500~2 000表示低迁移[19]。根据表5拟合KF可得SMX在LS、RC上的KOC分别为60.04、42.88,BPA在2种吸附剂上的KOC值分别为921.52、393.87。因此可以得出与吸附试验相同的结论,SMX在南充农业土壤中的迁移性极强,而BPA在LS中的迁移性极低,在RC中也表现为中等迁移性。
3 结论
(1)对于LC和RS吸附SMX和BPA 的过程,动力学准二级动力学模型与事实更加符合,而热力学Freundlich模型更加符合,2种土壤对SMX和BPA的吸附过程均属于多层化学吸附。
(2)在通常情况下土壤对SMX、BPA的吸附能力与SOM呈正相关,SOM在土壤对SMX(Radj2=0.919)的吸附过程中表现出比BPA(Radj2=0.747)更加强烈的影响,而DOM能增强土壤对SMX的吸附。
(3)SMX在LS和RC中的KOC分别为60.04、42.88,BPA在LS和RC中的KOC分别为921.52、393.87。因此SMX在2种农田土壤中均表现出较强的迁移能力,BPA在LS土壤中表现出较低的迁移能力,在RC中表现出中等迁移能力。
参考文献
[1] GUO T,LOU C L,ZHAI W W,et al.Increased occurrence of heavy metals,antibiotics and resistance genes in surface soil after longterm application of manure[J].Science of the total environment,2018,635:995-1003.
[2] 高鹏,牛一帆,任欣,等.滇池泥炭土对两种抗生素和双酚A的吸附[J].中国环境科学,2019,39(10):4239-4246.
[3] QIU W H,CHEN J S,LI Y J,et al.Oxidative stress and immune disturbance after longterm exposure to bisphenol A in juvenile common carp(Cyprinus carpio)[J].Ecotoxicology and environmental safety,2016,130:93-102.
[4] 杨慧敏,李云桂,武彩霞,等.川西北沙化土壤对双酚A的吸附特征[J].中国环境科学,2018,38(4):1424-1432.
[5] 滕明鹏,李峰元,罗军,等.南充市国家现代农业示范区发展研究[J].农学学报,2019,9(1):65-81.
[6] CHEN H,GAO B,LI H,et al.Effects of pH and ionic strength on sulfamethoxazole and ciprofloxacin transport in saturated porous media[J].Journal of contaminant hydrology,2011,126(1/2):29-36.
[7] OU Y H,CHANG Y J,LIN F Y,et al.Competitive sorption of bisphenol A and phenol in soils and the contribution of black carbon[J].Ecological engineering,2016,92:270-276.
[8] CHEN K L,LIU L C,CHEN W R.Adsorption of sulfamethoxazole and sulfapyridine antibiotics in high organic content soils[J].Environmental pollution,2017,231(Pt 1):1163-1171.
[9] FEI Y H,LEUNG K M Y,LI X Y.Adsorption of 17 αethyl estradiol with the competition of bisphenol A on the marine sediment of Hong Kong[J].Marine pollution bulletin,2017,124(2):753-759.
[10] LVAREZESMORS C,CONDECID M,FERREIRACOELHO G,et al.Adsorption/desorption of sulfamethoxypyridazine and enrofloxacin in agricultural soils[J/OL].Science of the total environment,2020,706[2019-11-05].https://doi.org/10.1016/j.scitotenv.2019.136015.
[11] FANG Z,HU Y Y,WU X S,et al.A novel magnesium ascorbyl phosphate graphenebased monolith and its superior adsorption capability for bisphenol A[J].Chemical engineering journal,2018,334:948-956.
[12] TFAILY M M,CHU R K,TOYODA J,et al.Sequential extraction protocol for organic matter from soils and sediments using high resolution mass spectrometry[J].Analytica chimica acta,2017,972:54-61.
[13] NIELSEN L,BANDOSZ T J.Analysis of sulfamethoxazole and trimethoprim adsorption on sewage sludge and fish waste derived adsorbents[J].Microporous and mesoporous materials,2016,220:58-72.
[14] FOUNTOULI T V,CHRYSIKOPOULOS C V.Adsorption and thermodynamics of pharmaceuticals,acyclovir and fluconazole,onto quartz sand under static and dynamic conditions[J].Environmental engineering science,2018,35(9):909-917.
[15] DUBEY S,GUSAIN D,SHARMA Y C.Kinetic and isotherm parameter determination for the removal of chromium from aqueous solutions by nanoalumina,a nanoadsorbent[J].Journal of molecular liquids,2016,219:1-8.
[16] HASANZADEH M,SIMCHI A,FAR H S.Nanoporous composites of activated carbonmetal organic frameworks for organic dye adsorption:Synthesis,adsorption mechanism and kinetics studies[J].Journal of industrial and engineering chemistry,2020,81:405-414.
[17] REGUYAL F,SARMAH A K.Adsorption of sulfamethoxazole by magnetic biochar:Effects of pH,ionic strength,natural organic matter and 17αethinylestradiol[J].Science of the total environment,2018,628/629:722-730.
[18] 謝超然,秦婷婷,王兆炜,等.干旱区绿洲土壤对磺胺甲恶唑的吸附特性及影响因素[J].兰州大学学报(自然科学版),2018,54(5):626-632.
[19] SHEN J,WANG X Z,ZHANG Z,et al.Adsorption and degradation of 14Cbisphenol A in a soil trench[J].Science of the total environment,2017,607/608:676-682.
