LncRNA MCM3AP-AS1靶向调控miR-16-5p表达对肺癌细胞增殖、迁移侵袭的影响及机制
2020-11-02赵天增黄国胜杨金华徐萌博郭彦伟
赵天增 黄国胜 杨金华 徐萌博 郭彦伟
(1南阳医学高等专科学校第一附属医院普胸外科,河南 南阳 473000;2郑州大学第五附属医院肿瘤内科)
肺癌是世界上最常见的癌症,也是癌症死亡的主要原因〔1〕,肺癌的转移性给疾病的治疗带来很大的困难,分子靶向治疗和精准治疗已是肺癌治疗的主要趋势〔2〕。研究肺癌的分子机制,为其治疗提供更有效的分子靶点是肺癌研究的热点。LncRNA和miRNA在肺癌组织和细胞系中异常表达,研究表明LncRNA与肺癌的发生、发展和转移等密切相关,miRNA与肺癌的发生、发展、诊断、预后及耐药性等有关〔3,4〕。有报道显示,LncRNA MCM3AP-AS1在胶质瘤内皮细胞〔5〕和肝细胞癌〔6〕中表达上调,干扰或沉默其表达可抑制胶质瘤细胞增殖和侵袭,抑制肝细胞癌细胞的增殖、克隆形成并诱导细胞凋亡。在乳头状甲状腺癌中,MCM3AP-AS1表达上调并促进癌细胞的增殖、迁移和侵袭〔7〕。miR-16在肺腺癌细胞中低表达,抑制肺腺癌细胞增殖并促进细胞早期凋亡〔8〕。但MCM3AP-AS1在肺癌细胞中的表达及其对肺癌的影响,且其与miR-16-5p在肺癌中的关系目前还尚不清楚。本研究探讨LncRNA MCM3AP-AS1对肺癌增殖、迁移和侵袭的影响及miR-16-5p在此影响中的作用。
1 材料与方法
1.1材料 人肺癌细胞株A549、SPC-A1和NCI-H460及人正常肺上皮细胞BEAS-2B购自ATCC;四甲基偶氮唑蓝(MTT)、二甲基亚砜(DMSO)和胰蛋白酶购自美国Sigma-Aldrich公司;Transwell板购自美国Corning公司;引物、MCM3AP-AS1抑制物(si-MCM3AP-AS1)和过表达载体(pcDNA-MCM3AP-AS1)、miR-16-5p模拟物(miR-16-5p)和抑制物(anti-miR-16-5p)、空载体pcDNA和相应阴性对照、双荧光素酶载体购自上海吉玛制药有限公司;兔源CyclinD1、p21、p27、基质金属蛋白酶(MMP)-2、GAPDH抗体均购自上海碧云天生物技术有限公司,兔源MMP-9、MMP-14抗体购自英国Abcam公司;实时荧光定量(qRT)聚合酶链式反应(PCR)试剂盒、购自美国Invitrogen公司。
1.2方法
1.2.1细胞培养 将肺癌细胞SPC-A1、A549和NCI-H460培养于RPMI-1640培养液中,人正常肺上皮细胞BEAS-2B培养在高糖DMEM培养液中,两种培养液中均添加10%胎牛血清、100 U/ml青霉素和100 μg/ml链霉素,培养条件:饱和湿度,37 ℃ 5%CO2培养箱中培养。传代保存。
1.2.2细胞转染 将对数生长期A549细胞稀释为1×106个/ml接种6孔板培养,融合度达到90%时根据转染说明书进行瞬时转染,用无血清OptiMEM培养液分别稀释Lipofectamine2000或不同载体(片段),将二者轻柔混匀,室温下孵育20 min后加入培养好的细胞中,培养6 h后换成RPMI1640完全培养基,收集转染48 h细胞,检测转染效果,进行后续实验。根据转染载体(片段)不同实验分组如下:si-NC组(转染si-NC)、si-MCM3AP-AS1组(转染si-MCM3AP-AS1)、miR-NC组(转染miR-NC)、miR-16-5p组(转染miR-16-5p mimics)、si-MCM3AP-AS1+anti-miR-NC组(共转染si-MCM3AP-AS1与anti-miR-NC)、si-MCM3AP-AS1+anti-miR-16-5p组(共转染si-MCM3AP-AS1与anti-miR-16-5p)。
1.2.3qRT-PCR检测RNA的表达 TRIzol试剂提取总RNA,根据反转录试剂盒步骤合成cDNA,置于于-80℃冰箱保存。按照说明书以取cDNA为模板进行反应,合成MCM3AP-AS1和miR-16-5p,运用2-ΔΔCt方法进行数据分析。
1.2.4MTT实验测定细胞活性 收集转染的A549细胞,消化细胞,离心后用培养基重悬细胞,稀释浓度为1×104个/ml,200 μl/孔接种于96孔板,在培养24 h、48 h和72 h时按照20 μl/孔加入MTT(5 mg/ml)试剂。孵育4 h后弃上清培养基,按照150 μl/孔加入DMSO,震荡10 min结晶溶解后酶标仪检测490 nm处的吸光度(A)值。
1.2.5Western印迹实验 室温下用RIPA裂解液裂解各组细胞20 min,超声破碎细胞,获得蛋白并检测浓度。进行十二烷基硫酸钠(SDS)-聚丙烯酰胺凝胶电泳(PAGE),转膜,室温封闭膜2 h,加入CyclinD1抗体(1∶1 500)、p21抗体(1∶800)、p27抗体(1∶1 500)、MMP-2抗体(1∶1 000)、MMP-9抗体(1∶1 000)、MMP-14抗体(1∶3 000)和抗GAPDH抗体(1∶1 200)一抗,4℃过夜,洗膜3次,然后加入稀释的二抗,室温孵育2 h,显影。以GAPDH为内参照分析蛋白水平。
1.2.6Transwell实验测定细胞迁移和侵袭 迁移实验:用无血清RPMI1640培养基调整细胞密度为1×105个/ml。Transwell下层培养孔加入500 μl含10%胎牛血清培养基作为迁移趋化物,Transwell上层小室加入100 μl细胞悬液,将上层小室置于24孔板中,培养24~48 h,弃去上层小室中的培养液,用棉签拭去上层小室膜表面细胞,甲醛固定下室膜表面细胞后结晶紫染色,显微镜观察计数。
侵袭实验:采用包被Matrigel基质胶的小室,使用前加入无血清培养液孵育2 h水化后备用。其余步骤同迁移实验。
1.2.7双荧光素酶报告系统实验 按照1.2.2的要求进行细胞培养,培养至细胞融合度为90%时,进行转染,将构建的MCM3AP-AS1野生型(WT-MCM3AP-AS1)和突变型(MUT-MCM3AP-AS1)双荧光素酶报告载体分别与miR-NC或miR-16-5p共转染融合度为90%的A549细胞,转染后培养48 h,收集细胞,室温RIPA缓冲液裂解20 min,离心收集裂解后的上清,加入荧光素酶底物,以海肾荧光素酶活性为内参照,用发光仪检测并计算相对萤火虫荧光素酶活性。同时将pcDNA、pcDNA-MCM3AP-AS1、si-NC、si-MCM3AP-AS1分别转染A549细胞,依次记为pcDNA组、pcDNA-MCM3AP-AS1组、si-NC组、si-MCM3AP-AS1组。qRT-PCR方法检测转染48 h后细胞中miR-16-5p表达水平。
1.3统计学处理 采用 SPSS19.0软件进行t检验、单因素方差分析。
2 结 果
2.1肺癌细胞和正常肺上皮细胞中LncRNA MCM3AP-AS1和miR-16-5p的表达情况 与BEAS-2B组相比,肺癌细胞系A549、SPC-A1和NCI-H460中MCM3AP-AS1表达量均显著升高(P<0.05),miR-16-5p表达量显著下降(P<0.05),见表1。两者在3种肺癌细胞系中的表达趋势一致,选择表达差异相对较大的A549细胞进行后续实验。

表1 LncRNA MCM3AP-AS1和miR-16-5p在肺癌细胞和正常肺上皮细胞中的表达
2.2抑制MCM3AP-AS1表达对肺癌A549细胞增殖的影响 si-MCM3AP-AS1组A549细胞中MCM3AP-AS1表达量、细胞活性(48 h、72 h)、增殖蛋白CyclinD1表达显著低于si-NC组(P<0.05),增殖负调节蛋白p21和p27表达显著高于si-NC组(P<0.05)。见图1,表2。
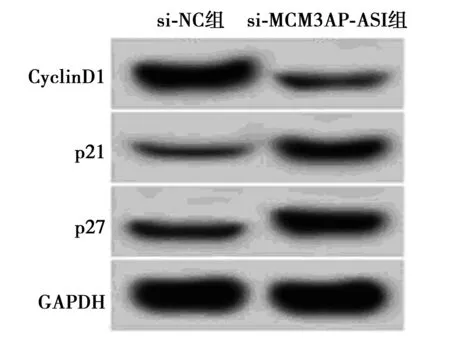
图1 抑制MCM3AP-AS1表达对肺癌A549细胞增殖相关蛋白表达的影响

表2 抑制MCM3AP-AS1表达对肺癌A549细胞增殖的影响
2.3抑制MCM3AP-AS1表达对肺癌A549细胞迁移、侵袭的影响 与si-NC组相比,si-MCM3AP-AS1组迁移细胞数和侵袭细胞数均显著下降(P<0.05),迁移和侵袭蛋白MMP-2、MMP-9和MMP-14均显著降低(P<0.05),见图2,图3,表3。
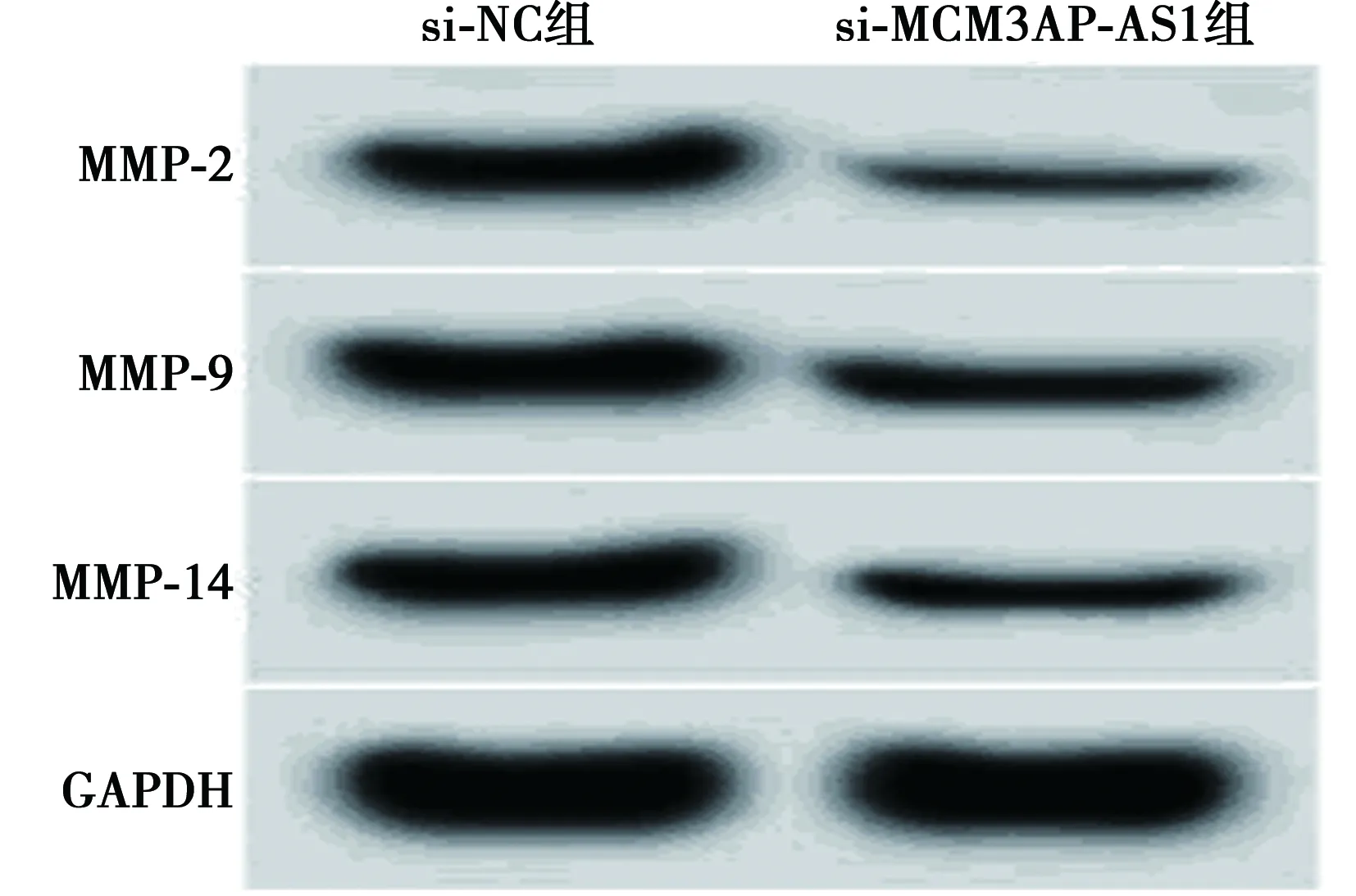
图2 抑制MCM3AP-AS1表达对肺癌A549细胞迁移、侵袭蛋白表达的影响

图3 抑制MCM3AP-AS1表达对肺癌A549细胞迁移、侵袭的影响(结晶紫染色,×200)

表3 抑制MCM3AP-AS1表达对肺癌A549细胞迁移、侵袭的影响
2.4过表达miR-16-5p对肺癌A549细胞增殖、迁移、侵袭的影响 miR-16-5p组的miR-16-5p表达量显著高于与miR-NC组(P<0.05),A549细胞活性(48 h、72 h)、增殖相关蛋白CyclinD1表达、迁移细胞数和侵袭细胞数、侵袭蛋白MMP-2和MMP-9表达均显著低于miR-NC组(P<0.05),p21表达表达高于miR-NC组(P<0.05),见表4,图4。
2.5MCM3AP-AS1靶向调控miR-16-5p的表达 MCM3AP-AS1与miR-16-5p之间存在互补的核苷酸序列,见图5。与转染miR-NC相比,转染miR-16-5p mimics显著降低WT-MCM3AP-AS1相对荧光素酶活性(P<0.05);与转染miR-NC相比,转染miR-16-5p mimics对MUT-MCM3AP-AS1相对荧光素酶活性无显著影响。见表5。与pcDNA组miR-16-5p表达量(1.02±0.09)相比,pcDNA-MCM3AP-AS1组(0.37±0.04)显著下降(P<0.05);与si-NC组miR-16-5p表达量(0.98±0.08)相比,si-MCM3AP-AS1组(2.75±0.28)显著上升(P<0.05),说明MCM3AP-AS1靶向负向调控miR-16-5p的表达。

表4 miR-16-5p过表达对肺癌A549细胞增殖、迁移、侵袭的影响
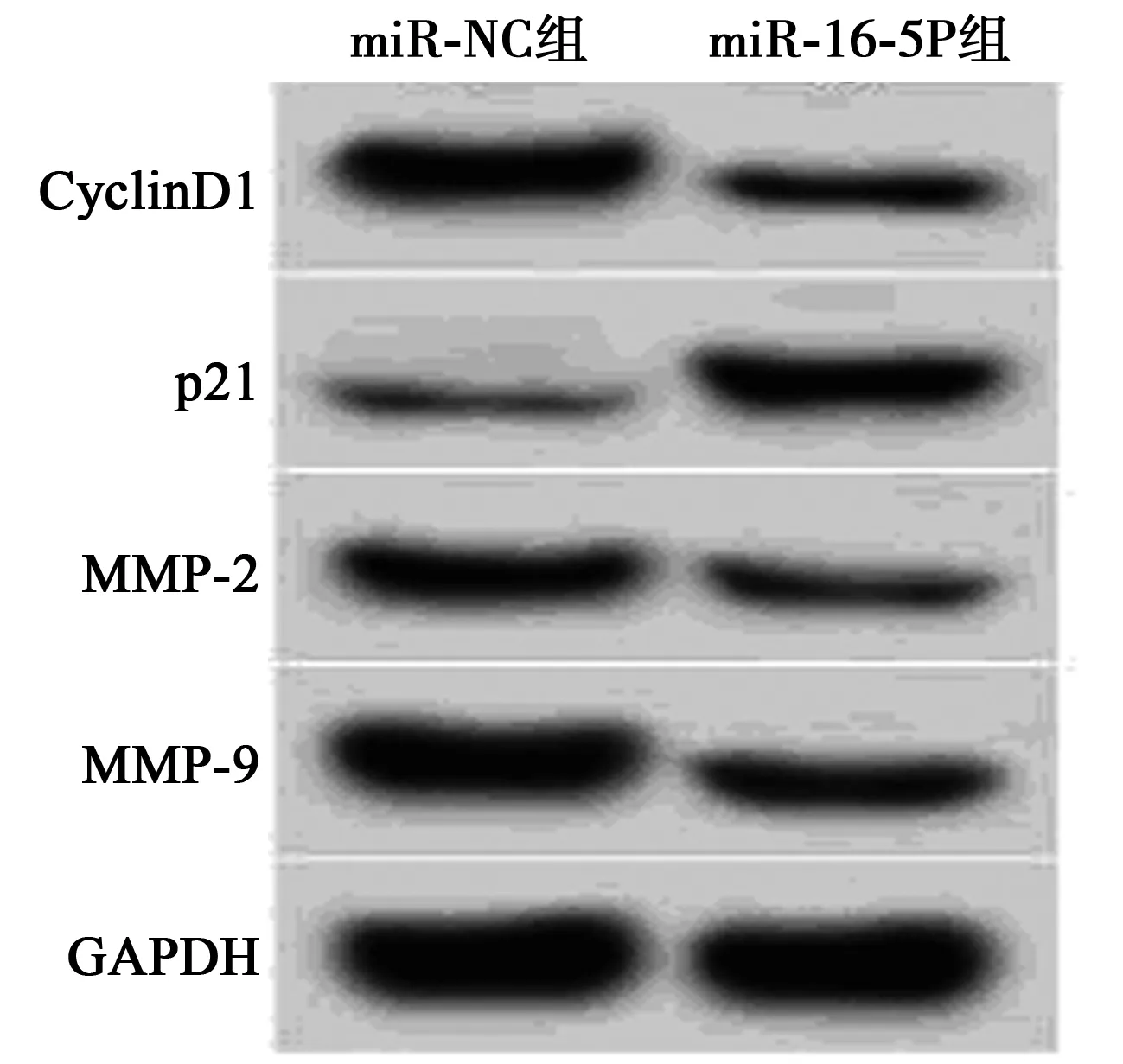
图4 miR-16-5p过表达对肺癌A549细胞增殖、迁移、侵袭相关蛋白的影响

图5 MCM3AP-AS1与miR-16-5p靶向结合

表5 双荧光素酶报告实验
2.6抑制miR-16-5p表达减弱MCM3AP-AS1抑制对A549细胞增殖、迁移、侵袭的影响 si-MCM3AP-AS1组miR-16-5p表达量显著高于si-NC组(P<0.05),细胞活性(48 h和72 h时)、增殖相关蛋白CyclinD1表达、迁移和侵袭细胞数、侵袭蛋白MMP-2和MMP-9表达均显著低于si-NC组(P<0.05),p21蛋白表达高于si-NC组(P<0.05);与si-MCM3AP-AS1+anti-miR-NC组相比,si-MCM3AP-AS1+anti-miR-16-5p组miR-16-5p表达量显著低于si-MCM3AP-AS1+anti-miR-NC组(P<0.05),细胞活性(48 h和72 h时)、增殖相关蛋白CyclinD1表达、迁移和侵袭细胞数、侵袭蛋白MMP-2和MMP-9表达均显著高于si-MCM3AP-AS1+anti-miR-NC组(P<0.05)p21蛋白表达高于si-MCM3AP-AS1+ anti-miR-NC组(P<0.05)。见图6,表7。

1~4:si-NC组、si-MCM3AP-AS1组、si-MCM3AP-AS1+anti-miR-NC组、si-MCM3AP-AS1+anti-miR-16-5p组

表7 抑制miR-16-5p表达逆转了下调MCM3AP-AS1表达对A549细胞增殖、迁移、侵袭的作用
3 讨 论
吸烟是肺癌的主要原因,预计2035年全球约有300万人因肺癌死亡〔9〕,而肺癌患者确诊时多为晚期,患者预后和生存质量较差。2014年,英国国家统计局报告称,诊断为远处转移性肺癌(Ⅳ期)的患者1年生存率仅为15%~19%〔10〕。因此研究肺癌的早期分子诊断和晚期治疗靶点也是肺癌临床所急需的。
LncRNA和miRNA调控肺癌的发生和发展,对肺癌的临床诊断、治疗和预后起重要作用〔11,12〕。研究表明,LncRNA MCM3AP-AS1在乳腺癌中表达上调,受雌激素正向调控,并与患者的无复发生存率较差有关〔13〕。MCM3AP-AS1在弥漫性胶质瘤样本中随着肿瘤分级的升高表达下调,与患者预后及恶性进展有显著相关性〔14〕。Zhu等〔15〕在对肺腺癌的LncRNA生物标志物的研究中发现MCM3AP-AS1在肺腺癌中与LINC00649存在竞争关系,具体的作用机制未有阐述。本研究结果说明MCM3AP-AS1在肺癌发展中具有重要作用。MCM3AP-AS1与miR-16-5p之间存在互补的核苷酸序列,提示miR-16-5p可能参与MCM3AP-AS1对肺癌发展和转移的调控过程。已有研究显示脊索瘤〔16〕和乳腺癌〔17〕中miR-16-5p表达下调,过表达miR-16-5p显著抑制脊索瘤和乳腺癌细胞增殖、迁移和侵袭,并诱导乳腺癌细胞凋亡。Fan等〔18〕也发现miR-16-5p非小细胞肺癌(NSCLC)患者血清中表达显著下调,其与miR-15b-5p和miR-20a-5p联合可能是NSCLC的诊断标志物。Liu等〔19〕最新结果表明,miR-16-5p在脂多糖(LPS)诱导的肺癌A549细胞损伤中表达下调,其通过靶向CXCR3抑制LPS诱导的A549细胞损伤。本研究结果Fan等〔18〕研究结果一致,过表达miR-16-5p可抑制A549细胞增殖、迁移、侵袭,证实了miR-16-5p在肺癌发展中的重要作用。
本研究显示,miR-16-5p是MCM3AP-AS1的靶基因,过表达或抑制MCM3AP-AS1分别下调或上调miR-16-5p表达水平,抑制miR-16-5p显著减弱下调MCM3AP-AS1对A549细胞的抗增殖和抗迁移和侵袭作用,这进一步证实了在肺癌中两者存在调控关系。
