长江中游湖泊表层沉积物多环芳烃的分布、来源特征及其生态风险评价*
2020-10-29万宏滨黄昌春
万宏滨,周 娟,罗 端,杨 浩,黄昌春,黄 涛
(1:南京师范大学地理科学学院,南京 210023) (2:江苏省地理信息资源开发与利用协同创新中心,南京 210023) (3:江苏省物质循环与污染控制重点实验室,南京 210023)
多环芳烃(Polycyclic aromatic hydrocarbons,PAHs)是环境中分布最广泛的一类持久性有机污染物,具有致癌、致畸、致突变毒性,对生态系统和人类健康都有严重危害,美国环境保护署(U.S. Environmental Protection Agency,EPA)已将16种PAHs列为优先控制污染物[1]. 环境中的PAHs主要由人类活动产生,其来源包括化石燃料(煤炭、石油等)及木材等生物质的不完全燃烧、石油泄漏、工业废水排放、工厂炼焦及汽车尾气排放等[1-3]. PAHs因其低溶解性及疏水性[4],在湖泊环境中主要吸附在悬浮物中,最终沉降到沉积物中. 由于PAHs在环境中的难降解性,沉积物中的PAHs经食物链生物放大与富集作用后将破坏生态系统并危害人类健康[5].
随着我国近几十年来能源消耗的快速增加,PAHs污染已经被认为是中国最严重的环境问题之一[1]. 目前,研究学者对我国PAHs的分布、来源及迁移转化机制等进行了大量的研究,主要集中于大气、扬尘、水体、沉积物以及土壤中[3,6-9]. 在这些环境介质中,湖泊沉积物中PAHs已成为研究热点,沉积物是环境中PAHs重要的汇和潜在污染源. 因而对湖泊沉积物中PAHs进行研究分析,可以更全面的了解环境中PAHs的污染状况及潜在风险,并有助于了解PAHs与人类活动经济发展之间的关系,更好的采取适当的措施预防和保护湖泊生态环境.
长江中游段长约1000 km,流经湖北、湖南、江西和安徽四省,水流平缓,有众多支流汇入. 该流域带城市形态呈条带状分布,人口密集,航运发达,经济发展迅速. 长江中游流域分布着大量的浅水湖泊,其中包括洞庭湖与鄱阳湖两大淡水湖,这些湖泊多属于宽广型,湖底沉积物淤积较厚,是长江流域的重要组成部分[10]. 目前国内已对长江流域及周边湖泊沉积物中PAHs污染进行了大量研究[8,11-13],鄱阳湖周溪湾的沉积物研究表明,近几十年来PAHs的排放量急剧上升,且PAHs来源也由煤燃烧向汽车尾气排放源转变[8]. 长江安庆段及毗邻湖泊沉积物研究发现,该地区PAHs主要来源于燃烧排放,不同湖泊存在不同的潜在来源[11]. Zhao等[12]利用沉积物基准法对长江中下游及淮河流域湖泊2008年的沉积物研究表明,该地区PAHs无生态风险. Li等[13]对长江中下游2014年湖泊沉积物研究发现,煤炭燃烧和汽车尾气排放是该区域PAHs的主要来源,国民生产总值GDP是影响该地区PAHs分布的关键因素,BaP和DahA在该地区有很高的毒性风险. 而随着2015年《长江中游城市群发展规划》的发布,长江中游经济带密集的重化工业进行了产业转移与转型升级,并重点发展经济效益高、污染小的第三产业,形成了城乡协调发展、绿色发展的新的发展模式[14-15]. PAHs作为环境中分布最广泛、与人类活动密切相关的持久性有机污染物,随着长江中游经济带近年来经济发展的变化应引起我们的持续关注. 对长江中游湖泊沉积物中PAHs的长期监测有助于了解其污染机理与人类活动有关的生态影响,掌握该区域湖泊沉积物中PAHs的分布特征,对于长江中游经济带绿色发展的环境保护与提升具有重要意义. 因此,本文通过检测分析2018年长江中游经济带12个湖泊沉积物中PAHs的含量、组成及分布特征,探讨该地区PAHs分布的影响因素,运用比值法和主成分分析法对其来源进行解析并采用风险商值模型对其生态风险进行评价,以期为当前长江中游经济带PAHs污染状况及防治提供科学依据,为我国湖泊沉积物中PAHs的赋存情况提供背景数据.
1 材料与方法
1.1 样品采集与处理
2018年7月对长江中游12个湖泊进行了表层沉积物采样,根据湖泊面积大小及地理环境等因素分别采集了长湖4个样点、洞庭湖5个样点、岳阳南湖2个样点、洪湖6个样点、黄盖湖5个样点、武昌东湖3个样点、梁子湖7个样点、武山湖3个样点、龙感湖6个样点,珠湖和黄大湖各采集4个样点,由于当时鄱阳湖湖泊采砂的原因,只采集了2个样点,总计51个样点(图1). 采用抓斗式采样器(型号KH0201,规格5 L)采集表层沉积物,并保存在装有冰袋的保温箱中运回实验室. 样品运回实验室后,进行冷冻干燥,然后研磨后过100目筛,进行各项指标的测定.
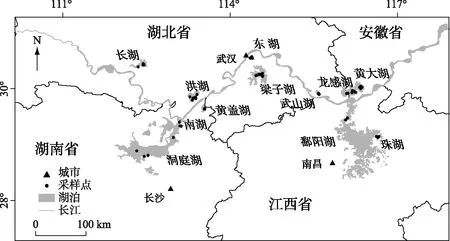
图1 长江中游流域12个湖泊采样点Fig.1 Location of the sampling sites from 12 lakes along the middle reaches of Yangtze River
1.2 多环芳烃含量测定
(1)样品提取与净化:使用电子天平称取2 g(精度0.001 g)样品倒入微波萃取管中,加入25 mL丙酮与正己烷1∶1混合溶剂,并加入100 ng(50 μL,2 mg/L)5种回收率指示物(萘-d8、苊-d10、菲-d10、-d12、苝-d12),进行微波萃取. 微波萃取条件为:以10℃/min升温至100℃,在100℃保持15 min. 经离心3次得到的上清液旋蒸至1 mL. 硅胶-氧化铝复合层析柱采用湿法装柱(内径13 mm,容量6 mL),自下而上分别为1.5 cm氧化铝、1.5 cm硅胶、1 cm无水硫酸钠(氧化铝与硅胶均在450℃灼烧6 h,在140℃下活化16 h后使用,无水硫酸钠在650℃灼烧10 h后使用),先使用10 mL正己烷冲洗净化层析柱,当流至液面相切时,然后将旋蒸至1 mL的样品浓缩液倒入层析柱中,使用30 mL二氯甲烷与正己烷1∶1混合溶剂进行少量多次冲洗,收集二氯甲烷与正己烷1∶1混合组分的洗脱液再次旋蒸至1 mL以内,使用正己烷定容至1 mL上机检测.
(2)样品检测:多环芳烃含量的检测使用日本岛津公司的气相色谱质谱联用仪(GC-MS QP2010Plus),不分流进样,进样量1 μL,色谱柱为HP-5石英毛细管柱(长30 m,厚0.25 μm,直径0.25 mm),载气为99.999%高纯氦气,流速为1.5 mL/min. 升温程序如下:初始温度为50℃,保持1 min,然后以15℃/min升温至180℃, 然后以5℃/min的速度将温度提高到280℃,保持10 min. 离子源温度200℃,接口温度280℃,离子源为电子轰击源(EI). 检测目标化合物为EPA优控的16种PAHs:萘(Naphthalene, Nap),苊烯(Acenaphthylene, Acy),二氢苊(Acenaphthene, Ace),芴(Fluorene, Flu),菲(Phenanthrene, Phe),蒽(Anthracene, Ant),荧蒽(Fluoranthene, Fla),芘(Pyrene, Pyr),苯并[a]蒽(Benzo(a)anthracene, BaA),(Chrysene, Chr),苯并[b]荧蒽(Benzo(b)fluoranthene, BbF),苯并[k]荧蒽(Benzo(k)fluoranthene, BkF),苯并[a]芘(Benzo(a)pyrene, BaP),茚苯[1,2,3-cd]芘(Indeno(1,2,3-cd)pyrene, InP),二苯并[a,h]蒽(Dibenzo(a,h)anthracene, DahA),苯并[ghi]苝(Benzo(g,hi)perylene BghiP). 采用选择性离子监测模式(SIM),EI电子源70 eV,质谱扫描范围45~600 amu. 通过样品中目标物与16种PAHs标准物质中目标物的保留时间、质谱图和碎片离子质荷比等信息比较,进行目标物的定性. 在对目标物定性分析的基础上,根据定量离子的峰面积,采用外标法进行定量分析,标准曲线采用5个浓度梯度(50、100、200、500和1000 ng/mL).
(3)质量控制:为了保证数据的可靠性,对实验全流程进行了严格的质量控制. 平均每14个样品加入1个空白样与平行样,并对实验样品加入了16种PAHs标准物质、5种氘代指示物进行回收率检测. 空白样品中PAHs总含量比实际样品含量低一个数量级以上,样品含量相对标准偏差小于10%. 所有沉积物样品PAHs含量均经过空白校正. 16种PAHs标准曲线相关系数均在0.999以上,加标回收率在77.13%~110.74%之间,方法检测限在0.08~0.78 ng/g之间,各PAH组分回收率及检测限见附录Ⅰ.
1.3 其他数据测定与收集
总有机碳(TOC)含量是使用日本岛津公司的TOC-L与SSM-5000A分析仪测得的总碳与总无机碳之差获得. 湖泊面积、位置、蓄水量等数据从《中国湖泊分布地图集》[16]中获得. 透明度通过塞氏盘实地测量获得,pH、溶解氧等数据通过YSI 6600 V2型多参数水质监测仪实地测量获得(表1). 研究中使用的能源消费量和车辆保有量等数据均来自当地统计年鉴中2016-2017年的统计数据. 各湖所使用的数据来源区域如下:长湖-荆州市[17]、洪湖-潜江市[18]、洞庭湖-益阳市[19]、南湖-岳阳市[19]、黄盖湖-咸宁市[20]、东湖-武汉市[21]、梁子湖-鄂州市[22]、武山湖-武穴市[23]、龙感湖-黄冈市[23]、鄱阳湖-九江市[24]、珠湖-上饶市[24]、黄大湖-安庆市[25].
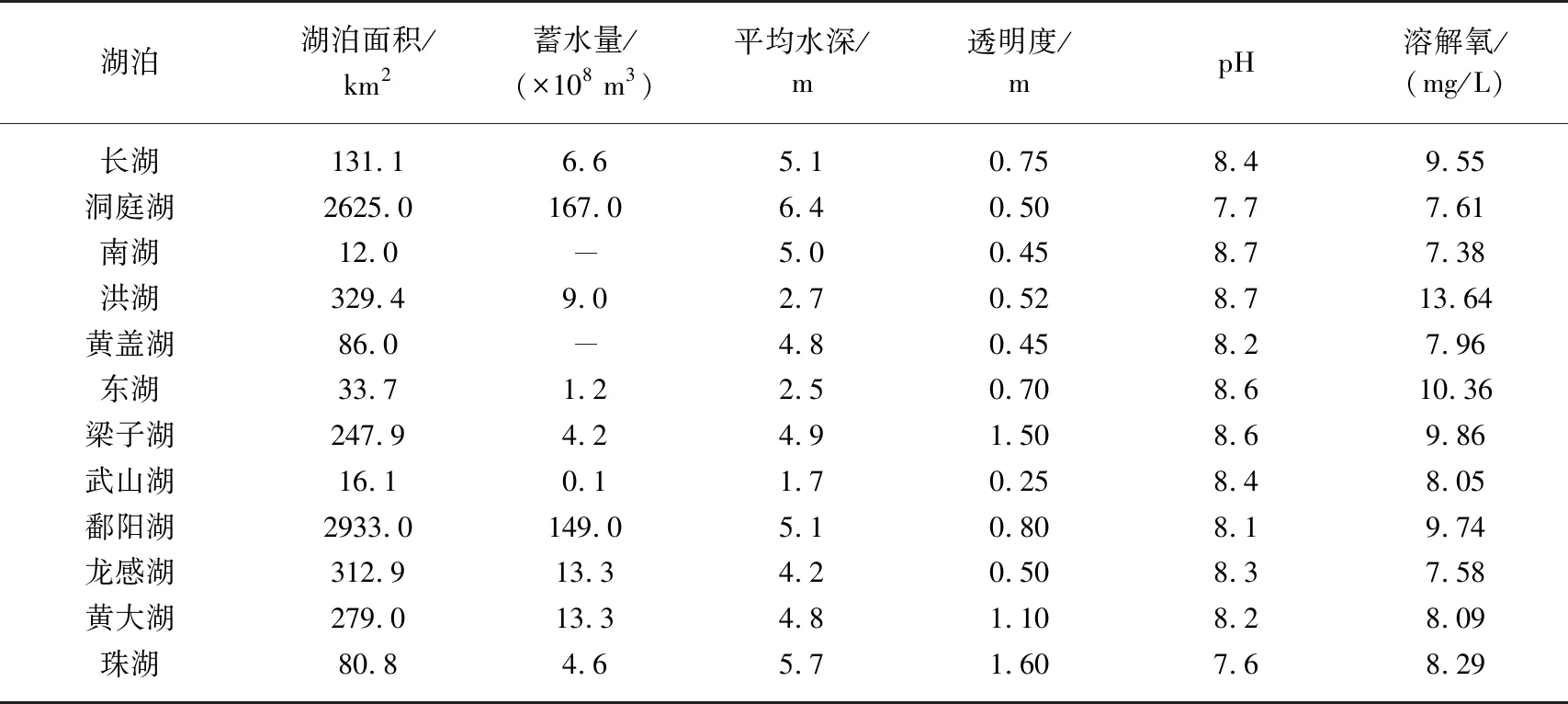
表1 本研究中12个湖泊的形态特征及湖沼特征
“-”表示此项数值缺失.
2 结果与分析
2.1 PAHs的含量分布特征
长江中游湖泊51个样点表层沉积物中均检测出16种优控PAHs,PAHs总含量范围为572.7~1766.2 ng/g(dw)(均值为976.5±285.0 ng/g(dw)),各个湖泊PAHs含量分布如图2所示. PAHs含量最高的湖泊为武汉市城区的东湖(1634.8±111.4 ng/g(dw)),其次是岳阳市的南湖(1352.5±286.1 ng/g(dw)). 东湖与南湖分别位于长江中游地区经济发达的武汉市、岳阳市两大城市内,由于两个城市的高度工业化,除来自生物质燃烧产生的PAHs外,还有城市径流、城市和工业废水排放以及工业炼焦等过程中产生的PAHs进入湖泊环境中. 此外,这两个湖泊为城市风景区,有大量的游客驾驶机动车游玩,机动车燃烧汽油等尾气排放也会产生大量的PAHs进入湖泊中. PAHs含量最低的湖泊为长湖(688.1±47.3 ng/g(dw)),长湖位于荆州市郊区,相比其他湖泊更靠近长江上游流域,该地区工业化及城市化进度较低于长江中游区域其他城市并且该湖泊周围区域主要为农业活动区域[17]. 从湖泊分布上看,武汉市东湖沉积物中PAHs含量显著高于长江中游地区除岳阳南湖以外的其他湖泊(P<0.05),而经济发展相对落后地区的长湖、洞庭湖、龙感湖和黄大湖沉积物中PAHs含量显著低于长江中游其他经济较为发达地区的湖泊(P<0.05).
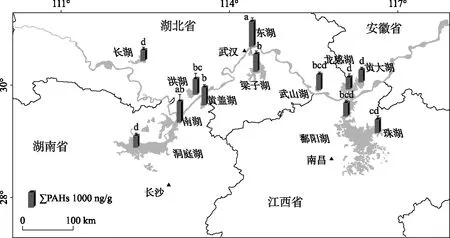
图2 长江中游流域12个湖泊沉积物中PAHs含量Fig.2 Contents of PAHs in sediments of 12 lakes in the middle reaches of the Yangtze River
将本次研究结果与之前长江中游湖泊沉积物中PAHs含量进行比较(表2),岳阳市南湖沉积物中PAHs含量在10年内增加了近5倍,岳阳市是长江中游区域的中心城市,近年来工业化、城镇化发展迅速,造成了污染物的过度排放. 而武汉市东湖沉积物中PAHs含量近年来虽然增长幅度较小,但其PAHs含量一直处于较高的水平,武汉市是长江中游城市群中唯一的特大城市,工业化、城镇化水平高,相应的排放出更多的污染物. 长江中游其他湖泊沉积物中PAHs含量相较之前均有一定程度的增加,这表明伴随着长江流域城市群经济的快速发展,相应的排放出更多的PAHs污染物进入了环境中. 表3汇总了国内外近些年来其他地区湖泊沉积物中PAHs含量情况,2018年长江中游地区湖泊沉积物中PAHs含量处于较高水平,远高于国内偏远地区的抚仙湖[26]、青海湖[27]、博斯腾湖[28]等湖泊,低于东部地区的巢湖[2]与太湖[29],远低于美国经济工业发达地区的湖泊[30-32].
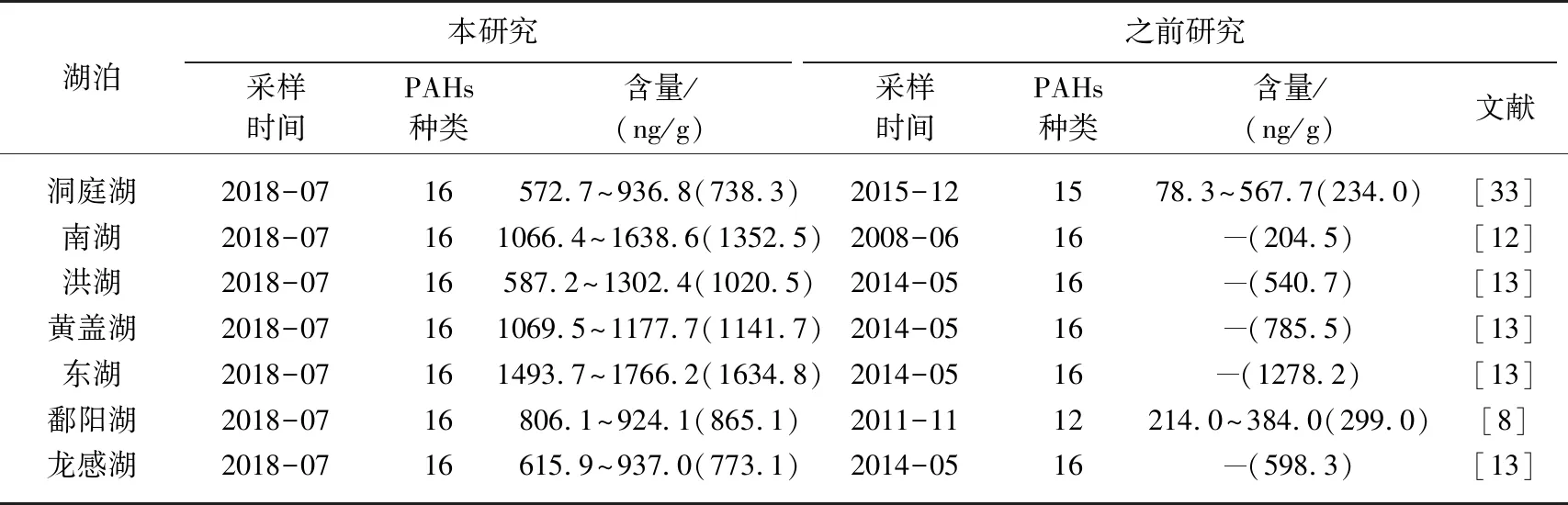
表2 长江中游湖泊沉积物不同时间PAHs含量比较
*括号内为∑PAHs含量平均值, “-”表示数值缺失.

表3 长江中游及国内外其他地区湖泊沉积物中PAHs含量比较
2.2 PAHs的组成分布特征
PAHs根据其分子量大小即苯环数量可分为低环(2~3环)、中环(4环)以及高环(5~6环)PAHs[40]. PAHs不同的组成特征反映出了其来源的差异[3,26,41]. 为明确长江中游湖泊沉积物中PAHs组成特征的相似性与差异性,故采用聚类分析的方法对12个湖泊沉积物中PAHs组成特征相进行分类,以每个湖泊的16种单体PAH含量作为起始数据分析,长江中游流域12个湖泊根据PAHs的组成特征被分为3种类型,如图3所示. 类型1包括8个湖泊,分别为长湖、洞庭湖、龙感湖、鄱阳湖、武山湖、洪湖、珠湖以及黄大湖,这些湖泊主要为经济发展相对落后的郊区及乡村地区的湖泊. 类型2包括3个湖泊,分别为岳阳市的南湖、咸宁市的黄盖湖以及鄂州市的梁子湖. 类型3只包括了1个湖泊,为长江中游流域城市化与工业化最发达的武汉市中的东湖. 基于聚类分析的3种类型湖泊沉积物中PAHs的组成特征如图3所示,3种类型湖泊沉积物中PAHs的苯环数组成具有一定的差异性与规律性. 类型1湖泊沉积物中PAHs主要成分为低环(2~3环)PAHs,占比为64.04%±7.02%;类型2中PAHs低环和中高环分布相对平均,分别为50.76%±5.17%和49.24%±5.17%;类型3中PAHs各环数分布相对平均,低环占比为35.35%±3.56%,中环占比为26.17%±0.45%,高环占比为38.48%±3.84%. 从类型1到类型3湖泊沉积物中PAHs的组分呈现了一定的规律性,即低环PAHs占比逐渐下降,而中环与高环PAHs占比逐渐上升,总体以低环PAHs为主. 低环PAHs占比较高可能是由于长江中游区域分布着大量农田,农业生产活动频繁,木材秸秆等生物质的低温不完全燃烧主要产生低环数PAHs[42-43],以及与近年来长江中游经济带的产业转型升级等绿色发展有关,如钢铁、有色金属及汽车等行业的清洁生产、节能减排等降低了中、高环PAHs比例的排放[44].

图3 长江中游流域湖泊聚类分析树状图及各类型湖泊沉积物中PAHs含量和组成Fig.3 Cluster analysis tree diagram of lakes in the middle reaches of the Yangtze River and PAHs contents and composition diagram of each group type
3 讨论
3.1 影响沉积物中PAHs含量水平的因素
PAHs的来源排放直接影响进入湖泊环境中PAHs的含量及组成,而PAHs的来源排放与能源消耗及人类活动密切相关,湖泊沉积物中PAHs的含量可能与一些社会经济数据相关,因此将各个湖泊沉积物中PAHs含量与其所在区域的能源消费量及车辆保有量进行相关性分析(表4). 能源消费量是指各种一次能源(煤碳、石油等)和二次能源(汽油、柴油等)消费的数量,被视为经济发展的同步指标,与城市化及工业化进程密切相关. 结果表明,沉积物中PAHs很大程度上受当地区域的经济发展程度影响. 车辆保有量及能源消费量与低环PAHs均无显著相关性,与中环及高环PAHs在0.01水平上均呈现出正相关性. 本研究区域湖泊沉积物中主要为低环PAHs,能源消费量及汽车保有量与低环PAHs无显著相关性,而与中环及高环PAHs有显著相关性的结果表明,经济发展所消耗的能源和汽车保有量仅是影响该区域湖泊沉积物中中环及高环PAHs含量水平的重要因素,但并不是影响该区域湖泊沉积物中PAHs含量水平的主要因素.

表4 PAHs含量与TOC、水体指标、 保有车辆及能源消费量相关性分析
进入湖泊沉积物中的PAHs含量受很多因素的影响,已有研究表明,沉积物中TOC含量是影响PAHs在湖泊沉积物中归趋分布的重要因素[3,45]. 许多学者认为沉积物中TOC可以与PAHs中的芳香环发生键合作用,从而影响PAHs在沉积物中的归趋[35,46]. 将沉积物样品中PAHs含量与沉积物中TOC含量及湖泊水体各项指标运用Pearson相关性分析发现,沉积物中TOC含量与低环PAHs含量在0.05水平上呈现出正相关性,与中高环PAHs及总PAHs含量在0.01水平上呈现出正相关性(表4). 而pH和溶解氧等水体指标与各环数PAHs含量之间均无显著相关性. 这表明,沉积物中TOC含量是影响长江中游湖泊表层沉积物中PAHs含量水平的主要因素.
3.2 沉积物中PAHs的来源
PAHs的来源包括自然源和人为源,但主要来源是人为源,这主要是由于能源燃料的燃烧,如汽车发动机燃料燃烧、化石燃料发电、冶炼焦炭、生物质燃烧等化学燃烧过程和其他来源产生[40,42,47]. 不同环数的PAHs其来源也有所不同,低环PAHs主要来源于石油产品的泄漏以及化石燃料和木材秸秆等生物质在低温条件下的不完全燃烧产生,中高环PAHs则主要来源于化石燃料和木材等生物质在高温下的不完全燃烧产生[40,42,47]. 由图3所示,本研究区域湖泊沉积物中低环数PAHs所占比例较高,主要为石油源以及化石燃料和生物质的低温燃烧. 但仅仅通过PAHs的环数分布来判断其来源是较为浅显的方法,故采用异构体比值法与主成分分析法相结合的办法来对该区域PAHs进行来源解析.
沉积物中单体PAHs含量的比值常被用来初步判断PAHs的来源,由于各种PAHs在水溶性、吸附特性等性质不同,其中环境中的稳定性也不同,因而选择具有相同物理化学性质的同分异构体比值来判断其来源[13,40-41,48-49],如Fla/(Fla+Pyr)、Ant/(Ant+Phe)、BaA/(BaA+Chr)和InP/(InP+BghiP). Fla/(Fla+Pyr)小于0.4表示为石油源,大于0.4表示为煤炭、木材等生物质的不完全燃烧源. Ant/(Ant+Phe)小于0.1表示为石油源,大于0.1则表示为燃烧源. BaA/(BaA+Chr)小于0.2表示为石油源,0.2~0.35之间为石油燃烧源,大于0.35为煤、木材等生物质燃烧源. InP/(InP+BghiP)小于0.2为石油源,0.2~0.5之间为石油燃烧源,大于0.5则为煤炭、木材等生物质燃烧源. 为分析长江中游流域湖泊沉积物中PAHs的来源,采用了这4种异构体比值对PAHs来源进行了分析,如图4所示. Fla/(Fla+Pyr)和Ant/(Ant+Phe)的比值表明,该区域湖泊沉积物中PAHs主要来源为煤炭和生物质的燃烧源. 从聚类分析得到的三种类型湖泊上分析,类型3湖泊沉积物中PAHs的来源均为煤炭和生物质等燃烧源,而类型1和类型2湖泊沉积物中PAHs的主要来源为煤炭和生物质燃烧源,还有部分来源为石油源. BaA/(BaA+Chr)和InP/(InP+BghiP)的比值结果与Fla/(Fla+Pyr)和Ant/(Ant+Phe)的比值结果相一致. 将异构体比值法的结果结合该区域PAHs的分布组成可以进一步得出,煤炭和木材秸秆等生物质的低温燃烧为长江中游流域湖泊沉积物中PAHs的主要来源.
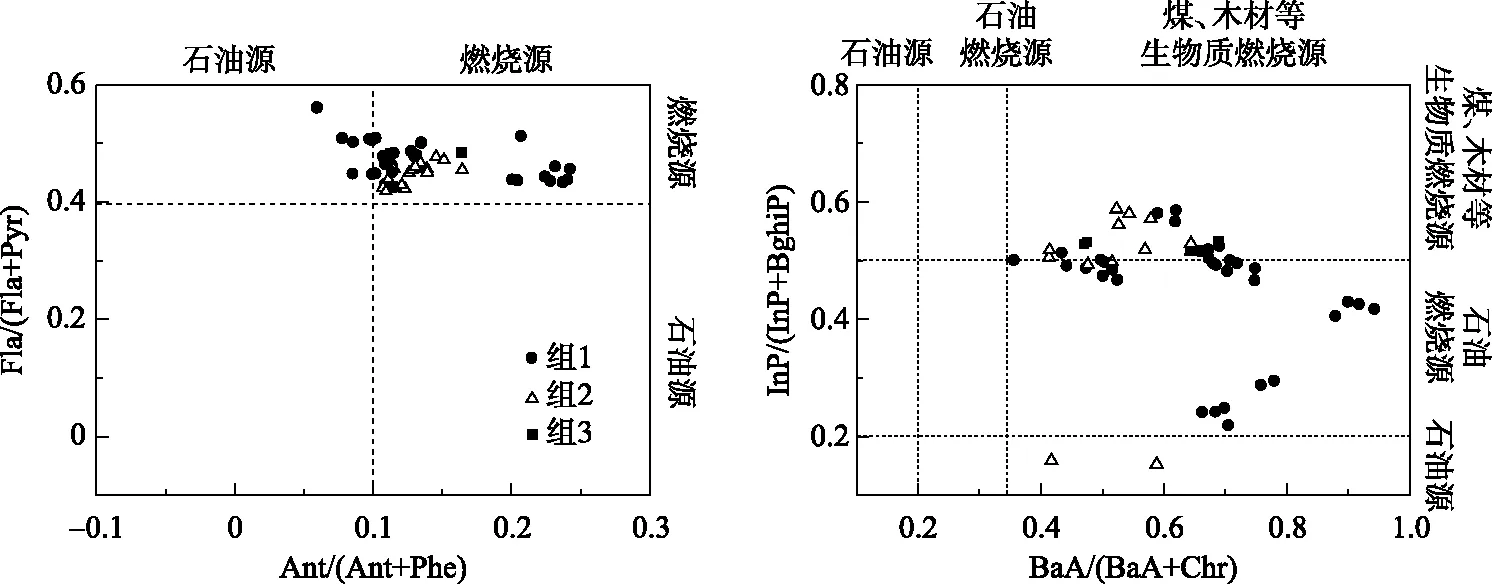
图4 长江中游湖泊沉积物中PAHs同分异构体比值Fig.4 Isomer ratios of PAHs in sediments of lakes in the middle reaches of the Yangtze River

图5 长江中游3类湖泊 沉积物中PAHs主成分载荷Fig.5 Principal component load diagram of PAHs in sediments of three types lakes in the middle reaches of the Yangtze River
为了进一步分析PAHs的来源,采用主成分分析法对3种类型湖泊沉积物中16种PAHs进行来源分析,结果如图5所示. 3种类型湖泊均提取了2个主成分,类型1两个成分的累计方差贡献率为73.84%. 主成分1方差贡献率为61.51%,高载荷值为高环的BaP、BaA、BghiP、BkF、Pyr、Chr、Fla以及InP. Pyr、Chr被认为是煤炭燃烧的标志物[50],因此,主成分1为煤、石油等化石燃料的燃烧源. 主成分2方差贡献率为12.33%,高载荷值为低环的Ant、Flu和Phe,被认为是木材秸秆燃烧源[51]. 因此,主成分2为木材秸秆等生物质低温燃烧源. 类型2中两个成分的累计方差贡献率为77.82%,主成分1的方差贡献率为60.99%,载荷值高的为Pyr、Acy、DahA、BkF、Fla以及BghiP,BkF及BghiP被认为是汽油和柴油机的排放产物[50],Pyr、DahA被认为是煤炭燃烧的标志物[50],而Fla被认为是焦炉排放物[50],因此,主成分1为机动车和机动船等的尾气排放、煤炭燃烧及工业炼焦源. 主成分2的方差贡献率为16.83%,主要加权在Nap、Ant和Flu,是木材秸秆等生物质燃烧的标志物[51]. 因此,主成分2归类为木材秸秆等生物质的低温燃烧源. 类型3中两个成分的累计方差贡献率为100%,表明这两个主成分解释了该组中PAHs的全部来源. 主成分1的方差贡献率为74.74%,主要加权在BbF、BkF、BaP、BaA以及Fla,BkF和BaA为汽油及柴油机的排放产物[50],Fla被认为是焦炉排放物[50]. 因此,主成分1归类为机动车和机动船等的尾气排放源及工业炼焦源. 主成分2的方差贡献率为25.26%,主要加权在Phe、Nap以及Flu,这些是木材等生物质燃烧的标志物[51]. 因此主成分2归类为木材等生物质低温燃烧源. 主成分分析的结果显示,3种类型湖泊中PAHs均含有煤炭及木材秸秆等生物质的低温燃烧源,这与该区域PAHs低环占比为主的分布特征及异构体比值的结果相同,但主成分分析的结果显示类型2和类型3的湖泊沉积物中PAHs还包括机动车和机动船等燃烧汽油、柴油的尾气排放源及工业炼焦等化石燃料的高温燃烧源.
综合该区域湖泊沉积物中PAHs的分布特征及异构体比值法和主成分分析法的结果表明,3种类型湖泊沉积物中PAHs的主要来源均为煤炭、木材等生物质的低温燃烧源;类型2和类型3湖泊沉积物中PAHs还有机动车、机动船等燃烧汽油、柴油的尾气排放源及工业炼焦等化石燃料的高温燃烧源. 中国是世界上最大的煤炭生产国,绝大多数城镇依靠煤炭产业,以煤炭为主要燃料,然而因为其燃烧设施陈旧及维护不善,导致大量未经处理的PAHs等污染物进入大气当中. 随着工业化、城市化的快速发展,长江中下游流域的能源消耗严重依赖煤炭资源,中国国家统计局2013年数据显示,长江中下游流域煤炭消费占总能源消费量的60%以上,大量的煤炭消耗成为了该地区PAHs的主要来源[52]. 长江中游地区耕地面积占全国耕地面积的9.25%,粮食总产量占全国粮食总产量的12.64%,是中国重要的粮食产地及农业地区,但大部分地区农业机械化程度较低,养地重视不足,秸秆等生物质的不合理利用[43]燃烧也成为了该地区PAHs的主要来源. 随着经济和社会的快速发展,中国的汽车保有量也在迅速增加,汽车的能源消耗已经成为影响我国石油消费的主要因素. 长江中下游流域地区作为我国经济最发达的地区之一,2014年数据显示,在过去的10年里,其汽车平均增长率高达15%以上[53]. 因此,机动车燃烧汽油、柴油排放的大量尾气也是长江中游区域环境中PAHs的重要来源.
3.3 沉积物中PAHs的生态风险评价
应用Kalf等于1997年提出的风险商值法[54](risk quotient,RQ)对长江中游流域湖泊沉积物中PAHs的生态风险进行评价. 这是一种简单且保守的生态风险表征方法,该方法通过计算每一种PAH的暴露含量与风险标准值的商,即风险商值,若风险商值大于1,则认为该PAH具有潜在生态风险,且值越大,其潜在生态风险越大[54]. 其公式如下:
RQ=CPAHs/CQV
(1)
式中,CPAHs为沉积物中PAHs的含量;CQV为沉积物中相应的PAHs的风险标准值. Kalf等[54]在此基础上提出了可忽略风险含量(negligible concentrations, NCs)和最高允许风险含量(maximum permissible concentrations, MPCs)两个界限值,其公式如下:
RQNCs=CPAHs/CQV(NCs)
(2)
RQMPCs=CPAHs/CQV(MPCs)
(3)
式中,CQV(NCs)为可忽略风险标准值;CQV(MPCs)为最高允许风险标准值. Kalf等主要提出了10种单体PAHs的生态风险标准值,2010年曹治国等[55]推断出了其他6种单体PAHs(Acy、Ace、Flu、Pyr、BbF和DahA)的生态风险标准值,如表5所示. 当RQNCs小于1时,表示沉积物中PAHs无生态风险;当RQNCs大于1且小于800而RQMPCs小于1时,表示PAHs有中等风险;当RQNCs远大于800或RQMPCs远大于1时,表示PAHs有很高风险,必须立即采取措施进行生态修复. 长江中游湖泊沉积物中PAHs的风险商值及风险标准值如表5及图6所示,单体PAH的RQNCs值除Chr、BaP、InP、DahA及BghiP外均大于1,而RQMPCs值除Nap外均小于1,表明长江中游流域单体PAH主要处于中等风险水平,但是Nap的RQMPCs值大于1,处于较高风险水平,需要加强对Nap输入来源的控制及污染修复. 从PAHs的总含量上看,长江中游流域湖泊沉积物中PAHs的RQNCs值均小于800,且RQMPCs值大于1,长江中游流域湖泊沉积物中PAHs整体呈中等风险水平.
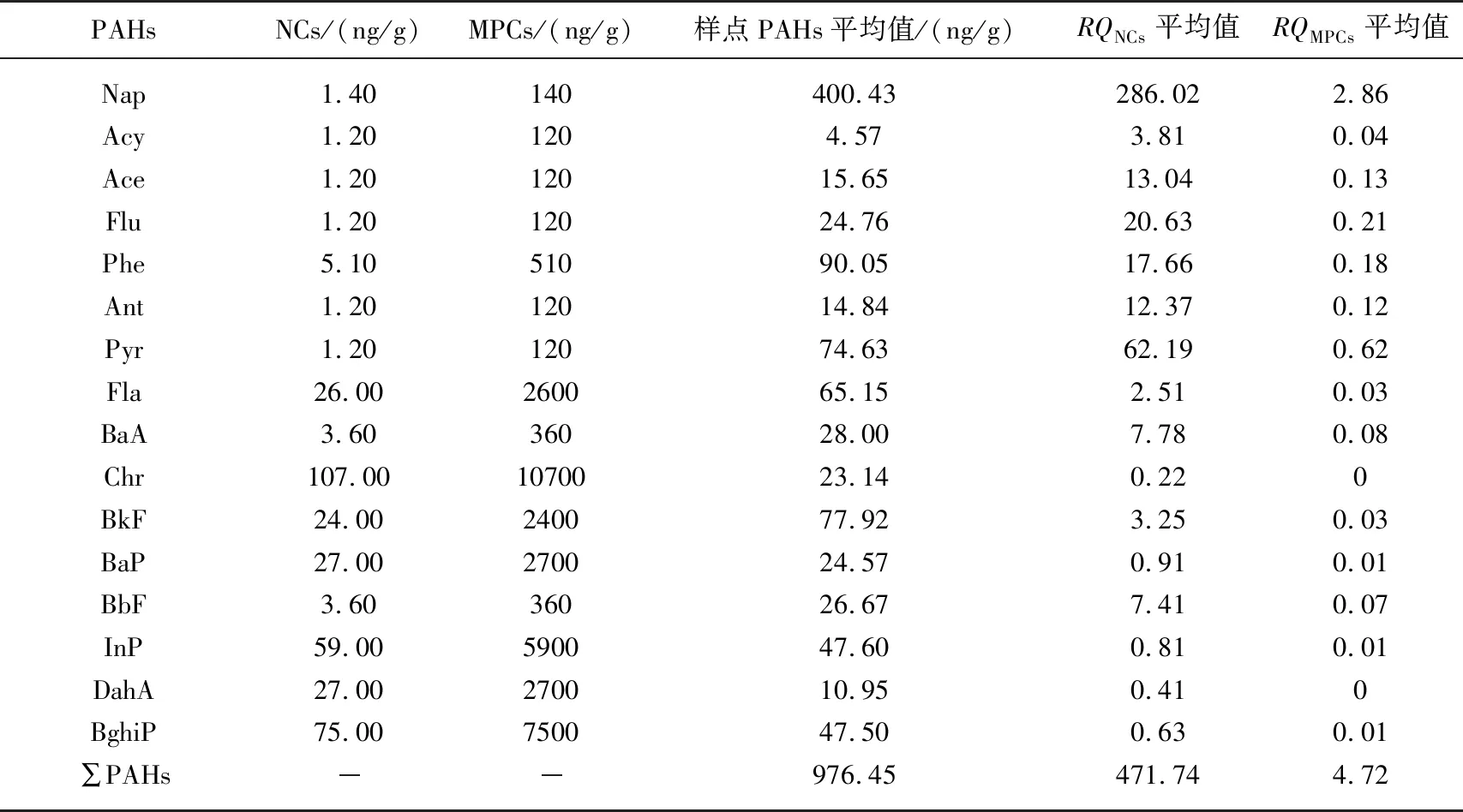
表5 沉积物中单体PAH的RQNCs和RQMPCs均值
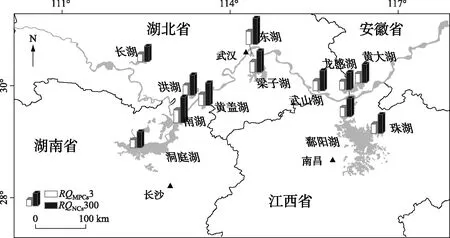
图6 长江中游湖泊沉积物中总PAHs风险商值Fig.6 Risk quotient of total PAHs in the sediments from lakes along the middle reaches of the Yangtze River
4 结论
1)长江中游流域湖泊沉积物中PAHs的总含量范围介于572.7~1766.2 ng/g(dw)之间,均值为976.5±285.0 ng/g(dw),与国内外其他地区湖泊沉积物相比,长江中游地区湖泊沉积物中PAHs含量总体处于较高水平. 与该区域之前的研究相比,本次研究长江中游地区湖泊沉积物中PAHs含量有不同程度的增加.
2)当地的能源消费量及汽车保有量仅与中环及高环PAHs有良好的相关性的结果表明,能源消费量及车辆保有量仅是影响该区域湖泊沉积物中中环及高环PAHs含量水平的重要因素. 湖泊沉积物中TOC含量与低环PAHs、中高环PAHs及总PAHs含量均有良好的正相关关系表明,沉积物中TOC含量是影响长江中游湖泊沉积物中PAHs含量水平的主要因素.
3)长江中游湖泊沉积物中PAHs的来源包括煤炭、木材等生物质的燃烧以及机动车和机动船等燃烧汽油、柴油的尾气排放源等. 该区域不同湖泊沉积物中PAHs来源具有一定的差异性,总体而言,煤炭、木材等生物质的低温燃烧是该区域湖泊沉积物中PAHs的主要来源. 风险商值法结果表明长江中游地区PAHs处于中等风险水平,仍需要长期监测与保护.
致谢:感谢中国科学院南京地理与湖泊研究所周永强、陈业和季鹏飞等同志在样品采集过程中提供的大力帮助.
5 附录
附录见电子版(DOI: 10.18307/2020.0606.)
