优化液质联用法对氟喹诺酮类药物残留的检测
2020-10-23戴菲菲广东省惠州市质量计量监督检测所
□ 戴菲菲 广东省惠州市质量计量监督检测所
氟喹诺酮(fluoroquinolones,FQs)类药物具有6-氟-7-哌嗪-4-诺酮环的特征结构,且具备酸碱两性,因其具有机体吸收快、组织浓度高、杀菌效果好、抗菌谱广等优势,故在治疗家禽感染性疾病中的应用十分广泛。氟喹诺酮类药物对革兰氏阳性菌、革兰氏阴性菌、细胞内病原菌、霉形体及某些耐药菌株都有很好的抗菌活性,常用药物包括恩诺沙星、环丙沙星、氧氟沙星、培氟沙星、诺氟沙星、沙拉沙星等。但是,随着氟喹诺酮类药物的广泛应用,其被滥用的问题也逐渐引起各方重视—长期食用氟喹诺酮类药物超标的肉类、蛋类等食物会致使人体内的抗生素蓄积,进而导致内分泌系统、消化系统、生殖系统等损伤,甚至产生细菌耐药性。当前,农业部制定了《食品安全国家标准 食品中兽药最大残留限量》(GB 31650-2019),发布《在食品动物中停止使用洛美沙星、培氟沙星、氧氟沙星、诺氟沙星4种兽药的决定》(农业部公告第2292号)等,以规范氟喹诺酮类药物的使用。
目前,适用于检测氟喹诺酮类药物残留的方法包括免疫分析法、微生物法、高效毛细管电泳分析法、高效液相色谱法、液相色谱-质谱联用法等,在《国家食品安全监督抽检实施细则》中采用的方法主要有《动物源产品中喹诺酮类残留量的测定 液相色谱-串联质谱法》(GB/T 20366-2006)、《动物源性食品中14种喹诺酮药物残留检测方法 液相色谱-质谱/质谱法》(GB/T 21312-2007)等。由于GB/T 20366-2006中不使用固相萃取柱,且提取过程需使用大量乙腈和正己烷,并存在旋蒸耗时长等问题,导致实验不够简便快捷。因此,笔者从提取、旋蒸、定容等方面对GB/T 20366-2006的方法进行了优化,以期为动物源食品中氟喹诺酮类药物残留的测定提供参考。
1 仪器设备
1.1 检测仪器
液相色谱-串联质谱仪:AB SCIEX API 4000,配有电喷雾离子源;
ZORBAX Eclipse Plus C18 600Bar (3×100mm,1.8μm)。
1.2 前处理设备
均质器、旋转蒸发仪、氮吹仪、涡旋混匀器、离心机、分析天平、移液器、聚四氟乙烯离心管等。
1.3 试剂
甲酸,优级纯;乙腈、正己烷,色谱纯;一级水。
1.4 氟喹诺酮类药物标准品
恩诺沙星(Dr.)、环丙沙星(Dr.)、诺氟沙星(Dr.)、恩诺沙星(Dr.)、氧氟沙星(Dr.)、沙拉沙星(Dr.)。
用乙腈配制成1000mg/L的标准溶液,并逐级稀释配制成混合标准工作液。
2 实验方法
参照《动物源产品中喹诺酮类残留量的测定 液相色谱-串联质谱法》(GB/T 20366-2006)。
3 结果与分析
3.1 优化提取体积
分别用5、10、20mL甲酸-乙腈溶液提取待测样品2次,使用提取溶液总体积为10、20、40mL,其余步骤按照GB/T 20366-2006进行。结果显示,提取溶液体积与回收率呈正相关,依次为40.3%~50.6%、66.8%~75.2%、69.5%~77.4%。当提取溶液总体积为20mL时,既能得到较好的回收率,又可以降低有机溶剂的使用量。因此,将甲酸-乙腈溶液20mL作为优化后的提取体积,同时正己烷的用量相应减少。
3.2 优化旋转蒸发
在进行旋转蒸发操作时,经常因提取溶液中的水分较多不易蒸干而耗费大量时间。本实验在正己烷除脂后,于下层提取溶液中加入适量无水硫酸钠以除去提取溶液中的水分,同时提高旋蒸温度以减少蒸干时间。如表1所示,添加无水硫酸钠的同时提高旋蒸温度对回收率无显著影响,且旋蒸用时缩短了6~8分钟。因此,将添加无水硫酸钠、50℃旋蒸作为优化后的旋蒸条件。
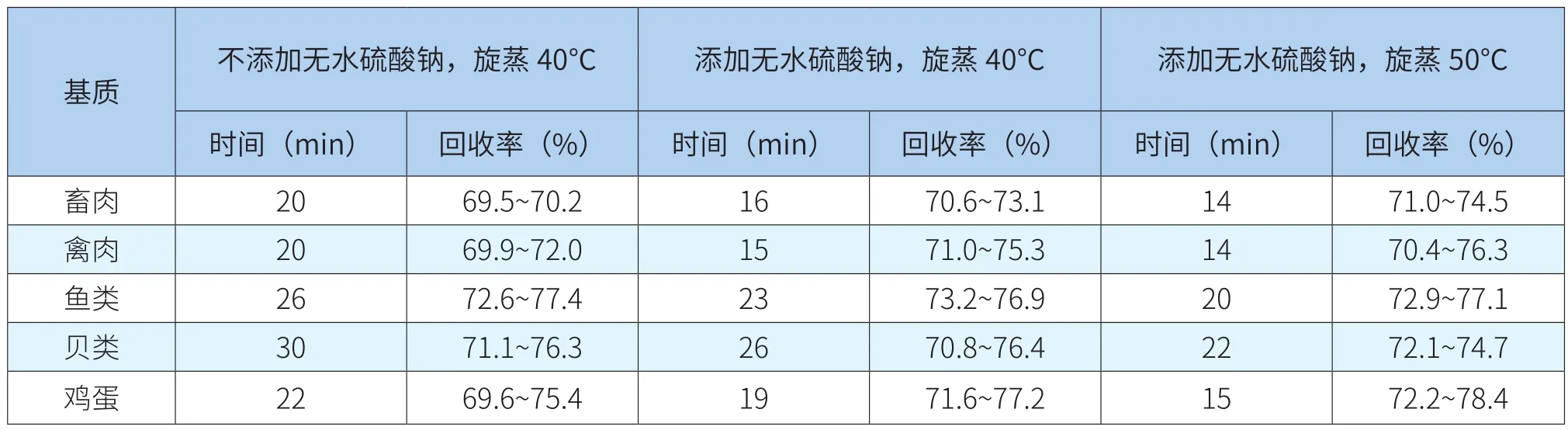
表1 不同旋蒸条件的用时和回收率
3.3 优化定容液
GB/T 20366-2006使用的定容液为甲酸-乙腈(2+98),由于乙腈比例太高,导致峰形不好,响应不高,定量不准确。本试验将定容液改为乙腈-0.1%甲酸-水(乙腈:水=2∶10)溶液后,峰形和响应都得到明显改善,回收率为85.1%~113.7%。因此,将乙腈-0.1%甲酸-水(乙腈:水=2∶10)溶液作为优化后的定容条件。
4 结论
研究结果显示,采用10mL甲酸-乙腈溶液提取2次,并相应减少正己烷用量,添加无水硫酸钠后于50℃旋蒸,用乙腈-0.1%甲酸-水(乙腈:水=2:10)定容,其余按照GB/T 20366-2006步骤进行,不仅能够在减少有机溶剂使用量的同时缩短实验用时,更可以改善峰形,提高响应值,进而得到令人满意的回收率。
