SrO-La2O3-P2O5系统玻璃的形成及性能
2020-10-21鲍孙,张超,郭甜,张晶晶,林海,王志强
鲍 孙, 张 超, 郭 甜, 张 晶 晶, 林 海, 王 志 强
( 大连工业大学 纺织与材料工程学院, 辽宁 大连 116034 )
0 引 言
磷酸盐光学玻璃属于低色散光学玻璃,在短波区的相对部分色散比一般冕牌玻璃大,具有特殊的相对部分色散,可作为消除二级光谱的特殊色散光学玻璃,能够提高光学成像清晰度,改善成像质量,优化成像系统。因此,磷酸盐光学玻璃具有很好的开发应用前景和市场需求,能够应用于诸多领域[1]。另外,磷酸盐玻璃相对于其他系统玻璃对稀土离子具有较好的溶解性,较长的荧光寿命,较小的非线性系数以及较大的光致暗化阈值,已经成为一种重要的光学基质材料[2]。
磷酸盐玻璃的系统性研究对于磷酸盐光学玻璃的发展有着至关重要的作用,然而目前对于磷酸盐玻璃系统性研究还很匮乏,理论体系还在不断完善。BaO-RmOn-P2O5和ZnO-RmOn-P2O5系统是磷酸盐玻璃系统中研究较全面和性能较好的[3]。戴世勋等[4]研究了BaO-Nb2O5-P2O5三元系统的玻璃形成区和玻璃特性。Kitamura等[5]研究了ZnO-Bi2O3-P2O5系统玻璃的光学性质,发现该玻璃系统的低P2O5含量区域(O、P摩尔比大于3.5)和高P2O5含量区域(O、P摩尔比小于3.5)的光学性能具有明显差异。陆春华等[6]研究了BaO-Al2O3-Sm2O3-P2O5体系玻璃的耐水、耐酸和耐碱性,讨论了组成对玻璃化学稳定性的影响。
SrO对于玻璃的作用介于CaO和BaO之间,目前还没有关于SrO-RmOn-P2O5体系的系统研究。本实验研究了SrO-La2O3-P2O5(SLP)三元系统玻璃的形成区域,探究了SrO摩尔分数变化对xSrO-10La2O3-(90-x)P2O5(5≤x≤30)系统玻璃结构、光学性能、热稳定性以及化学稳定性等性能的影响,旨在研制一种色散较低、稳定性较好的氧化锶添加镧磷酸盐光学玻璃。
1 实 验
1.1 试 剂
磷酸二氢铵,高级纯,上海太洋科技有限公司;碳酸锶,分析纯,山东西亚化学工艺有限公司;氧化镧,高级纯,上海太洋科技有限公司。
1.2 样品制备
采用传统的熔融-冷却法按摩尔比制备SrO-La2O3-P2O5三元系统玻璃。将准确称量的原料混合均匀后,快速移至刚玉坩埚中,在硅碳棒电热炉中进行熔制。为了消除强还原气氛对玻璃质量的不良影响,将配合料预先在260 ℃保温2 h,使磷酸二氢铵充分受热分解释放出氨气。然后升温至1 380 ℃下保温2 h,将熔制完毕的玻璃液浇铸在提前预热好的石墨模具后迅速转移至马弗炉中590 ℃退火处理1 h,随炉冷却至室温取出。将得到的玻璃样品进行加工处理,并取小块试样在玛瑙研钵中研磨过200目筛以供后续测试用。
1.3 性能表征
1.3.1 折射率测试
取规格为20 mm×20 mm×2 mm,两平行面精密抛光的块状玻璃样品,利用Metricon2010棱镜耦合仪进行折射率测试。折射率与入射波长的柯西色散公式为n=a+b/λ2,其中,a、b为柯西色散系数。利用柯西色散公式计算被测样品的折射率。样品在钠灯589.3 nm(D线)、氢灯486.1 nm(F线)与656.3 nm(C线)透射下的折射率值分别记为nD、nF和nC。阿贝数是光学系统设计中消除色差经常使用的参数,也是光学玻璃的重要性质之一,阿贝数越大,表明玻璃的色散越小。阿贝数vD=(nD-1)/(nF-nC)。
1.3.2 透过率分析
取抛光后平均厚度为2 mm样品,用UV-1800(PC)测试玻璃的透过率。测试波长范围为190~1 100 nm,步长为10 nm。
1.3.3 红外吸收光谱分析
采用America Perkin Elmer生产的Spectrum Two型傅里叶变换红外光谱仪测定样品红外吸收光谱,测试波长范围450~4 000 cm-1。测试样品过200目标准筛,在干燥的操作环境下测试。
1.3.4 特征温度和热膨胀系数分析
采用高温卧式膨胀仪(PCY型,湘潭湘仪仪器有限公司)测量玻璃的热膨胀曲线,确定样品的转变温度(tg)、软化温度(tf)和热膨胀系数(α20-300℃)。样品加工成长50 mm,直径为5 mm的圆柱体玻璃棒,设置升温速率为5 ℃/min,升温范围25~750 ℃。
1.3.5 密度测试
采用FA1104J新型高精度电子天平,精确度4×10-4g,通过内部预设的智能密度测量功能对样品密度进行测试。
1.3.6 化学稳定性测试
取规格为10 mm×10 mm×2 mm,六面精密抛光的玻璃样品,在90 ℃的去离子水中浸泡24 h,测量玻璃失重率,以此衡量玻璃的化学稳定性。
2 结果与讨论
2.1 SrO-La2O3-P2O5三元系统玻璃形成区
通过实验得知La2O3-P2O5二元系统玻璃中,La2O3的相对摩尔数在0~25形成玻璃。由文献[7]可知在SrO-P2O5二元系统玻璃中,SrO的相对摩尔数在0~55形成玻璃。在二元相图的基础上,绘制SrO-La2O3-P2O5系统玻璃三元相图,选取相图中一些点对应的原料比例称取原料进行熔制,再根据所得到的玻璃形成情况,在三元相图上对各组分所对应的点进行标注,从而得到比较完整的SrO-La2O3-P2O5三元系统玻璃形成区,如图1所示。图1中实心和空心的圆圈分别代表结晶以及透明玻璃组成,而半空心的圆圈表示该玻璃样品乳浊但不完全结晶。由此可见,SrO-La2O3-P2O5三元系统玻璃的形成区较小,受氧化镧的含量影响较大。SrO和La2O3都是以网络外体氧化物的形式处于磷酸盐玻璃网络外,但是La3+的电场强度较Sr2+的大。因此,在三元系统玻璃中,La3+主要起积聚作用,而Sr2+主要起断网作用。在La2O3-P2O5二元系统玻璃的基础上用SrO取代P2O5进一步提高镧磷酸盐玻璃的折射率以及降低玻璃的熔制温度。
根据SLP三元系统玻璃的形成区,选取摩尔组成为xSrO-10La2O3-(90-x)P2O5(5≤x≤30)的透明玻璃为研究对象,记为A组玻璃,具体组成见表1。
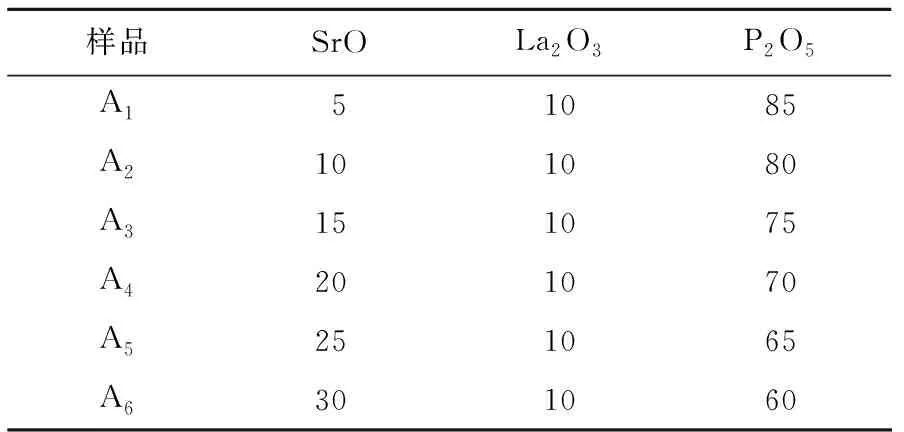
表1 玻璃样品摩尔组成Tab.1 The molar compositions of glass samples %
2.2 红外光谱分析

2.3 特征温度和热膨胀系数分析
玻璃的热膨胀系数主要由玻璃内部质点间作用力的大小决定。对于氧化物玻璃而言,热膨胀系数取决于阳离子与O2-之间的吸引力F大小。F=2Z/r2,其中,Z为阳离子电价,r为阴阳离子中心距。一般来说F越大,膨胀越困难,F越小则膨胀越容易[9]。Tg的变化反应了玻璃网络结构和组成的变化。Tg、Tf以及α20-300℃的变化趋势,如图3所示。随着SrO摩尔分数的增加,A组玻璃的热膨胀系数呈上升趋势,而玻璃特征温度整体呈现下降趋势,且两者均呈现非线性变化趋势。在SrO-La2O3-P2O5系统玻璃中,用SrO取代P2O5时,由于Sr2+比P5+电价小,并且Sr2+半径较P5+大,故随着SrO摩尔分数的增加,F逐渐减小,玻璃的热膨胀系数逐渐增大。SrO摩尔分数增加时,SrO提供的“游离氧”会破坏P—O—P键,产生非桥氧,玻璃网络结构完整性被破坏,从而使玻璃的特征温度下降。而低温时部分Sr2+对桥氧有一定的积聚作用,在一定程度上会增强玻璃网络结构紧密性[10],因此样品的特征温度和热膨胀系数曲线呈现非线性变化趋势。从总的趋势来看,过多的SrO会降低玻璃网络结构的完整性,使得玻璃热稳定性变差。
2.4 光学性能分析
2.4.1 组成变化对折射率的影响
总的来说,玻璃的折射率取决于玻璃内部离子的极化率和玻璃的密度。在测量玻璃的折射率和色散值时,是针对一定的波长确定的。样品的光学常数和玻璃密度情况如图4所示。由图4可见,随着SrO摩尔分数的增加,玻璃的密度先减小后增加。
玻璃的密度取决于网络紧密程度和网络空隙填充程度及组分中阳离子的原子量。用少量的SrO取代P2O5时,SrO起断网作用使网络疏松,导致密度略有下降。当进一步增加玻璃中SrO的摩尔分数时,Sr2+对于相邻磷氧四面体的聚集作用加强[11],同时大量的Sr2+填充在玻璃网络的空隙中,单位体积内的原子填充度增加,且锶离子的质量较大,故而使玻璃的密度上升。
当样品中SrO摩尔分数在5%~10%时,由于SrO提供的“游离氧”使得P—O—P断裂,产生非桥氧,而非桥氧极化率大,因此玻璃折射率上升,SrO摩尔分数进一步增加造成密度上升也使样品折射率提高;SrO摩尔分数在10%~30%时,玻璃密度的增加对样品折射率的增加起主导作用。由于Sr2+离子半径较小,可以在不使玻璃网络扩张的前提下填充到玻璃网络间隙中,玻璃密度增加,光在玻璃中的传播速度降低,从而玻璃的折射率增加。玻璃的色散符合加和原则,而P2O5与SrO平均色散相差不大,因此,SrO摩尔分数变化对玻璃色散影响较小[12-13]。
2.4.2 组成变化对透过率的影响
图5为A组玻璃中A1,A3和A5的透过率曲线,主要显示了玻璃从远紫外(190 nm)到近红外(1 100 nm)波长范围内玻璃透过率变化情况,该组其他试样的透过率曲线与三者相似。由图5可见,玻璃在远紫外波段的透过率很低,随着玻璃中SrO摩尔分数的增加,样品在可见光范围内透过率呈上升趋势,近红外波长范围内玻璃透过率变化较小,保持在90.0%左右。
虽然随着玻璃中SrO摩尔分数的增加,玻璃折射率增长的同时反射率也会增加,势必会造成玻璃透过率和吸收率之和的下降。但是,随着玻璃中P2O5含量的减少和“游离氧”数目的增多,都会使得网络结构完整性被破坏,可见光也就更加容易透过玻璃,玻璃的透过率上升。显然,玻璃网络结构变化对透过率的影响更明显。同时,单组样品在可见光(380~760 nm)和近红外波段(760~1 100 nm)范围内透明度较高且变化幅度较小,维持在90.0%左右。
2.5 化学稳定性分析
图6为A组玻璃的耐水失重率曲线,从图6中可以看出,玻璃整体的耐水性能较好,实验条件下失重不超过5.5 mg/cm2。SrO摩尔分数逐渐增加时,玻璃的失重率先增加再减小。玻璃的化学稳定性主要取决于玻璃结构的完整性和玻璃组分中离子的溶出能力。玻璃网络结构越完整,化学稳定性越好。离子半径越小,电价越低,网络空隙越大,离子越容易迁出,玻璃的稳定性也就越差。当玻璃中SrO摩尔分数较少时,SrO提供的“游离氧”对玻璃网络起破坏作用,但是Sr2+对相邻[PO4]磷氧四面体起到积聚作用,因此玻璃的失重率较低。继续增加玻璃中SrO摩尔分数,“游离氧”对玻璃网络的破坏作用进一步加强,导致玻璃的失重率增大,化学稳定性变差。磷酸盐玻璃结构中大量终端氧原子以及磷酸盐易溶于水是其化学稳定性差的主要原因,适当减少玻璃中P2O5的含量可以提高玻璃的化学稳定性。因此,当玻璃中SrO摩尔分数达到20%时,玻璃的失重率开始下降,同时考虑到Sr2+离子半径较大,在玻璃中迁移能力较差,也会使得玻璃的失重率下降,化学稳定性提高[14]。
3 结 论
(1)SrO-La2O3-P2O5三元系统玻璃的形成区域较小,玻璃形成受La2O3的含量影响较大,形成区内玻璃组分中La2O3的摩尔分数小于25%。
(2)对于摩尔组成xSrO-10La2O3-(90-x)P2O5(5≤x≤30)三元系统玻璃,当以SrO取代P2O5时,玻璃折射率上升,由1.568 0增加到1.586 3。玻璃在远紫外透过率极低,可以作为远紫外吸收材料使用。
(3)随着SrO摩尔分数增加,玻璃中“游离氧”数量的增多,对玻璃网络结构完整性破坏较大,转变温度下降,膨胀系数增大。玻璃耐水性能较好,耐水失重率随着SrO摩尔分数的增加先上升后下降。
