Nav1.5表达对结直肠癌多药耐药细胞迁移及侵袭的影响
2020-10-17胡瑶瑶汪谢嫒冯光勇岳国军杨明镇张贵海
胡瑶瑶,汪谢嫒,冯光勇,岳国军,杨明镇,张贵海
(1.遵义医科大学附属医院肿瘤医院,贵州 遵义 563099;2.湘南学院附属医院 肿瘤科,湖南 郴州 423000;3.深圳市盐田区人民医院,广东 深圳 518000;4.遵义医科大学附属第二医院,贵州 遵义 563000;5.遵义医科大学附属医院 介入科,贵州 遵义 563099)
结直肠癌(Colorectal cancer,CRC)是最常见的消化道肿瘤之一,约25% CRC患者在确诊时就已经发生远处器官转移[1],另约25% CRC患者在疾病治疗过程中发生转移[2],是其治疗失败的主要原因之一,而肿瘤细胞的侵袭及迁移是肿瘤远处转移的关键环节。电压门控性钠离子通道(Voltage-gated sodium channels,VGSCs)是由1个α亚基和4个β亚基构成的蛋白复合体,SCN1A-SCN11A基因编码的α亚基为功能亚基,共有9种亚型(Nav1.1~Nav1.9)[3]。VGSCs既可以在兴奋细胞中表达,也可以在“非兴奋”细胞和组织中表达,如:结直肠癌[4]、乳腺癌[5]、卵巢癌[6]及前列腺癌[7]等,且与肿瘤的转移有关[8]。河豚毒素(Tetrodotoxin,TTX)是VGSCs的特异性抑制剂,根据VGSCs对TTX的敏感性,VGSCs分为TTX敏感型(TTX-S)和TTX耐受型(TTX-R)。有研究发现,Nav1.5在结肠癌组织较正常组织呈高表达,并与结肠癌细胞侵袭势能有关[9],但其在CRC耐药细胞中表达情况及其与转移势能的关系尚不清楚。因此,本研究通过比较结直肠癌亲本细胞SW620和耐药细胞SW620/OxR 的Nav1.5功能及蛋白表达的差异,探讨Nav1.5功能变化对CRC耐药细胞侵袭、迁移的影响及可能机制。
1 材料与方法
1.1 细胞株与试剂 结直肠癌细胞株SW620购于上海生命科学院细胞库。 Leibovitz's L-15 培养基购自美国Gibco公司;胎牛血清(FBS)购自上海依科赛公司;基质胶(Matrigel)购自美国Corning公司;CCK8试剂盒购自ATGene公司;奥沙利铂(Oxaliplatin,Oxa)、5-氟尿嘧啶(5-fluorocrail,5-FU)和小鼠抗人β-actin单克隆抗体购自美国Sigma公司;河豚毒素(TTX)、兔抗人P-gp抗体购自美国Abcam公司;兔抗人Nav1.5单克隆抗体由以色列Alomone公司惠赠;PVDF膜(0.45 μm)和Transwell 小室(孔径8 μm)均购自美国 Millipore公司;BCA 蛋白浓度测定试剂盒购自北京百泰克公司。
1.2 细胞培养及耐药细胞建立 人结直肠癌SW620细胞使用含10% 胎牛血清,2 mmol/L L-谷氨酰胺的Leibovitz's15(L-15)培养基进行培养(37 ℃,0% CO2饱和湿度)。采用浓度递增法,逐渐增加L-15培养液中OxR的浓度直至临床血浆浓度(2 μmol/L),建立慢性抵抗OxR的SW620/OxR细胞株[10]。
1.3 方法
1.3.1 实验分组 实验设置分组:SW620组、SW620/OxR组及5-FU或TTX干预组。干预组为用含2.0 μg/mL 5-FU或30 μmol/L TTX的培养基培养72 h的SW620 和SW620/OxR细胞。
1.3.2 CCK-8法细胞增殖实验 取对数生长期细胞SW620和SW620/OxR均以5×103/孔,接种于96孔培养板(100 μL/孔)中,待细胞贴壁生长约70%后,分别加入含2.0 μg/mL 5-FU或30 μmol/L TTX或2 μmol/L Oxa继续培养72 h,设置调零孔(仅含培养液和CCK-8),以不含干预药物的细胞孔为对照,每组设5个复孔。在既定时间每孔加10 μL的CCK-8试剂,37 ℃孵育2 h,酶标仪检测A450 nm的吸光度值(OD值),以吸光度值反应细胞增殖力。
1.3.3 细胞迁移实验 采用孔径为8 μm的Transwell小室进行实验,取5×104/mL的单细胞悬液200 μL加入小室内室,下室加入500 μL含10% FBS的L-15培养液,培养72 h,取出小室PBS洗涤2次, 加4% 多聚甲醛固定20 min,再用5%结晶紫溶液染色20 min,棉棒拭去未透膜细胞。倒置显微镜下随机选取5个高倍视野拍照、计数,实验重复3次。
1.3.4 细胞侵袭实验 配置浓度为 25%的Matrigel 胶工作液包被Transwell小室,放回培养箱中静置1 h,L-15水化小室滤膜。后续实验步骤同细胞迁移实验。
1.3.5 Na+电流检测 全细胞膜片钳技术被用于结直肠癌细胞膜Na+电流水平检测。选取对数期生长的SW620、SW620/OxR及TTX干预细胞,制成单细胞悬液并计数,接种于35×10 mm的培养皿,37℃、100% 湿度及无CO2培养箱中培养至完全贴壁。去除培养皿内的培养基,将细胞外液加入培养皿后置于倒置显微镜下,三维操纵仪移动电极,伸向细胞表面,加压形成1 GΩ水平以上的高阻抗封接,破膜,形成全细胞记录的形式,予不同参数的钳制电压观察电流的变化,用Origin软件分析数据。
1.3.6 Western blot检测P-gp和Nav1.5蛋白表达水平 提取细胞总蛋白,BAC法测定蛋白浓度,6% 和10% SDS-PAGE电泳后,恒流电转至PVDF膜上,含10%PBST脱脂奶粉室温封闭1 h,与兔抗人抗体Nav1.5(1∶500)、兔抗人抗体P-gp(1∶2 000)及鼠抗人抗体β-actin(1∶5 000)4 ℃孵育过夜,再以过氧化物酶标记的山羊抗兔二抗(1∶5 000)室温孵育1 h,PBST漂洗3次,每次10 min。ECL发光试剂显影,BIO-RAD全自动图像采集图像,Quantity Qne软件分析目的蛋白相对表达量。

2 结果
2.1 CRC耐药细胞株的鉴定 CCK-8法结果分析显示,奥沙利铂(OxR,2 μmol/L)和5-氟尿嘧啶(5-FU,2.0 μg/mL)对SW620/OxR细胞的增殖无明显抑制作用(0.940±0.078,0.941±0.037,P均> 0.05),却能显著抑制SW620细胞的增殖,差异有统计学意义(0.447±0.049,0.515±0.023,P均<0.05,见图1);SW620/OxR与SW620细胞增殖能力也无明显差异(P>0.05,见图1)。Western blot结果也显示,SW620/OxR细胞P-糖蛋白(P-gp)的蛋白表达水平较SW620细胞显著增加,差异有统计学意义(1.20±0.06,0.60±0.07,P<0.05,见图2)。
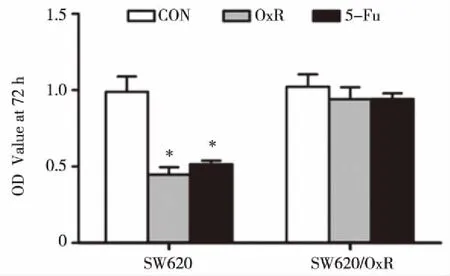
*:与对照组相比,OxR组和5-FU组对SW620/OxR细胞,SW620细胞的增殖比较,P<0.05。 图1 OxR与5-FU对CRC细胞增殖力的影响
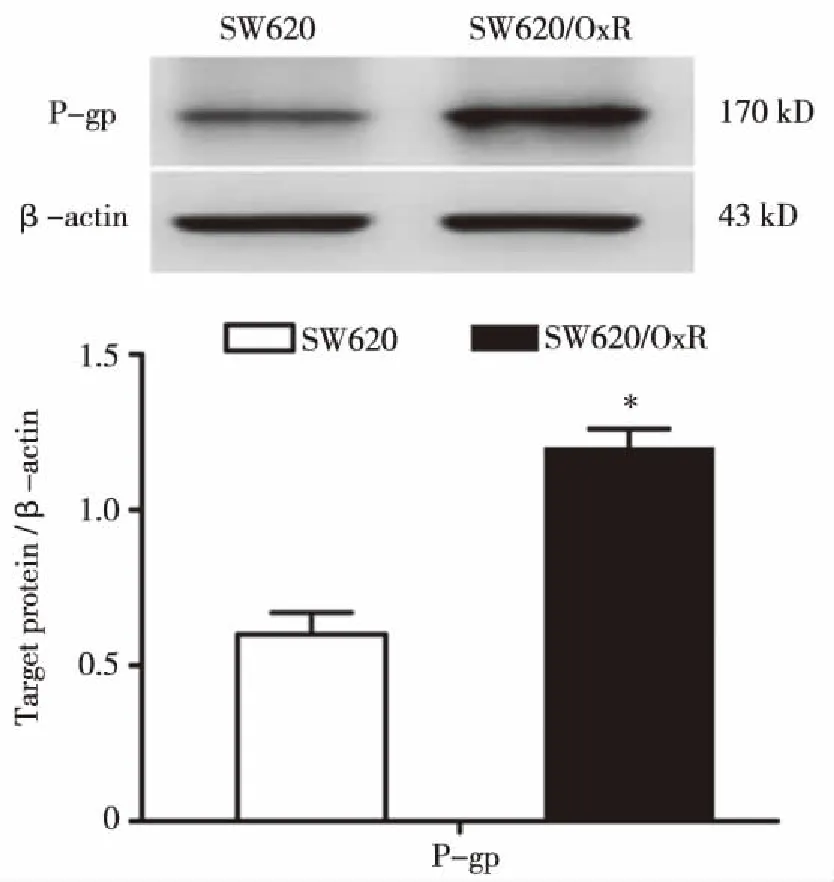
*:SW620/OxR细胞与SW620细胞P-gp蛋白水平比较,P<0.05。图2 CRC细胞P-gp蛋白表达水平
2.2 CRC细胞Na+电流密度及Nav1.5蛋白表达水平变化 采用10 μmol/L浓度的TTX抑制SW620 和 SW620/OxR细胞-10 mV的Na+电流密度,以排除其它因素对Nav1.5通道的干扰(见图3A、3B)。膜片钳检测结果显示,与SW620细胞比较,SW620/OxR细胞膜 Na+电流水平显著升高,差异有统计学意义(P<0.05,见图3C~F)。Western blot结果也显示,相较于 SW620细胞,SW620/OxR细胞Nav1.5蛋白表达水平也显著增加,差异有统计学意义(P<0.05,见图4)。

*:SW620/OxR细胞与SW620细胞电流密度对比,P <0.05,pA代表电流单位,mV代表电压单位。图3 CRC细胞在-10 mV出现最大Na+电流密度比较

SW620/OxR细胞与SW620细胞Nav1.5蛋白表达水平对比。图4 CRC细胞Nav1.5表达水平
2.3 TTX对CRC细胞增殖、迁移、侵袭及Nav1.5蛋白表达水平的影响 CCK-8法检测结果显示,30 μmol/L的TTX对SW620细胞和SW620/OxR细胞72 h的增殖力均无显著影响(P>0.05,见图5A );迁移实验却显示,SW620/OxR细胞迁移力较SW620细胞显著增加(P<0.05,见图5B),TTX均能显著降低SW620细胞和SW620/OxR细胞的迁移力(P均<0.05,见图5B)。侵袭实验显示,SW620/OxR细胞的侵袭力较SW620细胞明显增加,TTX均能显著降低SW620细胞和SW620/OxR细胞的侵袭力(P<0.05,见图5C)。 Western blot结果显示,TTX均能显著下调SW620细胞和SW620/OxR细胞Nav1.5蛋白表达水平(P<0.05,见图5D)。
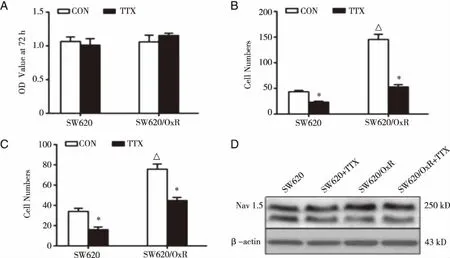
*:SW620/OxR细胞与SW620细胞迁移力对比,SW620/OxR细胞与SW620细胞侵袭力对比,P<0.05;△:TTX干预后,SW620/OxR细胞与SW620细胞迁移力比较,TTX干预后,SW620/OxR细胞与SW620细胞侵袭力比较,P<0.05;A:增殖;B:迁移;C:侵袭力;D:Nav1.5蛋白表达。图5 TTX对CRC细胞增殖、迁移、侵袭及Nav 1.5蛋白表达的影响
3 讨论
VGSCs是一种含有形成孔洞的α亚基和较小的、不形成孔洞的β亚基组成的异聚膜蛋白复合体,α亚基是其功能部分,β亚基具有调节α亚基在细胞表面表达及α亚基的门控的功能[11]。VGSCs除在心肌、神经等可兴奋细胞表达外,也可在“非兴奋”肿瘤组织中表达[4-7],并与部分肿瘤的转移有关[8]。转移是CRC治疗失败的最主要原因,而肿瘤细胞的迁移及侵袭是CRC远处转移的关键环节。目前,有研究发现Nav1.5在结肠癌组织呈高表达,且是CRC细胞促进侵袭基因网络的关键调控因子[12]。然而,关于Nav1.5表达与CRC多药耐药的关系及其对CRC耐药细胞迁移、侵袭的影响尚不清楚。
多药耐药(MDR)是导致肿瘤化疗和治疗失败的重要因素之一[13]。P-糖蛋白(P-glycoprotein,P-gp)是由MDR1基因编码的一种转运体,通过影响肿瘤细胞的药物转运在MDR中发挥重要作用。本研究显示,对奥沙利铂耐药的SW620/OxR细胞对5-氟尿嘧啶也产生耐药,P-gp表达水平也显著增加,与课题组以前研究报道一致[10]。Baptista-Hon等[14]研究发现,结直肠癌SW620细胞表达成人型和新生儿型Nav1.5变异体,两者均有相似的稳定失活状态。本研究结果发现,Nav1.5在转移性CRC亲本细胞SW620和耐药细胞SW620/OxR均有表达,SW620/OxR细胞Nav1.5表达水平及细胞膜Na+电流水平均显著高于SW620细胞,提示SW620/OxR细胞Na+电流增加可能源于Nav1.5表达上调,Nav1.5可能参与CRC多药耐药过程。House等[15]研究表明,来自同一结肠癌患者的原发灶SW480细胞Nav1.5表达水平低于转移灶SW620细胞。本研究同样也发现,来自同一SW620的亲本细胞Nav1.5蛋白表达水平明显低于耐药细胞。由此可见,Nav1.5在CRC不同阶段及不同状态表达不同,这可能与CRC 细胞部分生物学特性有关。Brackenbury 等[16]等研究显示,Nav1.5在转移性三阴(缺乏雌激素受体、孕激素受体和HER2)乳腺癌MDA-MB-231细胞中表达,且在体外能通过细胞外基质增强癌细胞的迁移和侵袭力。此外,Nelson等[17]研究显示,在高转移性乳腺癌MDA-MB-231细胞裸鼠移植瘤中,钠通道抑制剂苯妥英钠能抑制其向肝脏及肺脏的远处转移;A-803467作为一种强效的选择性Nav1.8钠通道阻滞剂[18],对ABCG 2介导的MDR有明显的抑制作用,也能显著提高H460/MX20(由人非小细胞肺癌亲本H460细胞通过逐步增加MX诱导的高表达ABCG2的耐药细胞株)细胞对ABCG2底物米托蒽醌及拓扑替康的敏感性及增强拓扑替康对裸鼠移植瘤的抗肿瘤作用[19]。本研究发现,SW620/OxR细胞的迁移力和侵袭力均较SW620细胞显著增加,而两种细胞的增殖力却无显著差异,提示CRC耐药细胞的迁移力和侵袭力增加可能与耐药细胞Nav1.5蛋白表达上调有关。Baptista-Hon等[14]研究表明,VGSCs抑制剂罗哌卡因能抑制转移性CRC SW620细胞的侵袭和Nav1.5通道的活性。为进一步明确Nav1.5功能与CRC细胞迁移和侵袭的关系,本研究应用钠通道抑制剂TTX,观察其对两种CRC细胞的Nav1.5表达、Na+电流及迁移和侵袭的的作用。本研究发现,30 μmol/L的TTX能显著降低亲本和耐药细胞的迁移及侵袭力,且下调两种细胞的Nav1.5表达水平及降低两种细胞的Na+电流水平,这进一步提示了Nav1.5能促进CRC细胞的迁移及侵袭,及Nav1.5抑制剂TTX抑制CRC细胞迁移、侵袭及Na+电流水平可能与Nav1.5表达下调有关。然而,本研究却显示,TTX对SW620和SW620/OxR细胞的增殖力无显著影响,由此可见Nav1.5可能不参与CRC细胞增殖的调控。目前,虽有研究认为Nav1.5编码基因SCN5A可通过细胞迁移、细胞周期控制基因和Wnt信号通路等调控CRC细胞侵袭[15],但尚无大规模临床试验研究证实VGSCs抑制剂对肿瘤的抑制效应[20]。因此,VGSCs抑制剂在抑制肿瘤侵袭及转移方面具有较大的潜能,其有望成为抗肿瘤治疗的新型靶向药物。
综上所述,CRC耐药细胞Na+内向电流增加可能源于Nav1.5表达上调,并参与CRC的多药耐药;Nav1.5能促进CRC细胞迁移及侵袭,TTX降低CRC细胞的迁移及侵袭力也可能部分与下调 Nav1.5蛋白表达有关。
