甘草酸二铵联合还原型谷胱甘肽治疗阿维A导致药物性肝损伤疗效观察
2020-10-13唐春翊郑义宏郑雯
唐春翊 郑义宏 郑雯
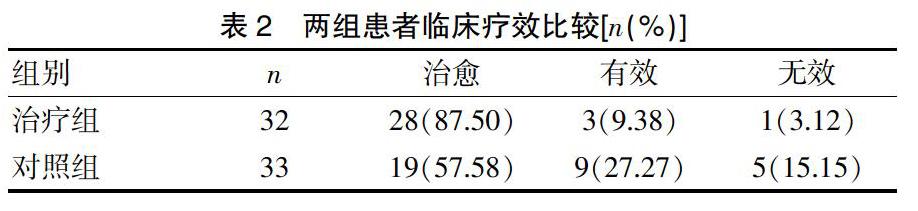
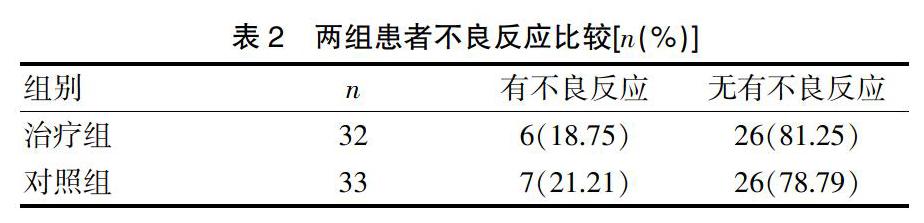
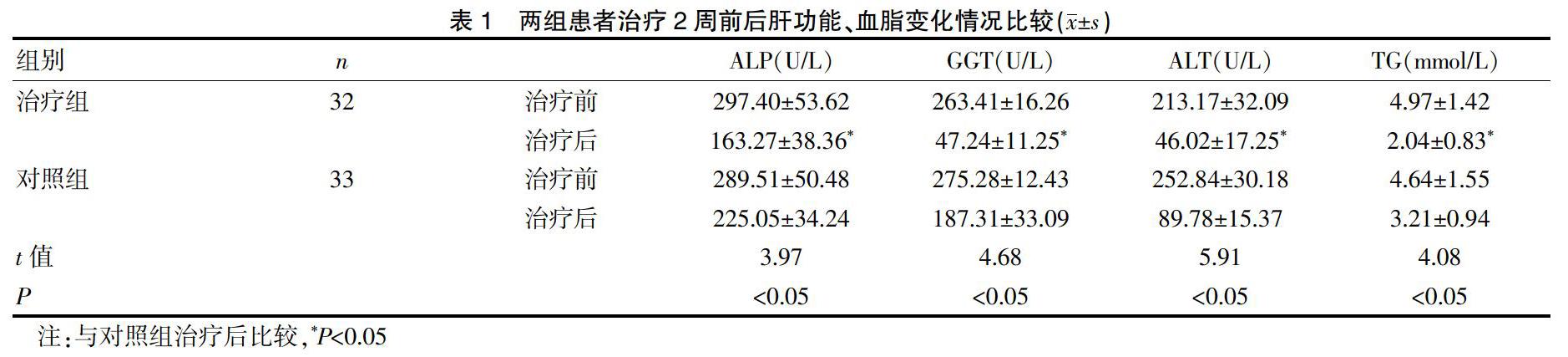
[摘要] 目的 探討甘草酸二铵联合还原型谷胱甘肽治疗阿维A导致药物性肝损伤的疗效。 方法 选取2019年1~12月口服阿维A所致药物性肝损伤患者65例,随机分为两组(治疗组32例,对照组33例),其中治疗组给予甘草酸二铵(甘草酸二铵150 mg+10%葡萄糖注射液250 mL,静点每日一次)联合还原型谷胱甘肽(还原型谷胱甘肽1.8 g+10%葡萄糖注射液250 mL,静点每日一次)治疗,2周为一疗程;对照组单独给予还原型谷胱甘肽治疗(用法剂量疗程与治疗组相同)。观察治疗前后两组患者肝功能(ALP、GGT、ALT等)和TG(血脂)的变化,比较两组临床疗效及不良反应。 结果 治疗后,两组患者肝功能指标和血脂均有显著改善,治疗组患者肝功能指标和血脂(甘油三酯)改善程度显著优于对照组,差异有统计学意义(P<0.05);治疗组治疗总有效率显著高于对照组;两组患者不良反应发生率比较,差异无统计学意义(P>0.05)。 结论 甘草酸二铵联合还原型谷胱甘肽治疗阿维A导致药物性肝损伤可显著改善患者肝功能并降低血脂,治疗总有效率高、不良反应少,适宜推广应用。
[关键词] 甘草酸二铵;还原型谷胱甘肽;阿维A;药物性肝损伤
[中图分类号] R512.6 [文献标识码] B [文章编号] 1673-9701(2020)24-0127-04
[Abstract] Objective To explore the therapeutic effect of diammonium glycyrrhizinate combined with reduced glutathione in the treatment of drug-induced liver injury caused by retinoin A. Methods From January to December 2019, 65 patients with drug-induced liver injury caused by oral Avita A were randomly divided into two groups(32 in the treatment group and 33 in the control group), of which the treatment group was given diammonium glycyrrhizinate(diammonium glycyrrhizinate 150 mg+10% glucose injection 250 mL, once a day) combined with reduced glutathione(reduced glutathione 1.8 g+10% glucose injection 250 mL, once a day). Two weeks was a course of treatment. The control group was given reduced glutathione alone(the dosage and dosage of the control group was the same as that of the treatment group). The changes of liver function(ALP, GGT, ALT, etc.) and TG(blood lipid) of the two groups of patients before and after treatment were observed. The clinical efficacy and adverse reactions were comgared between the two groups. Results After treatment, the liver function indexes and blood lipids of the two groups were significantly improved. The liver function indexes and blood lipids(triglycerides) of the treatment group were significantly better than those of the control group, and the difference was statistically significant(P<0.05). The total treatment effective rate of the treatment group was significantly higher than that in the control group. There was no statistically significant difference in the incidence of adverse reactions between the two groups(P>0.05). Conclusion Diammonium glycyrrhizinate combined with reduced glutathione in the treatment of retinoic acid-induced liver injury can significantly improve the liver function of patients and reduce blood lipids, with a high effective rate of treatment and fewer adverse reactions, which is suitable for popularization and application.
阿维A[化学名称:全反式-9-(4-甲氧基-2,3,6-三甲基苯基)-3,7-二甲基-2,4,6,8-壬四烯酸]是治疗重症银屑病(尤其是红皮病型银屑病、脓疱型银屑病)的一线药物[6],其作用包括影响细胞的分化及增殖、有效调节表皮角质形成细胞的终末分化、充分发挥其免疫调节的作用等,疗效远优于其他常规药物,受到全球范围的临床认可[7,8]。阿维A的主要不良反应包括皮肤黏膜瘙痒与干燥脱屑、肝损伤诱发DILI、白细胞和血小板增多、肌肉骨骼酸痛、血脂(TG)升高等[9],其中DILI与血脂(TG)升高较为严重[10],尤其是诱发DILI,在治疗银屑病的西药中排名第一(西药致DILI排名前五的药物品种依次是:(1)阿维A,占38.27%;(2)甲氨蝶呤,占34.57%;(3)来氟米特,占7.41%;(4)英夫利昔单抗,占3.33%;(5)别嘌醇,占3.33%[11]。
甘草酸二铵又称甘草酸二铵盐,是甘草酸异构体的产物,其分子式是C42H68N2016,为中药甘草有效成分的第三代提取物,在人体内具有活化氧化还原系统,激活SH酶、解毒作用等重要生理活性,对D-氨基抗半乳糖胺所致肝细胞线粒体及核仁的损害,明显阻止四氯化碳及硫代乙酰胺引起的ALT增高,改善肝脏受损组织,加速肝细胞恢复,很好地修复复合致病因子引起的慢性肝损害,改善免疫因子对肝脏的慢性损伤,因此具有较强的抗炎、保护肝细胞膜及改善肝功能的作用,使肝糖原及核酸含量增加,治疗多种肝毒剂所致肝脏损伤如DILI有显著疗效[12]。
还原型谷胱甘肽(Glutathione)是由谷氨酸、胱氨酸及甘氨酸组成的一种三肽,其分子式为C10H17N306S,即N-(N-L-γ-谷氨酰基-L-半胱氨酰基)甘氨酸。它是一种细胞内重要的调节代谢物质,既是甘油醛酸脱氢酶的辅基,又是乙二醛酶及磷酸丙糖脱氢酶的辅酶,既能够参与体内三羧酸循环及糖代谢、抑制脂肪肝形成,也能改善中毒性肝炎和感染性肝炎的症状,因此治疗各种肝病均有显著疗效。还原型谷胱甘肽在谷胱甘肽转移酶的作用下,能和过氧化物及自由基相结合,以对抗氧化剂对巯基的破坏,保护细胞膜中含巯基的蛋白质和含巯基的酶不被破坏,亦对抗自由基对重要脏器的损害,产生解毒和保护细胞的疗效[13]。
谷丙转氨酶(ALT)、谷氨酰转移酶(GGT)和碱性磷酸酶(ALP)等是DILI的诊断标志物[14],其中ALT(谷丙转氨酶)主要分布在肝细胞浆内,是反映肝细胞受损程度最灵敏的指标,肝细胞发生变性、坏死、中毒等受到损伤时,谷丙转氨酶释放入血液中,就会引起血清谷丙转氨酶偏高,其升高的程度与肝细胞受损的程度相一致;GGT谷氨酰转肽酶的活性与转氨酶水平和肝病变程度有良好的一致性,其升高与转氨酶正向线性相关,其异常率与肝组织病变的程度显著相关,因此是反映肝细胞损害程度的主要指标之一;谷氨酰转移酶(GGT)主要存在肝细胞膜、肝细胞微粒体和毛细胆管上,参与谷胱甘肽的代谢;肝细胞和胆管上皮细胞增生或癌变)时,血清ALP总活力可升高,且ALP水平升高是持续DILI的重要因素。因此发生DILI时,ALT、GGT和ALP出现相应改变。甘油三酯(TG)是脂质的组成成分,是甘油和3个脂肪酸所形成的脂,是人体内脂质的重要组成部分(除甘油三酯外,还包括胆固醇、磷脂、脂肪酸以及少量其他脂质),其主要功能是供给与储存能源,固定和保护肝脏等重要脏器。肝脏可利用糖、甘油和脂肪酸作原料,通过磷脂酸途径合成甘油三酯。DILI患者因肝细胞功能受损而产生脂代谢紊乱,血脂异常是DILI发生率和严重程度的危险因素[15]。临床观察结果表明,甘草酸二铵联合还原型谷胱甘肽治疗药物性肝损伤可迅速改善临床症状,减轻炎性细胞浸润及肝细胞坏死,肝损伤患者的ALT、ALP、TG水平,肝功能获得显著恢复。观察结果表明,二者联合治疗DILI安全、高效,且不良反应少,值得推广应用。
[参考文献]
[1] 苗素芹.评价阿维A治疗严重类型银屑病的临床疗效[J].中国实用医药,2015,10(17):175-176.
[2] Eise MD,Poterucha JJ,Talwalkar JA.Drug-induced liver injury[J].Mayo Clin Proc,2014,89(1):95-106.
[3] Kim SH,Naisbitt DJ.Update on advances in Research on idiosyncratic drug-induced liver injury[J].Allergy Asthma Immunol Res,2016,8(1):3-11.
[4] 熊晓梅,李玲,王斌.药物性肝损伤的基因多态性研究进展[J].中国医院药学杂志2020,40(4):109-114.
[5] 于乐成,茅益民,陈成伟.药物性肝损伤诊治指南[J].实用肝脏病杂志,2017,20(2):257-274.
[6] 孙洁,于锋,王坚. 337例药物性肝损伤的临床特点及相关药物分析[J].药学与临床研究,2013,(4):383-387.
[7] 趙晓冬,王淑安,李昕,等.阿维A和常规药物治疗重症银屑病临床效果对比研究[J].中国实用医药,2015,10(9):161-162.
[8] 陈卓林.阿维A治疗重症银屑病的临床疗效[J].临床合理用药杂志,2018,30(10):62-63.
[9] 林静,杨学平,单萍.阿维A所致不良反应[J].中国误诊学杂志,2010,21(7):5287.
[10] 赵冰洁,张江安,于建斌,等.阿维A对银屑病患者血脂影响的回顾性分析[J].临床皮肤科杂志,2017,46(6):406-408.
[11] 朱敬肖,葛斐林,刘亚蕾等.银屑病用药相关肝损伤分析[J].中国药物警戒,2019,16(5):277-280.
[12] 余梅香,李紫薇,杨婉花.甘草酸二铵制剂治疗药物性肝损害有效性与安全性的系统评价[J].中国现代应用药学,2019,36(4):478-484.
[13] 王准,龚天斌.3种常用改善肝功能药物治疗药物性肝损伤的效果比较[J].临床肝胆病杂志,2016,32(4):761-763.
[14] 蒙义军,余洪立,杨石.GLDH、GGT、ALT、ALP联合检测对药物性肝损伤诊断的临床意义[J]检验医学与临床,2019,16(6):1735-1737.
[15] 李旭,高普军.血脂异常是DILI发生率和严重程度的危险因素[J].临床肝胆病杂志,2019,35(8):1827.
(收稿日期:2020-04-20)
