生物铁锰氧化物的制备及其对Mn(II)吸附特征研究
2020-10-09张攀侯冬梅魏东宁罗琳
张攀 侯冬梅 魏东宁 罗琳


摘 要:利用驯化获得的铁锰氧化混合细菌制备生物铁锰氧化物(BFMO),采用比表面积测定仪(BET)、扫描电镜(SEM-EDS)和傅里叶红外变换光谱(FT-IR)对所生成的BFMO进行表征,通过考察投加量和pH值对Mn(II)吸附性能的影响,探究了BFMO对Mn(II)的吸附机理。结果表明:BFMO具有較大的比表面积(79.22 m2/g),孔体积为0.15 cm3/g,表面含有许多含氧官能团,有利于Mn(II)的吸附。SEM-EDS进一步表明生物铁锰氧化物中既含有铁锰氧化物,也有微生物菌体生成的细胞类物质。BFMO对Mn(II)的去除效果较好,在pH值为7.0、投加量为2 g/L、固液比为1 g∶500 mL时,吸附量为16.43 mg/g,吸附过程符合准二级动力学模型和Freundlich吸附等温模型,说明吸附过程主要由化学反应控制,属于多层吸附。
关键词:生物铁锰氧化物;锰离子吸附;反应动力学;表征分析
中图分类号:X131文献标识码:A文章编号:1006-060X(2020)08-0041-06
Abstract: Biological iron and manganese oxide (BFMO) was generated by Leptothrix discophora. The BFMO was characterized by specific surface area analyzer (BET), scanning electron microscopy-energy dispersive spectrometer (SEM-EDS) and Fourier transform infrared spectroscopy (FT-IR). The effects of dosage and pH value on the adsorption performance of Mn (II) were investigated, and the adsorption mechanism of BFMO for Mn (II) was explored. The results show that BFMO has a large specific surface area (79.22m2/g), a pore volume of 0.15 cm3/g, and many oxygen-containing functional groups on the surface, which is conducive to the adsorption of Mn (II). SEM-EDS further show that there are not only iron and manganese oxides in biological iron and manganese oxides, but also cellular substances produced by microbial bacteria. The removal effect of BFMO on Mn (II) is better. When pH value was 7.0, dosage was 2 g/L, solid-liquid ratio was 1 g: 500 mL, the adsorption capacity was 16.43 mg/g, the adsorption process was in accordance with the pseudo second-order kinetic model and Freundlich adsorption isotherm model, indicating that the adsorption process was mainly controlled by chemical reaction and belonged to multilayer adsorption.
Key words: biological and iron manganese oxide; Mn (II) adsorption; reaction kinetics; characterization analysis
锰及其化合物作为许多领域必要的工业原料,是我国国民经济建设的重要战略物资。但随着现代工业的发展,冶金、干电池生产、印染和纺织等行业产生大量高浓度含锰废水,这些废水经地表径流、氧化还原反应等途径进入人类的生活环境,对人体健康造成严重危害[1-2]。目前,投加吸附材料是去除环境水体中锰离子的主流方法,常用的吸附剂有磁性纳米颗粒[3]、改性氧化铝[4]、电解锰渣基沸石[5]、锰氧化物[6]等。其中锰氧化物具有表面活性强、对金属离子具有较强结合能力以及化学、热、辐射稳定性等特点,能吸附多种重金属元素和微量元素,不仅可以用于修复环境中的重金属污染,也可以氧化降解其他污染物[7-8]。
锰氧化物主要通过化学法合成获得,但是该方法存在成本能耗高、易产生有毒中间产物的缺点。近年来,微生物法合成的锰氧化物受到越来越多国内外学者的关注,通过生物法获得的锰氧化物较化学锰氧化物具有更大的比表面积,更强的吸附能力,对金属离子的去除效果也更明显[9-10]。然而在自然环境中铁、锰往往是同时存在的,因此,微生物在自然环境中形成的锰氧化物往往混有铁氧化物[11]。与此同时,有研究表明,铁的存在对于生物锰氧化物的形成以及金属离子的去除有明显促进作用[7-12]。因此,笔者通过铁锰氧化微生物菌群合成生物铁锰氧化物,并利用其去除水体中的锰离子,探究其吸附效果及吸附机理,为环境中含锰废水的处理提供新的途径和科学依据。
1 材料与方法
1.1 菌种的活化
用来制备生物铁锰氧化物的微生物细菌为实验室驯化获得的铁锰氧化混合细菌(HM-7),试验中采用的微生物培养基及培养条件如下。
PYCM改良培养基:蛋白胨0.5 g/L、葡萄糖0.3 g/L、酵母浸膏0.2 g/L、MnSO4·H2O 0.2 g/L、K2HPO4 0.1 g/L、MgSO4·7H2O 0.2 g/L、NaNO3 0.2 g/L、CaCl2 0.1 g/L、(NH4)2CO3 0.1 g/L、檸檬酸铁铵0.8 g/L,调节pH值为6.8~7.2,121℃灭菌30 min[13]。
菌种的活化:将混合菌群以2%的接种量接入新鲜的PYCM改良培养基中,在30℃、120 r/min的条件下连续培养6~7 d,完成菌种的活化。
1.2 生物铁锰氧化物的制备
配制PYCM改良培养基,向培养基中加入经过0.22 ?m的微孔过滤膜(有机系)过滤除菌的MnSO4·H2O(520 mg/L)和FeSO4·7H2O(100 mg/L)溶液。将活化好的铁锰氧化混菌按2%的接种量接种,在30℃、120 r/min条件下,在恒温摇床上连续培养12 d获得大量的生物铁锰氧化物沉淀。将生物铁锰氧化物沉淀以4 000 r/min的速度离心,离心后过滤除去上清液,将沉淀物用去离子水反复洗涤3次,置于真空冷冻干燥机中冷冻干燥48 h,将沉淀物研磨均匀保存备用。
1.3 生物铁锰氧化物的表征
SEM-EDS表征:利用扫描电子显微镜(日本日立,冷场发射S4800)分析材料的微观形貌和组织结构,放大倍数为5 000倍;BET表征:利用多通道比表面积及孔径分析仪(麦克默瑞提克仪器有限公司,Gemini-2390),使用气体吸附系统在-195.85℃下,根据N2吸附-脱附等温线测定生物铁锰氧化物比表面积和孔隙;FT-IR(傅里叶变换红外光谱)表征:利用傅里叶变换红外光谱仪(日本岛津,IRTracer-100)确定存在于生物铁锰氧化物表面的化学官能团。
1.4 生物铁锰氧化物对Mn(II)的吸附试验
采用MnSO4·H2O制备40 mg/L的Mn(II)溶液,Mn(II)溶液的pH值用NaOH/HCl调至7.0左右,称取0.1 g生物铁锰氧化物于100 mL聚乙烯塑料瓶中,加入50 mL配制好的Mn(II)溶液,摇匀放置于振荡箱中30℃,170 r/min振荡,分别在5、10、15、20、30、40、60、120、240、360、480、600 min取样,样品过0.22 ?m微孔过滤膜(有机系)后取滤液,测定滤液中Mn(II)浓度(用电感耦合等离子体光谱仪测定:ICP-OES,N-8300 上海关河仪器设备有限公司)。每组样品均设置3个平行。
1.5 吸附动力学试验
分别在5、10、15、20、30、40、60、120、240 min取样,其他试验条件同1.4,计算生物铁锰氧化物对Mn(II)的吸附量,使用准一级吸附动力学模型和准二级吸附动力学模型拟合试验数据,分析生物铁锰氧化物对Mn(II)的吸附动力学特征。准一级动力学的线性方程如下。
1.6 吸附等温线
设置溶液中Mn(II)初始浓度分别为2、5、10、20、40、60、80、100 mg/L,调节溶液初始pH值为7.0左右,反应温度分别为20、30、40℃,振荡4 h(170 r/min),以0.22 ?m微孔过滤膜(有机系)过滤取滤液,测定吸附前后溶液中的Mn(II)的浓度。
1.7 pH值和投加量对Mn(II)吸附的影响
1.7.1 pH值对生物铁锰氧化物吸附Mn(II)的影响 使用0.1 mol/L NaOH或HCl依次调节悬浮液pH值为5.0、6.0、7.0、8.0和9.0,每个pH值试验均设置3组平行,其他试验条件同1.4。平衡后取出样品,测定样品的Mn(II)浓度,计算出生物铁锰氧化物对Mn(II)的吸附量。
1.7.2 投加量对生物铁锰氧化物吸附Mn(II)的影响 依次称取生物铁锰氧化物0.05、0.10、0.15、0.20、0.25 g,即投加量为1、2、3、4、5 g/L,每个投加量试验均设置3组平行样品,其他试验条件同1.4。计算生物铁锰氧化物对Mn(II)的吸附量。
试验数据采用Microsoft excel、SPSS和Origin 8.0等软件进行统计分析。
2 结果与分析
2.1 生物铁锰氧化物的理化性质表征分析
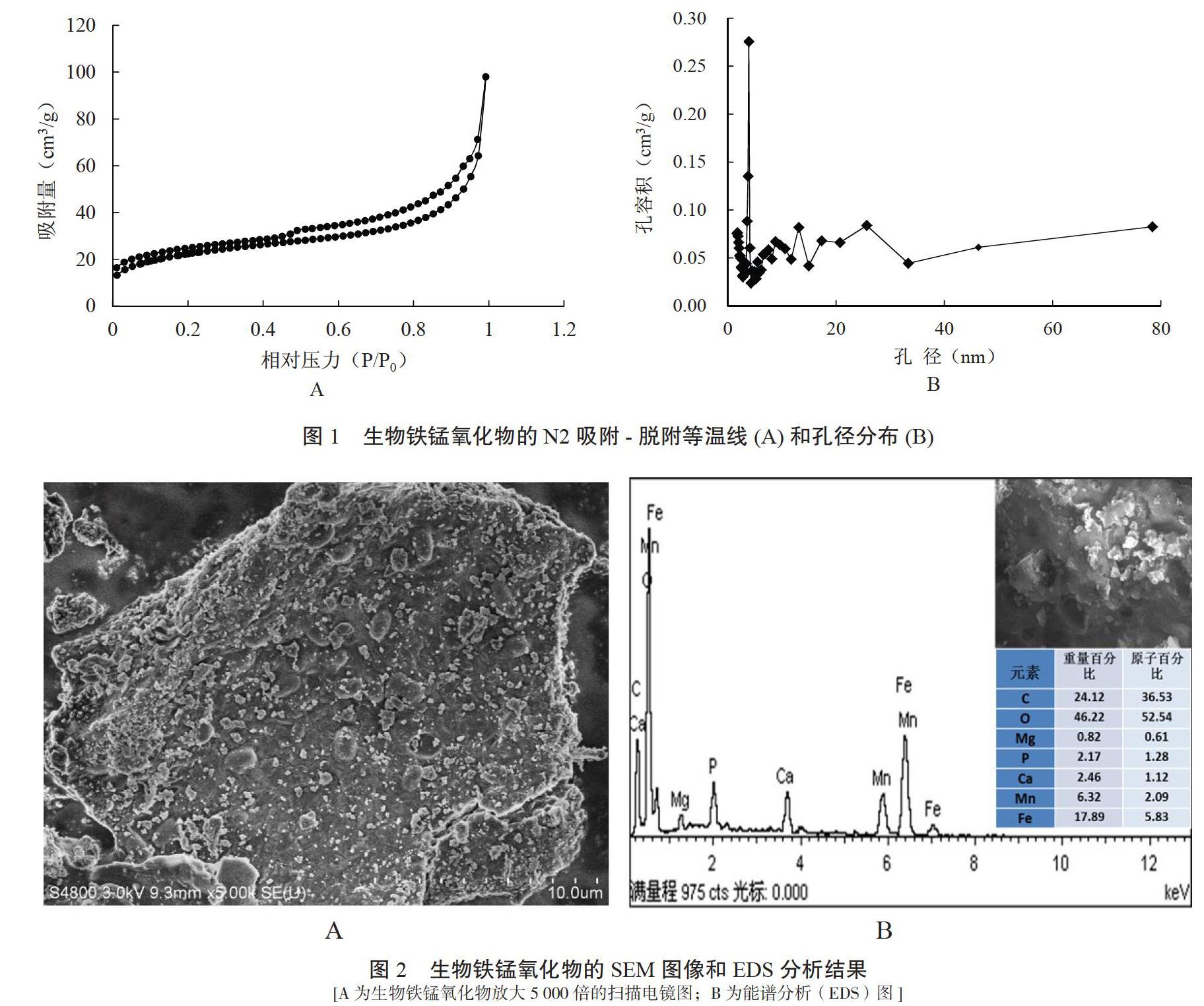
由图1可知,生物铁锰氧化物的比表面积为79.22 m2/g,孔体积为0.15 cm3/g。从图1A中可以看出,生物铁锰氧化物N2吸附等温线符合具有滞后环的IV型等温线,属于典型的介孔物质吸附曲线。样品在相对压力(P/P0)为0.5~0.9时有一个陡峭的突越,这是由于N2在孔道中毛细凝聚所致[5]。由图1B可知,生物铁锰氧化物中介孔孔径的范围为1.5~80 nm,这些介孔结构的存在有利于Mn(II)的吸附[14]。
生物铁锰氧化物的SEM-EDS如图2A所示,生物铁锰氧化物中含有大量的块状物,分布较为均匀,且附着有类似于细菌的颗粒物;通过生物铁锰氧化物的EDS分析(图2B)可以发现,产物中Fe峰最高,且C和O元素的含量较高,说明产物中除了微生物生成的铁锰氧化物之外,还有部分的微生物菌体成分存在。
由图3可知,在3 600~3 000 cm-1内所呈现的较强而且宽的吸收峰,属于—OH和—NH的混合伸缩振动[15],1 641 cm-1的吸收峰属于典型的酰胺I带(C=O,CN的伸缩振动),1 400 cm-1和1 068 cm-1的吸收峰分别归于羧基(C=O)的对称伸缩振动和C—O—C的伸缩振动[16-17]。据文献报道,—OH、C—O等基团能参与到对Mn(II)的吸附反应中,促进Mn(II)的吸附[18]。而425 cm-1的吸收峰为锰氧化物(MnO2)特征吸收峰[19]。郭峰等[20]、李圭白等[21]研究发现二氧化锰对Mn(II)具有较大的吸附能力,且会促进Mn(II)的催化氧化作用,并生成锰质活性滤膜。561 cm-1处的吸收峰在650~500 cm-1内,为铁氧化物的Fe—O特征吸收峰[22]。有研究表明Fe—O为活性官能团,容易与环境中的金属离子形成络合物,并提高对重金属的吸附能力[23]。这些特征官能团的存在说明该研究中生成的生物铁锰氧化物具备对金属离子尤其是Mn(II)的吸附潜力,可以作为潜在的吸附材料使用。
2.2 吸附动力学过程
由图4A可知,生物铁锰氧化物吸附Mn(II)在4 h时基本达到平衡,因此试验中的吸附平衡时间为4 h;吸附过程可以分为快速吸附和慢速吸附2个阶段,在60 min前生物铁锰氧化物对Mn(II)的吸附为快速吸附阶段,吸附量随时间的延长而迅速提高,在此阶段对Mn(II)的吸附达到其平衡吸附容量的74.39%;60 min后,生物铁锰氧化物对Mn(II)的吸附速率下降,吸附过程在240 min时,吸附速率放缓且趋于吸附平衡。这可能是由于生物铁锰氧化物表面的活性位点和官能团多,吸附开始时,生物铁锰氧化物表面吸附亲和力较高的官能团先被占用,因此吸附效率高;随着时间的延长,生物铁锰氧化物表面活性位点逐渐减少,有限的吸附位点逐渐饱和,同时,当重金属离子扩散到生物铁锰氧化物内部时,扩散阻力逐渐增大,扩散速度降低,使得吸附速率逐渐变得缓慢,最后基本趋于稳定。
利用准一级动力学模型和准二级动力学模型来描述生物铁锰氧化物吸附Mn(II)离子的过程,吸附动力学参数如表1所示,2种动力学模型拟合效果均较好,相关系数(R2)均大于0.9。与准一级动力学相比,生物铁锰氧化物准二级动力学模型的相关系数更大,且准二级动力学模型所得的平衡时吸附量更接近实际得到的平衡吸附量。因此,生物铁锰氧化物对Mn(II)的吸附过程更符合准二级动力学模型,这说明在生物铁锰氧化物对Mn(II)的吸附过程中起主要作用是化学吸附[24]。
2.3 等温吸附过程
图5A和图5B分别为不同温度下生物铁锰氧化物对Mn(II)吸附的Langmuir和Freundlich等温线模型线性拟合。2种吸附等温线的参数如表2所示。Freundlich等温吸附模型的R2在温度范围为20~40℃内均大于0.9,相较于Langmuir等温吸附模型高,因此,生物铁锰氧化物对Mn(II)的吸附过程更符合Freundlich等温模型,说明此吸附过程属于多分子层吸附。
从表2的结果可以看出,在温度分别为20、30、40℃下,1/n的最大值为0.934 5,均小于1,说明吸附质容易被吸附[25]。当温度超过最适温度后,吸附能力降低。得到的吸附规律与试验数据相符,进一步说明Freundlich吸附等温线符合生物铁锰氧化物吸附Mn(II)的过程。
2.4 投加量和pH值对生物铁锰氧化物吸附锰的影响
由图6A可知,最初生物铁锰氧化物对Mn(II)吸附量随投加量的增加而迅速增大,当投加量为2 g/L时,达到最大吸附量(16.05 mg/g),去除率為81.43%;之后缓慢的下降,当投加量为3~5 g/L时,吸附量稳定在15.30 mg/g左右。因此,试验中的生物铁锰氧化物的最佳投加量为2 g/L,固液比为1 g∶500 mL。
pH值是影响Mn(II)吸附效果的重要因素,它既能够影响吸附材料表面官能团的有效性,也能影响Mn(II)在水中的存在形态和化学特征,生物铁锰氧化物在pH值为5~9时对于溶液中的Mn(II)的吸附效果的影响见图6B。由图6B可知,当pH值为5时,生物铁锰氧化物对Mn(II)的吸附效果较差,吸附量仅为11.49 mg/g;随着pH值的增加,生物铁锰氧化物对于Mn(II)的吸附量随之增加,当pH值达到7时,吸附量达到最大,为16.43 mg/g,去除率也达到最大(82.16%);而当pH值>7时,吸附量出现下降,由最大吸附量16.43 mg/g下降至15.23(pH值=8)和13.49(pH值=9)mg/g;说明pH值=7时,生物铁锰氧化物对Mn(II)的吸附效果最好。
当水中的pH值较低时,溶液中的H+含量较高,溶液中存在着阳离子竞争作用,这种竞争作用会减少生物铁锰氧化物表面的金属吸附位点,导致吸附量较低。同时pH值较低的环境会使吸附剂表面质子化,使得生物铁锰氧化物表面的—OH、C=O等官能团带正电,与水体中的Mn(II)产生排斥力,从而不利于生物铁锰氧化物对Mn(II)的吸附[26]。随着溶液pH值的上升,生物铁锰氧化物表面逐渐带有负电荷,生物铁锰氧化物吸附金属离子主要为静电力的作用,同时,由于pH值的升高,OH-含量变大,可与生物铁锰氧化物上面的H+结合,导致H+竞争力的下降,使生物铁锰氧化物上有更多的位点可供金属离子吸附[27]。当pH值大于7,可能由于溶液中的锰离子形成不溶性的Mn(OH)2,占据了吸附剂表面的吸附位点,使锰的吸附量降低,且碱性环境也可能影响吸附剂的电离度及表面特性,导致对锰的吸附降低[28]。
3 结 论
生物铁锰氧化物的比表面积为79.22 m2/g,孔体积为0.15 cm3/g,存在着孔径1.5~80.0 nm的介孔结构。生物铁锰氧化物表面含有大量的含铁锰颗粒,同时伴随有微生物菌体带来的细胞类物质。
生物铁锰氧化物对Mn(II)吸附过程更符合准二级动力学模型和Freundlich吸附等温模型,说明吸附过程主要由化学反应控制,属于多分子层吸附;当pH值=7.0、投加量为2 g/L、固液比为1 g∶500 mL时,生物铁锰氧化物对Mn(II)的吸附效果最好,吸附量为16.43 mg/g。
参考文献:
[1] Papina T S,Eirikh A N,Serykh T G,et al. Space and time regularities in the distribution of dissolved and suspended manganese forms in Novosibirsk Reservoir water[J]. Water Resources,2017,44(2):276-283.
[2] Doula M K. Removal of Mn2+ ions from drinking water by using Clinoptilolite and a Clinoptilolite–Fe oxide system[J]. Water Research,2006,40(17):3167-3176.
[3] Etale A,Tutu H,Drake D C. Application of maghemite nanoparticles as sorbents for the removal of Cu(II), Mn(II) and U(VI) ions from aqueous solution in acid mine drainage conditions[J]. Applied Water Science,2016,6(2):187-197.
[4] Khobragade M U,Pal A. Adsorptive removal of Mn(II) from water and wastewater by surfactant-modified alumina[J]. Desalination and Water Treatment,2016,57(6):2775-2786.
[5] 常 军,贾福康,胡成山,等. 电解锰渣基沸石对锰离子的吸附性能研究[J]. 无机盐工业,2019,51(9):61-66.
[6] 李金成. 负载锰氧化物滤料对高锰地下水处理技术研究[D]. 青岛:中国海洋大学,2011.
[7] Bai Y H,Yang T T,Liang J S,et al. The role of biogenic Fe-Mn oxides formed in situ for arsenic oxidation and adsorption in aquatic ecosystems[J]. Water Research,2016,98:119-127.
[8] Spiro T G,Bargar J R,Sposito G,et al. Bacteriogenic manganese oxides[J]. Accounts of Chemical Research,2010,43(1):2-9.
[9] Bai Y H,Jefferson W A,Liang J S,et al. Antimony oxidation and adsorption by in situ formed biogenic Mn oxide and Fe–Mn oxides[J]. Journal of Environmental Sciences-china,2017,54(4):126-134.
[10] Wang H W,Lv Z, Song Y,et al. Adsorptive removal of Sb(III) from wastewater by environmentally-friendly biogenic manganese oxide (BMO) materials:Efficiency and mechanisms[J]. Process Safety and Environmental Protection,2019,124:223-230.
[11] 宋嬌艳,袁 林,杨志丹,等. 铁锰复合氧化物对铅离子的吸附特征及影响因素研究[J]. 西南大学学报(自然科学版),2014(7):135-142.
[12] 傅金祥,冯 青,周东旭,等. 原水铁锰含量对细菌除铁除锰效能的影响[J]. 供水技术,2008,2(5):22-24.
[13] 姚 远,周志华,许旭萍,等. 铁锰氧化菌的筛选及其生物学特性研究[J]. 福建师范大学学报(自然科学版),2009,25(4):100-104.
[14] Gupta V K,Ganjali M R,Nayak A,et al. Enhanced heavy metals removal and recovery by mesoporous adsorbent prepared from waste rubber tire[J]. Chemical Engineering Journal,2012,197:330-342.
[15] Zhao J H,Liu J,Li N,et al. Highly efficient removal of bivalent heavy metals from aqueous systems by magnetic porous Fe3O4-MnO2:Adsorption behavior and process study[J]. Chemical Engineering Journal,2016,304:737-746.
[16] Schmitt J,Flemming H. FTIR-spectroscopy in microbial and material analysis[J]. International Biodeterioration & Biodegradation,1998,41(1):1-11.
[17] Zhu L,Qi H Y,Lv M L,et al. Component analysis of extracellular polymeric substances(EPS)during aerobic sludge granulation using FTIR and 3D-EEM technologies[J]. Bioresource Technology,2012,124:455-459.
[18] 徐雅迪. 柠檬酸改性酵母吸附剂对锰的吸附性能研究[D]. 武汉:华中科技大学,2016.
[19] Lu J B,Liu H J,Zhao X,et al. Phosphate removal from water using freshly formed Fe-Mn binary oxide: Adsorption behaviors and mechanisms[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects,2014,455(1):11-18.
[20] 郭 峰,李 星,杨艳玲,等. 滤料特性对锰砂滤池启动期除铁除锰效能的影响[J]. 中国给水排水,2018,34(7):16-20, 25.
[21] 李圭白,梁 恒,余华荣,等. 锰质活性滤膜化学催化氧化除锰机理研究[J]. 给水排水, 2019, 45(5):6-10, 75.
[22] 何皎洁. MnO2/Fe3O4复合吸附剂的制备及吸附水中铅、铜的研究[D]. 哈尔滨:哈尔滨工业大学,2011.
[23] 林丽娜,黄 青,刘仲齐,等. 生物炭-铁锰氧化物复合材料制备及去除水体砷(Ⅲ)的性能研究[J]. 农业资源与环境学报, 2017,34(2):182-188.
[24] 王彤彤,马江波,曲 东,等. 两种木材生物炭对铜离子的吸附特性及其机制[J]. 环境科学,2017,38(5):2161-2171.
[25] Alizadeh B,Ghorbani M,Salehi M A. Application of polyrhodanine modified multi-walled carbon nanotubes for high efficiency removal of Pb(II) from aqueous solution[J]. Journal of Molecular Liquids,2016,220(220):142-149.
[26] Kadirvelu K,Kavipriya M,Karthika C,et al. Mercury (II) adsorption by activated carbon made from sago waste[J]. Carbon,2004, 42(4):745-752.
[27] 付 軍,范 芳,李海宁,等. 铁锰复合氧化物/壳聚糖珠: 一种环境友好型除磷吸附剂[J]. 环境科学,2016,37(12):4882-4890.
[28] Idris S A M. Adsorption, kinetic and thermodynamic studies for manganese extraction from aqueous medium using mesoporous silica[J]. Journal of Colloid and Interface Science,2015,440:84-90.
(责任编辑:张焕裕)
