鸡蛋中硝基咪唑类药物及其代谢物残留风险筛查
2020-09-30梁飞燕辛丽娜林小莹
梁飞燕,辛丽娜*,林小莹
广西-东盟食品检验检测中心(南宁 530021)
硝基咪唑类药物是一类具有5-硝基咪唑环结构的化合物,其作用机制主要是破坏细菌细胞胞浆中的硝基还原酶,从而干扰细菌DNA代谢过程,引起细菌DNA螺旋链的损伤、断裂、解旋,进而导致细菌死亡。硝基咪唑类主要用于抗滴虫、抗阿米巴原虫和抗厌氧菌感染,对禽类弧菌性肝炎、禽类毛滴虫病、大肠杆菌和沙门氏菌感染等有良好疗效。但该类药物具有细胞诱变性、动物致癌毒性[1],其代谢物与原药具有相似的潜在毒性[2],故欧盟、美国、日本等已规定甲硝唑、地美硝唑禁用于食品动物。我国农业部第235号公告对甲硝唑、地美硝唑做出规定:允许在食品动物中使用,但是不得在动物食品中检出。
目前,对于动物性食品中硝基咪唑类药物残留的检测方法,我国目前现行的标准有GB/T 21318—2007《动物源性食品中硝基咪唑残留量检验方法》、SN/T 1928—2007《进出口动物源性食品中硝基咪唑残留量检测方法液相色谱-质谱质谱法》、农业部1025号公告-2-2008《动物性食品中甲硝唑、地美硝唑及其代谢物残留检测液相色谱-串联质谱法》、农业部1025号公告-22-2008《动物源食品中4种硝基咪唑残留检测液相色谱-串联质谱法》等,但这些标准只适用于禽畜肉及其内脏、水产品、蜂蜜、乳及乳制品,对于禽蛋中硝基咪唑类药物残留,缺乏相应的国家标准,导致监管部门在执行禽蛋质量安全监管中无理可据,给监管带来了一定困难。
大多数硝基咪唑类药物半衰期长,在体内吸收迅速而且完全并能保持有效浓度,蛋白结合率低,在体液和组织中分布广泛[3],对治疗鸡生殖系统疾病及一些传染病引起的生殖系统验证效果好,若不遵守兽药休药期规定,在蛋鸡产蛋期使用此类兽药,可能会导致硝基咪唑类药物在鸡蛋中的残留。考察和掌握鸡蛋中硝基咪唑类药物及代谢物的残留情况,对建立健全我国标准体系提供技术支持,为监管部门提供监管依据,对保障公众的饮食安全和公共卫生安全都具有重要的意义。为此,通过建立液相色谱-串联质谱法,对鸡蛋中硝基咪唑类药物及代谢物展开风险监测筛查。
1 材料与方法
1.1 仪器与设备
QTRAP4500三重四极杆液质联用仪(美国AB公司),配30A高效液相色谱仪(日本岛津公司);PGC753e型电子天平,艾德姆衡器(武汉)有限公司;Multi Reax型全自动振荡器,Heidolph公司;X3R型高速冷冻离心机,Thermo公司;Genius NM32LA型氮气发生器,PEAK公司;ATR Autovap S60型多样品自动浓缩仪,力德生物科技(上海)有限公司;Milli-Q Advantage A10超纯水机,德国Millipore公司;PRime HLB固相萃取小柱(6 mL,500 mg),美国Waters公司;MCX阳离子交换柱(6 mL,150 mg),美国Waters公司。
1.2 试剂
甲硝唑标准品,中国食品药品检定研究院;地美硝唑(二甲硝咪唑)标准品,Bepure公司;洛硝哒唑(罗硝唑)标准品,Dr. Ehrenstorfer公司;2-甲硝咪唑标准品,CATO公司;异丙硝唑标准品,Dr. Ehrenstorfer公司;4-硝基咪唑标准品,Dr. Ehrenstorfer公司;苯硝咪唑标准品,WiTEGA公司;羟基甲硝唑(甲硝唑代谢物)标准品,Bepure公司;羟甲基甲硝咪唑(洛硝哒唑、2-甲硝咪唑代谢物)标准品,WiTEGA公司;乙酸铵,色谱纯,美国Tedia公司;甲酸,分析纯,广东省化学试剂工程技术研究开发中心;水,超纯水。
1.3 试验方法
1.3.1 样品处理
取约2.50 g(精确到0.01 g)均质后的鸡蛋于50 mL聚酯离心管中,加入90%乙腈水溶液至10.0 mL,涡旋振荡10 min,在1 000 r/min条件下冷冻离心5 min。取上层提取液置于Oasis PRiME HLB固相小柱(500 mg,6 mL,无需活化)内,以1 s/滴的速度过柱,收集4.0 mL流出液,于40 ℃氮气吹干至小于0.5 mL,用10%乙腈水溶液定容至1.0 mL,涡旋溶解2 min,以10 000 r/min离心5 min,取上清液,经0.22 μm滤膜过滤后待测。
1.3.2 标准储备溶液的配制
分别准确称取10.0 mg 9种标准品于10 mL容量瓶中,用乙腈溶解并定容至刻度,制成1 mg/mL的单标储备溶液。分别吸取0.1 mL至同一100 mL容量瓶中,用乙腈稀释至刻度,制成1 μg/mL的混合标准溶液。
1.3.3 基质标准曲线的配制
称取2.50 g鸡蛋样品空白基质,分别加入混合标准溶液,按1.3.1方法处理样品,制得质量浓度分别为0.5,1,5,10,20和50 ng/mL的基质混合标准工作溶液,以浓度为横坐标,相应定量离子的色谱峰面积为纵坐标,绘制标准曲线。
1.4 仪器条件
1.4.1 色谱条件
色谱柱为CAPCELL PAK C18MGⅢ-H(3 μm,2.0 mm×100 mm),流动相A为0.1%甲酸水,流动相B为乙腈,梯度洗脱程序见表1。流速0.3 mL/min,进样量20 μL,柱温35 ℃。

表1 梯度洗脱程序
1.4.2 质谱条件
电喷雾离子源(ESI),多反应监测(MRM);正离子扫描模式。电喷雾电压(IS)5 500 V;离子源温度(TEM)550 ℃;气帘气(CUR)流速35 L/min;雾化气(GS1)流速55 L/min;辅助加热气(GS2)流速55 L/min;射入电压(EP)10 V。

表2 9种组分的质谱参数
2 结果与讨论
2.1 条件的优化
2.1.1 仪器条件的优化
因C18色谱柱比C8柱具有更强的保留性,故考察了4种不同厂家的C18色谱柱CAPCELL PAK C18MGⅢ-H(3 μm,2.0 mm×100 mm)、Waters ACQUITY UPLC® BEH C18(1.7 μm,2.0 mm×150 mm)、Agilent ZORBAX Eclipse Plus C18(1.8 μm,2.1 mm×150 mm)、Phenomenex Kinetex XB-C18(1.7 μm,2.1 mm×100 mm)对9种待测组分的分离效果和柱效[4-5]。结果发现:CAPCELL PAK C18MGⅢ-H(3 μm,2.0 mm×100 mm)对9种待测组分的分离度和峰形更好,且分辨率高,因此选用该色谱柱进行测定。
分别采用甲醇-水、乙腈-水、乙腈-0.1%甲酸水、乙腈-5 mmol/L乙酸铵水溶液等多种流动相进行考察。采用乙腈-0.1%甲酸水溶液时待测组分离子质谱的分离度和响应值最高[6-9]。所以采用多反应监测模式正离子进行测定,通过调节质谱的电喷雾电压(IS)、离子源温度(TEM)、气帘气(CUR)等参数,采用响应最强和次强的子离子分别作为定量离子和定性离子。通过梯度洗脱改变流动相的比例,使9种待测组分达到完全分离,保留时间重现性好,灵敏度高,见图1。

图1 仪器条件优化效果图
2.1.2 前处理条件的优化
鸡蛋的主要成分是蛋白质和脂肪,乙腈具有沉淀蛋白的作用。试验发现:90%的乙腈更利于硝基咪唑类药物的提取,回收率较高且峰形较好,故采用90%乙腈作为提取溶剂。
PRIME HLB固相小柱填料为水可浸润性的亲水亲脂平衡共聚物,使用前无需活化和平衡,对各种蛋白、磷脂、盐等基质干扰物具有吸附保留作用。试验比较了Waters HLB固相小柱、MCX阳离子交换固相萃取小柱和PRIME HLB固相小柱的提取效果[10-13],结果发现:Waters HLB固相小柱过柱时易造成柱子堵塞,回收率低且平行性差;MCX阳离子交换固相萃取小柱由于净化不完全,造成基质效应大而导致回收率偏低;PRIME HLB固相小柱净化效果好,净化过程简单、快速,提取回收率高,见图2,故采用PRIME HLB固相小柱进行净化。
2.2 方法学验证
2.2.1 线性范围、检出限和定量限
按试验方法配制系列基质标准曲线,采用选定的仪器条件进行检测,以待测组分定量离子浓度为横坐标、相应峰面积为纵坐标,绘制工作曲线。结果显示,9种组分在0.5~50 μg/mL范围内与峰面积呈良好的线性关系,相关系数为0.996 1~0.999 0。在鸡蛋基质空白中添加适当浓度的标准溶液,以定量离子按信噪比S/N=3、S/N=10分别计算检出限和定量限,9种组分的检出限为0.001 6~0.020 μg/kg,定量限为0.005 3~0.067 μg/kg,结果见表3。

图2 使用PRiME HLB净化效果离子流图
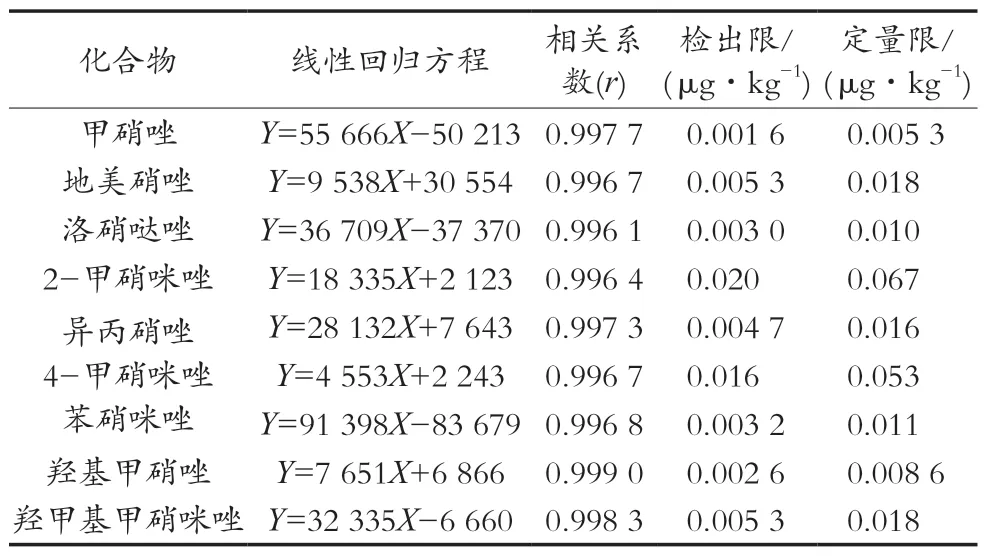
表3 鸡蛋中9种组分的线性方程、相关系数及检出限、定量限
2.2.2 回收率和精密度
在鸡蛋空白基质中添加低、中、高3个不同浓度水平的标准溶液,按试验方法制备样品并上机测定,每个浓度水平各3份,测定回收率和精密度。结果显示,低、中、高3个浓度水平的回收率为86.0%~109.41%,RSD为0.41%~5.60%,均符合国家标准相关要求,结果见表4。

表4 鸡蛋中9种组分加标回收率及精密度(n=3)
2.3 实际样品的检测
为了对鸡蛋中硝基咪唑类药物及代谢物进行风险筛查,在农贸市场、超市等流通领域共采样82批次,采用了此次试验建立的方法进行检测,检测结果见表5。4批次样本检出硝基咪唑类药物,检出率为4.88%,检出组分为甲硝唑、地美硝唑、羟基甲硝唑、羟甲基甲硝咪唑,检出甲硝唑、地美硝唑的样品均检出其相应代谢物羟基甲硝唑、羟甲基甲硝咪唑。

表5 样品测定结果
3 结论与讨论
动物源性食品中兽药残留风险评估主要是采用食品安全指数来进行评价的[14],食品安全指数为每日膳食暴露量与某药物的每日允许摄入量(ADI)的比值。其中,每日允许摄入量(ADI)是保障兽药不对人体健康造成潜在危害的“临界值”,是评判兽药安全性的根本标准。每日允许摄入量(ADI)值的设置,是通过一系列严格且复杂的毒理学、药理学或微生物学安全性评价程序而得到的。动物源性食品中兽药最高残留量(MRL)的设置也是通过对药物的化学性质、代谢、残留实验数据分析,饮食暴露评估等确定的。甲硝唑、地美硝唑因没有足够数据或缺乏相关数据来确定食品中该药物或其代谢物的残留安全水平,但是相关健康问题已成为严重关注问题,因此大部分国家对此类药物在食品中的残留,规定不得在食品动物上使用该类药物或不得在动物食品中检出。我国农业部第235号公告规定甲硝唑、地美硝唑允许作治疗用,但不得在动物性食品中检出;农业部第193号公告亦规定了硝基咪唑类:甲硝唑、地美硝唑及其盐、酯及制剂禁止以促生长的目的用于所有食品动物。硝基咪唑类药物在动物食品中残留给人体带来的健康风险已得到了有关部门的关注和重视。
对于鸡蛋中硝基咪唑类药物残留的检测,我国缺乏配套的标准方法。为此次鸡蛋中硝基咪唑类药物及其代谢物的风险筛查,建立了硝基咪唑类药物及代谢物的检测方法,该方法简单快速、灵敏、准确,可用于禽蛋中兽药残留的大批量筛查,为食品安全监管部门提供技术支持,对鸡蛋中硝基咪唑类药物及代谢物检测标准的研究和制定提供一定的参考作用。硝基咪唑类药物主要用于禽类感染性疾病,并具有促生长作用,此类药物在鸡蛋中的残留,可能是养殖户超剂量使用或不遵守休药期规定而导致的。通过对鸡蛋中硝基咪唑类药物及代谢物的残留风险筛查和分析,了解和掌握鸡蛋中硝基咪唑类药物残留的现状和原因,为农业部门指导兽药的科学、合理、安全使用提供依据,为食品安全监管部门对鸡蛋中兽药残留的监管提供新思路,在一定程度上有利于提高鸡蛋质量安全。
