利用表面增强拉曼光谱(SERS)技术快速检测水与尿液中舒芬太尼的研究
2020-09-29陈志杰马小卫陈薪璇韩斯琴高娃2哈斯乌力吉
陈志杰,马小卫,陈薪璇,韩斯琴高娃2,*,哈斯乌力吉
(1.二四二医院 眼科,黑龙江 哈尔滨 150066;2.内蒙古民族大学附属医院,内蒙古 通辽 028007;3.哈尔滨工业大学 可调谐(气体)激光技术国家级重点实验室,黑龙江 哈尔滨 150080)
舒芬太尼(C22H30N2O2SC6H8O7)属于阿片类药物,是目前临床手术中最常用的麻醉药品[1],其镇痛活性是芬太尼的9.3倍,吗啡的2 304倍。但舒芬太尼会导致典型的阿片类药物症状,过量使用会引起如呼吸抑制、心搏停止等副作用,并且会使患者产生药物依赖,甚至引发死亡[2]。2019年4月1日,公安部、国家卫生健康委员会、国家药品监督管理局联合发布了《关于将芬太尼类物质列入非药用类麻醉药品和精神药品管制品种增补目录的公告》。因此快速、准确地检测芬太尼类药物,对管制药品的监督和管理具有重要意义。
目前对舒芬太尼的检测方法主要有高效液相色谱法(HPLC)、气相色谱-质谱联用法(GC-MS)、液相色谱-质谱联用法(LC-MS)[3-5]等。虽然这些方法都具有很高的灵敏度,但是样品预处理步骤繁琐,仪器设备体积较大、价格昂贵,不利于现场快速检测。因此建立一种快速、高效、简便的鉴定方法具有一定的意义。
随着纳米技术的发展,以金或银等贵金属纳米颗粒作为基底的表面增强拉曼散射(SERS)技术将检测灵敏度提高了数百万倍,很好地克服了传统拉曼光谱信号微弱的缺陷,被广泛应用于药物分析[6-8]和食品安全[9-11]等领域。目前,虽然已有采用SERS对舒芬太尼进行定性分析[12]及对血浆中舒芬太尼进行检测的报道[13],但未见采用该技术对水和尿液中的舒芬太尼进行检测的研究。由于吸毒者一般将舒芬太尼稀释后使用,且通过吸毒者的尿液可检测该类药物,因此对水和尿液中舒芬太尼的检测具有一定意义。
1 实验部分
1.1 仪器与试剂
使用BWS415-785H型便携式拉曼光谱仪采集拉曼光谱,其激发光源为785 nm,光谱测量范围为68~2 700 cm-1,光谱分辨率小于3 cm-1,激光功率为80 mW,积分时间为5 s。使用日本日立公司的SU8010扫描电子显微镜获得银溶胶的扫描电镜图(SEM)。
硝酸银(AgNO3)、柠檬酸钠(C6H5Na3O7)(国药集团化学试剂有限公司);抗坏血酸(C6H8O6,阿法埃莎(中国)化学有限公司);枸橼酸舒芬太尼注射液(1 mL/50 μg/支,宜昌人福药业公司)。人工尿液(创峰自动化科技有限公司)。
1.2 样品的制备
舒芬太尼水溶液的制备:先用枸橼酸舒芬太尼注射液配制质量浓度为10 μg/mL的标准水溶液,然后用去离子水稀释成2、1、0.5、0.1、0.05、0.01 μg/mL梯度质量浓度的舒芬太尼水溶液。
舒芬太尼尿液样品的制备:参照Han等[14]的方法对尿液进行前处理,具体步骤如下:将一定浓度的枸橼酸舒芬太尼水溶液与人工尿液按体积比1∶9进行混合,得到质量浓度分别为2、1、0.5、0.25、0.1 μg/mL的尿液样品。取80 μL该样品添加到1.5 mL的EP管中,加入同体积10 g/L的NaOH溶液将pH值调至11.0。随后加入固体NaCl,使溶液充分饱和,最后加入80 μL环己烷萃取。充分混合后静置1 min,取上层清液作为待测样品。
1.3 银溶胶的制备
参考Qin等[15]的方法制备银溶胶,制备步骤为:首先配制250 mL含6.0×10-4mol/L抗坏血酸和3.0×10-3mol/L柠檬酸钠水溶液,将混合溶液缓慢搅拌,水浴加热至30 ℃,快速加入2.5 mL 0.1 mol/L AgNO3,并在900 r/min转速下反应15 min。然后加热至100 ℃并煮沸2 h。将制备好的银溶胶冷却至室温,于4 ℃下避光储存。
2 结果与讨论
2.1 银溶胶的表征
图1A为银溶胶的SEM图,可以看出,银溶胶形状近似球形,且分散性良好,平均直径约56 nm,其粒径分布图见图1B。
2.2 舒芬太尼拉曼特征峰的归属
利用Gaussian 09W软件包含的DFT理论[16],使用混合密度泛函B3LYP方法对舒芬太尼的分子结构进行优化,并计算理论拉曼光谱。同时,测定了6 μg/mL舒芬太尼水溶液的SERS光谱,结果如图2所示。可以看出,与理论计算相比,实际测得的特征峰位置发生了微小的频移,但基本可以一一对应。这是由于实验过程中舒芬太尼分子在银溶胶表面发生了化学吸附[17]所致。舒芬太尼的特征峰峰位归属见表1。

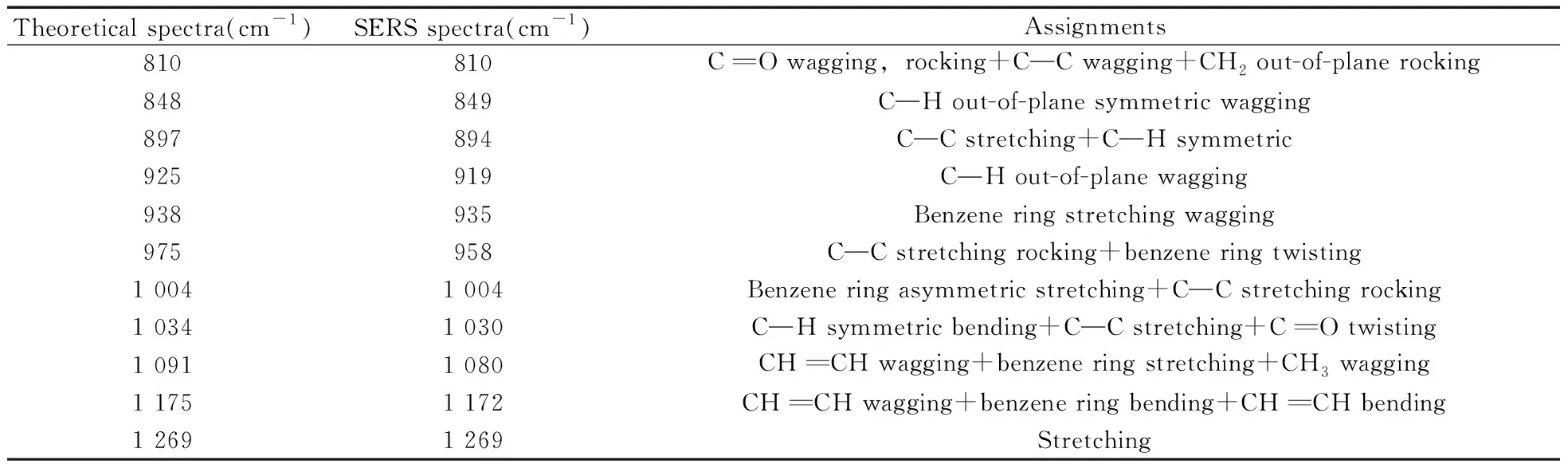
表1 舒芬太尼理论和实验振动频率Table 1 Theoretical and experimental vibration frequencies of sufentanil
2.3 SERS增强因子的计算
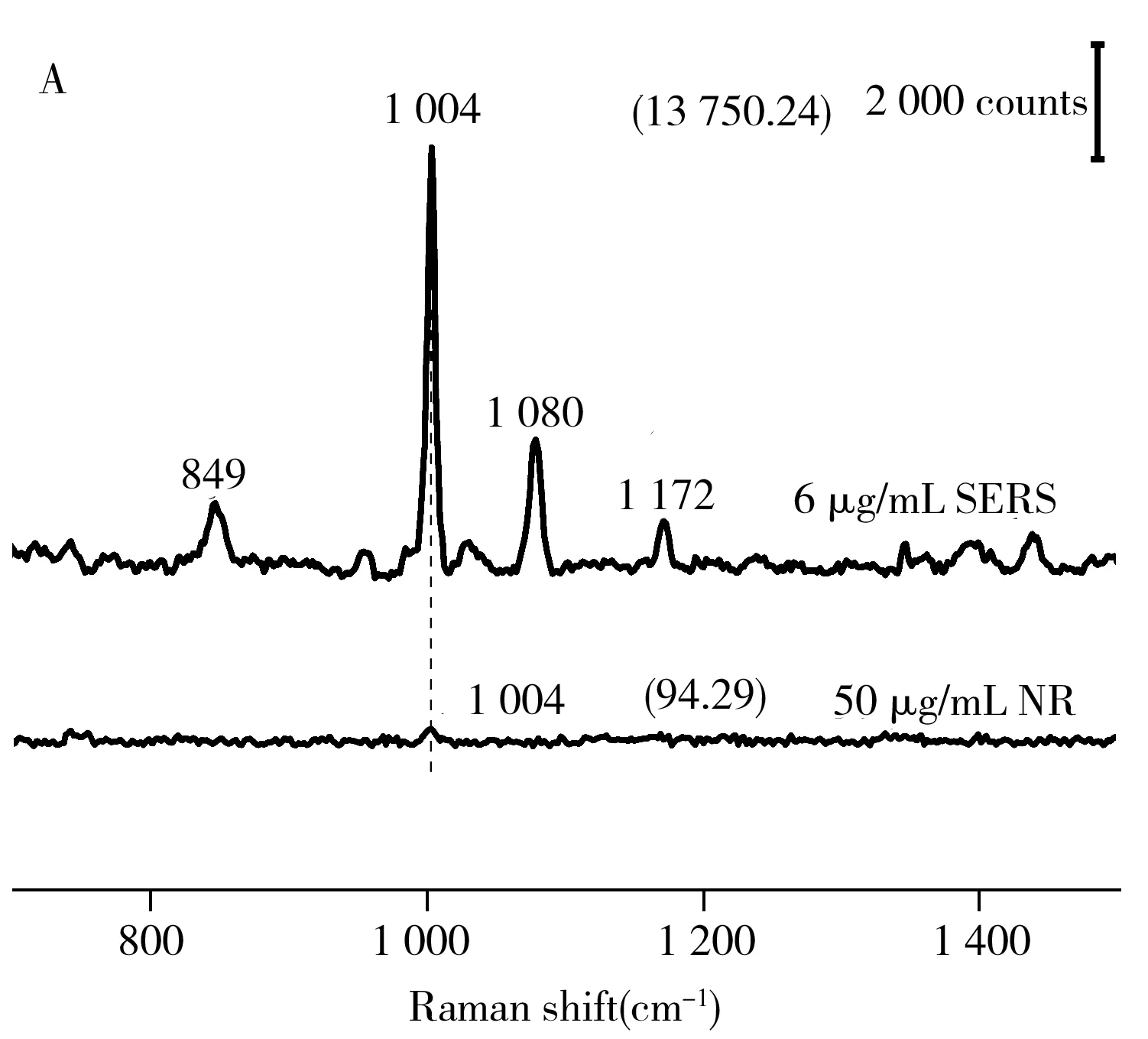
为了确定银溶胶的增强效果,测量了6 μg/mL舒芬太尼水溶液的SERS光谱和50 μg/mL舒芬太尼水溶液的常规拉曼光谱,结果见图3A,并根据公式(1)计算增强因子AEF[18]:
(1)
式中,ISERS和Inormal分别为SERS光谱与常规拉曼光谱的特征峰强度,CSERS和Cnormal分别为SERS光谱与常规拉曼光谱检测时的样品浓度。
根据式(1)得出增强因子为1.215×103,表明银溶胶对舒芬太尼有很好的放大作用,可对低浓度的舒芬太尼进行检测。另外,为了排除银溶胶自身拉曼信号对样品特征峰的影响,对银溶胶的拉曼信号进行了检测。从图3B可看出,银溶胶本身无明显拉曼信号,不会影响样品的检测。
2.4 促凝剂的选取
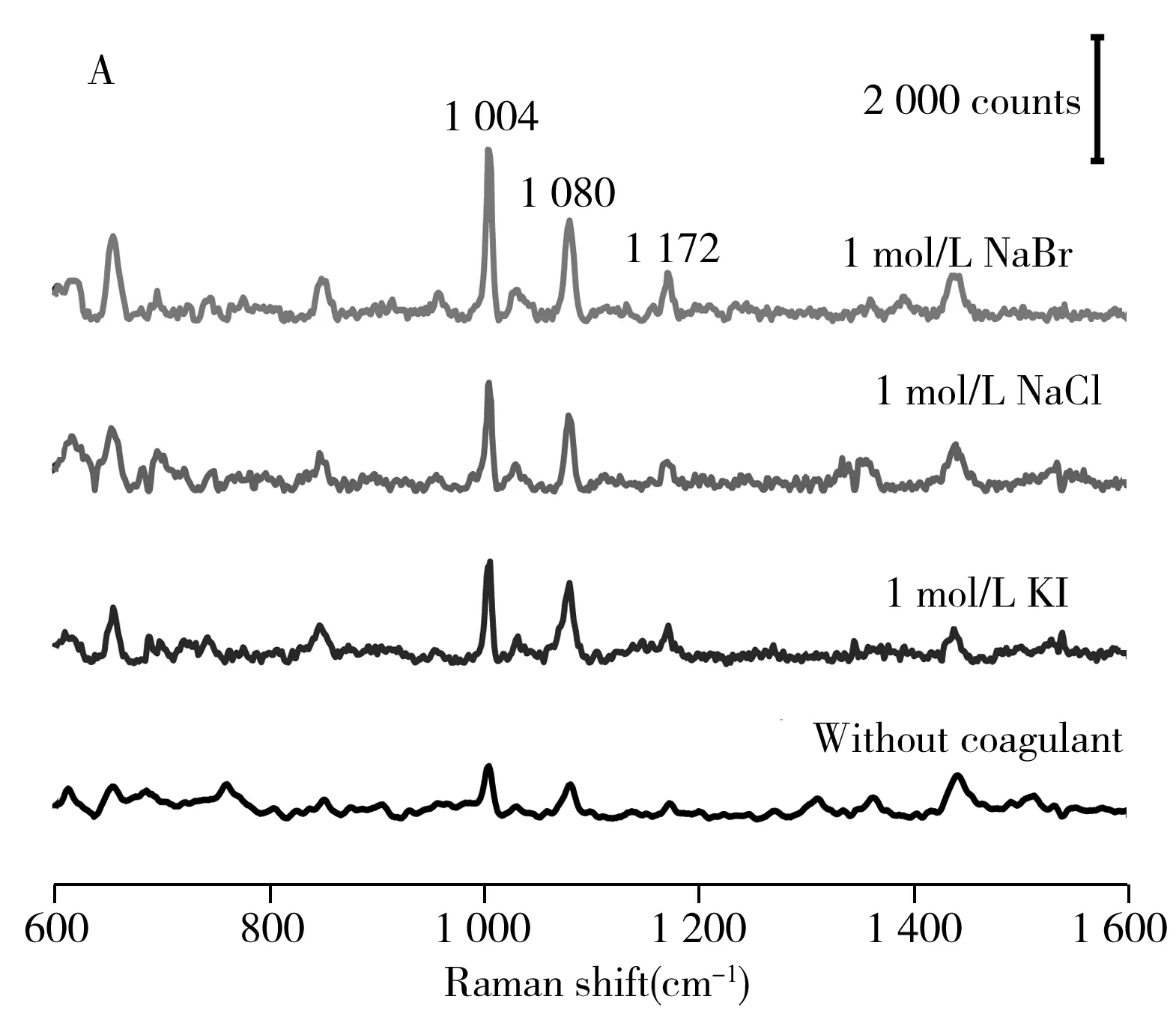
相关研究显示,卤素离子可提高银溶胶的增强效果。这是因为,向银溶胶中加入卤素离子时,由于卤素离子在银纳米颗粒表面的吸附能力大于柠檬酸根,且可与Ag形成化学键,因此将置换掉银纳米颗粒表面的柠檬酸根,从而破坏溶胶体系的电势平衡,使得溶胶颗粒聚集,金属溶胶的增强效果得以显著改善[19-22]。
本文选取NaBr、NaCl和KI 3种无机盐的水溶液作为促凝剂进行对比研究,结果如图4A所示。从图可看出,加入促凝剂之后,银溶胶的增强作用有了明显提高。在相同浓度(1 mol/L)下,上述3种促凝剂中NaBr溶液的增强效果最好,这可能是由I-、Cl-和Br-3种离子的吸附特性不同导致的。适量的无机盐可起到良好的增强作用,但过量则会导致银溶胶颗粒过度聚集,对增强效果不利[12]。如图4B所示,当NaBr溶液的质量浓度分别为0.051 5、0.103 0、0.154 5、0.206 0 g/mL时,位于1 004 cm-1处特征峰的相对强度分别为2 097.98、2 247.97、4 031.07、2 606.18 a.u.,即0.154 5 g/mL NaBr溶液的增强效果最好。
另外,本文还对比研究了样品、银溶胶和促凝剂的体积混合比对SERS增强效果的影响。结果显示,当样品、银溶胶和促凝剂的体积混合比为3∶5∶2时,SERS增强效果最好。
因此本实验中选用0.154 5 g/mL的NaBr水溶液作为促凝剂,且每次检测时样品、银溶胶和促凝剂的体积比均为3∶5∶2(当舒芬太尼水溶液的质量浓度分别为0.01、0.1、0.5、1、2 μg/mL时,样品、银溶胶和促凝剂物质的量之比分别约为1∶63∶38 659、1∶6.3∶3 866、1∶1.26∶773、1∶0.63∶386和1∶0.315∶193)。使3种液体充分混合后进行SERS检测。
2.5 重复性测定
为了研究方法的重复性,在相同实验条件下对舒芬太尼水溶液进行15次重复测定,结果如图5所示,计算得到舒芬太尼水溶液位于1 004、1 080 cm-1处拉曼特征峰强度的相对标准偏差(RSD)分别为2.5%和2.7%,表明利用SERS技术检测舒芬太尼具有很好的重复性。
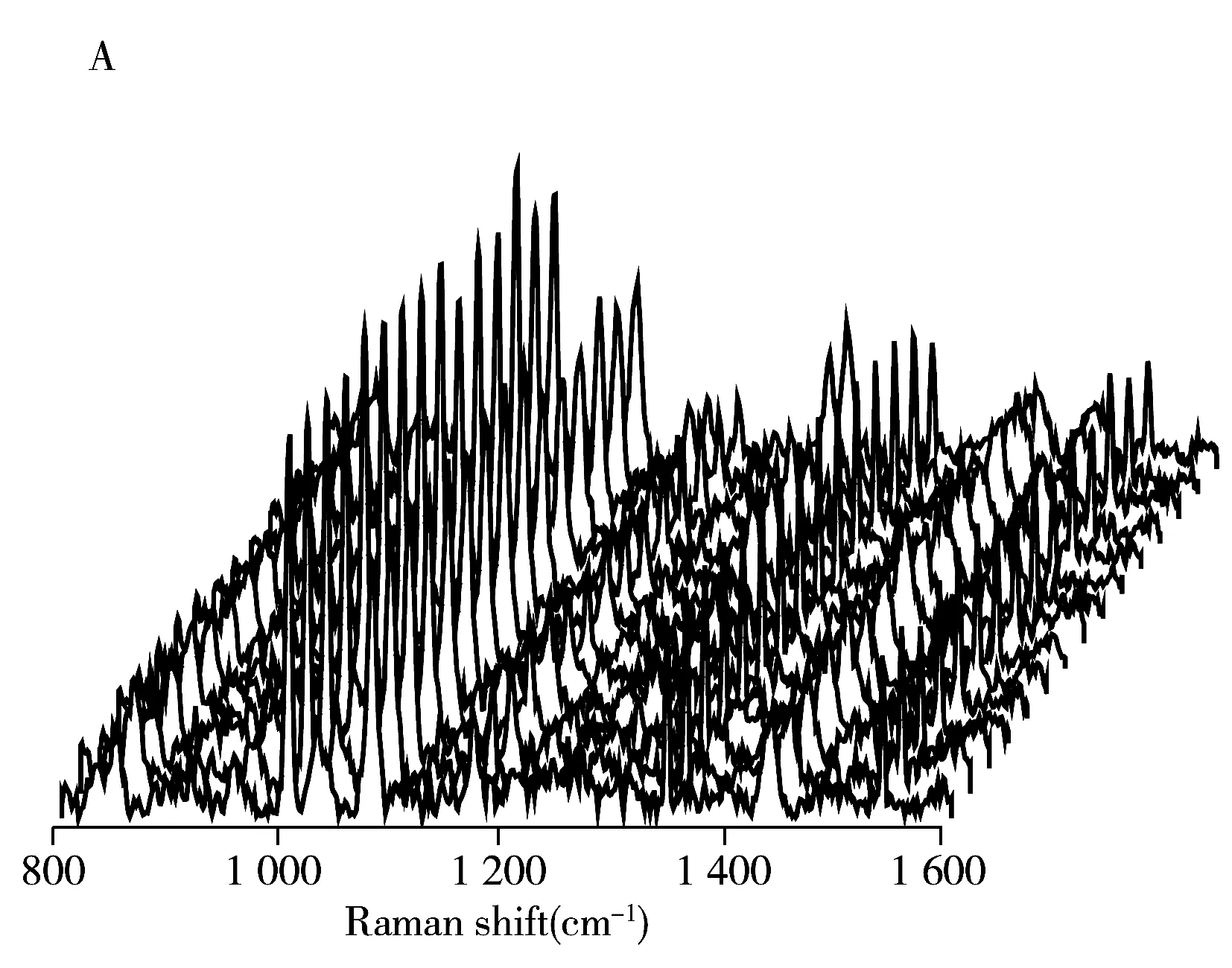
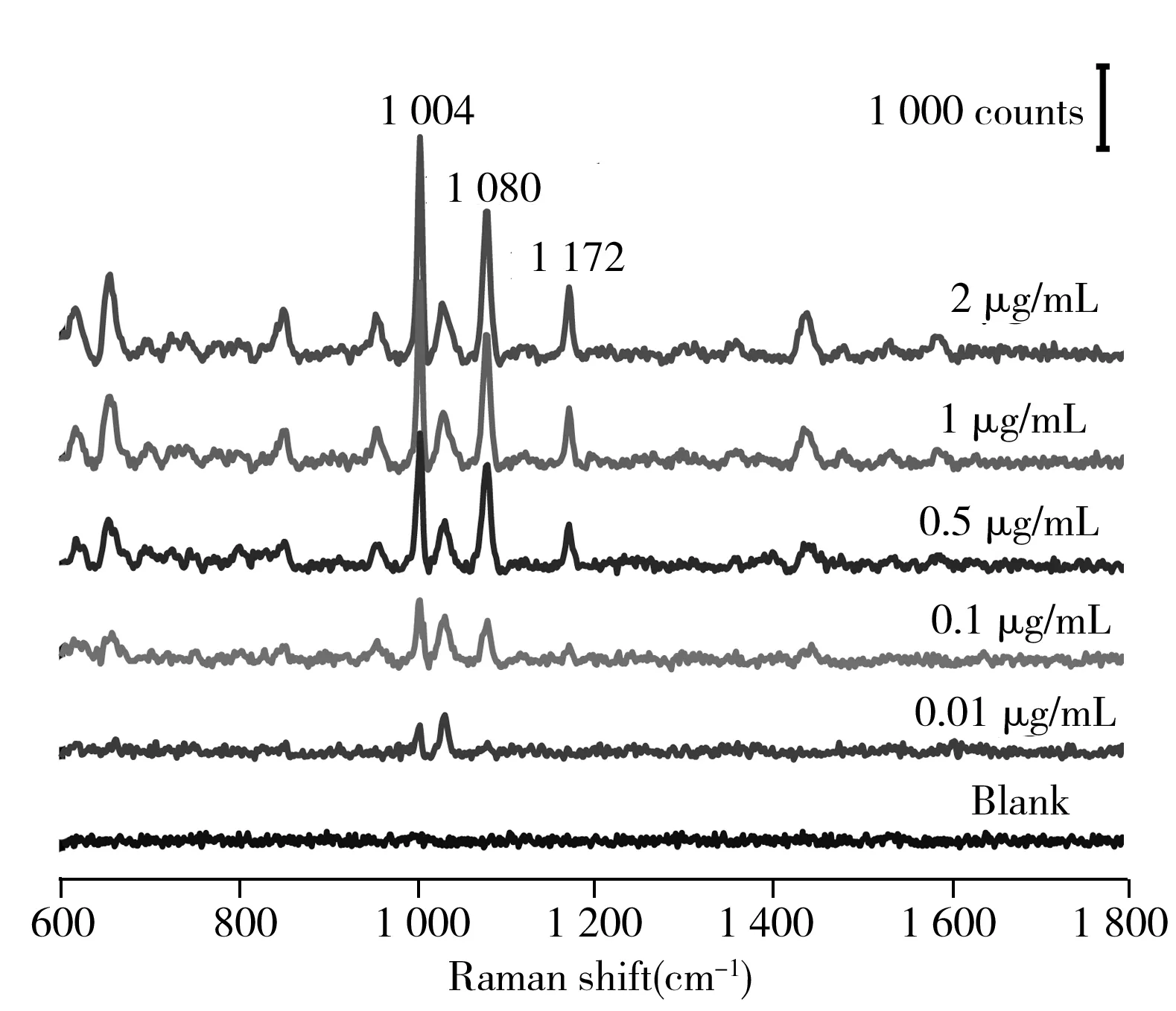
图6 不同质量浓度舒芬太尼水溶液的SERS光谱图Fig.6 SERS spectra of sufentanil in aqueous solution with dirrerent mass concentrations
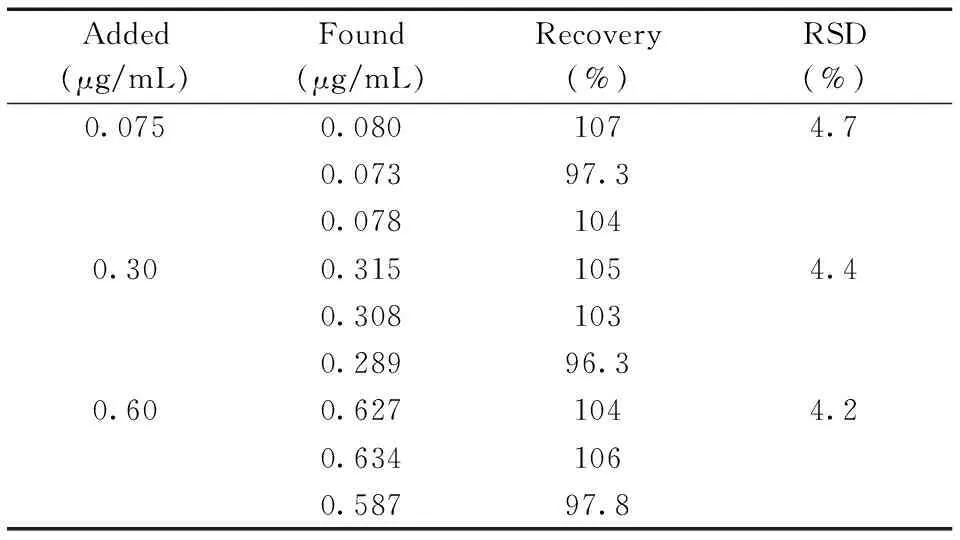
表2 舒芬太尼水溶液的回收率及相对标准偏差Table 2 Recoveries and RSDs of sufentanil in aqueous solution
2.6 水溶液中舒芬太尼的检测
不同质量浓度舒芬太尼水溶液的SERS光谱图如图6所示,空白对照组为去离子水。根据图6,对位于1 004 cm-1处的特征峰强度随舒芬太尼水溶液质量浓度的变化进行线性拟合,发现舒芬太尼质量浓度(x)在0.01~0.5 μg/mL范围内与其特征峰强度(y)呈线性关系,线性方程为y=2 446.29x+179.28,相关系数为r2=0.979。此外,根据检出限(LOD)的定义(特征峰强度等于3倍信噪比时的样品浓度)[23],计算得到LOD为0.09 μg/mL。
为了验证该方法的可靠性,配制质量浓度分别为0.075、0.30、0.60 μg/mL的舒芬太尼加标水溶液样品,并根据线性方程计算出回收率及RSD(n=3),结果见表2。其回收率为96.3%~107%,RSD为4.2%~4.7%。
2.7 人工尿液中舒芬太尼的检测
不同质量浓度芬太尼尿液的SERS光谱图如图7所示,空白对照组为尿液。根据图7,对位于1 004 cm-1处特征峰的强度(y)随舒芬太尼尿液质量浓度(x)的变化进行线性拟合,结果显示,舒芬太尼尿液质量浓度(x)在0.25~6 μg/mL范围之内与特征峰强度(y)呈线性关系,线性方程为y=80.07x+176.51,相关系数为r2=0.968,计算得LOD(3倍信噪比)约为1.55 μg/mL。
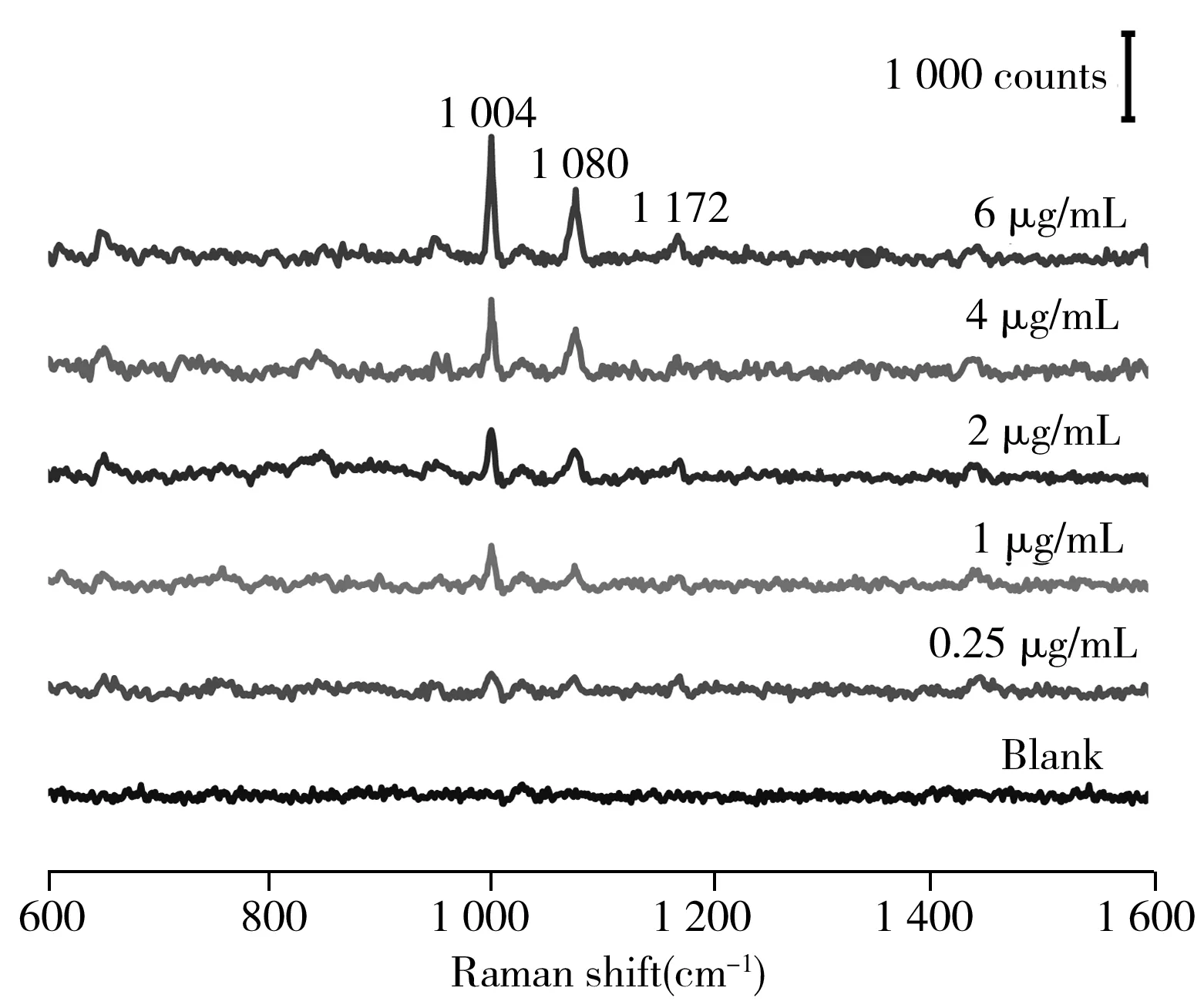
图7 不同质量浓度舒芬太尼尿液的SERS光谱图Fig.7 SERS spectra of sufentanil with different mass concentrations in urine
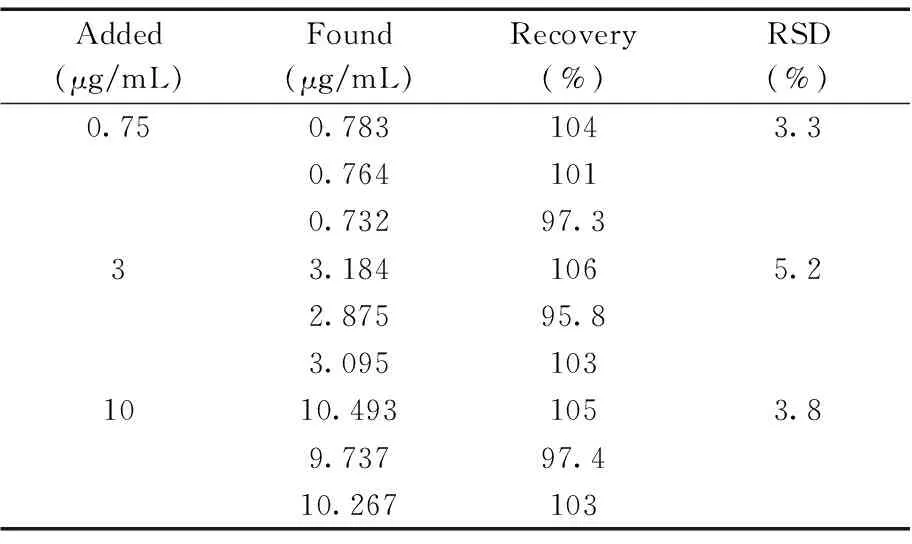
表3 舒芬太尼人工尿液的回收率及相对标准偏差Table 3 Recoveries and RSDs of sufentanil in artificial urine
由于所检测水溶液和尿液样品的质量浓度范围不同,使得两个拟合曲线的斜率差异较大。这是因为当样品质量浓度较低时,特征峰强度随样品质量浓度的增加而迅速上升;而当样品质量浓度较高时,出现饱和现象,导致特征峰强度随样品质量浓度的增加缓慢上升或降低[24]。
同样,为了验证该方法的可靠性,配制质量浓度分别为0.75、3、10 μg/mL的舒芬太尼加标人工尿液样品,并根据线性拟合曲线计算回收率及相对标准误差,结果如表3所示。实际样品的回收率为95.8%~106%,RSD(n=3)为3.3%~5.2%。
3 结 论
本文基于SERS技术对水溶液和尿液中的舒芬太尼进行研究。通过密度泛函理论对舒芬太尼的拉曼光谱进行了计算,并与实验值对比,进而对特征峰进行了归属。然后以银溶胶作为活性基底,NaBr水溶液为促凝剂,对舒芬太尼的水溶液和尿液进行SERS检测。在水溶液和尿液中,舒芬太尼的检出限分别为0.09、1.55 μg/mL。该方法具有快速、准确、无损、操作简便等优点,为水和尿液中舒芬太尼的快速检测打下了良好的基础。
