脑小血管病致血管性认知功能障碍相关因素分析
2020-09-15张德绸葛建华叶丽莎冯启峰
张德绸 葛建华 叶丽莎 冯启峰
1)西南医科大学附属中医医院,四川 泸州 646000 2)西南医科大学附属医院,四川 泸州 646000
缺血性脑小血管病(ischemic small cerebral vessel disease,ICSVD)指脑内小血管缺血性改变引起的一系列临床症状,发病机制主要为动脉硬化引起,可为脑内小动脉、微动脉、毛细血管等,损害此类血管负责大脑皮质及髓质的血供,引起该区域脑及神经组织系列病理及生理性改变[1-2]。目前针对ICSVD发病机制尚不完全清楚,但诸多学者进行了系列相关研究[3-4]。随着疾病发生、发展可致头昏、头痛、步态不稳、跌倒、认知功能障碍及痴呆、老年性抑郁症等多种临床症状,也是引起血管性认知功能障碍(vascular cognitive impairment,VCI)重要亚型之一[5-6]。ICSVD患者早期神经损伤临床表现较轻,随病程发展患者会出现步态异常、认知能力及生活自理能力等下降,最终发展为血管性痴呆(vascular dementia,VD)[7]。而ICSVD引起的VCI多发生在早期,且具有可逆性,故早发现、早诊断及早干预往往可获得良好预后,目前临床对ICSVD及VCI的治疗缺乏有效手段,主要是治疗高血压、抗血小板及降血脂等,疗效报道不一[8-9]。相关研究报道ICSVD引起的VCI发生可能与抽烟、饮酒、脑血管功能评分、颈动脉内膜厚度及系列血检指标等危险因素存在相关性[10-11]。通过对ICSVD引起的VCI相关危险因素进行研究,为早期诊断治疗提供客观参数及科学依据。
1 资料与方法
1.1入组标准纳入标准:(1)诊断符合2015年《中国脑小血管病专家共识》诊断标准;(2)年龄55~80岁;(3)头颅MRI提示脑白质血管源性高信号,同时满足Fazekas评分≥2分及腔隙灶≥2个;(4)3个月及以上认知功能或记忆出现障碍,经日常生活能力量表(activity of daily living,ADL)、Hachinski缺血评分表(Hachinski ischemic scale,HIS)、蒙特利尔认知量表(Montreal cognitive assessment,MoCA),通过量表评分诊断为血管性认知功能障碍(vascular cognitive impairment,VCI)。MoCA评分<26分、≥17分[12];HIS≥7分。
排除标准:(1)<6个月新出现大面积脑梗死、脑出血及脑积水;(2)非血管源性的脑白质病变及其导致的认知功能障碍;(3)有痴呆既往史;(4)家属或患者拒绝。
对照组来自于西南医科大学附属中医医院门诊30例体检人员,年龄55~80岁,既往无精神神经系统疾病史,头颅MRI及神经系统检查无异常,MoCA评分≥26分。
1.2危险因素(1)高血压:1周内收缩压(systolic blood pressure,SBP)≥140 mmHg或舒张压(diastolic blood pressure,DBP)≥90 mmHg或已诊断并治疗原发性高血压;(2)糖尿病:空腹血糖(fasting blood-glucose,FBG)>7.0 mmol/L或随机血糖>11.1 mmol/L且≥2次,或已诊断并治疗糖尿病;(3)冠心病:已诊断并治疗冠心病,或冠脉造影及冠脉CTA确诊患者;(4)血检血脂异常或已诊断并治疗高脂血症;(5)吸烟:≥10支/d,≥5 a;饮酒:≥100 mL/d,≥3 a;(6)颈动脉粥样硬化:超声颈动脉内膜-中膜厚度检测(intima-media thickness,IMT)>1.2 mm并突向管腔;(7)血同型半胱氨酸(homocysteine,Hcy)、总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、低密度脂蛋白(low density lipoprotein,LDL)检测。
1.3临床资料及相关指标采集2016-01—2018-12收治ICSVD及ICSVD合并VCI患者80例,男48例,女32例,年龄55~80(66.15±8.32)岁。其中ICSVD组32例,ICSVD合并VCI组48例,对照组30例(表1)。搜集符合纳入标准人员一般信息,如既往史、个人史(吸烟、饮酒、高脂饮食)、家族史;另外采集血压SBP及DBP、头颅 MRI、血管彩超IMT、FBG、TC、TG、LDL、Hcy等。本研究通过院临床伦理委员会审批,患者均签署相关医疗法规文书。
2 结果
3组受教育年限、不良习惯及合并疾病比较差异有统计学意义(P<0.05),但ICSVD组与ICSVD合并VCI组两两比较差异无统计学意义(P>0.05)。见表2。
3组彩超IMT、血压及血检指标经统计学处理差异有统计学意义(P<0.05);ICSVD组与ICSVD合并VCI组两两比较差异无统计学意义(P>0.05),但ICSVD组与ICSVD合并VCI组IMT和Hcy比较差异有统计学意义(P<0.05)。见表3。

表1 3组一般资料比较
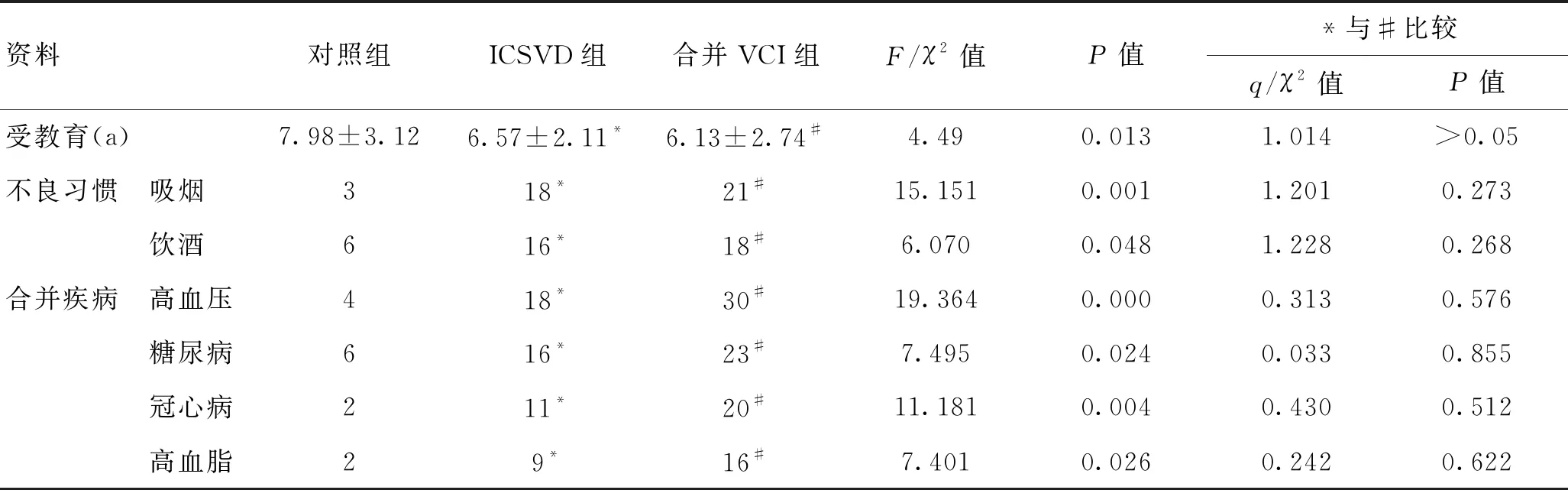
表2 3组受教育年限、不良习惯及合并疾病比较
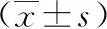
表3 3组IMT、血压及血检指标比较
3 讨论
随着中国人口老年化程度逐渐加剧,脑血管疾病发病率逐年攀升,同步孕育科学技术的不断发展,ICSVD致VCI逐渐被临床工作者发现并认识,主要病变为脑缺血致大脑认知贮备代偿功能逐渐丧失并耗竭,导致患者认知功能逐渐下降[13-14],专家认为脑小血管犹如“风暴”过后的全脑灾难,目前已成为VCI的最常见病因[15-16]。ICSVD可导致患者认知功能障碍、情感障碍、生活自理能力下降甚至丧失,而导致ICSVD危险因素很多,包括不可干预因素和可干预因素;其中不可干预因素包括性别、年龄;可干预危险因素包括高血压、糖尿病、高脂血症、高Hcy、吸烟、饮酒等。目前临床上较常见的“三高”(高血压、高血糖、高血脂)、吸烟及饮酒往往被患者所忽视。
本研究显示教育年限越短发生ICSVD及VCI越高,且受教育年限越短ICSVD合并VCI发病率越高,分析原因为受教育时间越长,受教育者对健康越发重视,日常生活习惯相对规律、不良习惯相对较少。吸烟与饮酒不良习惯与ICSVD及VCI发病率呈正相关,长期吸烟可致脑低灌注、血脑屏障破坏、记忆力下降等影响认知功能,增加痴呆发生,且重度吸烟是认知功能独立危险因素[17-18]。最新研究显示长期大量饮酒是导致痴呆症最重要危险因素,尤其对年龄<65岁的早发性痴呆患者[19]。3组合并疾病比较显示,高血压、糖尿病、冠心病、高血脂等发生率与ICSVD及VCI发病率呈正相关,且血压(SBP、DBP)、FBG、血脂(TC、TG、LDL)与ICSVD及VCI发病率呈正相关。考虑原因为长期高血压可引起心、脑、肾等多个靶器官损害,特别是血压高致动脉硬化、斑块形成、管腔狭窄,又因脑小动脉大多为终末动脉,与其他动脉脉无吻合支,这种特殊解剖学使其供血区脑组织易出现低灌注和缺血性损伤,因此低灌注和缺血也可能ICSVD的发病机制[20-22],低灌注、脑缺血、缺氧致神经元凋亡导致认知功能逐渐下降,是引起ICSVD致VCI重要危险因素[23-24]。高血糖可通过神经毒性和氧化应激反应导致脑部血液流变学改变、脑组织缺血或缺氧,致神经细胞变性并凋亡。高脂血症可加速动脉粥样硬化发生、发展,最终引起脑白质脱髓鞘即脑白质疏松症,因此高血糖、高血脂亦是ICSVD危险因素重要组成部分[25-26]。ICSVD组及ICSVD合并VCI组不良习惯、合并疾病比较无明显差异(P>0.05),表明ICSVD发生致VCI可能与病程存在一定关系,长期高血压、高血糖、高血脂致脑部血管动脉粥样硬化加重,脑组织供血减少致缺血缺氧,甚至脑白质脱髓鞘,导致VCI发生,但本文尚缺少病程作为危险因素分析。
彩超IMT是无创颈动脉检查首选方法,广泛应用于颈动脉硬化病变筛查及随访等,其对动脉管腔狭窄位置及程度、硬化斑块部位及大小等能进行有效监测,与正常人群比较,数值越高表明动脉管腔越细小或管腔狭窄越严重[27]。血清Hcy是人体含硫氨基酸的一个重要代谢中间产物,与动脉粥样硬化等心血管疾患存在一定影响或危险关系,血液中高Hcy可致体内胶原蛋白及弹性蛋白增加,加速动脉粥样硬化,同时刺激炎性因子释放及直接对神经元毒性作用等导致神经细胞凋亡,是ICSVD独立危险因素之一[28-29]。本研究显示IMT及血清Hcy数值越高,发生ICSVD及VCI越高,表明IMT及血清Hcy可能是ICSVD及VCI发生的重要独立因素之一。ICSVD组及ICSVD合并VCI组比较差异有统计学意义(P<0.05),表明颈动脉IMT数值越高,颈动脉管径越细或狭窄,血清Hcy数值越高,动脉粥样硬化越严重,两项指标具有病理学上的一致性。
ICSVD是目前神经科医师值得引起重视的疾病,且是在多种基础疾病和不良生活习惯等因素影响下对脑组织特别是小血管、微血管、脑白质等持续性损害,神经元逐渐凋亡,致VCI发生,严重可致血管性痴呆,所以在临床实际工作中加强认识ICSVD影像学改变、典型临床表现等,提高重视,特别是合并高血压、糖尿病、冠心病、高血脂、高Hcy及吸烟、饮酒者,积极完善相关检查,早期预防和干预,做到早发现、早诊断、早治疗,并戒烟、戒酒,同时积极改善脑功能,是降低或避免ICSVD、阻断或减少VCI发生、发展重要措施,给更多患者及家庭带来福音。
