钯-氧化锌纳米管修饰电极同时检测多巴胺、抗坏血酸和尿酸
2020-09-14唐倩陈梦妮朱国栋刘建允
唐倩 陈梦妮 朱国栋 刘建允
摘 要 以PdCl2和Zn(Ac)2为起始物,采用静电纺丝方法结合高温煅烧,成功制备了钯-氧化锌(Pd-ZnO)中空纳米管。Pd的存在改善了ZnO晶体颗粒的均匀性,调控纤维向中空管状结构转变。利用扫描电子显微镜、透射电子显微镜、X射线衍射等表征技术证明了纳米管内径为240 nm,Pd纳米粒子粒径约为80 nm,且在纳米管上均匀分布。X射线光电子能谱证明,Pd纳米粒子主要以PdO形态存在。所得的Pd-ZnO修饰玻碳电极对多巴胺(DA)、抗坏血酸(AA)和尿酸(UA)均显示出良好的催化活性。采用差分脉冲伏安法测定含DA、AA和UA的混合液,三者的氧化峰电位在此修饰电极上可完全分离,对应的线性范围分别为3.0×107~3.0×105 mol/L(R2=0.9967)、1.0×105~1.0×103 mol/L(R2=0.9991)和6.0×106~6.0×104 mol/L(R2=0.9935),检出限(S/N=3)分别为1.0×108 mol/L、1.0×106 mol/L和3.0×106 mol/L。此电极重现性及稳定性良好,可同时测定样品中的DA、AA和UA。
关键词 多巴胺; 抗坏血酸; 尿酸; 钯; 氧化锌; 脉冲伏安法
1 引 言
多巴胺(DA)、抗坏血酸(AA)和尿酸(UA)作为生物活性小分子,在人体中枢神经系统、新陈代谢和循环系统中发挥了重要作用[1] 。这些生物活性物质的缺乏或失调可导致多种疾病,如人体内DA的失调会引发心脏病、帕金森病等; AA的严重缺乏可能使人罹患败血症[1] ; UA在体内失调会引起痛风、高血压、高尿酸症等[2] 。因此,DA、AA和UA的检测对某些疾病的诊断具有重要意义。
电化学法因其具有选择性高、灵敏度好、操作简单和成本较低等特点而得到广泛应用。然而DA、AA、UA三者的氧化峰电位十分接近,常规电极检测时电化学信号易互相干扰,影响检测的灵敏度与选择性[3] 。采用纳米复合材料修饰电极可有效调节其氧化还原电位,提高选择性。近年来,研究者利用各种材料,如石墨烯[4] 、碳纳米管[5] 、金属[6] 或导电聚合物[7] 等,制备出复合材料修饰电极,以同时检测DA、AA和UA。氧化锌(ZnO)因其优异的光学、催化、电化学等特性在电池、光电催化和传感等领域得到广泛应用[8] 。贵金属钯(Pd)具有电导率高、催化活性强并且稳定性高等特点[9],其卓越的导电性、氧化还原特性及特殊选择性使之成为理想的电极催化材料[10] 。Pd-ZnO纳米复合材料兼具良好的电子导电性和有效电催化活性[11] 。Li等[12] 制备的Pd-ZnO催化剂对硝基酚加氢反应具有较高催化活性; Cao等[13] 利用Pd-ZnO纳米棒制备了选择性乙醇气体传感器。但Pd-ZnO复合材料在传感、催化等应用中,发现Pd在ZnO中的均匀分布特性及材料活性仍需进一步改善。
本研究采用静电纺丝技术制备Pd-ZnO纳米复合材料,通过改变前驱液中Pd含量调节复合材料结构,从而得到均匀、稳定的Pd-ZnO中空纳米管复合物,通过简单的滴涂法制备了Pd-ZnO复合物修饰玻碳电极(Pd-ZnO/GCE)。不同于其它纳米修饰电极,Pd-ZnO/GCE修饰材料制备简单、成本低廉,且电极的灵敏度高、选择性好,可以有效实现DA、AA和UA的同时检测。
2 实验部分
2.1 仪器与试剂
DW-P303-1ACF0高压直流电源(天津东文高压电源有限公司); 恒流注射泵(保定兰格恒流泵有限公司); 扫描电子显微镜(SEM)、透射电子显微镜(TEM)(日本JEOL公司); D/Max-2550 PC X-射线衍射仪(XRD,日本Rigaku公司); PHI-5000V Ersaprobe X-射线光电子能谱仪(XPS,ULVCA-PHI公司); DAJGW-360B接触角测量仪(美国科诺工业有限公司); μAUTOLAB-Ⅲ电化学工作站(瑞士万通中国有限公司); 采用三电极系统:GCE(d=3 mm)为工作电极,Ag/AgCl(3 mol/L NaCl)为参比电极,铂丝为辅助电极。
聚乙烯吡咯烷酮(PVP,MW 1300000)、聚甲基丙烯酸甲酯(PMMA,MW 12000) (Acros Organics 公司); DA和UA(分析纯,百灵威科技); 醋酸锌(Zn(Ac)2)、AA和PdCl2(国药集团化学试剂有限公司); 实验用水为超纯水(18.2 MΩ cm,Thermo公司)。
2.2 Pd-ZnO纳米纤维的制备
将PVP和PMMA(质量比为1:0.8,总含量10% (w/v))加入DMF溶剂,搅拌溶解得到混合液。随后加入Zn(Ac)2(8%)及适量PdCl2,于60℃水浴中搅拌形成均匀纺丝液。调整纺丝电压为11 kV、注射流速为0.5 mL/h、接收距离为15 cm,制得PdCl2-Zn(Ac)2/PVP-PMMA复合原丝纳米纤维。将其置于马弗炉中,以25℃/h升温至500℃,保持1 h,得到Pd-ZnO纳米复合物(Pd-ZnO)。调节PdCl2在纺丝液中的含量为0、0.1%、0.4%、1%、2%、3%,得到一系列不同Pd含量的Pd-ZnO复合材料(ZnO、Pd(0.1)-ZnO、Pd(0.4)-ZnO、Pd(1)-ZnO、Pd(2)-ZnO、Pd(3)-ZnO)。
2.3 Pd-ZnO修飾GCE
GCE依次采用1.0、0.3和0.05 μm的氧化铝粉末抛光,在水和无水乙醇混合溶液中超声清洗2 min,用N2吹干,备用。
将Pd-ZnO纳米复合物样品混合均匀,纯水中超声分散3 h。取适量分散液滴涂于GCE表面,自然晾干,得到Pd-ZnO修饰GCE,不同Pd含量对应的修饰电极分别标记为ZnO/GCE、Pd(0.1)-ZnO/GCE、Pd(0.4)-ZnO/GCE、Pd(1)-ZnO/GCE、Pd(2)-ZnO/GCE和Pd(3)-ZnO/GCE。
2.4 实验方法
室温下,取0.1 mol/L HAc-NaAc缓冲溶10 mL,采用循环伏安法(CV)研究Pd-ZnO/GCE的电化学性能; 采用差分脉冲伏安法(DPV)检测DA、AA和UA。电位扫描范围为0.1~0.7 V,脉冲振幅为50 mV,脉冲周期为100 ms,电压梯度为5 mV,采样时间为500 ms。
3 结果与讨论
3.1 材料的表征及亲水性研究
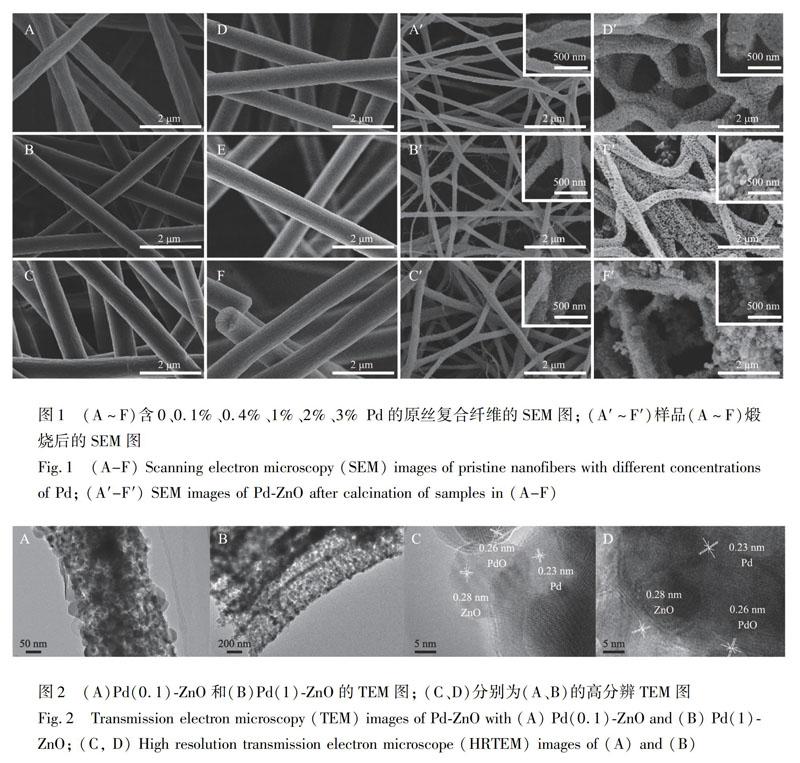
图1 A~1F为Pd含量分别为0、0.1%、0.4%、1%、2%、3%时制备的PdCl2-Zn(Ac)2/PVP-PMMA复合原丝纤维的SEM图。由图1可知,随着Pd含量增加,溶液的电导性和可纺性增强,所得纤维表面更加光滑,直径略变大。对应煅烧后样品的SEM形貌如图1中A′~F′所示。Pd含量低时,煅烧后纤维收缩明显,且高温过程导致部分纤维融合而不均匀。当纺丝液中Pd含量逐渐增加至1%时,纤维形貌明显改善,且纤维向中空纳米管状结构转变
(图1D′右上方插图)。但Pd含量过高时,纳米颗粒有团聚现象,导致纳米管坍塌。Pd(1)-ZnO样为纳米管结构,且连续性及均匀性最好。
图2A和2B分别为Pd(0.1)-ZnO和Pd(1)-ZnO复合纤维的TEM图像,图2C和2D为相应的高分辨TEM图像(HRTEM)。Pd(0.1)-ZnO呈实心的纤维,纤维表面由Pd和ZnO纳米颗粒构成,颗粒大小不均一。在图2C和2D中可清晰看到ZnO(100)[14],和Pd(111)、(101)[15] 的晶格條纹。Pd(1)-ZnO样品呈现清晰的中空纳米管结构,颗粒均匀致密,同时HRTEM结果显示 Pd与ZnO纳米粒子之间具有较好的相容性。结果表明,复合纤维中存在适量的Pd可改善ZnO的成核,抑制较大晶体生长,增加均匀性。
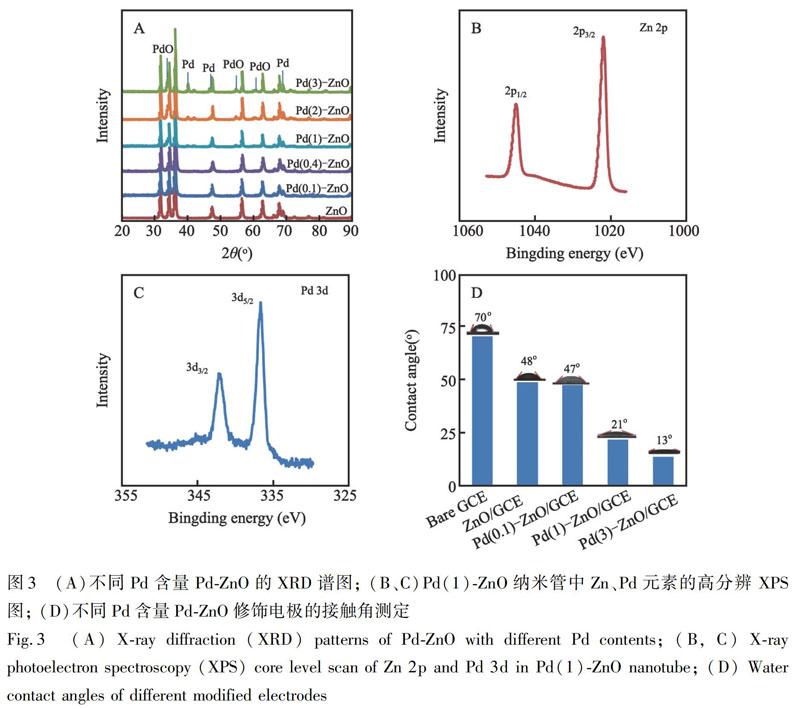
采用XRD研究了不同含量Pd复合材料的晶体结构。图3A中曲线分别为ZnO、Pd(0.1%)-ZnO、Pd(0.4%)-ZnO、Pd(1)-ZnO、Pd(2)-ZnO和Pd(3)-ZnO样品的XRD图。在2θ为 31.7°、 34.4°、 36.2°、 47.5°、 56.5°、 62.8°、 66.4°、 67.9°和69.0°处,呈现典型ZnO纤锌矿晶体结构的衍射峰[16] 。Pd含量增加时,Pd及PdO的特征衍射峰变得明显(如图中标示),说明Pd在复合物中以Pd和PdO形式存在。
进一步采用XPS分析Pd(1)-ZnO中元素化学形态。图3B和3C分别为元素Zn和Pd的高分辨XPS扫描图。在1021.7 和1044.8 eV处出现ZnO的Zn 2p3/2和2p1/2 特征结合能峰[13] ; Pd元素的结合能峰出现在336.2和341.8 eV,对应于PdO的Pd 3d5/2 和Pd 3d3/2[11] 。说明Pd-ZnO纳米管中Pd主要以PdO形式存在,Pd单质形态的含量较少。
将Pd-ZnO复合材料滴涂于GCE表面,考察其表面亲水性。如图3D所示,Pd-ZnO在GCE表面的修饰明显改善了其亲水性,且随着Pd含量增加,其水接触角逐渐减小。因ZnO含有亲水基团(羟基)[17],在负载Pd后,由于颗粒更小更均匀,其表面活性羟基含量更多,亲水性进一步增强,这有利于改善对应电极的电化学性能。
3.2 Pd-ZnO/GCE电极的电化学特性
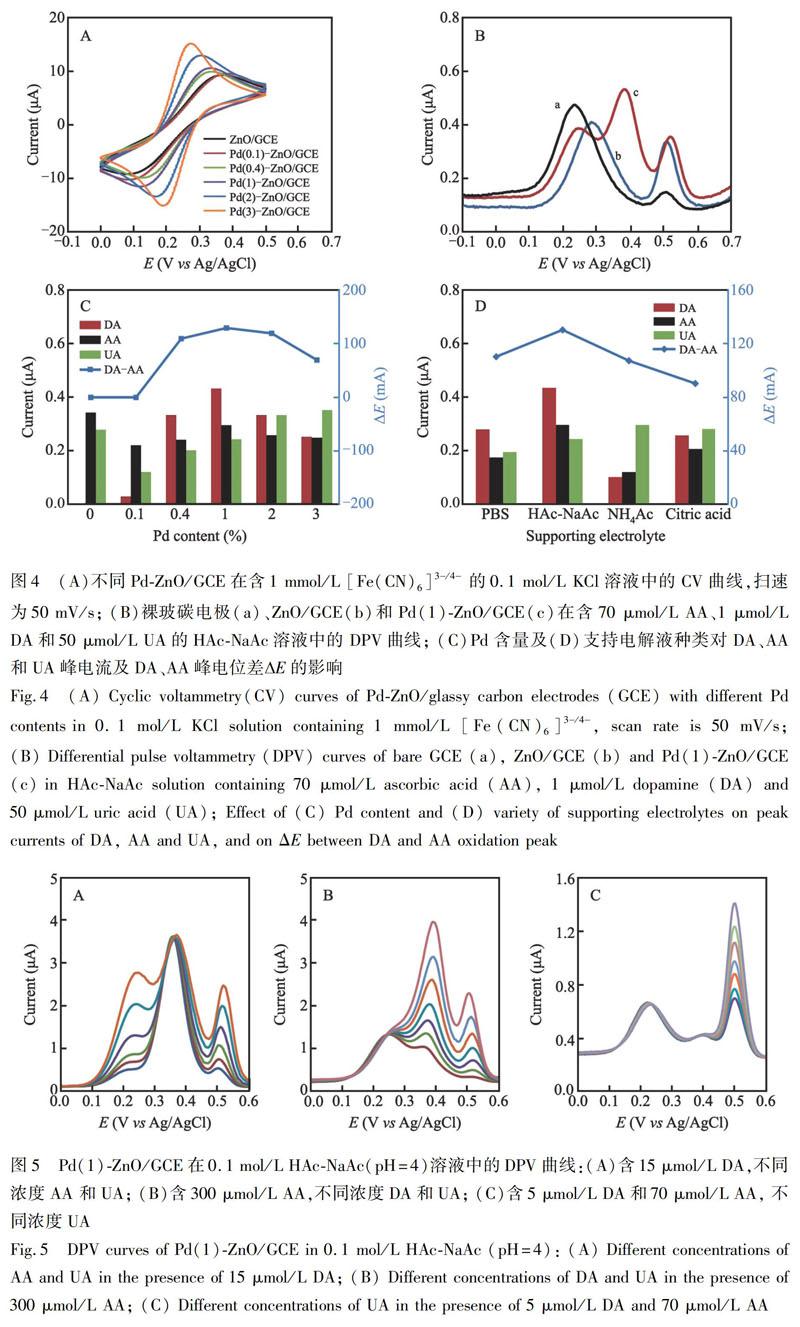
不同Pd含量的Pd-ZnO/GCE在1 mmol/L [Fe(CN)6]3/4 中的循环伏安曲线如图4A所示,随着Pd含量增加,峰电流逐渐增大,这可能是由于Pd的存在提高了材料的导电性和亲水性,从而促进了电子转移,更有利于溶液中离子在电极表面的扩散和传输。
3.3 DA、AA和UA在Pd-ZnO/GCE电极上的测定及条件优化
3.3.1 DA、AA和UA的DPV响应 分析了Pd(1)-ZnO/GCE在含1 mmol/L DA、 70 mmol/L AA、 50 mmol/L UA的混合溶液中的DPV曲线(图4B)。在裸GCE(a)和ZnO/GCE(b)表面,仅出现两个氧化峰,而在Pd(1)-ZnO/GCE(c)表面,则有3个明显的氧化峰。这主要因为在裸GCE和ZnO/GCE表面,AA和DA的氧化峰重合,不能分辨。而在Pd(1)-ZnO/GCE上,AA、DA和UA的氧化峰分别出现在0.25、0.38和0.51 V,三者互不干扰,证明Pd与DA的结合作用较强,促进了DA在电极表面富集,信号增大; 同时,由于结合态较稳定,使其在电极表面的氧化电势正移,从而使AA、DA的响应信号分开。上述结果表明,Pd-ZnO/GCE可用于AA、DA和UA的同时检测。
3.3.2 DA、AA和UA测试条件的优化 (1)Pd含量的影响 研究了不同Pd含量的Pd-ZnO/GCE在混合溶液(1 μmol/L DA、70 μmol/L AA、50 μmol/L UA)中的催化氧化性能。图4C为DA、AA和UA在不同电极上的DPV响应对应的DA-AA峰电位差(E)及各自的电流值。随着Pd含量的增加,DA-AA峰E增大,同时,DA和 AA的峰电流呈现先升后降的趋势,Pd(1%)-ZnO/GCE电极的E及峰电流最大。UA的峰电流随Pd含量的增加而增大。考虑到三者同时检测,结合SEM表征结果可知,过量的Pd会引起纳米管的结构坍塌、比表面积降低、活性位点减少,从而影响检测结果。因此,后续实验选择Pd(1%)-ZnO/GCE为工作电极。(2)支持电解液的影响 比较了DA、AA和UA在0.1 mol/L的HAc-NaAc、PBS、Citric acid和NH4 Ac缓冲溶液中的差分脉冲伏安响应。DA、AA和UA的峰电流值及对应的DA-AA峰ΔE如图4D所示,在HAc-NaAc缓冲溶液中,DA-AA峰ΔΕ最大,响应电流最大。因此,选择0.1 mol/L HAc-NaAc缓冲溶液作为支持电解质。
3.3.3 DA、AA 和 UA 的选择性检测 选用Pd(1)-ZnO/GCE,考察DA、AA和UA 共存时相互干扰情况,实验结果如图5所示。图5A表明,固定DA浓度(15 μmol/L),AA和UA浓度分别在1.0×104~7.0×104 mol/L、7.0×105~4.0×104 mol/L范围内变化,二者电流随其浓度增加而逐渐增大,DA电流不变; 图5B表明,固定AA浓度(300 μmol/L),DA与UA浓度分别在3.0×106~3.0×105 mol/L、3.0×105~3.0×104 mol/L范围变化时,二者电流线性增加,且不干扰AA的信号; 图5C表明,固定DA、AA的浓度不变,UA浓度在3.0×105~1.5×104 mol/L范围内,不干扰DA和AA的响应。综上,此电极可以实现DA、AA和UA的选择性测定。
3.4 DA、AA 和 UA 同时检测的标准曲线
在最优实验条件下,对系列DA、AA和UA混合溶液进行测定,得到相应DPV曲线,如图6A所示。随浓度增加,溶出峰电流逐渐增强,AA、DA和UA分别在0.25、0.38和 0.51 V处出现明显的氧化峰,线性范围分别为1.0×105~1.0×103 mol/L(R2=0.9991)、3.0×107~ 3.0×105 mol/L(R2=0.9967)和 6.0×106~ 6.0×104 mol/L(R2=0.9935),检出限(S/N=3)分别为1.0×106 mol/L、1.0×108 mol/L和3.0×106 mol/L,且三者互不干扰。与文献报道的结果(表1)相比,Pd(1%)-ZnO/GCE的线性范围宽、检出限低,可以实现DA、AA和UA的同时检测。
使用同一根电极在1 μmol/L DA、70 μmol/L AA和50 μmol/L UA的混合溶液中連续检测6次,各自对应的峰电流相对偏差值(RSD)<10%; 采用相同方法制备5根修饰电极,在相同条件下,DA、AA和UA检测结果的RSD分别为10%、13%和15%,表明此修饰电极具有良好的重现性和稳定性。
3.5 实际样品分析
将人尿样品经0.25 μm膜过滤后,用0.1 mol/L HAc-NaAc溶液(pH=4)将样品稀释50倍,采用本方法检测。样品中UA浓度为36.7 μmol/L。标准加入实验结果见表2。DA、AA和UA的加标回收率分别为99.3%、98.8%和105.5%,相对标准偏差(RSD,n=3)在1.6%~ 3.3%之间,可满足实际样品的分析要求。
4 结 论
采用静电纺丝及高温煅烧技术,通过调节Pd盐起始浓度,制备了Pd均匀负载的ZnO中空纳米管。Pd的存在改善了ZnO的微观形貌及结构,增加了活性位点。同时,由于Pd含量高并在纳米管表面分布均匀,大大提高了Pd-ZnO纳米管修饰电极的导电性及对DA、AA和UA氧化的催化活性,使三者氧化峰电位较好分离。Pd-ZnO/GCE成功用于DA、AA和UA的同时检测,三者互不干扰,具有高灵敏度和选择性,检测线性范围宽,检出限低。此修饰电极有望用于实际样品中DA、AA和UA的同时检测。
References
1 Zhang W J,Liu L,Li Y G,Wang D Y,Ma H,Ren H L,Shi Y L,Han Y J,Ye B C. Biosens. Bioelectron.,2018,121: 96-103
2 Temoin Z. Sens. Actuators B,2013,176(6): 796-802
3 Huang X,Tan C L,Yin Z Y,Zhang H. Adv. Mater.,2014,26(14): 2185-2204
4 Zhao Y N,Zhou J,Jia Z M,Huo D Q,Liu Q Y,Zhong D Q,Hu Y,Yang M,Bian M H,Hou C. Microchim. Acta,2019,186 (2): 92
5 Shruthi C D,Venkataramanappa Y,Suresh G S. J. Electrochem. Soc.,2018,165(10): B458-B465
6 Zhang L H,Khungwa J,Liu Y,Li L,Wang X H,Wang S T. J. Electrochem. Soc.,2019,166 (8): H351-H358
7 Li D D,Liu M,Zhan Y Z,Su Q,Zhang Y M,Zhang D D. Microchim. Acta,2020,187 (1): 1-10
8 LU Yuan-Yuan,CHEN Meng-Ni,GAO Yi-Li,YANG Jian-Mao,MA Xiao-Yu,LIU Jian-Yun. Chinese J. Anal. Chem.,2015,43(9): 1395-1401
卢圆圆,陈梦妮,高屹立,杨健茂,马小玉,刘建允. 分析化学,2015,43(9): 1395-1401
9 Yao Y,Zhong J,Lu Z W,Liu X,Wang Y Y,Liu T,Zou P,Dai X X,Wang X X,Ding F,Zhou C L,Zhao Q B,Rao H B. Microchim. Acta,2019,186(12): 795
10 Ismail A A,Bahnemann D W,Al-Sayari S A. Appl. Catal. A,2012,431-432: 62-68