碳纳米管修饰玻碳电极的循环伏安实验的改进*
2020-09-14毛秋平
陈 媛,毛秋平
(华南理工大学化学与化工学院,广东 广州 510640)
循环伏安法是一种重要的电化学研究方法,是在工作电极、参比电极中间加上对称的三角波扫描电压,记录工作电极上得到的电流与施加电位的关系曲线,即循环伏安图(图1)。在三角波的前半部会记录一个峰形的阴极波,后半部记录一个峰形的阳极波。从循环伏安图的波形,氧化还原峰形电流的数值,比值,峰电位等可以判断电极反应的可逆性[1-2]。
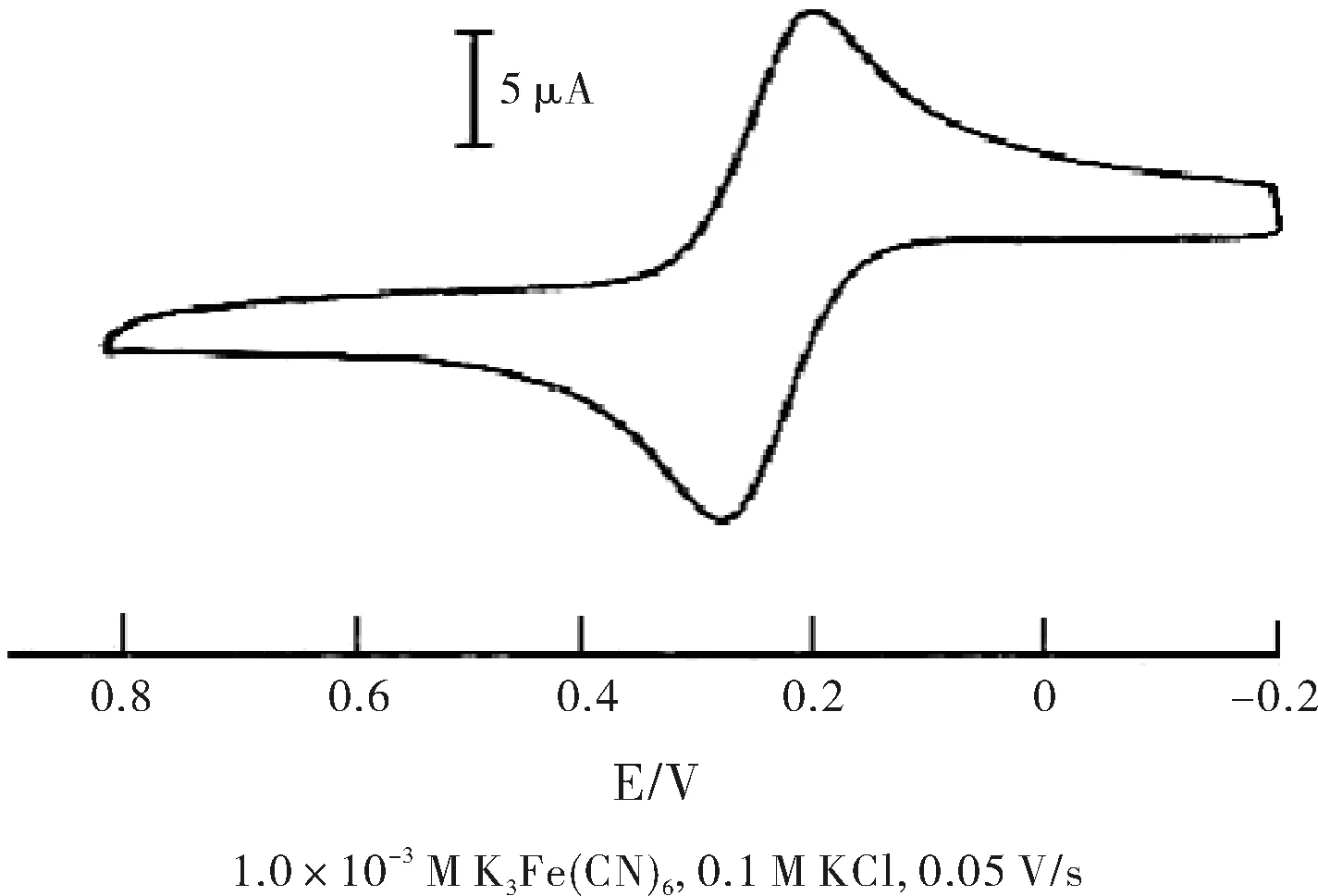
图1 循环伏安图
1 实验目的和内容
本实验使用电化学工作站测定玻碳电极在不同扫描速度下的氧化和还原峰电位,通过扫描速度的平方根和响应的电流值用origin软件绘制标准标准曲线图,拟合出线性方程,在25 ℃时,可以根据Randles-Sevcik公式计算电极的有效面积:
式中ip为峰电流,A;A为电极的有效面积,cm2;D0为反应物的扩散系数,cm2/s;v为扫速,V/s;n为电极反应的电子转移数;C0为反应物的浓度,mol/cm3[3]。
通过该实验,加深学生对循环伏安实验的认识。
2 试剂和仪器
试剂:铁氰化钾,硝酸钾,氯化钾,氢氧化钠,N,N-二甲基甲酰胺(分析纯),广州化学试剂有限公司;碳纳米管,α-Al2O3粉(0.05 μm粒径),上海仙仁仪器仪表有限公司;高纯水。
仪器:瑞士万通Autolab电化学系统,玻碳电极(d=3 mm)为工作电极,饱和甘汞电极为参比电极,铂丝电极为辅助电极,带三个孔的25 mL的电解池,上海仙仁仪器仪表有限公司;20 μL数字电动移液器,大龙仪器有限公司。
3 实验步骤
3.1 溶液配置
吸附分散剂:50 mg碳纳米管溶于100 mL高纯水中,每次使用前超声分散均匀。
5 mmol/L K3Fe(CN)6溶液(含5 mmol/L K4Fe(CN)6+0.1 mol/L KCl):0.1646 g K3Fe(CN)6,0.2112 g K4Fe(CN)6,0.7455 g KCl,高纯水溶解后定容到100 mL容量瓶。
1 mol/L NaOH:40 g NaOH加高纯水溶解到1 L容量瓶。
3.2 电极处理
将玻碳电极在麂皮上用α-Al2O3粉(0.05 μm粒径)抛光粉抛光后,清理干净表面的污物,转移到超声波清洗仪中清洗,每次3秒,重复清洗2次即可。如图2所示,将玻碳电极,饱和甘汞参比电极,铂丝辅助电极都插入到一个带三个孔的25 mL的电解池中,容器里面先装上配制好的1 mol/L NaOH活化电极,再清洗干净三根电极,再装上5 mmol/L K3Fe(CN)6溶液测定玻碳电极的氧化还原峰电位、电流值。

图2 电极装置图
3.3 电极测试
依次接上工作电极、参比电极和辅助电极;开启电化学系统及计算机电源开关,启动电化学程序,在菜单中依次选择设定Setup、方法Technique、循环伏安法CV、参数Parameter,输入的参数,见表1。

表1 实验参数
(1)点击Run 开始扫描,记录氧化还原峰电位Epc、Epa及峰电流Ipc、Ipa;
(2)电极的活化:将表面处理好的电极置于1 mol/L的NaOH溶液中于-1.5到1.5 V电位下,扫速为1 V/s,灵敏度为1e-3,扫描20周,然后用蒸馏水清洗干净后吹干电极表面。
(3)根据上表参数,重新扫描,记录氧化还原峰电位Epc、Epa及峰电流Ipc、Ipa;
(4)改变扫描速率,分别为0.02 V/s、0.05 V/s、0.1 V/s、0.2 V/s、0.5 V/s,作循环伏安图;
(5)以氧化还原峰电流Ipc、Ipa分别与扫速的平方根v1/2作图,求算线性相关系数R。
(6)根据Ipc与扫速的平方根v1/2作图得到的线性回归方程,计算所使用的玻碳电极的有效面积。
(7)碳纳米管修饰电极的制备:称取25 mg碳纳米管于50 mL高纯水中,用超声波清洗仪超声分散后得到黑色悬浮液,用20 μL数字电动移液器移取20 μL悬液滴加在上述玻碳电极表面,用冷风使气流小而垂直地吹干溶剂,保证碳纳米管均匀地分布在玻碳电极表面。
(8)碳纳米管修饰电极的循环伏安曲线测定:将制备好的碳纳米管修饰电极按照上述步骤2相同的方法进行循环伏安扫描,记录不同扫描速率下的氧化还原峰电位记录氧化还原峰电位Epc、Epa及峰电流Ipc、Ipa,保存谱图,根据Randles-Sevcik公式计算修饰后的电极面积[3-5]。
4 结果和讨论
4.1 铁氰化钾溶液配制的浓度和组成探究
试验了1 mmol/L K3Fe(CN)6溶液、5 mmol/L K3Fe(CN)6溶液、5 mmol/L K3Fe(CN)6溶液(含0.5 mol/L硝酸钾)、5 mmol/L K3Fe(CN)6溶液(含5 mmol/L K4Fe(CN)6+0.5 mol/L KCl)、5 mmol/L K3Fe(CN)6溶液(含5 mmol/L K4Fe(CN)6+0.1 mol/L KCl),发现5 mmol/L K3Fe(CN)6溶液(含5 mmol/L K4Fe(CN)6+0.1 mol/L KCl)得到的循环伏安图对称性最好。
4.2 碳纳米管修饰电极制备条件的选择
分别试验了高纯水和N,N-二甲基甲酰胺溶解碳纳米管,发现玻碳电极的有效面积和电化学性质变化相差不大,故选择更安全环保的高纯水溶解碳纳米管。在碳纳米管修饰电极的制备过程中,为了把玻碳电极表面的溶剂除掉,我们试验了四种方法,分别是:红外灯烤干、真空烘箱烘干、自然晾干和电吹风吹干。其中红外灯和真空烘箱烘烤第一次,试验效果很好,阴阳极峰对称,两峰电流相等,峰峰电位差约为70 mV,但是随着烘烤的次数增加,试验效果越来越差,玻碳电极耗损得很严重,而且是不可逆的,考虑到玻碳电极比较昂贵,为了尽量保护玻碳电极,降低试验成本,不选择红外灯烤和真空烘箱烘干。自然晾干理论上不管是科研工作还是检测机构分析测试工作中都是最佳的试验方法,但是自然晾干需要24 h,这样本科生不能及时看到试验结果,此方法也不可行。最后我们选择电吹风吹干的方法,既保护了电极又缩短溶剂挥发的时间,试验效果也能满足阴阳极峰对称,两峰电流相等,峰峰电位差约为70 mV。
4.3 实验数据分析

表2 实验结果与数据分析
表2实验结果表明电极修饰前,两峰的电流值相等(Ipc/Ipa=1),峰峰电位差Ep约为70 mV(理论值约59 mV),电极的循环伏安图出峰效果理想,表明电极表面处理得好,工作电解液5 mmol/L K3Fe(CN)6溶液(含5 mmol/L K4Fe(CN)6+0.1 mol/L KCl)配制的浓度和组成得到的循环伏安图峰形最好。
根据Randles-Sevcik公式:在25 ℃时,ip=2.69×105n3/2AD01/2C0v1/2,计算出的玻碳电极有效面积碳纳米管修饰后是修饰前的约两倍大,说明碳纳米管修饰电极制备条件的选择中,用高纯水来溶解效果良好,比用其他有机溶剂溶解更环保。
5 结 语
本文介绍了本科教学实验中关于循环伏安法测定玻碳电极的有效面积的方法,学习了化学修饰电极的制作方法,了解了电极修饰前后的电化学性质变化。试验了铁氰化钾溶液配制的浓度和组成,得到最佳的工作电解液,即5 mmol/L K3Fe(CN)6溶液(含5 mmol/L K4Fe(CN)6+0.1 mol/L KCl)。同时试验了制备修饰电极的碳纳米管的溶剂,得到高纯水可以作为溶剂,效果比其他有机溶剂更绿色、环保,使本科生在本科教学中增强环保、低碳、节能的意识[6]。
