不同BMI慢性肾脏病患者临床进展危险因素分析
2020-09-07罗红艳陆晓华马丹娜闫学慧郑亚莉
罗红艳,王 慧,陆晓华,马丹娜,闫学慧,保 莉,郑亚莉
随着生活方式的改变,机体长期摄入过剩能量、体内脂质增加而导致体重增加,超重和肥胖已被广泛重视。依据体重指数(BMI)评估肥胖程度,对于中国人群[1],BMI≥25 kg/m2为超重,BMI≥28 kg/m2为肥胖。前期研究已证实,肥胖参与慢性肾脏病(CKD)进展,而评估不同BMI范围的CKD患者临床进展危险因素的文献报道较少。通过收集宁夏回族自治区人民医院肾内科住院患者的相关病史资料,评估不同BMI慢性肾脏病患者临床进展危险因素,重视慢性肾脏病进展传统因素以外的影响指标,以进一步延缓CKD的进展。
1 资料与方法
1.1 一般资料:选取2015年1月-2018年12月收住宁夏回族自治区人民医院肾内科的153例CKD患者,即肾脏结构或功能异常,或肾小球滤过率(eGFR)<60 mL/(min·1.73 m2)持续3个月[2]。依据MDRD公式[3]获得估算eGFR,依据慢性肾脏病分期标准:eGFR≥90 mL/(min·1.73 m2)为CKD 1期;eGFR 60~89 mL/(min·1.73 m2)为CKD 2期;eGFR 30~59 mL/(min·1.73 m2)为CKD 3期;eGFR 15~29 mL/(min·1.73 m2)为CKD 4期;eGFR<15 mL/(min·1.73 m2)或已透析为CKD 5期;文中以CKD 1~4期患者为研究对象。 依据中国成人超重和肥胖症预防控制指南[4],以BMI将患者分为2组:BMI正常组83例(BMI<25 kg/m2),超重组70例(BMI≥25 kg/m2)。
1.2 排除标准:糖尿病药物相关及内分泌性肥胖者;急性或急进性肾炎;感染、发热者;家族性高脂血症;使用成分不明或肾毒性药物者。
1.3 相关研究指标收集及检测:记录患者的年龄、性别、原发病;平均动脉压(MBP)计算:MAP=1/3收缩压+2/3舒张压。实验室指标:血指标均为晨起空腹标本:血清肌酐(Scr)、空腹血糖(FBG)、血尿酸(UA)、C反应蛋白(CRP)、甘油三酯(TG)、胆固醇(CHOL)及24 h 尿蛋白定量等均在医院检验中心生化室统一检测;用MDRD公式估算eGFR[3]。
1.4 统计学方法:采用SSPS 19.0统计软件,符合正态分布的计量资料2组间均数比较采用独立样本t检验,组间的比较采用χ2检验,多因素相关性分析采用Logistic回归分析,以P<0.05为差异有统计学意义。
2 结果
2.1 2组患者临床资料分析:153例患者中,BMI正常组83例(BMI<25 kg/m2),超重组70例(BMI≥25 kg/m2)。BMI正常组(非超重)占54.24%,其中男性患者73.1%;超重组占45.75%,其中男性患者69.1%。BMI正常组平均年龄(38±9.6)岁,超重组年龄(41±7.8)岁,2组间性别、年龄比较差异无统计学意义(P>0.05)。平均动脉压在2组间比较差异无统计学意义;原发病方面,2组前三位主要病因:BMI正常组有慢性肾小球肾炎、IgA肾病、膜性肾病,但超重组局灶性节阶性肾小球肾炎(FSGS)多于BMI正常组,2组比较差异有统计学意义,见表1。
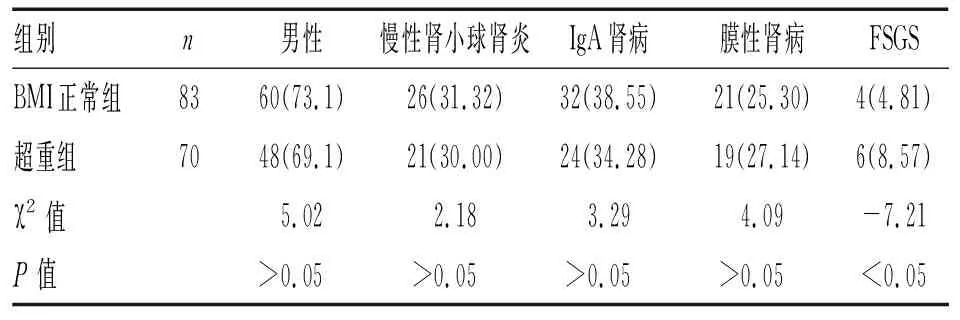
表1 2组患者临床资料比较[n(%)]
2.2 2组患者实验室指标比较:超重组患者UA增高、CRP增高、TG增高、24 h 尿蛋白定量增多,与BMI正常组相比差异均有统计学意义(P<0.05);而超重组患者,eGFR、Scr、FBG与BMI正常组比较差异无统计学意义(P>0.05),见表2。
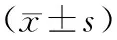
表2 2组患者实验室指标比较
2.3 多元Logisti回归分析:2组患者以eGFR为因变量,以年龄、UA、CRP、CHOL、TG、FBG等为自变量,分析2组eGFR与各指标之间的关系。BMI正常组患者eGFR与尿酸呈负相关,而超重组患者eGFR与CRP、UA、CHOL呈负相关性,见表3-表4。
表3 BMI正常组Logisti回归分析

表4 超重组Logisti回归分析
3 讨论
肥胖导致的肾损害已受到广泛重视,早在1974年 Weisinger等已提出肥胖可出现蛋白尿等肾脏损害[5]。已有统计显示中国超重率逐渐增加,至2015年已增高至30%[6]。因而估算肥胖和超重的重要指标之一BMI至关重要,BMI的变化在肾脏疾病中的影响不容忽视。故本文旨在分析不同BMI的CKD患者病情进展的影响因素,收集住院病历资料并做了相关统计学分析。
在临床资料分析结果中提示,入组患者年龄、性别差异无统计学意义,2组间比较结果可排除年龄、性别对结果的影响。高血压肾损害[7]已被广泛认知,良性高血压病史多年,逐渐出现蛋白尿,病理上可表现为肾小动脉损害,随着病情进展至缺血性肾损害,肾小球硬化进一步加重肾损害。本研究2组患者平均动脉压无差异,排除血压差异导致肾脏病进展的因素,故进一步比较了2组患者的血糖、血脂等代谢方面指标。在原发病资料分析方面,超重组患者局灶性节阶段性肾小球硬化(FSGS)发病率高于BMI正常组,查阅文献资料提示肥胖可导致肾脏损害,被称为肥胖相关性肾小球疾病(ORG)[8-9]。在临床上表现为蛋白尿,病理上光镜可见肾小球体积变大,依据病理表现不同分为不同类型。若只见肾小球体积增大,称为肥胖相关性肾小球肥大(OB-GM);在肾小球体积肥大的基础上合并阶段性或球性肾小球的硬化改变等称为肥胖相关性肾小球硬化症(OB-FSGS)。本研究原发病类型中FSGS高于对照组,与文献中结果一致。
众所周知,蛋白尿是CKD病情进展的独立危险因素[10],本研究结果也证实超重组24 h 尿蛋白定量高于BMI正常组,蛋白尿同样是加重超重患者肾脏病进展的危险因素之一。同时在文献中得知,BMI增高了患者常合并炎症改变和代谢相关性疾病[11]。脂肪细胞不仅可以储存能量同时具有内分泌功能,可分泌多种脂肪因子,如瘦素、肿瘤坏死因子a(TNF-a)及CRP等炎性因子[12],构成肥胖患者的慢性炎症状态,参与肾小球肥大及细胞外基质增多等病理损伤。刘志红[13]等研究发现在ORG中,炎性因子的基因表达上调;Liu等[14]观察到在小鼠脂肪组织中敲除肥大细胞,小鼠体内的炎性水平明显下降。本研究结果显示,超重组患者血CRP水平增高,进一步Logistic分析提示,在超重组CRP与eGFR呈负相关性,而在BMI正常组中,CRP与eGFR无相关性,提示血CRP水平增高是超重患者慢性肾脏病进展的危险因素之一,需重视BMI增高患者炎症状态及肾脏疾病的影响。高尿酸血症可形成尿酸盐沉积,导致炎症反应和免疫活化等,出现肾损伤,分为急性和慢性尿酸相关的肾损害,其中慢性尿酸肾损害可表现为肾小管间质的损害[15]。研究结果提示不同BMI组患者中尿酸差异有统计学意义,进一步在相关性分析中提示,尿酸在2组中均与eGFR呈负相关性,提示尿酸可加重慢性肾脏病患者损害,且在超重组尿酸水平高于BMI正常组,与目前文献中报道结果一致。BMI增高常合并血脂异常,研究结果提示超重组患者甘油三酯及胆固醇水平均高于对照组,进一步相关性分析提示在超重组血脂与eGFR呈负相关性。其可能的机理是脂质沉积可损伤血管内皮细胞、影响血管内血流动力学。细胞内脂质的增加可促进系膜基质增生、蛋白的发生等,导致肾小球损伤[16]。
研究结果提示不同BMI组患者血肌酐及eGFR水平无统计学差异,与文献中报道BMI增高患者肾损害明显结果不完全一致。考虑其可能的原因是本研究包括CKD 1~4期不同程度eGFR水平的患者,且BMI增高的患者常合并血流动力学改变,早期肾脏血流量增加[17]、肾小球滤过率增加,出现高压力、高灌注和高滤过,影响患者实际eGFR水平,故eGFR在2组间无统计学差异。但持续长期“三高状态”,损伤内皮细胞、上皮细胞等,出现蛋白尿及肾小球肥大、硬化表现,导致肾损害。文献中有报道,BMI增高患者常合并胰岛素抵抗,而胰岛素抵抗[18]可刺激产生多种细胞因子等而导致肾损害,故本研究分析不同BMI 2组患者空腹血糖水平,差异无统计学意义。考虑其可能原因是入组时排除了糖尿病患者,在今后研究中将结合胰岛素水平、糖化蛋白等,分析胰岛素抵抗与慢性肾脏病进展可能的相关性。
总之,不同BMI的慢性肾脏病患者,临床进展危险因素不同。在蛋白尿、血尿酸水平等常见导致肾脏病恶化的危险因素外,BMI增高患者的炎症状态、血脂也与CKD相关,可加重病情恶化,临床应注意控制患者的体重、血脂、炎症状态,有益于延缓CKD进展。
