腐植酸尿素在农业生产和面源污染防控中的研究与应用
2020-09-04薄录吉刘兆辉曲召令王艳芹
薄录吉,李 冰,李 彦*,刘兆辉,曲召令,王艳芹
(1.山东省农业科学院农业资源与环境研究所,农业农村部黄淮海平原农业环境重点实验室,山东省环保肥料工程技术研究中心,山东 济南 250100;2.山东省地矿工程勘察院,山东 济南 250014;3.山东省农业环境保护和农村能源总站,山东 济南 250100)
尿素是我国农业生产上应用最普遍、用量最大的氮肥,施入土壤后,小部分以分子态溶于土壤溶液中,并通过氢键作用被土壤吸附,其他大部分在脲酶的作用下水解成碳酸铵和碳酸氢铵,而土壤中的铵态氮(NH4
+-N)在硝化细菌作用下进一步转化生成硝态氮(NO3--N)。若NH4+-N 和NO3--N 不能及时被作物吸收利用,极易造成氮素损失,如NH4+-N 主要通过氨挥发损失,NO3--N 主要通过淋溶和反硝化损失。研究表明,尿素当季利用率仅为28%~41%,平均为33.7%[1-2],其余大部分通过氨挥发和淋洗等途径损失,不但造成资源浪费,也给环境带来巨大压力。
腐植酸是在复杂地球化学作用下形成的一类大分子芳香族有机化合物,含有羧基、酚羟基、羰基等活性基团[3],这些活性基团可对土壤脲酶活性产生抑制作用,从而减缓尿素在土壤中的分解速度,增强尿素的缓释性能,进而提高尿素的肥效并减少对环境的污染[4-5]。基于此,将尿素与腐植酸通过一定工艺加工形成腐植酸尿素不仅可显著提高氮肥利用率,增加作物对氮的吸收利用,提高作物产量和品质,还可以改善土壤质量,降低氮肥损失[6]。在减肥增效与绿色发展的大形势下,腐植酸尿素在农业生产和面源污染防控中具有广阔的应用前景。本文系统概述了腐植酸的活化方法、腐植酸与尿素反应机理、腐植酸尿素生产工艺及其在农业生产和面源污染防控中的应用进展,为化肥使用零增长行动方案和农业面源污染防控提供参考。
1 腐植酸活化方法
腐植酸活化是指对通过一定手段使腐植酸分子量变小或在分子构架上增加活性基团,以提高其活性的过程,主要是改变腐植酸的分子结构,将难以被植物吸收的腐植酸转变成易被吸收的活性有机质[7],可通过3 种途径实现腐植酸活化[8]:一是增加现有腐植酸分子结构单元上的活性官能团数量;二是提高官能团质量,主要通过引入相关原子或原子团,使官能团呈亲电子或亲核状态,激活或提高某些基团的反应能力;三是切断某些化学键,适当降低反应当量和分子量,将复杂的物质变成简单的物质。完成上述途径有3 种方法,即物理活化法、化学活化法、生物活化法。物理活化法主要有机械活化和超声波活化,化学活化法主要有碱溶酸析法、氧解法、催化法、磺化和磺甲基化法等,生物活化法主要是微生物活化法。上述各种活化方法均能够有效提高活性腐植酸的数量和质量,但在活化提取条件、工艺过程和效果上各有特点[9],具体见表1。
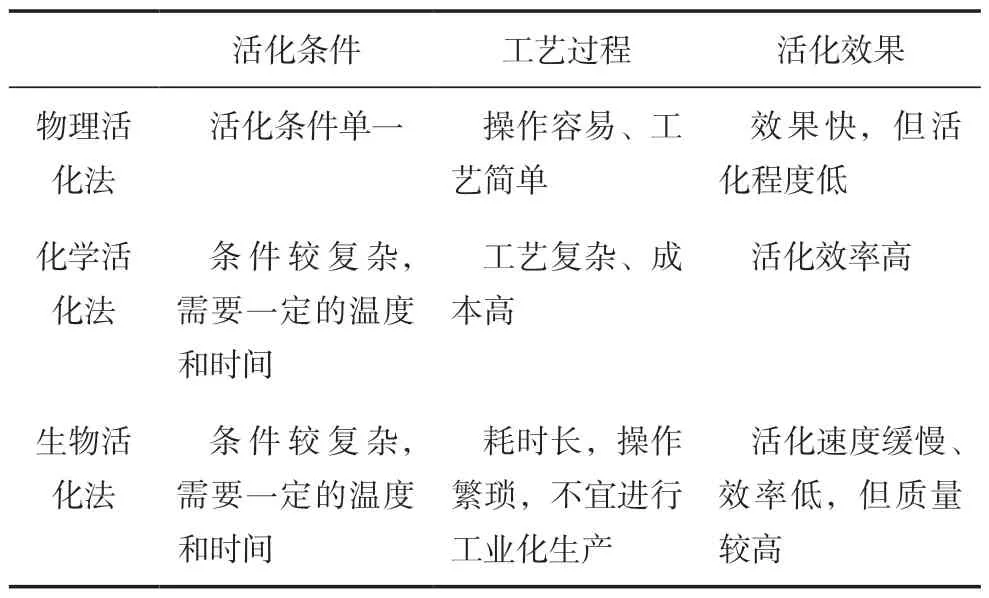
表1 腐植酸活化方法比较
1.1 物理活化法
1.1.1 超声波活化
超声波是一种频率高于20 000 Hz 的声波,穿透能力强,作用于液体时可产生大量小气泡,引发空化效应,空化效应可产生局部高温、高压,促使水分子形成OH 和HO2等自由基。这些含有未配位电子的自由基可直接氧化水溶液中的腐植酸,反应过程为:OH 自由基降解大分子的联结基团,使腐植酸形成小分子碎片,然后HO2自由基继续深入氧化,最终使腐植酸的O/C 和H/C 提高,酚羟基和醌基增加,芳香结构减少,从而达到活化腐植酸的目的[10-12]。
基于上述超声波活化机理,钟世霞等[13]研究发现超声波能够显著提高风化煤中游离腐植酸的产率,且产率与水煤比、超声波功率、超声时间均呈正相关,同时获得了超声波活化风化煤腐植酸的最佳条件,即水煤比8∶1、超声波功率200 W、处理时间25 min,此条件下风化煤中游离腐植酸含量较原风化煤提高6.56 倍。继续提高超声波功率至500 W 和延长活化时间至40 min,风化煤中游离腐植酸含量较原风化煤中提高7.67 倍[14]。樊兴明等[11]利用超声波活化处理泥炭,发现泥炭中水溶性腐植酸含量(黄腐酸)增加了144%。丁方军等[15]研究得出不同的结论,即超声波活化未能活化腐植酸,可能是所选用超声波的波段和频率强度不够所致。
1.1.2 机械活化
机械活化是利用剧烈的机械振动等方式对原料煤进行粉碎,使腐植酸分子的内部结构发生变化,最终促使弱化学键以及烷基支链的断裂,腐植酸分子量变小,溶解性能提高[10]。研究表明,腐植酸在机械的强烈粉碎下会发生轻度氧化降解,含氧官能团数量增加,活性增强[16]。贺文强等[8]发现,将褐煤粉碎至0.180 ~0.250 mm 时难溶于水,粉碎至0.5 μm 则可在水中形成悬浮液,水溶性腐植酸可提高至5%。机械活化相对比较环保,但成本较高,效果有限,通常结合其它方法联合使用[17]。
1.2 化学活化法
1.2.1 碱溶酸析法
碱溶酸析法是利用腐植酸的羧基、酚羟基等含氧功能团与碱类物质反应生成可溶性腐植酸盐并加酸调节pH 值使其固液分离的过程[18]。该反应过程属于离子交换,常用的碱性物质有NaOH、KOH、Na2CO3等,具体流程见图1。

图1 碱溶酸析法工艺流程
陈晓玲[19]以巢湖泥炭为原料研究确定了腐植酸最佳活化工艺,碱液浓度为1.0%的NaOH 和Na2CO3混 合 液(VNaOH:VNa2CO3=1∶1), 固 液 比为1∶10,120℃加热溶解,最后稀硫酸酸化,腐植酸活化率可提高24.9%。邹静等[20]以风化煤为原料,对已有腐植酸活化工艺进行了调整,获得的新工艺:碱液浓度、反应温度、反应时间分别为 浓 度2.0%的NaOH 和Na2CO3混 合 液(VNaOH:VNa2CO3=1∶1)、50℃、60 min,该条件下腐植酸提取产率超过75.9%。王亚军等[21]将碱液浓度(VNaOH:VNH4HCO3= 4∶1)调整为0.5 mol/L,固液比为1∶10,反应温度为90 ~100℃,提取时间为1 h,稀盐酸酸化,该条件下风化煤腐植酸提取率高达86.5%。郭雅妮等[22]以陕西黄陵风化煤为原料,获得腐植酸最佳工艺条件为,18%的盐酸煮沸25 min,碱液(NaOH)浓度为0.8 mol/L,固液比为1∶12,沸水反应时间为60 min。Garcia 等[23]对比了不同碱提取腐植酸的效果,发现焦磷酸铵提取的腐植酸具有官能团多且分子质量小的特点,是较好的提取试剂。
1.2.2 氧解法
腐植酸的活性与其分子量和含氧官能团数量直接相关,氧化主要是增加腐植酸结构中含氧官能团数量,其氧化活化难易程度取决于腐植酸结构,其中,长链脂肪结构、氢化芳香结构以及醚、酯键可被氧化成羰基和羧基结构,芳环中的酚结构氧化成醌[24]。常用氧化剂有HNO3、KMnO4、K2Cr2O7、O3、H2O2、KClO4、Cl2等, 其 中HNO3和Cl2在 常温下具有很强的氧化性,这是因为HNO3和Cl2会生成活性氧原子(2HNO3+H2O →NO2+NO+2H2O+2[O],Cl2+H2O →OCl-+H2Cl →2HCl+[O]), 活性氧原子可将腐植酸分子结构破坏,使其分子质量显著减小,C、H 含量降低,O、N 含量增加[25],芳香环的缩合度和复杂程度降低,羧基含量提高[26]。除常温下的氧化活化外,大部分氧化活化工艺需要结合温度等参数,郭雅妮等[22]利用H2O2活化风化煤腐植酸,获得了最佳活化工艺(H2O2浓度0.9 mol/L、碱液浓度0.5 mol/L、固液比1∶8、反应时间30 min,沸水浴)。周孝菊等[27]利用H2O2进一步研究了不同氧解条件对褐煤腐植酸含量的影响,结果发现,在氧解时间24 h、H2O2浓度20%、液固比0.8 mL/g 条件下,腐植酸和含氧官能团数量增加。
1.2.3 催化法
除碱溶酸析法和氧解法外,催化法也是腐植酸活化的一种重要手段。张水花等[28]以N-Mn-TiO2作为催化剂、H2O2作为氧化剂,对云南曲靖褐煤腐植酸活化进行了探索,结果表明,在催化剂和氧化剂双重作用下,腐植酸羧基含量升高、酚羟基含量降低,黄腐植酸产率提高了32.2%。郭雅妮等[22]在碱溶酸析法的基础上添加催化剂NHPI,获得了陕西黄陵风化煤腐植酸的最佳催化活化工艺(盐酸浓度18%,煮沸25 min,催化剂为NHPI、固液比1∶8、NaOH 浓度为0.5 mol/L、反应温度和时间分别为100℃和30 min),腐植酸活化率可达32.6%~39.6%。马盼等[29]研究了自制Fe2O3/TiO2和FePc(NO2)4/ TiO2复合粒子催化剂对腐植酸活化的影响,总腐植酸的产率分别提高了19.0%~31.3%,游离腐植酸产率提高了7.0%~14.4%。Yang 等[30]研究得出了催化条件下最优活化提取条件,即催化剂为活性碳负载硫酸镍,活化剂为硝酸,固液比为1∶4(g/mL),反应温度为95 ℃,反应时间为80 min。此外,还有其它催化剂,如碳纳米管负载硫酸镍、活性碳负载V2O5、Ce-Ti-Ox/ CNTs 复合粒子、CNTs/Ni/Fe2O3、TiO2、蒙脱石、紫外光等[31-37],这些催化剂在一定条件下也有较好的活化效果。
1.2.4 磺化和磺甲基化法
磺化和磺甲基化法指腐植酸中芳香氢或脂肪氢被磺基(-SO3H)或磺甲基(-CH2SO3H)取代的一种方法[24]。一般认为磺化是发生在醌羰基的间位,磺甲基化则是发生在酚羟基邻位的芳核上,磺化和磺甲基化主要试剂有浓H2SO4、Na2SO3、NaHSO3、CH2O-SO3等。由于风化煤中含有较多羧基且酚羟基少,芳核上未被取代的空位较少,而褐煤和泥炭中的酚结构较多,所以磺化、磺甲基化通常用于褐煤和泥炭腐植酸的活化[16]。
1.3 生物活化法
生物活化是将特殊的菌种接种到腐植酸上,通过微生物的繁殖代谢对腐植酸的结构和官能团产生影响,以此来提高腐植酸的活性[8]。在腐植酸生物活化过程中,棕腐酸羟基、亚甲基和羧基含量减少,黑腐酸芳香度降低、羟基和羧基含量增加。樊兴明等[11]将腐植酸原料、微生物菌及水按照20∶0.2∶100 的质量比例混合后发酵一定时间,黄腐酸含量可增加93.9%~394%。张亚婷等[38]利用溶煤菌株(黄绿青霉XK-b、黄杆菌XK-c)对腐植酸进行活化,发现XK-c 处理后腐植酸活化率达36.34%,XK-b 处理后黄腐酸产率高达66.3%。进一步的研究表明,腐植酸的活化率随着生物菌剂量的增加而增加[39]。
通过对前人的研究结果进行综合分析,发现细菌、真菌和放线菌3 大类微生物均可活化腐植酸(表2),主要机理是微生物分泌到细胞外的碱性物质、螯合剂和表面活性剂、生物酶等对矿源腐植酸进行降解[40]。Quigley 等[41]早在1989 年发现微生物可通过分泌生物胺、多肽及其衍生物等碱性物质活化腐植酸,在此基础上,研究学者进一步发现部分具有耐高温且对蛋白酶不敏感、具有蛋白类似结构的碱性物质,其含有的νN-H、νC=O和δN-H是与腐植酸活化相关的主要功能基团[42];螯合剂作用机理主要是微生物产生的螯合剂可与矿物源腐植酸中的金属离子形成金属螯合物,使大分子结构解体从而达到活化的目的[18];表面活性剂主要通过增加腐植酸表面的亲水性,促进酶的吸附等实现腐植酸活化[43-44];生物酶主要通过打断腐植酸分子的共价键将大分子结构降解[45],生物酶主要包括木素过氧化物酶、锰过氧化物酶、漆酶等氧化酶和酯酶等非氧化酶[46]。一般情况下,单一微生物种类活化微生物能力有限,通常是多种微生物协同对腐植酸进行活化,所以腐植酸生物活化也是多种机理共同作用的结果。

表2 活化腐植酸的微生物种类
2 腐植酸与尿素相互作用机理
国外早在20 世纪70 年代就开展了腐植酸与尿素反应的机理研究,梁宗存等[5]在90 年代对两者的主要反应机理进行了详细评述,认为主要有3 种作用机理:非交换吸附假说、氢键和自由基反应假说、络合假说和羰(醛)基亲核加成假说。非交换吸附假说认为腐植酸从尿素溶液中以非交换吸附固定氮,这个过程主要是由腐植酸大分子的外围部分桥键实现的,属于化学吸附;氢键和自由基反应假说主要基于红外光谱分析和ESR 验证,反应过程中氢键和自由基起到主要作用;络合假说主要基于腐植酸中羧基和酚羟基与尿素反应过程中产物的状态提出的;羰(醛)基亲核加成假说主要基于有机含氮碱类物质与腐植酸反应提出的,该反应过程中氮的当量恰好与腐植酸中的羰(醛)基氧当量相近,由此认为腐植酸与含氮碱反应在羰(醛)上进行。
在上述研究的基础上,武丽萍等[55]采用化学与波谱结合的方法对包裹型腐植酸尿素进行了化学组成结构方面的机理研究,包裹型腐植酸尿素由游离尿素颗粒核心和表面反应层组成,主要特征是腐植酸在尿素表面形成一层较稳定的包膜,腐植酸尿素的抗压强度比普通尿素提高了48.0%,同时还有少量活性腐植酸渗入尿素颗粒孔隙中,反应过程中出现了三键和双键破坏、稳定性复合物形成、碳链缩短、双键结构增加等变化[56],主要机理包括腐植酸羧基与尿素酰胺基发生的离子交换反应、氢键缔合形成的化学吸附及形成稳定的自由基、腐植酸的渗透形成的物理吸附[55]。
3 腐植酸尿素生产工艺
由于腐植酸在农业应用上的优势及腐植酸尿素的广阔应用前景,国内外对腐植酸尿素的生产工艺开展了广泛的研究,目前腐植酸尿素生产工艺方法可以概括为以下几种:溶剂法,包裹法,热熔法。
3.1 溶剂法
溶剂法主要有两种工艺,一是以有机溶剂为介质生产腐植酸尿素,该工艺最早由日本学者在20世纪60 年代(日本特许公告348375 和348376)提出,主要以液氨和甲醇、乙醇、丙酮等有机溶剂为介质,在高温高压条件下制备腐植酸尿素;在此基础上,日本学者继续改进工艺,提供了一种在腐植酸溶液中加入尿素、甲醛和腐植酸进行缩聚制备腐植酸尿素甲醛缩合物的方法。但是,上述工艺需采用常规化工高压设备,反应条件较为苛刻,生产中加入了有害有机溶剂,而且生产成本比较高,均未实现工业化绿色清洁生产[4,6,57]。
第二种工艺方法是以水为溶剂制备腐植酸尿素,该工艺由中国科学院山西煤炭化学研究所和江苏省通州市合作开发,特点是工艺条件温和,用水和少量添加剂作介质,常压、反应温度为90 ~100 ℃,该工艺降低了缩二脲的生成、减少了环境污染,同时还应用于实际生产,建立了年产6 000 t 的中试生产装置[57-58],具体工艺流程见图2。在该工艺的基础上,程亮等[59]研究了低温条件下腐植酸尿素的制备工艺,获得了最佳工艺参数:以水为溶剂,以纳米腐植酸和尿素为原料,反应温度47.6 ℃,反应时间1.81 h,活化剂为质量浓度是50%的十二烷基硫酸钠,固液体摩尔比9∶1,络合剂浓度0.14 mol/L,腐植酸尿素产率达到90.6%。该工艺条件下腐植酸尿素粒度大小均匀且分散性良好,粒径为70 ~90 nm,比表面积189.85 m2/g,平均孔径10.2 nm,孔容0.86 cm3/g,具有较高热稳定性。
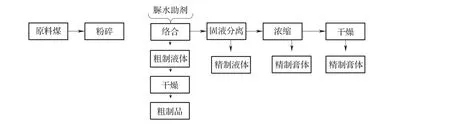
图2 以水为溶剂制备腐植酸尿素的工艺流程
3.2 热熔法
热熔法指尿素在熔融状态下加入腐植酸或腐植酸盐,混合后得到腐植酸尿素。国内有较好的技术储备,如中国专利CN102260112A 公布了一种在尿素熔融液介质中制备腐植酸尿素络合物的方法,该方法是将尿素放入反应器中,搅拌加热至熔融后加入腐植酸,继续搅拌10 ~90 min 制的固体腐植酸尿素[60],该工艺生产流程短、设备操作简便,易于连续生产,无污染排放。中国专利CN109369306A 和CN102584498A 公布了一种腐植酸尿素的制备方法,该方法采用腐植酸产品与熔融尿素为原料,经动态混合反应后可造粒得到腐植酸尿素[61-62],所述方法具有操作简便、能耗低、成本低,而且腐植酸与尿素反应充分,生成的腐植酸尿素稳定性好,可连续性、大规模生产,对环境友好,无三废排放等特点。具体工艺流程见图3。虽然热熔法腐植酸与尿素反应充分、腐植酸尿素产率较高,但氮损失较多,且容易形成缩二脲,这些是实际生产中需要注意的问题。

图3 腐植酸尿素熔融制备方法
针对上述问题,林海涛等[6]优化了工艺,有效避免了氮损失和缩二脲的形成,具体工艺为:将风化煤(0.30 mm)与尿素(0.15 mm)以1∶1 的比例在混合机内充分混合均匀,之后投入反应器内,在额定时间内经额定温度加热完成反应,反应结束物料温度为80 ~85℃,物料自然冷却后粉碎造粒得到腐植酸尿素(图4)。该工艺特点是腐植酸与尿素经在反应器中以干法形式直接进行络合反应,摒弃了传统釜式反应器的缺点,做到了腐植酸尿素的连续投料、出料,解决了造粒和烘干的难题,腐植酸尿素络合率高(络合态氮含量大于20%),整套工艺设计简捷,设备造价低。

图4 改进型热熔法腐植酸尿素生产工艺流程
3.3 包裹法
腐植酸尿素包裹工艺指在具有一定黏性的黏结剂作用下将腐植酸包裹在尿素表面形成一层较稳定的半透性包裹膜。该方法优点是不需要高温,氮损失少,无缩二脲形成,但由于腐植酸仅在尿素表面包涂,腐植酸尿素中络合态氮一般不超过10%。武丽萍等[55]采用机械振荡和滚动方式将活化腐植酸包涂在尿素颗粒表面,其中活性腐植酸与尿素的配比分别为2.5∶97.5 和20∶80,经静置、渗透、干燥后制得两种包裹型腐植酸尿素。姜剑平等[63]研究了不同包涂比[尿素与腐植酸比例100∶(2.5 ~10)]、不同包涂方法(阶梯圆盘反应包裹、搅拌包裹、改良转鼓包裹)、不同添加剂(促进剂、辅助脲酶抑制剂)、不同干燥温度、不同烘干方式(回转烘干、复合振动立式烘干)等工艺参数对腐植酸尿素产品的影响,最后确定了最佳工艺流程(图5),明确了具体工艺参数,即腐植酸适宜用量为尿素量的5%~20%,包涂方法为改良转鼓方式,烘干方式为40 ~50 ℃条件下的复合振动立式烘干。

图5 传统包裹法腐植酸尿素生产工艺流程
4 腐植酸尿素在农业生产中的应用
4.1 腐植酸尿素在粮食作物上的应用
腐植酸尿素对主要粮食作物产量及氮素利用率的影响见表3,从表中可以看出,与尿素处理相比,腐植酸尿素处理小麦、玉米、水稻和马铃薯产量分别提高12.1%、11.6%、5.4%和24.7%,腐植酸尿素处理小麦、玉米和水稻氮素利用率分别提高16.9%、16.6%和10.1%。腐植酸尿素对马铃薯的增加效果最佳,其次是小麦、玉米、水稻,这可能是由于腐植酸尿素旱地更容易发挥其缓释功能,增加肥效,而水的存在加快腐植酸尿素的分解。在氮素利用率方面,腐植酸尿素处理氮素利用率显著高于尿素处理。与尿素处理相比,腐植酸尿素处理小麦和玉米氮素利用率提高数量接近。除此以外,腐植酸尿素处理还可显著改善玉米品质,如提高玉米粗蛋白和精蛋白含量[64]。
4.2 腐植酸尿素在经济作物上的应用
腐植酸尿素对经济作物产量及氮素利用率的影响见表4,从表中可以看出,与尿素处理相比,腐植酸尿素处理棉花、甘蔗、甘薯和花生产量分别提高8.5%、18.4%、21.1%和15.6%,腐植酸尿素处理棉花和甘蔗氮素利用率分别提高12.5%和8.6%。在作物生长方面,腐植酸尿素处理可显著增加根系干重,促进不定根向贮藏根分化,提高根系总活力、总根长、根直径、根表面积、根体积、根系超氧化物歧化酶、过氧化物酶和过氧化氢酶的活性,增加根系可溶性蛋白质含量,降低丙二醛含量[81];在品质方面,腐植酸尿素处理甘蔗糖分、理论糖产量和净收益分别比尿素处理高1.24%、3 430 kg/hm2和4 458 元/hm2[82]。
4.3 腐植酸尿素在蔬菜作物上的应用
腐植酸尿素对蔬菜作物产量及氮素利用率的影响见表5,从表中可以看出,与尿素处理相比,腐植酸尿素处理黄瓜、大葱、番茄、夏阳菜、蒜薹和蒜头产量分别提高29.7%、15.7%、4.83%、18.1%、55.7%和5.8%,腐植酸尿素处理黄瓜和大葱氮素利用率分别提高15.0%和16.7%。在品质方面,腐植酸尿素可显著提高蔬菜Vc 含量、蛋白质含量和姜辣素含量,降低硝酸盐含量[87-88],同时还能提高夏阳菜包棵率,降低蔬菜发病率[89]。
4.4 腐植酸尿素在果树生产中的应用
腐植酸尿素对果树产量、品质及氮素利用率的影响见表6,从表中可以看出,与尿素处理相比,腐植酸尿素处理苹果、梨和哈密瓜产量分别提高10.7%、14.2%和11.1%,腐植酸尿素处理哈密瓜氮素利用率提高9.2%。除对产量和氮素利用率影响以外,腐植酸尿素还能显著提高水果品质,从外观形貌看,腐植酸尿素处理水果优级果产率比尿素处理分别提高9.4%~13.3%[6],从营养角度看,腐植酸尿素处理可提高水果边糖、心糖和Vc 含量,降低糖梯度[90]。

表3 腐植酸尿素对主要粮食作物产量及氮素利用率的影响
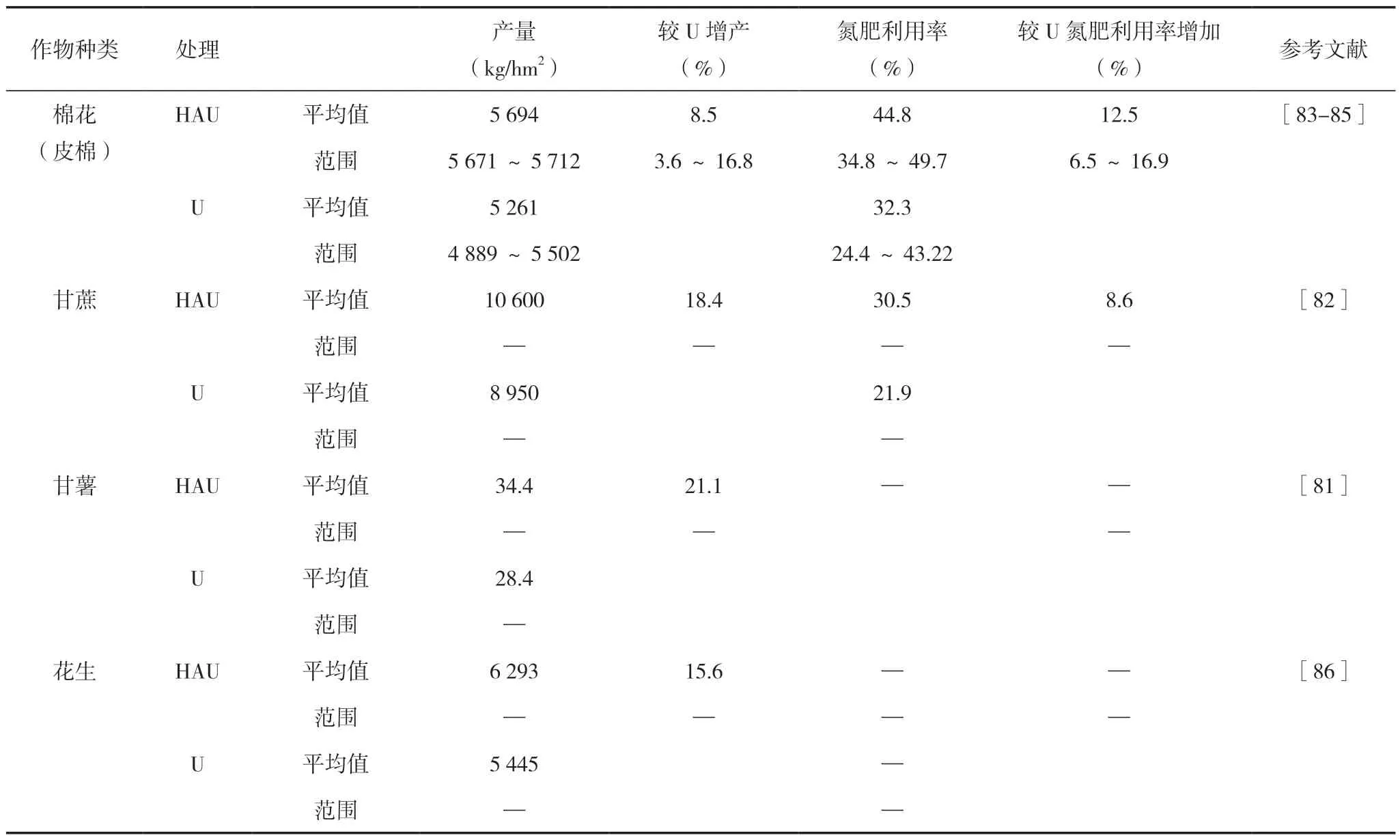
表4 腐植酸尿素对经济作物产量及氮素利用率的影响
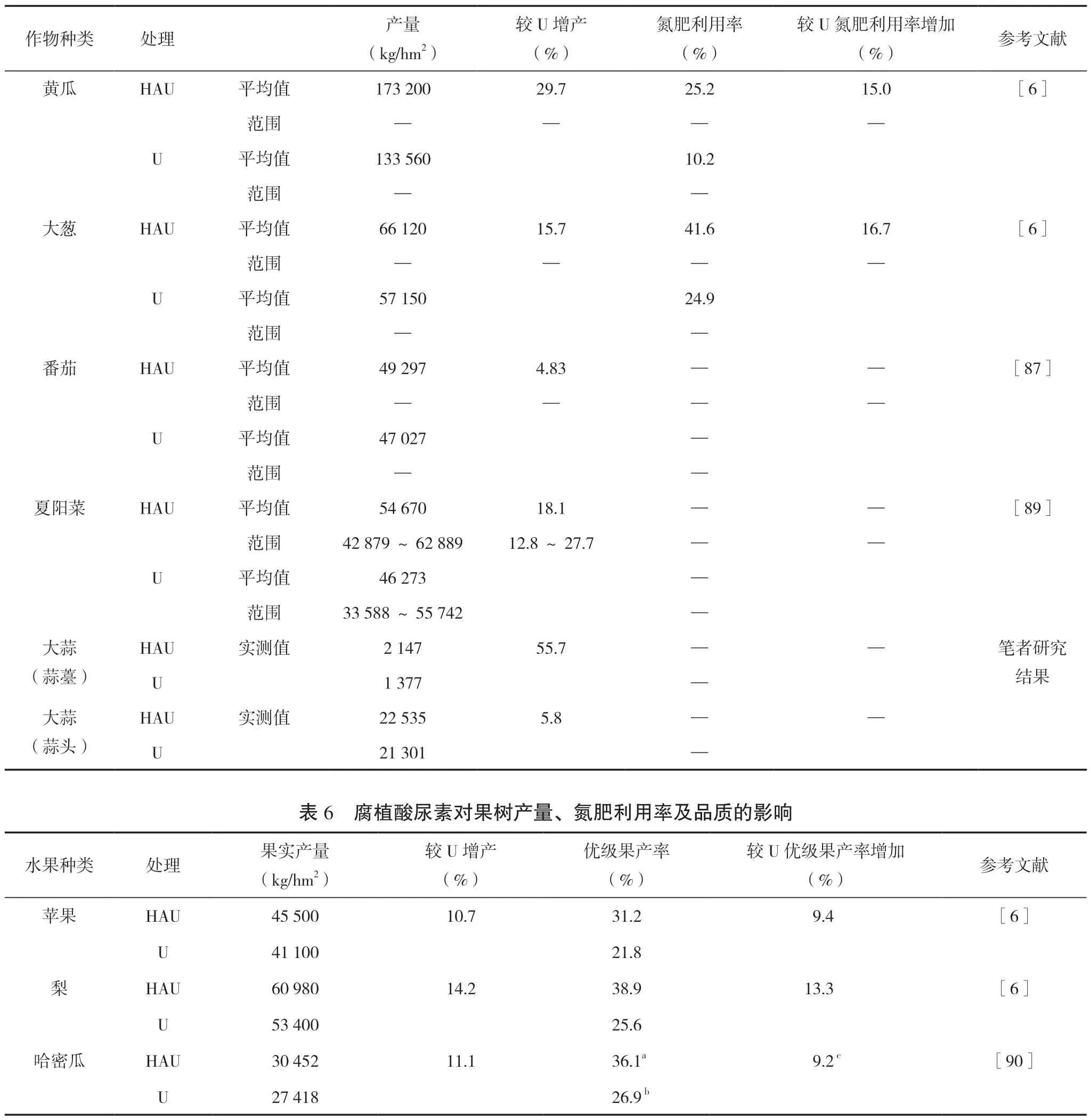
表5 腐植酸尿素对蔬菜产量及氮素利用率的影响
5 腐植酸尿素在农业面源污染防控中的应用
腐植酸尿素在农田生产应用过程中表现出较好的增产效果,氮肥利用率也有较大的提升,从另一方面也说明腐植酸尿素的应用大大降低了氮在环境中的排放和农业面源污染发生机率,大量的研究也证实了这一结果[6,91-97]。在控制氨挥发排放方面,与普通尿素相比,腐植酸尿素对氨挥发的抑制率达33.3%~59.2%[91-92,94-95],一方面是因为腐植酸具有脲酶抑制剂的作用,可降低土壤脲酶活性,抑制尿素水解,从而降低氨挥发[98];另一方面,尿素水解产生的NH4+可与腐植酸结合生成稳定的腐植酸铵盐,从而降低氨挥发[96]。也有学者得出相反的结果,腐植酸尿素并未降低氨挥发[99],在一定程度上增加了氨挥发[74],这可能与腐植酸类型和腐植酸用量不同有较大关系。在氮淋溶控制方面,柱状淋溶试验结果表明,腐植酸尿素处理氮淋失量比尿素处理降低6.7%~28.3%[93,95];田间试验结果表明,腐植酸尿素处理氮淋失量比尿素处理降低25.3 ~10.9 kg/hm2(17.9%~56.1%)[6],笔者所在团队近年的研究结果表明,大蒜-玉米周年轮作腐植酸尿素处理全氮和全磷淋失量分别比尿素处理减少12.3 和0.38 kg/hm2,氮磷流失防控效果显著。此外,腐植酸尿素0 ~40 cm 土壤铵态氮和硝态氮含量低于尿素处理而40 ~60 cm 土壤铵态氮和硝态氮含量高于尿素处理也说明腐植酸尿素可有效控制氮素向地下淋溶[74]。在反硝化气体排放控制方面,腐植酸尿素可显著降低N2O 排放,平均降幅69.0%[74,91]。
6 展望
随着2015 年农业农村部发布《到2020 年化肥使用量零增长行动方案》,减肥增效已成为我国农业绿色高质量发展的一个重要突破口。腐植酸尿素因其独特的优势,必将为农业转型升级注入新的活力,尽管如此,腐植酸尿素的生产及其在农业生产和面源污染防控方面的应用、推广仍存在许多问题。
(1)腐植酸的活化及其与尿素结合后的有效性。首先,腐植酸主要来源于草炭、风化煤和褐煤等低阶煤,分子量较大[100],多数是难溶且难直接发挥作用。因此,腐植酸的有效活化是其肥料化的前提,目前腐植酸活化方法较多,但单一活化能力有限或存在一定缺陷,下一步需要加强腐植酸单一活化技术向联合活化技术的研发。其次,从成本和功效等方面看,腐植酸尿素中腐植酸含量和浓度不是越大越好,需要加强腐植酸用量与作物类型匹配度方面的研究。
(2)腐植酸尿素的生产工艺。总体来看,腐植酸尿素的生产工艺比较健全,但在实际生产过程中仍存在许多不成熟的地方,而且评价体系及生产体系缺乏统一标准,应尽快研发制定腐植酸尿素生产工艺方面的系列标准。
(3)腐植酸尿素的应用推广。应充分利用腐植酸的优势,加快腐植酸尿素产业化进程,以适应绿色农业高质量发展的需求。此外,进一步加强腐植酸尿素在其它农作物上的效果研究,同时注重腐植酸尿素在土壤质量提升和环境保护中的研究与应用。
