鸡传染性支气管炎病毒种子批的建立
2020-08-31汪宏才汪辉王红琳
汪宏才 汪辉 王红琳


摘要:为保证传染性支气管炎抗原的质量,测定了3种不同来源的传染性支气管炎病毒株的EID50,选取滴度最高的病毒株作为毒种,建立了传染性支气管炎病毒WH株种子批,并对冻干毒种进行了毒价测定。结果表明, 含毒尿囊液在冻干前后毒价无显著性差异,毒种的EID50在10代内无变化。冻干毒种在-40 ℃和-15 ℃保存1年,其毒价基本不变。经检验种子批未受到细菌及其他微生物的污染。
关键词:传染性支气管炎;WH株;种子批
中图分类号:S852.5 文献标识码:A
文章编号:0439-8114(2020)10-0120-003
DOI:10.14088/j.cnki.issn0439-8114.2020.10.028 开放科学(资源服务)标识码(OSID):
Abstract: In order to ensure the quality of infectious bronchitis antigen, the EID50 of infectious bronchitis virus strains from three sources were determined and the virus strains with high titer as virus species were selected, and the seed batch of infectious bronchitis virus WH strain were established. The poison value of freeze-dried seed poison was determined. The results showed that there was no significant difference in the poison value of toxic allantoic fluid before and after freeze-drying, and the EID50 of the virus had no change within 10 generations. The poison value of freeze-dried seed poison remained basically unchanged when it was stored at -40 ℃ and -15 ℃ for one year. The seed batch was not contaminated by bacteria and other microorganisms.
Key words: infectious bronchitis; WH strain; seed batch
雞新城疫(Newcastle Disease, ND)和鸡传染性支气管炎(Infectious Bronchitis, IB)是影响地方鸡的两种主要病毒性疾病[1],造成雏鸡成活率、成鸡产蛋率严重下降。为降低ND、IB对中国养禽业的影响,减少免疫次数,降低免疫成本,开展鸡ND、IB二联活疫苗的研制。ND采用耐热无毒的HB92株,该毒株具有免疫鸡能将疫苗毒传给同群非免疫鸡的自然传播性等特性[2]。禽传染性支气管炎病毒WH株是湖北省农业科学院畜牧兽医研究所自行分离的IBV毒株。进化分析表明,该毒株与M41株、H120株以及H52株属于同一分支,因此也属于Massachusetts型。为建立鸡传染性支气管炎WH株种子批系统,按照2015版《中国兽药典》的相关规定,结合IB最新研究进展和方法,对毒种的含量、毒力、安全、效力检验与无菌检验等进行了试验,为生产合格的鸡新城疫、传染性支气管炎二联活疫苗的生产奠定基础。
1 材料与方法
1.1 材料
1.1.1 主要材料 IBV毒种1号为冻干毒, EID50为10-7.1/0.1 mL;2号为SPF鸡胚尿囊液毒,EID50为 10-6.9/0.1 mL;3号为气管、肾脏混合组织毒,未进行EID50的测定。1~3号毒种全部置于-80 ℃超低温冰箱冷冻保存。SPF鸡胚购于北京梅里亚维通实验动物技术有限公司。试验用雏鸡是使用SPF种蛋自行孵化,并在禽用隔离器中饲养。
1.1.2 主要试剂与设备 检验培养基购自海博生物技术有限公司,禽白血病检测试剂盒购自IDEXX公司。毒种冻干使用美国LABCONCO冻干机,ELISA检测使用Thermo MK3酶标仪。
1.2 方法
1.2.1 IBV毒种预处理 1号毒种加入适量无菌PBS溶液进行复原。2号毒种为尿囊液毒种,解冻后直接使用。3号毒种是组织毒,将混合组织剪碎后,置于2 mL无菌EP管中,加入适量PBS溶液进行组织捣碎,3 000 r/min离心10 min后取上清,0.22 μm滤膜过滤后备用。
1.2.2 IBV WH株EID50测定 参考文献[3],分别将3种经过预处理的毒种,用无菌PBS溶液进行10倍系列稀释,分别吸取10-5、10-6、10-7、10-8 4个稀释度,每个稀释度分别尿囊腔接种9~11 d SPF鸡胚5枚,每胚0.1 mL置于孵化器中,37 ℃进行孵化,记录其鸡胚死亡情况,24 h内死亡鸡胚不计,144 h内死亡的鸡胚随时取出,置于4 ℃保存。至144 h取出所有胚,解剖未死亡鸡胚,观察致侏儒情况,统计后计算EID50,将EID50最大的毒株作为建立种子批的毒种。
1.2.3 IBV WH株种子批冻干 将EID50最大毒株用无菌PBS溶液进行10-2稀释,尿囊腔接种9~10日龄SPF鸡胚15枚,0.1 mL/胚,弃去24 h内死胚,收获32~36 h SPF鸡胚尿囊液,加入适量蔗糖牛奶作为冻干保护剂,按一定比例混匀后进行冷冻干燥。
1.2.4 冻干品EID50的测定 将冻干后的WH株,随机抽取3瓶,分别加入适量PBS溶液复原,然后按照“1.2.2”的方法测定EID50。
1.2.5 安全性检测 将冻干品随机抽取1瓶,用生理盐水稀释至105.0EID50。选取1日龄、30日龄、60日龄的健康易感鸡各10只, 分别滴鼻1滴(约0.03 mL),检验毒株对不同日龄SPF鸡的安全性。试验鸡应全部健康,无呼吸异常及神经症状。
1.2.6 特异性检验 根据冻干后病毒含量的测定结果,用生理盐水稀释至10-3.5EID50/0.1 mL,与等量抗IBV特异性血清混和均匀,在室温下作用1 h后,尿囊腔内接种10日龄SPF鸡胚10枚,每胚0.2 mL。置于37 ℃下观察24~144 h,应不引起特异性死亡及鸡胚病变,至少有8个以上鸡胚健活。
1.2.7 保存期试验 将WH株冻干品随机抽取若干支,分成两组,分别置于-40、-15 ℃冰箱保存180、365 d,分别测定其EID50。
1.2.8 毒种纯净性检验 按《中国兽药典》[4]2015版附录的规定,对种子批进行无菌检验,结合分子生物学方法,进行支原体检验和外源病毒检验[5-7]。
1.2.9 毒种的传代 将WH株冻干毒,用无菌PBS溶液复原后,按10-2进行稀释后,接种10日龄SPF鸡胚3枚,置于37 ℃进行孵化,弃去24 h死亡鸡胚,收获36 h尿囊液,置于-80 ℃冻存。按该法进行传代至15代,分别抽取5、10、15代,按“1.2.2”进行病毒含量测定,选取病毒含量大于10-7.0EID50/0.1 mL的病毒代次作为最高代次。
2 结果与分析
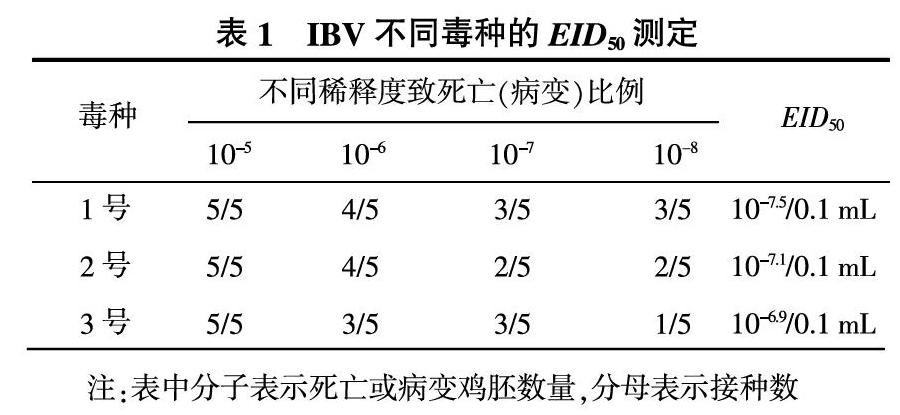
2.1 IBV WH株的EID50测定结果
根据病毒含量的测定结果(表1), 1~3号IBV毒株的EID50分别为10-7.5/0.1 mL、10-7.1/0.1 mL和 10-6.9/0.1 mL,1号毒株的病毒含量最高,因此选用1号毒种作为种子批的毒株。
2.2 IBV WH株种子批的冻干
将1号毒种接种SPF鸡胚后,无菌收获尿囊液,加入蔗糖牛奶保护剂后,分装于西林瓶中进行真空干燥,2 mL/瓶,按照2015版《中国兽药典》附录中物理性状检验要求,冻干完成后进行物理性状、 真空度、 剩余水分等项目检测, 结果符合要求(表2)。
2.3 冻干品病毒含量的测定
冻干后IBV WH株随机抽检3瓶进行病毒含量的测定,结果分别为10-7.3EID50/0.1 mL、10-7.5EID50/0.1 mL和10-7.5EID50/0.1 mL,经t检验,与冻干前病毒含量(10-7.5EID50/0.1 mL)相比,无显著性差异(P>0.05)。
2.4 冻干品的安全性检验
3组试验组观察至14 d,全部表现正常,无明显临床反应,结果符合要求(表3)。
2.5特异性试验
观察至144 h,10枚SPF鸡胚未出现死亡。解剖发现鸡胚大小正常,无侏儒胚、无肉眼可见病变。
2.6 保存期试验
将WH株冻干品分别置于-40 ℃和-15 ℃保存180 d和365 d,其病毒含量无明显变化(表4)。
2.7 毒种纯净性检验
毒种接种TG、TSB培养基,观察7 d,均无细菌、无霉菌生长,结果合格(表5)。接种支原体培养基,移植3代后WH株冻干毒均呈阴性(表6)。新城疫病毒、禽白血病病毒和禽网状内皮组织综合症病毒检测结果也均为阴性(表7)。
2.8 毒种传代情况
IBV WH株冻干毒经SPF鸡胚传代后, 测定第5代、第10代和第15代毒种的病毒含量分别为10-7.5EID50/0.1 mL、10-7.3EID50/0.1 mL和10-6.9EID50/0.1 mL(表8),选取大于10-7.0EID50/0.1 mL的代次作为最高代次,因此将毒种传代次数限制在10代以内。
3 结论
通过对3种鸡传染性支气管炎病毒株的毒力检测,筛选出1株滴度高、毒力稳定、安全性好的WH株。对冻干种子批进行了检测,各项指标符合《中国兽药典》的要求,可以作为鸡新城疫、传染性支气管炎二联疫苗生产的种子批。
参考文献:
[1] 杨 峻, 罗青平, 温国元, 等. 湖北省地方鸡主要疾病流行病学调查[J]. 湖北农业科学, 2013,52(17):4164-4166, 4174.
[2] 杨 峻, 黎秋华, 邵华斌. 鸡新城疫病毒HB92株生物学特性研究(Ⅲ)——最小免疫剂量及免疫期试验[J]. 湖北畜牧兽医, 1996(3):11-12.
[3] 王新卫, 贾文科, 王泽霖, 等. 传染性支气管炎病毒M41株种子批的建立[J]. 安徽农业科学, 2008,36(9):3663-3664, 3729.
[4] 中国兽药典委员会. 中华人民共和国兽药典(2015年版)三部[M]. 北京: 中国农业出版社, 2016.
[5] 畢玉彧, 管子言, 黄晓姣, 等. 部分种鸡场常用活疫苗中ALV的PCR检测[J]. 广西畜牧兽医, 2014(4):171-174.
[6] 楚电峰, 杜元钊, 冯嫣芳, 等. 家禽活疫苗中禽白血病病毒污染检测方法比较[J]. 中国动物检疫, 2017(8):108-113.
[7] 胡晓苗, 张丹俊, 侯宏艳, 等. 活毒疫苗中禽白血病病毒污染的检测方法探讨[J]. 安徽农业科学, 2013, 41(26):10669-10670, 10725.
