帕金森病运动并发症中西医结合诊治专家共识(2020)
2020-08-27帕金森病运动并发症中西医结合诊治专家共识写作组
帕金森病运动并发症中西医结合诊治专家共识写作组
帕金森病(Parkinson disease,PD)是一种中老年人常见的神经系统退行性疾病。主要临床症状包括运动迟缓、静止性震颤、肌强直等运动症状和嗅觉减退、便秘、抑郁等非运动症状[1]。左旋多巴替代治疗是其最主要的临床治疗方法,贯穿疾病全程,该药物在PD晚期可诱发运动并发症,增加疾病的致残性进而影响患者的生活质量,成为PD治疗的重点与难点[2]。PD运动并发症是指随着疾病进展和药物治疗而出现的临床异常表现,主要类型包括运动波动和异动症[3]。
中西医在PD运动并发症的诊疗中各有优势,但尚未形成统一共识。为了提高PD诊疗水平,充分发挥中西医诊疗PD运动并发症的优势,更好地指导我国PD的临床实践,上海中西医结合学会神经系统慢病管理专业委员会(筹)组织国内中西医领域从事PD和脑病研究的专家,在以往中国PD治疗指南[2,4-5]基础上,综合近年来PD运动并发症最新循证医学证据[6-9],参考国内中西医结合的常用疗法,结合专家临床经验,充分考虑疗效、风险及经济等多方面因素进而形成此专家共识。此共识仅为学术性指导建议,在临床实践中,应结合患者和医疗的具体情况,进行中西医结合的个体化诊疗。
1 流行病学及危险因素
我国PD患者运动并发症中“剂末”现象和异动症的发生率分别为46.5%和10.3%[10]。其发生受多种因素影响,依据目前研究现状,可将其危险因素分为可控和不可控因素,前者包括药物使用的起始时间、种类和方式等,后者包括年龄、性别和临床亚型等[11-12]。
2 临床分型
2.1 运动波动运动波动指随着疾病的进展以及药物的长期治疗,患者对药物产生波动性反应,依据其临床表现与给药周期的关系,可分为“剂末”现象、“开”期延迟或无“开”期、“开-关”现象和“冻结”步态4型。
2.1.1“剂末”现象:这是PD治疗中最常见且最早出现的运动并发症,指患者对一剂多巴胺能药物的反应在服用下一剂药物之前会减弱(通常少于4 h),并出现相应的运动症状(如运动迟缓、震颤、僵硬以及起坐困难等)或非运动症状(如疼痛、感觉异常、抑郁、焦虑、静坐不能以及重复刻板动作等)。再次给药后上述症状明显缓解(有时仅持续1~2 h)[3]。“剂末”现象中症状的波动与给药周期相关,可以预测。
2.1.2“开”期延迟或无“开”期:指一些中晚期PD患者服用原剂量的多巴胺能药物时,出现症状改善启动时间延迟或无症状改善的现象[3]。“开”期延迟或无“开”期症状的波动与给药周期无关,而与药物吸收情况有关,较难预测。
2.1.3“开-关”现象:指患者对药物产生不可预测的“开”或“关”反应,表现为在下一次服药之前,会毫无征兆地突发运动功能“关”的症状,患者在“关”时处于严重运动不能,而在“开”时常伴异动。“开-关”现象中症状的波动与给药周期无关,不可预测[3]。
2.1.4“冻结”步态:指患者在起步、转弯以及接近目标/即将到达目的地时突然出现某些异常的下肢运动阻滞动作。根据发病与服药周期的关系,可分为“开期”冻结和“关期”冻结。根据对药物的反应,可分为多巴胺反应性冻结、多巴胺抵抗性冻结和多巴胺诱导性冻结[3,6-9]。
2.2 异动症异动症指PD患者出现舞蹈样、投掷样和肌张力障碍等刻板重复的不自主运动。多起始于症状严重侧下肢远端,并逐渐影响四肢和躯干[3,11-12]。依据其临床表现以及与药物浓度(突触间隙多巴胺浓度)的关系,可分为剂峰异动、“关期”肌张力障碍和双相性异动3型。
2.2.1剂峰异动:最常见,指在药物浓度达到高峰时,出现头颈部(头部来回摇摆)、躯干和四肢舞蹈样、投掷样以及肌张力障碍等不自主动作,偶可累及呼吸肌。其临床表现模式为帕金森症状-症状改善-异动-症状改善-帕金森症状(Parkinsonism-improvement-dyskinesia-improvement-Parkinsonism, I-D-I),异动症状多于服药30 min后出现,持续约1~3 h[3]。
2.2.2“关期”肌张力障碍:指在药物浓度降至低谷时出现受累严重一侧肢体足趾伸展或屈曲,跖屈曲内收变形,伴明显肌痉挛性疼痛,通常在夜间或清晨发生[3]。
2.2.3双相性异动:指在药物浓度尚未达到高峰以及药物浓度尚未降至低谷时,出现以下肢(下半身)舞蹈样或徐动样为主的不自主运动,会出现刻板重复的奇异步态,继之发展为“关期”肌张力障碍伴足趾疼痛,其临床表现模式为帕金森症状-异动症状-改善-异动症状-帕金森症状(Parkinsonism-dyskinesia-improvement-dyskinesia-Parkinsonism, D-I-D)的双相特征。异动症状多在服药15 min后出现,持续15 min左右[3,6-12]。
3 西医临床治疗策略
PD运动并发症的西医治疗应遵循“预防为主,诊治并重”原则,治疗中应兼顾改善运动症状和延缓运动并发症的发生,推荐“一保、双控”治疗理念[12]。“一保”是指在PD全程治疗中始终以保证患者的生活质量为目标;“双控”是指在全程治疗中双重监控运动并发症的发生风险与用药方案。对运动并发症发生风险较高的患者,临床选择药物及剂量均应谨慎,药物选择倾向于多巴胺受体激动剂、单胺氧化酶-B(MAO-B)抑制剂或小剂量左旋多巴;对运动并发症发生风险较低的患者,临床用药应足量,建议选择左旋多巴及其他多巴胺能药物,从而最大程度地改善患者的运动及非运动症状,以提高患者的生活质量。对于已发生运动并发症的患者,西医治疗应在遵循《2014年中国帕金森病治疗指南(第三版)》的基础上,结合患者具体情况给予个体化治疗[5](图1)。各分型治疗推荐意见如下阐述。
3.1 运动波动
3.1.1“剂末”现象:(1)添加儿茶酚-O-甲基转移酶(COMT)抑制剂[6-9]如恩他卡朋及左旋多巴/卡比多巴/恩他卡朋(LCE)。
(2)调整左旋多巴的给药间隔:缩短左旋多巴给药间隔,应在前一剂作用消失之前给予下一剂药物,同时药物的每日总剂量需要酌情增加。
(3)添加或更换不同类型的多巴胺受体激动剂:逐渐增加多巴胺受体激动剂剂量至达到满意疗效且不出现副作用为止,如吡贝地尔、普拉克索、罗替戈汀、罗匹尼罗等。
(4)添加MAO-B抑制剂:雷沙吉兰可以延长“开”期,缩短“关”期,减少运动波动。司来吉兰缺乏循证证据,但临床治疗“剂末”现象有效[6-9]。
(5)改用左旋多巴控释剂:左旋多巴控释剂在出现“剂末”现象早期使用作用明显,但其生物利用度低,需增加药物剂量20%~30%。
(6)可加用金刚烷胺或苯海索。
(7)经药物调整,治疗效果仍不满意者,可行外科手术治疗。苍白球内侧核(GPi)脑深部电刺激(deep brain stimulation,DBS)手术和丘脑底核(STN)DBS均有效。此外,单侧苍白球损毁术对“剂末”现象亦有疗效。
3.1.2“开期”延迟或无“开期”:(1)首先判断是否存在药物间的相互作用。口服铁剂、含铝/镁的抗酸剂、维生素B6和降脂药物均会降低左旋多巴的生物利用度,进而降低疗效。
(2)停用抗胆碱能药物,如苯海索。
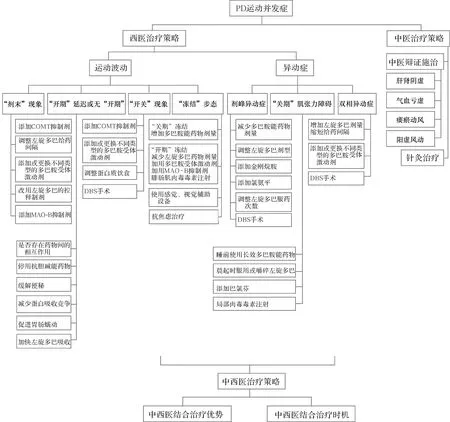
注:PD:帕金森病;MAO-B:单胺氧化酶-B;COMT:儿茶酚-O-甲基转移酶;DBS:脑深部电刺激图1 PD运动并发症的中西医结合治疗策略
(3)缓解便秘,如采用高纤维饮食及服用乳果糖等泻药。
(4)减少饮食中高蛋白、高脂肪的摄入,可尝试饭前1 h或饭后2 h服用左旋多巴制剂。
(5)促进胃肠道蠕动,多潘立酮可促进胃排空,但应注意多潘立酮的不良反应。
(6)加快左旋多巴吸收,可将左旋多巴制剂溶于维生素C溶液或碳酸饮料中服用,也可嚼碎后吞服。
3.1.3“开-关”现象:(1)添加COMT抑制剂:滴定添加COMT抑制剂,避免导致异动症。
(2)添加或更换不同类型的多巴胺受体激动剂,如吡贝地尔、普拉克索、罗替戈汀、罗匹尼罗。
(3)调整蛋白质摄入:通常于晚餐时摄入大部分的日常所需蛋白质。
(4)外科手术。
3.1.4“冻结”步态:(1)“关期”冻结:增加左旋多巴或其他多巴胺能药物剂量。
(2)“开期”冻结:可尝试减少左旋多巴剂量,加用多巴胺受体激动剂、MAO-B抑制剂。此外,腓肠肌局部注射肉毒毒素可能会有帮助。
(3)使用感觉、视觉辅助设备:视觉提示或听觉刺激均可帮助患者起步。
(4)抗焦虑治疗:由于焦虑会使“冻结”步态加重,治疗焦虑可能会有帮助。
3.2 异动症
3.2.1剂峰异动:(1)减少多巴胺能药物剂量:为避免运动波动发生,可依次减少抗胆碱能药物、MAO-B抑制剂、多巴胺受体激动剂以及左旋多巴剂量。
(2)调整左旋多巴缓释剂为左旋多巴的普通剂型,尤其是异动症状出现在下午或傍晚者。
(3)添加金刚烷胺。
(4)添加氯氮平,注意药物不良反应,监测血常规。
(5)调整左旋多巴服药次数:若左旋多巴的剂量较大,可在总剂量不变的基础上,改用小剂量的左旋多巴多次给药,避免出现运动波动。
(6)外科手术:GPi-DBS和STN-DBS对剂峰异动均有效,GPi-DBS疗效可能更佳。此外,单侧苍白球损毁术有效。
3.2.2“关期”肌张力障碍:(1)睡前服用左旋多巴控释剂,长效多巴胺受体激动剂。
(2)晨起时服用或嚼碎左旋多巴药物,嚼碎服用后一般10~20 min起效。
(3)添加巴氯芬。
(4)痉挛肌肉局部注射肉毒毒素。
3.2.3双相异动:(1)增加左旋多巴剂量,缩短给药时间间隔。此方法仅在短期内有效,同时可能诱发剂峰异动。
(2)添加或更换不同类型的多巴胺受体激动剂。
(3)DBS手术:对于双相异动患者,STN和GPi为有效治疗靶点。
4 中医临床治疗策略
在中医临床实践中,运动波动的治疗主要针对PD“风、火、痰(瘀)、虚”的病机,调整PD本身脏腑功能及气血阴阳平衡。异动症的治疗应该标本兼治,即以PD为基本,加强平肝潜阳熄风治疗,同时给以解毒祛邪之品。其中,对于剂峰异动在辨证治疗基础上加强熄风止颤;对于“关期”肌张力障碍,在辨证治疗基础上加强搜风剔络、熄风止痉[13-16](图1)。迄今,PD运动并发症的中医治疗仍缺乏高质量的临床研究证据,故其中医治疗均基于中医理论及临床经验,推荐策略以中医经典方剂为参照。
4.1 中药辨证施治
4.1.1肝肾阴虚:(1)主症:震颤剧烈、强直、动作迟缓或剂峰异动、“关期”肌张力障碍。
(2)次症:头晕目眩,耳鸣,夜尿频多、尿失禁,或急躁易怒,失眠多梦,盗汗,大便秘结,舌体瘦小,舌质红,舌苔少或光剥无苔,脉弦细或沉细。
(3)推荐治法:滋补肝肾,育阴熄风。
(4)基本方药:大定风珠加减[17]:白芍、地黄、麦冬、龟板、牡蛎、鳖甲、阿胶、五味子等。
(5)对症加减:剂峰异动:合镇肝熄风汤并酌加天麻、钩藤、全蝎、蜈蚣、黄芩、野菊花、丹皮等加强平肝熄风、解毒通络[18-19];“关期”肌张力障碍:合芍药甘草汤配以全蝎、蜈蚣、僵蚕、蝉蜕、蚤休等熄风止痉、解毒通络。
4.1.2气血亏虚:(1)主症:震颤较剧、强直、动作迟缓,或有低血压、体位性低血压,或剂峰异动、“关期”肌张力障碍。
(2)次症:面色无华,神疲乏力,动后气促,心悸健忘,头晕,纳呆,便秘,失眠多梦,舌体胖大质淡红,苔薄白,脉弦细弱。
(3)推荐治法:益气扶正,养血熄风。
(4)基本方药:人参养荣汤合止颤汤[20]或天芪平颤方[21]:人参、白术、茯苓、黄芪、当归、白芍、熟地黄、五味子、桂心、钩藤、制首乌等。
(5)对症加减:剂峰异动:酌加全蝎、蜈蚣、黄芩、野菊花、丹皮等以通络解毒[18-19];“关期”肌张力障碍:合芍药甘草汤配以全蝎、蜈蚣、僵蚕、蝉蜕、鸡血藤等熄风止痉、解毒通络。
4.1.3痰瘀动风:(1)主症:强直明显、震颤、动作迟缓,或剂峰异动、“关期”肌张力障碍。
(2)次症:面色晦黯,表情呆板,头晕眼花,皮脂外溢,夜寐不安,舌质紫黯或夹瘀斑,舌苔薄白或厚腻,脉弦滑。
(3)推荐治法:化瘀散结,祛痰熄风。
(4)基本方药:摧肝丸合血府逐瘀汤加减[22]:胆星、钩藤、黄连、僵蚕、天麻、桃仁、红花、当归、生地黄、牛膝、川芎、赤芍、甘草、柴胡等。
(5)对症加减:剂峰异动:合天麻钩藤饮加全蝎、蜈蚣、黄芩、野菊花、丹皮等通络解毒[18-19];关期肌张力障碍:合五虎追风散(蝉蜕、天南星、天麻、全蝎、僵蚕)[23]配以蜈蚣、地龙、豨签草、伸筋草等熄风止痉、解毒通络。
4.1.4阳虚风动:(1)主症:震颤、强直、动作迟缓;或剂峰异动、“关期”肌张力障碍。
(2)次症:面色苍白,表情呆板,头晕眼花,畏寒肢冷,小便清长,舌质淡,舌苔薄白,脉沉细。
(3)推荐治法:温肾养肝,熄风止痉。
(4)基本方药:右归丸合温肾养肝方[24]加减:熟地黄、制附子、肉桂、山药、山茱萸、菟丝子、鹿角胶、枸杞子、肉苁蓉、益智仁、钩藤、白芍、乌药。
(5)对症加减:剂峰异动:加全蝎、蜈蚣等通络解毒[19];“关期”肌张力障碍:加全蝎、蜈蚣、僵蚕、蝉蜕、桂枝、鸡血藤、葛根等温经止痛、解毒通络。
4.2 针灸治疗
4.2.1基本治疗:(1)治法:补益肝肾,益气养血,熄风止痉,宁神定颤为主,针灸并用。
(2)基本穴位:百会、四神聪、本神、合谷、风池、太冲、阳陵泉,三阴交,足三里[25];焦氏头针疗法可取舞蹈震颤区、运动区、足运感区等;国标头皮穴疗法可取顶中线、顶颞后斜线、顶旁1线、顶旁2线、枕下旁线等。动留针30 min左右。
(3)辨证选穴:肝肾亏虚、气血不足加肝俞、肾俞、太溪,用补法;痰浊动风加丰隆、膻中、中脘、阴陵泉,用平补平泻法。
(4)对症加减:剂峰异动:加用神庭、本神、四神聪、神门配合百会穴,加强镇静安神、健脑益智的功效[26];根据症状出现部位,可选用上肢的阳池、阳溪、曲池、尺泽;下肢的中封、太溪、阴陵泉、委中等。关期肌张力障碍:在PD常规治疗基础上,以取上下肢阴经穴为主(靳三针中的挛三针),上肢挛三针:极泉、尺泽、内关;下肢挛三针:鼠蹊、阴陵泉、三阴交[27]。
4.2.2其他疗法:可应用电针疗法、温针灸、耳针。
(1)电针疗法可用于头针和体针,选取疏密波强刺激20~30 min。
(2)运用灸法时,应灸至患者感到艾灸热力达到颅内或穴位深层。
(3)耳针可取皮质下、神门、枕、颈、肘、腕、指、膝等穴,采用毫针刺法或药丸压贴。
5 中西医结合治疗策略
中西医结合治疗PD运动并发症的策略主要是明确中西医结合治疗的优势及治疗的时机(图1)。
5.1 中西医结合治疗优势PD运动并发症主要源于疾病慢性进展及西医药物治疗,故现已对西医治疗PD诱发运动并发症的相关机制及临床表现进行了较为深入的研究。目前西医对于运动并发症的治疗优势体现在临床分型及循证证据较为充分明确,但缺乏对疾病整体治疗的理念。而中医整体观念和辨证论治的理念正是对西医治疗不足的有效补充。中医防治PD运动并发症的优势,一方面突出了疾病治疗的整体理念,秉承“治病求本”的特点,以恢复患者“阴平阳秘”的状态为目标,增强患者自身对于运动并发症的抵抗能力,从而避免运动并发症的发生;另一方面发挥中药对西药“增效减毒”的作用,通过增强西药疗效,减少西药用量,从而预防运动并发症的发生。因此中西医结合治疗可通过“辨识兼顾,防治并举”的优势互补达到对PD运动并发症的有效防治,进而改善疾病预后,提高患者生活质量。
5.2 中西医结合治疗时机中西医结合治疗PD运动并发症的启动时机应贯穿疾病全程。PD患者应尽早启动中西医结合治疗,发挥中医药对运动并发症的预防作用。而对于已发生运动并发症的患者,中西医结合治疗既可加强西药对运动症状的改善作用,同时对运动并发症中的非运动症状(如疼痛、感觉异常、抑郁、焦虑、静坐不能以及重复刻板动作等)改善更加显著。
5.3 中西医结合协作管理PD治疗的中西医结合协作管理需要西医和中医专科医生共同完成,在明确中医和西医治疗策略的基础上,根据患者具体临床特征和中医证型以及中药和西药的药效特点,制定中西医结合治疗PD的具体方案,继而定期评估临床疗效,相应增减药物种类、剂量及疗程。
总之,目前尚无能够逆转或者阻遏PD运动并发症发生发展的有效方法,因此PD运动并发症的临床诊治应立足国情,在西医治疗的基础上,彰显中西医结合优势,重视患者个体化、精准化诊疗方案。在“辨识兼顾,防治并举”的中西医结合理念指导下,在临床实践中,应发挥中西结合治疗的优势,把握中西医结合的治疗时机,掌握中西医结合的治疗策略,不断提高PD运动并发症的临床诊治水平。
利益冲突:所有作者均声明不存在利益冲突
执笔者:刘振国 李文涛
参与讨论人员(按姓氏笔画顺序排序):
丁正同(复旦大学附属华山医院)、万新华(中国医学科学院北京协和医院)、王长德(上海中西医结合医院)、王青(南方医科大学珠江医院)、王振福(解放军总医院第二医学中心)、王晓平(上海交通大学医学院附属同仁医院)、王涛(华中科技大学同济医学院附属协和医院)、东贵荣(上海中医药大学附属岳阳医院)、卢晓东(杭州师范大学附属医院)、叶民(南京医科大学附属明基医院)、冯涛(首都医科大学附属天坛医院)、朱晓冬(天津医科大学总医院)、刘军(上海交通大学医学院附属瑞金医院)、刘春风(苏州大学附属第二医院)、刘卫国(南京医科大学附属脑科医院)、刘振国(上海交通大学医学院附属新华医院)、刘毅(上海中医药大学附属市中医医院)、李文涛(上海中医药大学附属市中医医院)、李如奎(上海中医药大学附属市中医医院)、杨文明(安徽中医药大学第一附属医院)、吴云成(上海交通大学附属第一人民医院)、汪锡金(上海交通大学医学院附属新华医院)、张克忠(南京医科大学第一附属医院)、张宝荣(浙江大学医学院附属第二医院)、陈生弟(上海交通大学医学院附属瑞金医院)、陈海波(北京医院 国家老年医学中心)、金莉蓉(复旦大学附属中山医院)、赵杨(南京中医药大学附属南京中医院)、赵虹(上海中医药大学附属岳阳医院)、胡兴越(浙江大学医学院附属邵逸夫医院)、袁灿兴(上海中医药大学附属龙华医院)、聂志余(同济大学附属同济医院)、徐世芬(上海中医药大学附属市中医医院)、徐评议(广州医科大学附属第一医院)、曹学兵(华中科技大学同济医学院附属协和医院)、黄东雅(同济大学附属东方医院)、黄卫(南昌大学第二附属医院)、崔桂云(徐州医科大学附属医院)、商慧芳(四川大学华西医院)、谢安木(青岛大学附属医院)、靳令经(同济大学附属同济医院)、薛峥(华中科技大学同济医学院附属同济医院)、魏江磊(上海中医药大学附属曙光医院)
