聚乙烯亚胺修饰的碳点荧光探针用于检测汞离子
2020-08-21陈丽娟刘仁勇赵丹闫叶寒
陈丽娟 刘仁勇 赵丹 闫叶寒
摘 要 以维生素C(Vc)为碳源,以聚乙烯亚胺(PEI)为掺杂氮剂, 通过一步水热合成法制备了可发射蓝色荧光的水溶性碳点荧光探针(PEI-Vc CDs)。基于Hg2+对PEI-Vc CDs探针良好的荧光猝灭效果,建立了一种快速检测Hg2+的方法。在0.022~20 μmol/L浓度范围内,PEI-Vc CDs探针荧光猝灭程度与Hg2+浓度呈良好的线性关系,检出限为22 nmol/L(S/N=3)。其它金属离子 (Na+、K+、Ca2+、Mg2+、Mn2+、Fe3+、Co2+、Ni2+、Zn2+、Cd2+、Ag+、Ba2+和Pb2+)不会引起探针荧光强度的显著改变,表明此探针对Hg2+具有高的选择性。将此探针用于河水、自来水和矿泉水等实际水样中Hg2+的检测,结果令人满意。
关键词 汞离子; 重金属离子; 聚乙烯亚胺; 碳点; 荧光分析
1 引 言
汞離子(Hg2+)是一种高毒性重金属离子,易被生物体吸收,但不能被生物体降解,最终通过食物链富集,对人或动物的神经系统、免疫系统、肾脏和心脏造成危害,导致认知功能和运动功能障碍[1~3]。我国生活饮用水国家标准规定,饮用水中Hg2+含量不得超过5.0 nmol/L[4],因此,检测水环境中的Hg2+对保护人类健康具有重要的意义。检测Hg2+的传统方法主要有原子吸收光谱法[5,6]、原子发射光谱法[7,8]、电感耦合等离子体质谱法[9,10]、电化学方法[11~13]和分光光度法[14,15]等。这些方法灵敏度高,能够满足痕量分析的需求,但是存在仪器设备昂贵、测试成本高、操作繁琐等问题。相对而言,荧光分析法具有灵敏度高、选择性好、响应速度快、操作简单等优点,已被用于检测多种重金属离子[16~28]。
碳点(Carbon dots, CDs)粒径通常小于10 nm,主要由sp2/sp3碳和氧/氮基团构成,是一种具有荧光特性的碳基颗粒,广泛用于生物和化学传感以及食品分析、环境监测等领域。Goncalves等[18]通过激光消融法制备碳点,对Hg2+有良好的猝灭作用,然而该方法在活化碳点的过程中需用大量浓HNO3,导致碳点荧光量子产率降低。Yuan等[19]利用二硫代氨基甲酸铜(CuDTC2)修饰碳点,实现了对Hg2+高灵敏度和选择性检测,方法简单,但是采用了Cu2+,引入了新的重金属污染物。发展简单、低成本、可大规模制备高品质碳点的方法,是目前研究的热点。水热法是一种简单、高效合成碳点的方法。胥月等[20]采用水热合成法处理苹果汁,制备高品质的碳点,对Hg2+具有高灵敏度、高选择性的响应。采用氨基化合物作为掺杂氮源,可提高碳点的荧光量子产率[21,22]。
本研究选用廉价易得的维生素C(Vitamin C,Vc)为碳源,以聚乙烯亚胺(Polyethyleneimine,PEI)为氮掺杂剂,通过一步水热法合成了一种环境友好的新型碳点荧光探针(PEI-Vc CDs)。利用Hg2+对PEI-Vc CDs的选择性猝灭效应,建立了检测Hg2+的方法,并用于实际水样中Hg2+的测定。
2 实验部分
2.1 仪器与试剂
RF-5301PC荧光光谱仪(日本岛津公司);JEM-2100 PLUS高分辨率透射电镜(日本电子公司);iS50FT-IR傅里叶-红外光谱仪、iCAP-RQ电感耦合等离子体质谱仪(美国Thermo Fisher Scientific公司);Milli-Q超纯水处理系统(美国Millipore公司)。
KCl、NaCl、无水CaCl2、MgCl2、Fe(NO3)3、CoCl2、Hg(NO3)2、Pb(NO3)2和AgNO3(分析纯,国药集团化学试剂有限公司);硫酸喹啉、聚乙烯亚胺(Mn=600)、NiSO4、Mn(Ac)2、MgCl2、Vc和CdCl2(分析纯,阿拉丁生化科技股份有限公司)。实验用水为超纯水。
2.2 PEI-Vc CDs荧光探针的合成
参照文献[23]的方法合成PEI-Vc CDs探针并稍作改进,采用Vc代替柠檬酸作为碳源,PEI代替乙醇胺作为氮掺杂剂,并采用水热法合成。具体步骤如下: 取10 mL 0.5 mol/L Vc溶液置于50 mL反应釜中,再缓慢滴入10 mL 0.5 mol/L PEI溶液,所用PEI与Vc的摩尔比为1:1。在200℃水热反应6 h。冷却至室温,得到的棕色液体过0.45 μm滤膜,除去悬浮颗粒。产物在超纯水中透析8 h,然后冷冻干燥,获得PEI-Vc CDs粉末,将其分散在超纯水中,配制成浓度为100 μg/mL的探针溶液,备用。
2.3 对Hg2+的荧光检测
为抑制Hg2+水解,其储备溶液采用等浓度的稀HNO3溶液配制。取1.7131 g Hg(NO3)2·H2O溶解在100 mL 0.05 mol/L HNO3溶液中, 得到0.05 mol/L Hg2+标准储备液。适当稀释储备液得到工作液,将不同浓度的Hg2+工作液(0.0, 2.5, 5.0, 7.5, 10.0, 12.5, 17.5和20 μmol/L)与PEI-Vc CDs探针溶液(2 μg/mL)混合孵育。在350 nm激发光下,测量380~600 nm范围的荧光光谱。以荧光猝灭效率为纵坐标((F0-F)/F0(其中, F0代表探针未加入Hg2+的荧光强度,F代表加入Hg2+后的荧光强度),Hg2+浓度为横坐标,绘制标准曲线。
2.4 选择性实验
利用各金属离子(Na+、K+、Ca2+、Mg2+、Mn2+、Fe3+、Co2+、Ni2+、Zn2+、Cd2+、Ag+、Ba2+和Pb2+)的可溶性盐配制其工作溶液,浓度均为0.1 mol/L,采用与2.3节相同相同方法,测定金属离子与探针混合体系的荧光光谱,考察PEI-Vc CDs探针体系的选择性。
2.5 熒光量子产率的测定
以硫酸奎宁(Quinine sulfate)为标准参照物,在0.1 mol/L H2SO4中,其荧光量子产率为54.6%。测定待测样品和标准参照物两种稀溶液的荧光积分面积(350 nm激发)和溶液的吸光度(350 nm),以荧光积分面积为纵坐标,吸光度为横坐标,绘制标准曲线,按式(1)计算样品的量子产率:
ΦF sample=ΦF standard·AstandardAsample·FsampleFstandard·η2sampleη2standard(1)
其中, ФF为荧光量子产率,A和ΣF为激发波长(350 nm)处的吸光度和荧光积分面积, η为所用溶剂的折射率,下标Standard和Sample分别表示标准参照物硫酸奎宁和待测样品PEI-Vc CDs探针。
3 结果与讨论
3.1 探针的表征 以廉价易得的Vc为碳源,水溶性良好的氨基化合物PEI为氮掺杂剂,通过一步水热法制备了一种荧光碳点(PEI-Vc CDs),合成路线如图1所示。采用透射电镜(TEM)和傅里叶变换红外光谱(FT-IR)表征了PEI-Vc CDs的形貌和结构。由TEM图(图2)可见,PEI-Vc CDs在水中分散性良好,粒径约为3 nm。与PEI和Vc分子的红外光谱比较(图3),PEI-Vc CDs的红外光谱在3425 cm1处出现NH的伸缩振动,2962和2841 cm1处的峰是CH的伸缩振动峰,1636 cm1处的峰为CO的特征振动峰,表明PEI-Vc CDs表面存在羰基和氨基基团。图4A是PEI-Vc CDs探针在不同激发波长(310~380 nm)下的荧光光谱,最大激发波长为350 nm,吸收光谱(图4B曲线a)中最大吸收峰位于350 nm处,最大荧光发射峰位于441 nm(图4B曲线b)。以硫酸奎宁为参照物,测得PEI-Vc CDs探针量子产率为34.6%。
3.2 探针的稳定性
考察了PEI-Vc CDs探针的荧光稳定性。在室温条件下,使用20 kW脉冲氙灯作为紫外灯光源,激发波长为350 nm,探针溶液与光源的距离约为70 cm,每隔5 min记录探针溶液的荧光光谱,结果见图5。 经过100 min连续照射, 最大发射波长441 nm处的荧光强度几乎未变, 表明PEI-Vc CDs探针荧光稳定性好,抗光漂白能力强,可用于分析检测。
3.3 可行性分析
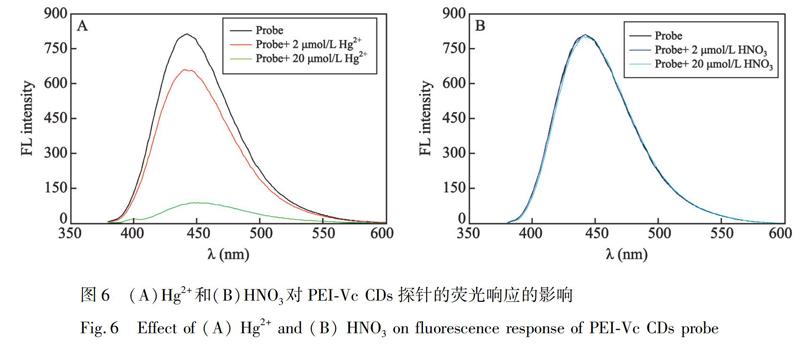
考察了Hg2+对PEI-Vc CDs探针的荧光猝灭性能,如图6A所示,当溶液中不存在Hg2+时,探针发射很强的荧光;当Hg2+浓度为2 μmol/L时,探针荧光强度下降,Hg2+浓度为20 μmol/L时,荧光强度显著下降,猝灭率达到90%。为排除Hg2+储备液中HNO3的干扰,将等浓度的HNO3与PEI-Vc CDs探针溶液混合,未见探针荧光强度下降(图6B)。上述结果表明,探针荧光的猝灭是由Hg2+引起的,且Hg2+浓度越大,荧光淬灭程度越大,因此,可采用PEI-Vc CDs探针检测Hg2+。
3.4 PEI-Vc CDs探针用于Hg2+检测
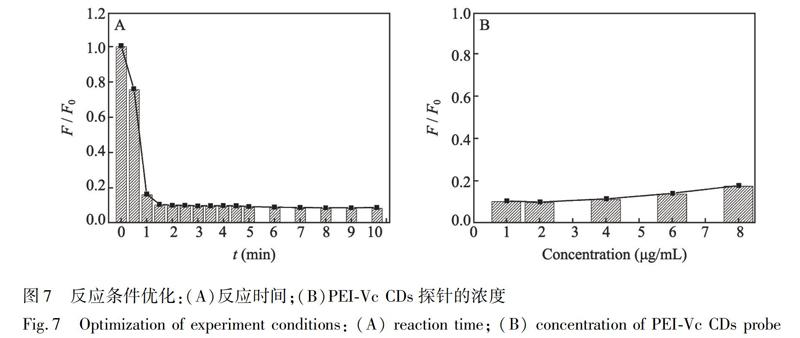
考察了Hg2+与探针之间的动力学响应,如图7A所示,加入Hg2+后,体系荧光强度快速下降,2 min后达到稳定,说明Hg2+和PEI-Vc CDs探针的反应速度快,可迅速达到平衡。因此,后续实验的反应时间选择2 min。进一步考察了探针浓度对Hg2+的影响(图7B),结果表明,
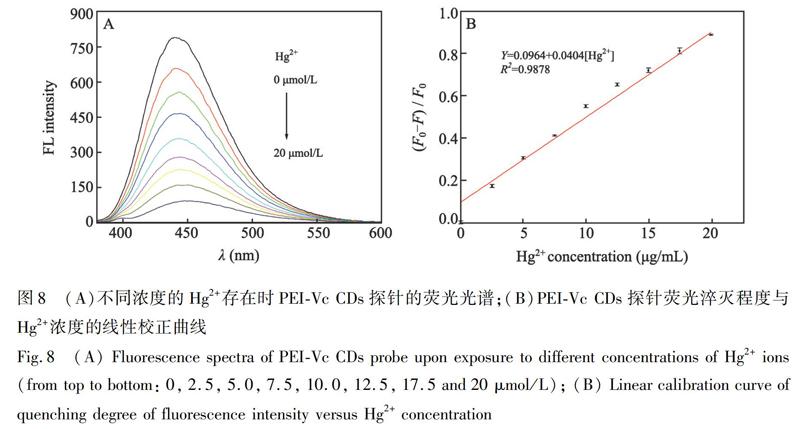
探针溶液浓度为2 μg/mL时, Hg2+对其荧光猝灭程度最大。2 μg/mL PEI-Vc CDs探针溶液在不同浓度Hg2+存在下的荧光光谱如图8A所示,随着Hg2+浓度从0逐渐增加至20 μmol/L,探针的荧光逐渐被猝灭。Hg2+浓度在0.022~20 μmol/L范围内,探针荧光猝灭程度((F0-F)/F0)与Hg2+浓度呈良好的线性关系(图8B),线性关系为(F0-F)/F0=0.0964+0.0404[Hg2+],相关系数(R2)为0.9878,检出限(LOD,S/N = 3)为22 nmol/L。随着Hg2+浓度从0逐渐增加至20 μmol/L,探针的量子产率由34.6%降至0.64%。与基于聚合物[19~21]、有机小分子[22~24]、无机纳米颗粒[25~27]制备的Hg2+荧光探针相比(表1),本研究合成的PEI-Vc CDs探针具有水溶性好、线性范围宽等优点。
3.5 Hg2+选择性响应
选择常见的金属离子Na+、K+、Ca2+、Mg2+、Mn2+、Fe3+、Co2+、Ni2+、Zn2+、Cd2+、Ag+、Ba2+和Pb2+,探究其对PEI-Vc CDs探针的荧光响应。如图9A所示,2 μmol/L Hg2+引起探针荧光强度显著下降,10倍浓度的上述常见金属离子对探针的荧光强度影响非常小,表明PEI-Vc CDs探针能够选择性识别Hg2+。对于20 μmol/L Hg2+,50 倍浓度的Na+、K+、Ca2+、Mg2+, 20 倍浓度的 Mn2+、Fe3+、Co2+、Ni2+、Zn2+、Cd2+、Ag+、Ba2+、Pb2+ 共存时,对探针的荧光强度的影响很小(图9B)。上述结果表明,PEI-Vc CDs探针对Hg2+的选择性高,抗干扰能力强。
3.6 实际样品分析
实际水样包括六安市淠河河水、自来水以及市售矿泉水。测定前,河水需过滤,去除悬浮颗粒;矿泉水和自来水均直接进行测定。采用PEI-Vc CDs探针体系,对3种水样进行检测,均未检出Hg2+。同时,利用电感耦合等离子体质谱法(ICP-MS)做对照测试,在3种水样中也未检出Hg2+。加标回收实验结果见表2, 3个浓度水平下的加标回收率在94.0%~105.5%之间,表明PEI-Vc CDs探针体系具有良好的实用性和分析性能,可用于实际水样中Hg2+的分析。
4 結 论
采用水热合成法制备了一种新型PEI-Vc CDs荧光探针,探针水溶性好,粒径均匀。Hg2+浓度在0.022~20 μmol/L 范围内,探针荧光猝灭程度与Hg2+浓度呈良好的线性关系,检出限为22 nmol/L。将本方法用于实际水样中Hg2+的测定,结果令人满意。本研究构建的PEI-Vc CDs荧光探针在水环境监测与分析方面有良好的应用潜能。
References
1 DAI Shu-Gui. Environmental Chemistry, Higher Education Press, 2006: 165
戴树桂. 环境化学(第二版). 高等教育出版社, 2006: 165
2 Zhang Y, Jiang H, Wang X. Anal. Chim. Acta, 2015, 870: 1-7
3 Nolan E M, Lippard S J. Chem. Rev., 2008, 108(9): 3443-3480
4 GB 5749-2006. Sanitary Standard for Drinking Water Quality. National Standards of the Peoples Republic of China
生活饮用水卫生标准. 中华人民共和国国家标准. GB 5749-2006
5 Vicentino P D O, Brum D M, Cassella R J. Talanta, 2015, 132: 733-738
6 Panichev N A, Panicheva S E. Food Chem., 2015, 166: 432-441
7 LUO Hong, HOU Xian-Deng, LONG Zhou. Chinese J. Anal. Chem., 2015, 43(9): 1291-1295
罗 虹, 侯贤灯, 龙 舟. 分析化学, 2015, 43(9): 1291-1295
8 Yuan X, Yang G, Ding Y, Li X M, Zhan X F, Zhao Z J, Duan Y X. Spectrochim. Acta B, 2014, 93(2): 1-7
9 Ma S S, He M, Chen B B, Deng W C, Zheng Q, Hu B. Talanta, 2016, 146: 93-99
10 Cheng H Y, Chen X P, Shen L H, Wang Y C, Xu Z G, Liu J H. J. Chromatogr. A, 2018, 1531: 104-111
11 Chen D M, Gao Z F, Jia J, Li N B, Luo H Q. Sens. Actuators B, 2015, 210: 290-296
12 Kanchana P, Sudhan N, Sukeri A, Jayaraman M, Manisankar P, Sekar C. RSC Adv., 2015, 5(84): 68587-68594
13 ZHU Xi, CHEN Li-Fen, LIN Zhen-Yu, CHEN Guo-Nan. Chinese J. Anal. Chem., 2009, 37(3): 131
朱 希, 陈丽芬, 林振宇, 陈国南. 分析化学, 2009, 37(3): 131
14 Ulusoy H I. J. AOAC Int., 2014, 97(1): 238-244
15 Chen L, Li J H, Chen L X. ACS Appl. Mater. Interfaces, 2014, 6(18): 15897-15904
16 Childress E S, Roberts C A, Sherwood D Y, Leguyader C L M, Harbron E J. Anal. Chem., 2012, 84(3): 1235-1239
17 Yan Y, Krishnakumar S, Yu H, Ramishetti S, Deng L W, Wang S H. J. Am. Chem. Soc., 2013, 135(14): 5312-5315
18 Goncalves H, Jorge P A S, Fernandes J R A, Joaquim C G E. Sens. Actuators B, 2010, 145: 702-707
19 Yuan C, Liu B H, Liu F, Han M Y, Zhang Z P. Anal. Chem., 2014, 86(2): 1123-1130
20 XU Yue, TANG Chun-Jing, HUANG Hong, SUN Chao-Qun, ZHANG Ya-Kun, YE Qun-Feng, WANG Ai-Jun. Chinese J. Anal. Chem., 2014, 42(9): 1252-1258
胥 月, 汤纯静, 黄 宏, 孙超群, 张亚鲲, 叶群峰, 王爱军. 分析化学, 2014, 42(9): 1252-1258
21 Zhu S J, Meng Q N, Wang L, Zhang J H, Song Y B, Han J, Zhang K, Sun H C, Wang H Y, Yang B. Angew. Chem., Int. Ed., 2013, 52(14): 3953-3957
22 Qu D, Zheng M, Zhang L G, Zhao H F, Xie Z G, Jing X B, Haddad R E, Fan H Y, Sun Z C. Sci. Rep., 2014, 4: 5294
23 Zhang Y, Liu X, Fan Y,Guo X, Zhou L, Lv Y, Lin J. Nanoscale, 2016, 8: 15281-15287
24 Wei Y, Li B M, Wang X, Duan Y X. Analyst, 2014, 139(7): 1618-1621
25 Yan F Y, Shi D C, Zheng T C, Yun K Y, Zhou X G, Chen L. Sens. Actuators B, 2016, 224: 926-935
26 Lan M H, Zhang J F, Chui Y S, Wang P F, Chen X F, Lee C S, Kwong H L, Zhang W J. ACS Appl. Mater. Interfaces, 2014, 6(23): 21270-21278
27 Yan Y H, Yu H, Zhang K, Sun M T, Zhang Y J, Wang X K, Wang S H. Nano Res., 2016, 9(7): 2088-2096
28 PENG Tao, WANG Jian-Yi, XIE San-Lei, YAO Kai, SUN Shu-Juan, ZENG Yu-Yang, JIANG Hai-Yang. Chinese J. Anal. Chem., 2018, 46(3): 373-378
彭 涛, 王见一, 谢三磊, 姚 凯, 孙淑娟, 曾于洋, 江海洋. 分析化学, 2018, 46(3): 373-378
29 Huang W J, Wu W H. J. Appl. Polym. Sci., 2012, 124: 2055-2061
30 Fan L J, Zhang Y, Wayne E J. Macromolecules, 2005, 38(7): 2844-2849
31 Wan C F, Lin H Y, Chien C, Wu A T. Luminescence, 2014, 29(6): 698-701
32 Petdum A, Panchan W, Sirirak J, Promarak V, Sooksimuang T, Wanichacheva N. New J. Chem., 2018, 42(2): 1369-1402
33 Wang S, Liu R Q, Li C C. Nanoscale Res. Lett., 2018, 13(1): 235-241
34 Yuan C, Zhang K, Zhang Z P, Wang S H. Anal. Chem., 2012, 84(3): 9792-9801
A Novel Fluorescent Probe for Mercury Ion Detection
Based on Polyethyleneimine Modified Carbon Dots
CHEN Li-Juan1, LIU Ren-Yong1, ZHAO Dan2, YAN Ye-Han*2
1(College of College of Materials and Chemical Engineering, West Anhui University, Luan 237012, China)
2(College of Environment and Tourism, West Anhui University, Luan 237012, China)
Abstract A novel carbon dots (CDs) fluorescent probe was prepared by pyrolyzing the mixture of ascorbic acid (Vc) and polyethyleneimine (PEI) aqueous solution through hydrothermal method for rapid, simple and on-site detection of mercuric ion. The particle size of CDs was characterized by TEM to be 3 nm with a good dispersivity. The fluorescence of the CDs could be quenched by Hg2+, while remained nearly constant when exposed to other metal ions including Na+, K+, Ca2+, Mg2+, Mn2+, Fe3+, Co2+, Ni2+, Zn2+, Cd2+, Ag+, Ba2+ and Pb2+, implying its good selectivity. A good linear relationship between the fluorescence quenching degree (F0-F)/F0 of probe and Hg2+ concentration was obtained with correlation coefficient (R2) of 0.9878, and the detection limit (S/N=3) for Hg2+ was 22 nmol/L in aqueous solution. In addition, the probe was used to determine Hg2+ in real water samples, and the recoveries ranged from 94.0% to 105.5% in river water, tap water and mineral water samples, proving its good practical applicability for detection of Hg2+ in complex water samples.
Keywords Mercury ion; Heavy metal ions; Polyethyleneimine; Carbon dots; Fluorescence analysis
(Received 29 August 2019; accepted 28 May 2020)
This work was supported by the National Natural Science Foundation of China (No. 21804100), the Natural Science Foundation of Anhui Province (Nos. KJ2018A0416, 1808085QB and the Science Foundation of West Anhui University (Nos.WXZR201801, WGKQ201702020).
2019-08-29收稿; 2020-05-28接受
本文系國家自然科学基金项目(No. 21804100)和安徽省自然科学基金项目(Nos.KJ2018A0416, 1808085QB资助
* E-mail: yanyh@mail.ustc.edu.cn
