三七花质量标准研究
2020-08-21王培珍卜其涛许世辉董志颖张成中
倪 敏,王培珍,卜其涛,许世辉,董志颖*,张成中,*
(1.上海中医药大学附属中医院,上海200120;2.第二军医大学药学系,上海200433;3.安徽省阜阳市食品药品检验检测中心,阜阳236015;4.上海中医药大学中药学院,上海200120)
三七花又称田七花,为五加科植物三七(Panax notoginseng(Burk.)F.H.Chen ex C.Chow.)的干燥花序。《中药大辞典》记载三七花具有清热,平肝,降压等功效。可用于治疗高血压,头昏,目眩,耳鸣,急性咽喉炎等症[1]。三七花是三七全株中含三七皂苷成分最高的部位,其含量可达10%以上,除三七皂苷外还含有其他多种皂苷,如人参皂苷Rb1、Rb2、Rb3等,另外,还有多糖、黄酮、氨基酸、挥发油等多种活性成分及K、Na、Ca、Mg、Al、Cl、P、S、Fe、Zn、Cu、Si、Mn 和 Ni等微量元素[2~3]。其中,三七皂苷为三七花最主要的药理活性成分[4],具有扩张血管[5]、修复血管[6]、修复皮肤创伤[7]、降血压[8]、镇痛、抗炎、止血和造血[9]等功能;人参皂苷作为三七花主要活性成分之一对神经系统、心血管系统都有一定的保护作用,在抗癌方面也有重要作用[10]。鉴于人参皂苷Rb2、Rb3活性明确易于获得,故本实验以其为对照品。近年来,随着国民收入的提高,人们对养生保健也越来越重视,三七花茶饮凭借其优良的口感迅速发展,并远销海外,成为了三七资源整合利用的重要组成部分[11]。三七花在医药、保健、食品饮料、化妆品等方面具有广泛应用,但查阅文献发现,有关三七花质量控制的研究多集中于性状鉴别、理化鉴别等方面,且仅简单收载于上海、重庆、四川等地市的地方标准中,《中华人民共和国药典》(下称 《中国药典》)中还未能收载三七花的相关质量标准。恰逢三七花的质量标准为新版安徽省中药饮片炮制规范编修的立项要求之一,故开展本次实验研究为三七花质量标准的建立提供一定的借鉴。
1 试药与仪器
1.1 试药
本实验收集到产自广西、云南等地共10批三七花药材,批号见表1,经阜阳市食品药品检验检测中心主任药师许世辉鉴定为五加科人参属植物三七(Panax notoginseng(Burk.)F.H.Chen ex C.Chow.)的干燥花。人参皂苷Rb2(批号:111715-201203,纯度:93.8%),购自中国食品药品检定研究院;人参皂苷Rb3(批号:111686-201504,纯度:97.0%),购自中国食品药品检定研究院。乙腈为色谱纯,水为自制超纯水,其他试剂均为分析纯。
1.2 仪器
LEICA DM500型双目显微镜(德国laica公司);E100H型超声波清洗仪(德国Elma公司);梅特勒-托利多分析天平 (METTLER TOLEDO公司);SYZD型多功能振荡器 (山东申仪电子科技有限公司);SYLD-1型电子调温电炉(山东申仪电子科技有限公司);SX2-2.5-10型高温箱型电炉 (上海博讯实业有限公司);GZX-9023 MBE数显鼓风干燥箱(上海博讯实业有限公司);LC-20系列岛津液相色谱仪(岛津株式会社);超声波提取仪 (上海精密仪器仪表有限公司);FST-Ⅲ-2.0普利菲尔超纯水机 (上海富诗特仪器设备有限公司);数码照相机(日本佳能公司);半自动薄层点样及成像仪(瑞士CAMAG有限公司)。
2 方法与结果
2.1 炮制工艺
三七花以花类药材入药,采收花序干燥或阴干,以净制法为主[12]。故具体方法拟定为取原药材,除去泥沙、茎叶等杂质,干燥。
2.2 性状鉴别
呈不规则半球形、球形或伞形,直径约0.5~2.5cm;有花80~100朵;放大镜下观察,花梗被微绒毛;小花梗细短,基部具有鳞片状苞片;花萼绿色,先端通常5齿裂;花瓣5,黄绿色。质轻。气微,味甘、微苦[13]。
2.3 显微粉末鉴别
三七花粉碎过筛。本品粉末黄绿色。导管易见,多为螺纹导管或环纹导管;花粉粒众多,圆形或类圆形,可见2~3个萌发孔;气孔不等式,副卫细胞4~5个;树脂道碎片含黄色分泌物。详见图1~4。

图1 导管Fig.1 Catheter
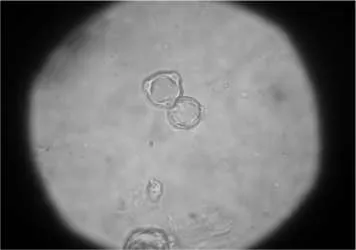
图2 花粉粒Fig.2 Microspore
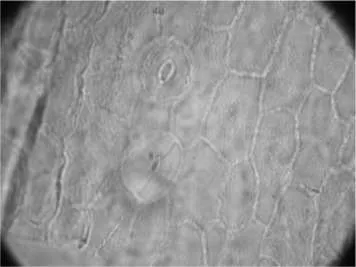
图3 不等式气孔Fig.3 Inequality stomata
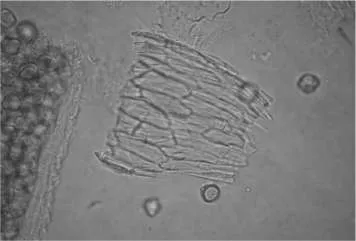
图4 树脂道碎片及分泌物Fig.4 Resin fragments and secretions
2.4 薄层鉴别[14]
取本品药材粉末0.5g,加水约10mL,搅匀,再加以水饱和的正丁醇10mL,密塞,振摇约10min,放置2h,离心,取上清液,加3倍量以正丁醇饱和的水,摇匀,放置使分层(必要时离心),取正丁醇层,置蒸发皿中,蒸干,残渣加甲醇1mL使溶解,作为供试品溶液。另取人参皂苷Rb3对照品,用甲醇制成每1mL含1mg的溶液,即得对照品溶液。照薄层色谱法试验,吸取供试品溶液1μL,对照品溶液2μL,分别点于同一高效硅胶G薄层板上,以正丁醇-乙酸乙酯-水(4:1:5)10℃以下放置的上层溶液为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,于105℃加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点,结果见图5;置紫色外光灯(365nm)下检视,显相同的荧光斑点,结果见图6。
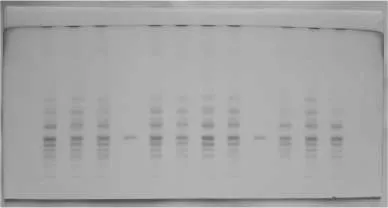
图5 供试品薄层色谱Fig.5 TLC for Test sample
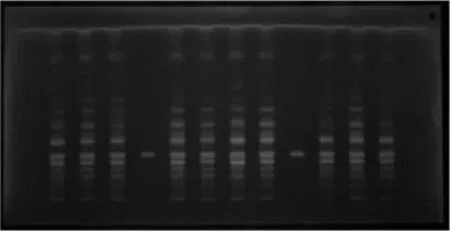
图6 供试品薄层色谱(紫外灯365nm波长下)Fig.6 TLC for Test sample(Under UV light,λ=365nm)
(从左到右依次为 1.SQH-1-001、2.SQH-1-002、3.SQH-1-003、4. 人参 皂 苷 Rb3、5.SQH-1-004、6.SQH-1-005、7.SQH-1-006、8.SQH-1-007、9.人参皂苷Rb3、10.SQH-1-008、11.SQH-1-009、12.SQH-1-010 From left to right:1.SQH-1-001、2.SQH-1-002、3.SQH-1-003、4.ginsenosideRb3、5.SQH-1-004、6.SQH-1-005、7.SQH-1-006、8.SQH-1-007、9.ginsenoside Rb3、10.SQH-1-008、11.SQH-1-009、12.SQH-1-010)
2.5 水分测定
参照 《中国药典》2015年版四部0832水分测定法第二法共测定10批次三七花的水分。结果见表1。
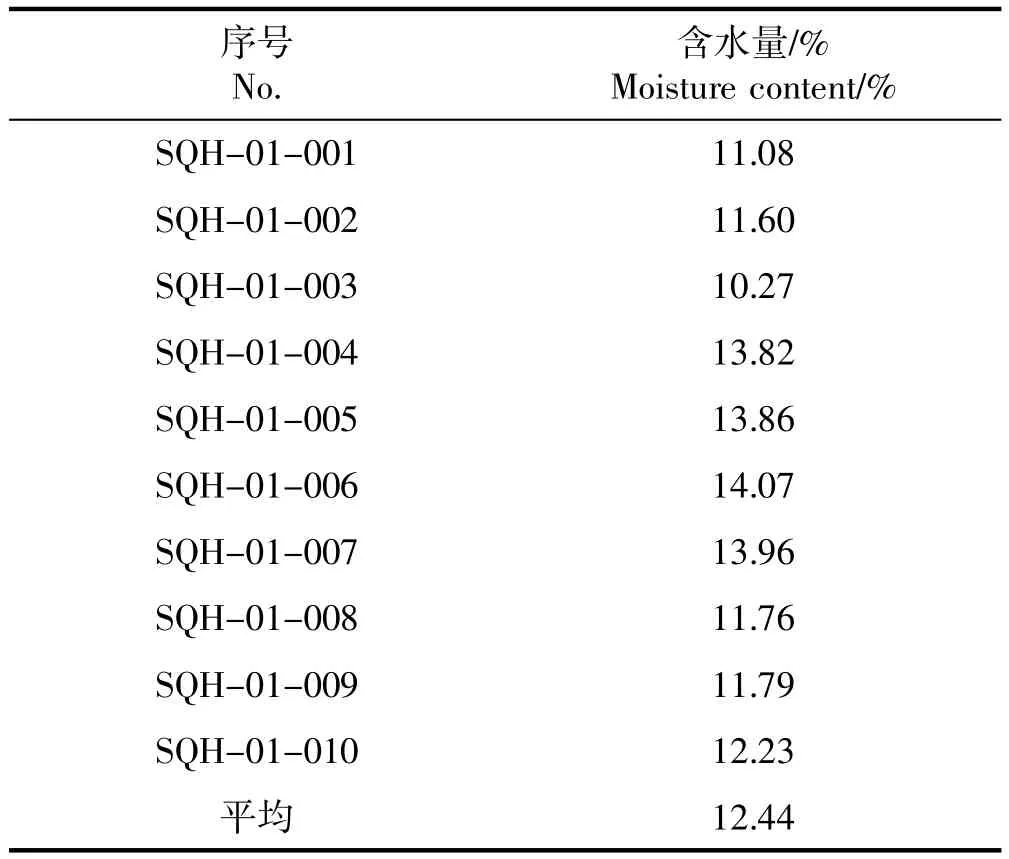
表1 含水量测定Table 1 Moisture content text
从以上结果可知三七花饮片的水分在10.27%~14.07%之间。应以统计学方法分析测试数据,基于测试数据,设定水分限度的公式如下:
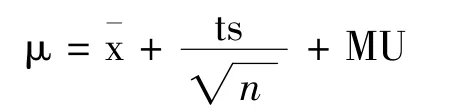
注:是样本的平均数;t是置信水平为99%的学生t检测值 (单尾);s是样本的标准偏差;n是样本的批数;MU是不确定度评估。
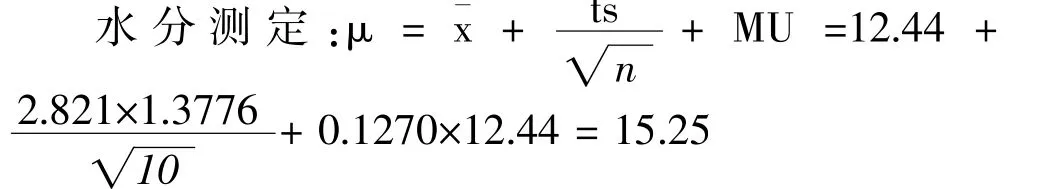
根据计算结果,拟定水分限度应不得过15.0%。
2.6 总灰分和酸不溶灰分测定
2.6.1 总灰分测定 参照 《中国药典》2015年版四部2302灰分测定法共测定10批次三七花饮片总灰分。结果见表2。
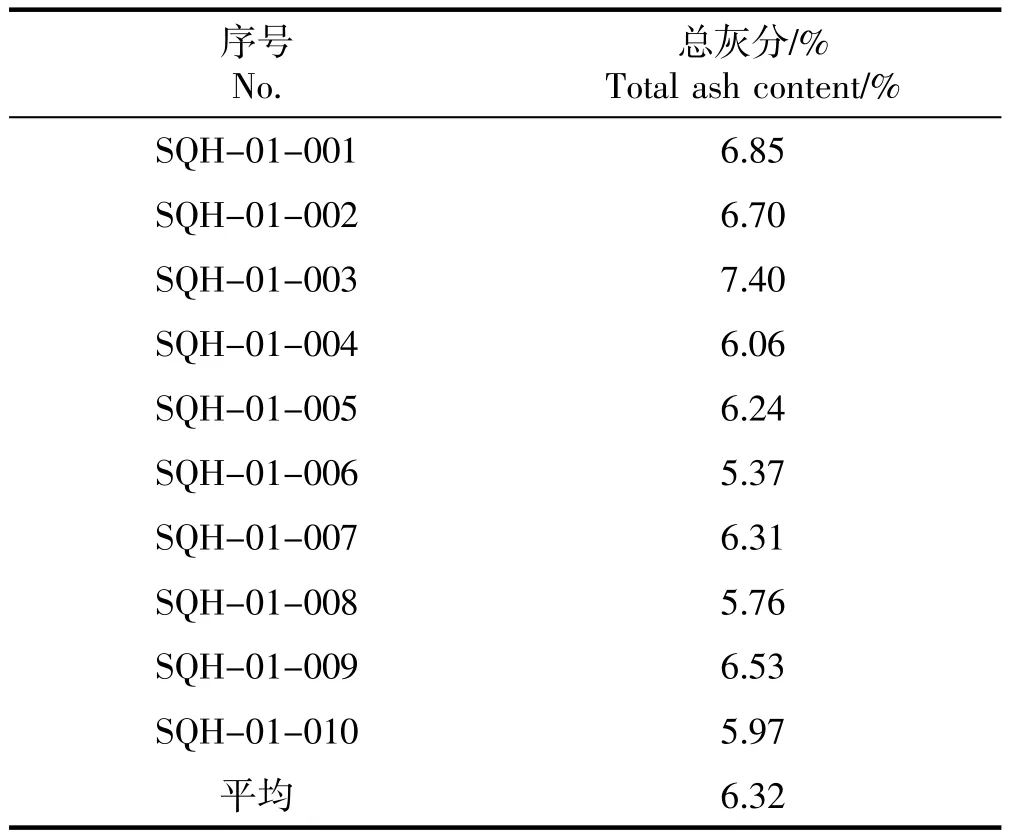
表2 总灰分测定Table 2 Total ash content text
从以上结果可知10批三七花饮片的总灰分在5.37%~7.40%之间。应以统计学方法分析测试数据,基于测试数据,设定总灰分限度的公式如下:
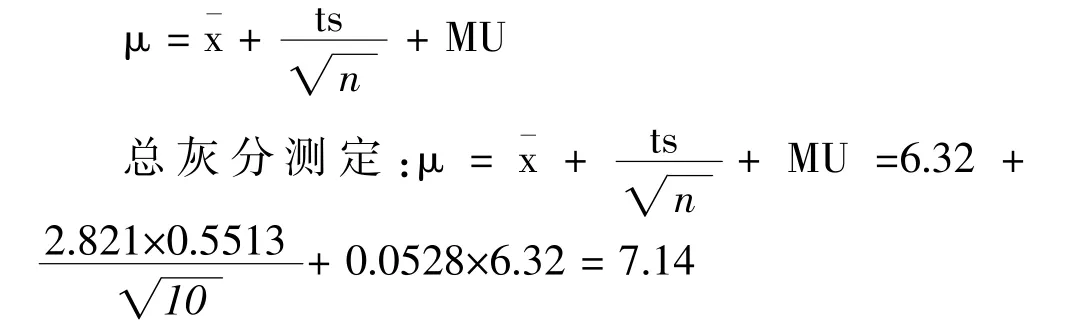
根据计算结果,拟定总灰分限度应不得过7.0%。
2.6.2 酸不溶灰分测定
共测定10批次三七花饮片的酸不溶性灰分,其平均值为0.09%,拟定不列入限度要求。酸不溶性灰分主要考察泥沙污染,而三七花为地上部分,且10批三七花酸不溶性灰分结果都很低,说明污染不明显,所以只规定总灰分,酸不溶性灰分不做限度要求。
2.7 浸出物测定
用水作溶剂,照水溶性浸出物热浸法测定,共测定10批次三七花饮片浸出物(具体方法参照《中国药典》2015年版四部2201浸出物测定法)。结果见表3。
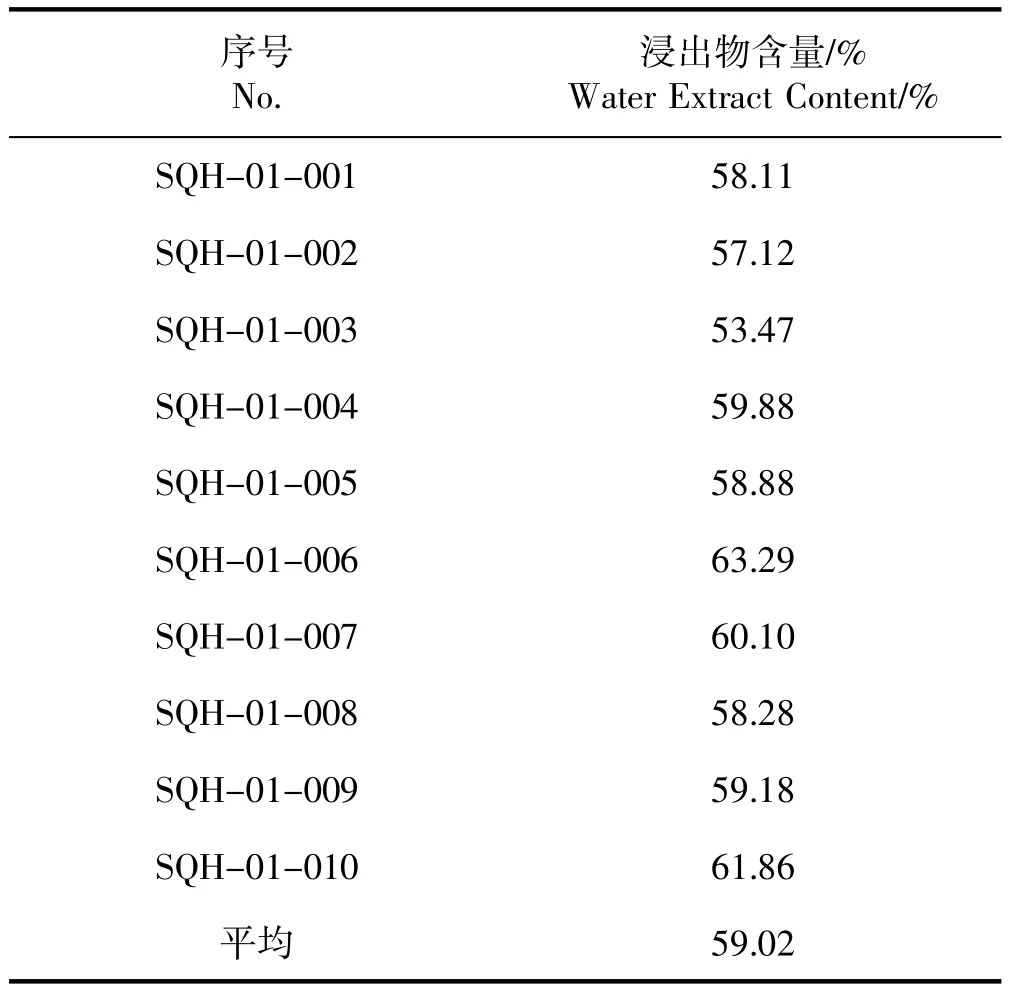
表3 水浸出物含量实验Table 3 Water extract content text
从以上结果可知10批三七花饮片的浸出物在53.47%~63.29%之间。应以统计学方法分析测试数据,基于测试数据,设定浸出物限度的公式如下:

拟定照水溶性浸出物测定法 (参照 《中国药典》2015年版四部2201)测定,用水作溶剂,浸出物不得少于49.0%。
2.8 含量测定
照高效液相色谱法 (《中国药典》2015年版四部0512)测定。
2.8.1 色谱条件与系统适用性试验
以十八烷基硅烷键合硅胶为填充剂;以乙腈-水(32:68)为流动相;检测波长为203nm,理论板数按人参皂苷Rb3峰计算应不低于5000。
2.8.2 对照品溶液的制备
取人参皂苷Rb2、人参皂苷Rb3对照品适量,精密称定,加甲醇制成每1mL约含20μg的溶液,即得。
2.8.3 供试品溶液的制备
取本品粉末(过2号筛)约0.25 g,精密称定,置50ml量瓶中,加甲醇45mL,超声处理(功率240W,频率45kHz)60min,放冷,加甲醇至刻度,摇匀,滤过,取续滤液,即得。
2.8.4 线性范围考察
精密称取纯度为93.8%的人参皂苷Rb2对照品10.75mg,置50 mL容量瓶中,加甲醇稀释至刻度,摇匀,得对照品溶液储备液,分别精密量取一定量的的对照品储备液稀释成浓度分别为 0.0403、0.0807、0.1008、0.1210、0.1613、0.2017 mg·mL-1的对照品溶液;精密称取纯度为97.0%人参皂苷Rb3对照品19.80mg,置50 mL容量瓶中,加甲醇稀释至刻度,摇匀,得对照品溶液储备液,分别精密量取一定量的的对照品储备液稀释成浓度分别为0.0768、0.1536、0.1921、0.2305、0.3073、0.3841mg·mL-1的 对 照 品 溶液,注入液相色谱仪,测定含量,以浓度为纵坐标、峰面积为横坐标得标准曲线f(x)=2,291,845.94351 x-478.50000 (r=0.99994)及f(x)=2,328,302.59251 x+2,319.57143(r=0.99992)。
2.8.5 重复性试验
取SQH-01-010样品约0.25g,精密称定,置50mL量瓶中,加甲醇45mL,超声处理(功率240W,频率45kHz)60min,放冷,加甲醇至刻度,摇匀,滤过,取续滤液,测定含量,平行取样测定5次,计算每次人参皂苷Rb2、人参皂苷Rb3的含量及RSD%,结果见表4。
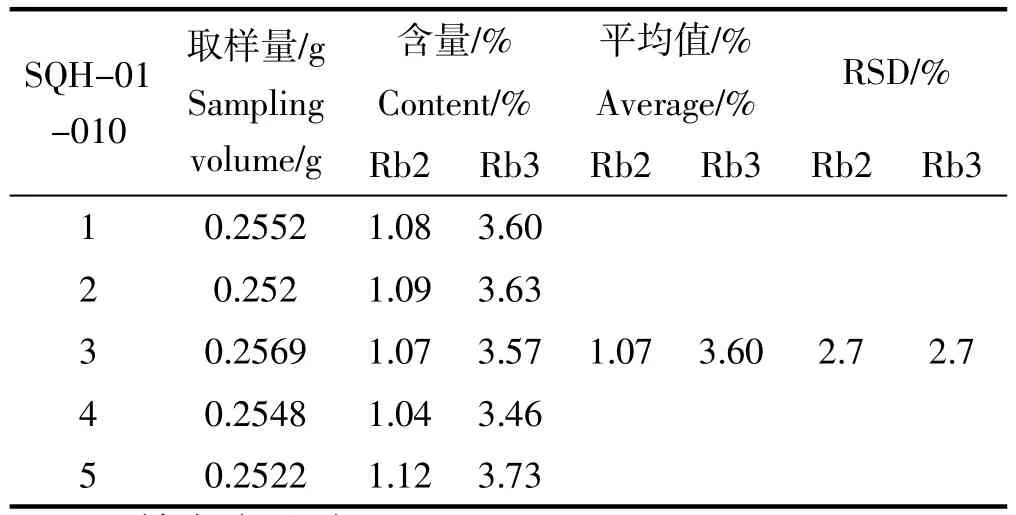
表4 重复性实验(n=5)Table 4 Repeated text(n=5)
2.8.6 精密度试验
精密称取人参皂苷Rb2对照品10.75 mg、人参皂苷Rb3对照品19.80mg,置50 mL容量瓶中,加甲醇超声使溶解,定容,摇匀,滤过,取续滤液10 μL注入液相色谱仪,测定峰面积,平行测定5次,计算RSD%,结果见表5。
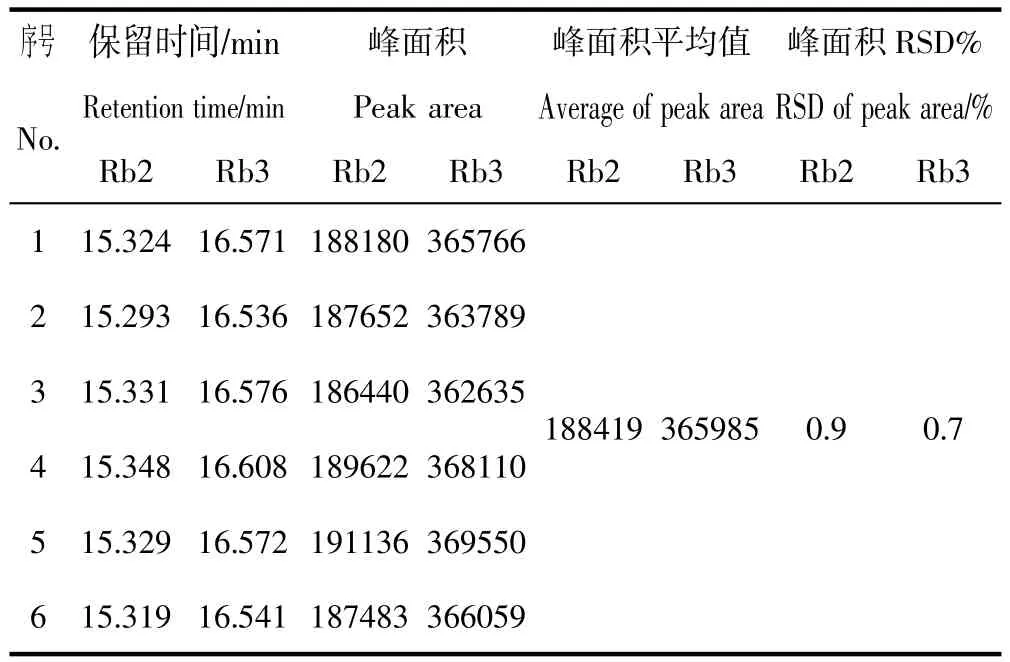
表5 精密度试验(n=6)Table 5 Precision text(n=6)
2.8.7 稳定性试验
取样品SQH-01-001适量,按供试品溶液的制备项下,同法制备样品溶液,分别在 0、4、8、12、24h 等,分别进样,测定人参皂苷Rb2、Rb3的含量并计算RSD%值,结果见表6。
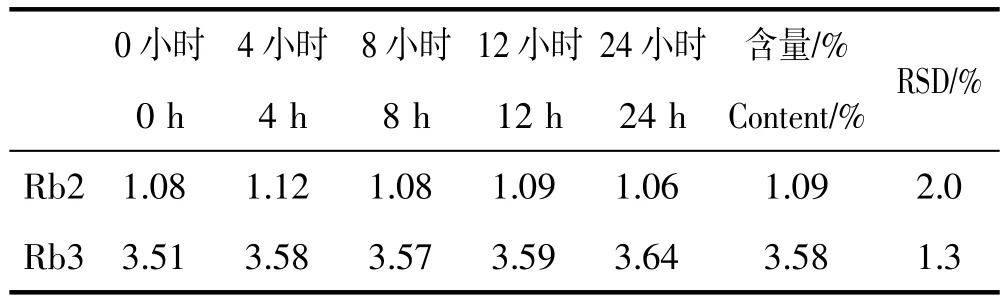
表6 稳定性试验(n=2)Table 6 Stability text(n=2)
2.8.8 加样回收率试验
取SQH-01-001样品约0.12g,精密称定,精密加入含人参皂苷Rb2、Rb3的对照品溶液,按供试品溶液制备方法处理,得相关溶液,进液相色谱仪处理,计算含量及加样回收率,结果见表7。
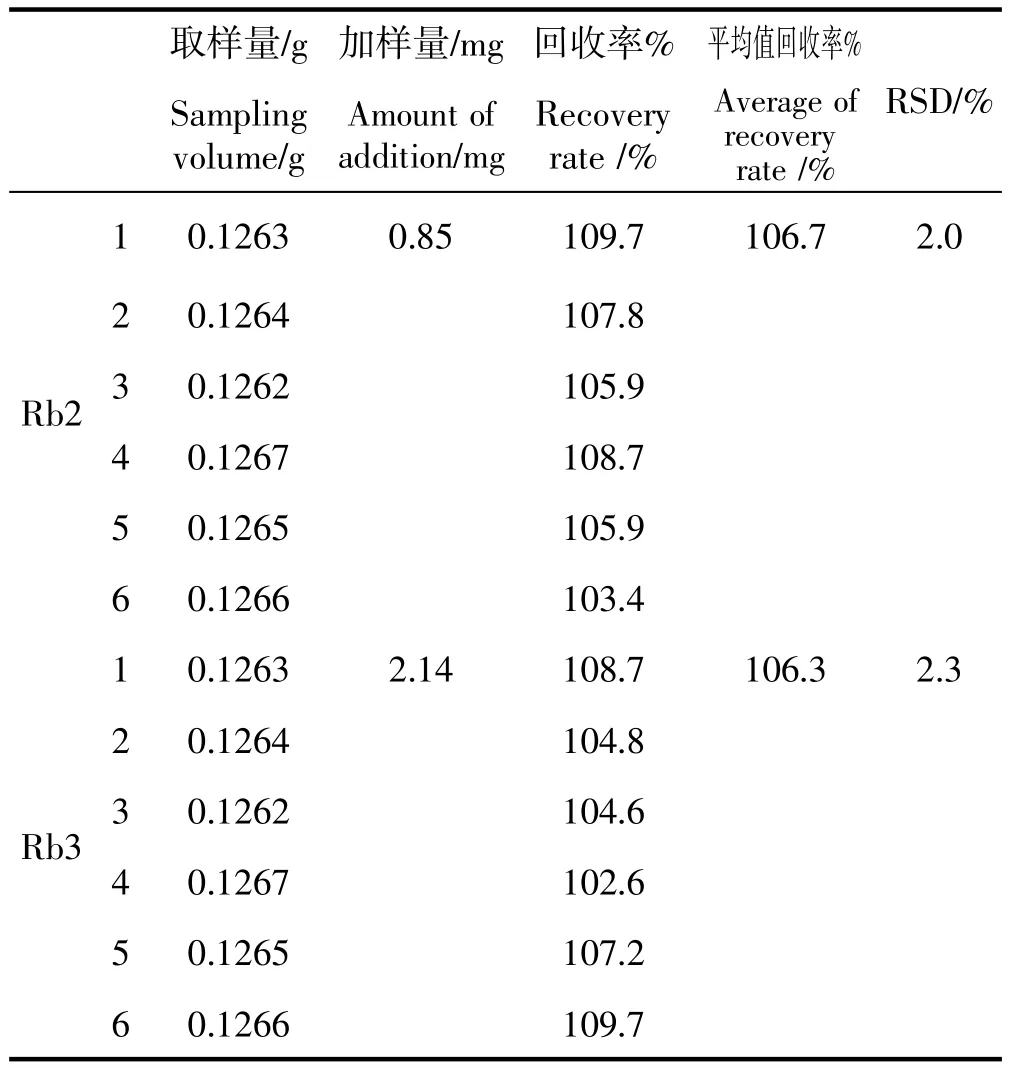
表7 加样回收率实验(n=6)Table 7 Recovery rate text(n=6)
2.8.9 样品测定
测定10批样品结果见表8,根据数据计算,参照《中国药典》2015年版相关原则,拟定含量限度为:按干燥品计算本品含人参皂苷Rb2不得少于1.0%、人参皂苷Rb3不得少于3.0%。
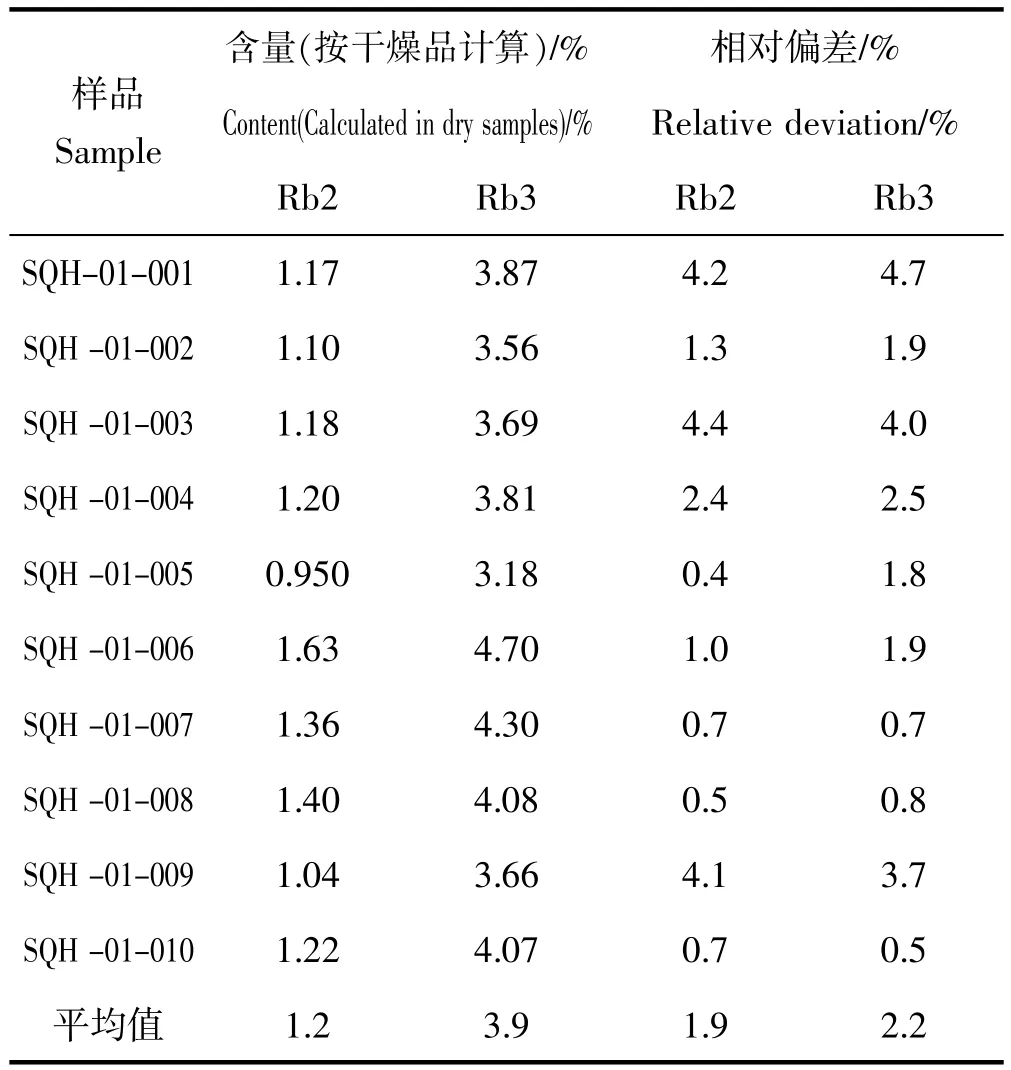
表8 含量测定实验(n=10*2)Table 8.Content determination text(n=10*2)
3 讨论
3.1 方法学考察
提取条件的选择:溶剂选取甲醇,分别测定不同料液比及不同提取时间提取的含量,结果显示,当料液比相同时,提取60min较30min的提取率更高,故选择称取0.25g,用甲醇定容至50mL,超声60min为提取条件。
3.2 薄层鉴别
三七花是三七全株中含人参皂苷最多的部位,且以Rb族为主[15]。鉴于三七花中的有效成分人参皂苷Rb3活性明确,单体标准物质易于获得符合法定标准的成品,在三七各部位中仅在三七花和三七茎中存在[16]。且人参皂苷Rb3在易混药材人参花中含量极低,可作为特征化合物用于鉴别人参花与三七花[17],故本实验以其作为对照品进行薄层鉴别。
3.3 含量测定
含量测定在药材质量控制中是最为重要的一部分,根据含量测定的结果可以判断该药材是否经历了规范的制备流程,淘汰有效成分含量过低的药材,从而保证药材质量,保证疗效。本次实验中尚存在一些不足,在加样回收率实验中,理论要求加样回收率在92%~105%,RSD<5%,但实测结果差中Rb2的平均回收率为106.7%,Rb3的平均回收率为106.3%,RSD为2.3%,与理论要求存在一定差异。在样品测定实验中,部分批次样品数据相对偏差大于2%。故在日后在对三七花有效成分含量测定的研究中,还需对实验条件进一步优化,从而建立更加完备的质量标准。
4 结论
根据实验结果可以看出,性状特征,显微特征鉴别定、波层色谱法鉴别等实验能够对三七花进行真伪鉴定,水分、灰分等检查以及浸出物测定等能够控制三七花的优劣。含量测定以人参皂苷Rb2、人参皂苷Rb3为指标,实验测定分别应不得少于1.0%和3.0%,但方法学考察稍有偏离标准要求,需进一步研究。本实验研究符合国家有关中药材质量标准制定要求,能够对三七花的质量控制提供标准依据。
