清开灵注射液对脑缺血大鼠急性期病理形态学、炎症因子及凋亡基因Bcl-2和p53表达的影响∗
2020-08-08单洁龄李志强吴书菊
单洁龄 李志强 吴书菊△
(1.上海市浦东新区浦南医院,上海 200125;2.上海中医药大学附属曙光医院,上海 200021)
缺血性脑血管病是世界范围内常见的高危疾病,约占脑血管疾病的70%~80%,是因脑部血液循环障碍引发缺血、缺氧,导致局部脑组织变性坏死,脑组织受损[1]。脑缺血在发生和发展中多伴有炎症反应,在急性期尤为明显。凋亡是脑缺血神经元死亡的主要方式,是目前脑缺血机制研究的热点。目前研究认为,Bcl-2和p53是最重要的调控基因[2]。中医学认为急性期脑缺血的机制为痰瘀互结、兼夹气血不足、脾胃升降失调,所致脑脉不通,治宜活血醒脑开窍[3-4]。清开灵注射液具有清热解毒、化痰通络、醒神开窍之功效,用于治疗热病神昏、中风偏瘫、神志不清等脑血管病,具有较好的临床疗效[5],但其作用机制研究尚不明确。本研究旨在观察清开灵注射液对脑缺血模型大鼠急性期的脑组织病理学、炎症因子及脑细胞凋亡相关蛋白的影响,旨在为临床应用提供科学依据。
1 材料与方法
1.1 实验动物
60只SPF级SD大鼠,雌雄各半,体质量(200±20)g,购于上海邦耀生物科技有限公司,动物许可证号:SYXK(沪)2018-0034。置于(23±2)℃室温中,昼夜节律,自由饮水进食,适应环境7 d后于9∶00~17∶00进行实验。
1.2 药物与仪器
清开灵注射液(广州白云上制药有限公司,批号181205);尼莫地平注射液(上海信谊金朱药业有限公司,批号190407);水合氯醛(国药集团化学试剂有限公司),苏木素和伊红以及TTC(Sigma公司)、BCA蛋白定量试剂盒和trizol试剂盒(武汉博士德生物工程有限公司)、兔p53和Bcl-2抗体(Sigma公司),PCR试剂盒(南京诺唯赞生物科技有限公司);免疫组组织化学试剂盒购于凋亡试剂盒和DAB显色试剂盒购于武汉博士德生物工程有限公司;GAPDH抗体购与Cell Signaling Technology公司;PBS缓冲液和二抗由碧云天生物技术研究所提供;其他试剂均为分析纯购于天津市广成化学试剂有限公司;氯化钠注射液(批号07112133)由山东康宁药业有限公司提供,实验用水为超纯水。
1.3 分组与造模
将评分相近的60只SD大鼠随机分为4组,每组15只,即假手术组、模型组、阳性组和实验组。参考文献[6]制备脑缺血大鼠模型,将除假手术组外的大鼠,采用水合氯麻醉,俯卧固定于手术台,采用改良线栓法制作脑缺血大鼠模型,分组分笼饲养,不禁食水。假手术组大鼠仅用玻璃分针游离出双侧颈总动脉不做结扎处理。造模成功后7 d,阳性组给予尼莫地平注射液10 mg/kg腹腔注射;实验组给予清开灵注射液50 mg/kg腹腔注射,对照组和模型组均给予同体积的0.9%氯化钠注射液腹腔注射,连续7 d。
1.4 神经功能评分 采用BBB运动功能评分[7]评价运动功能,于术后7 d后对各组大鼠进行神经行为学评分并记录结果,分为各关节活动能力、后肢步态及协调能力以及运动过程中爪的精细动作等3部分,共21分,评分越高运动功能越理想。采用Garcia评分法[8]对各组大鼠神经功能进行评分,总分计3~18分,得数越低,损伤程度越重。
1.5 标本采集与检测
1.5.1 脑组织梗死情况及神经细胞凋亡检测 造模7 d后,颈椎脱臼法处死大鼠后迅速剥取脑组织,置于-20℃冰箱中15 min。取出脑组织,剥离海马CA1区,0.9%氯化钠注射液清洗,固定48 h后,二甲苯脱脂,酒精脱水,石蜡包埋,切片。取切片置于2%TTC染色液中染色,避光孵育30 min,10%甲醛固定,通过经图像分析系统测量脑梗死面积。其中梗死的脑组织呈白色,正常的脑组织为红色。取切片脱蜡脱水,置于TUNEL试剂盒反应液和复合液中进行DAB显色,苏木素染色5 min后封片,阴性对照置于蒸馏水中,显微镜下观察神经细胞凋亡情况,选取5个400倍视野分别计数凋亡细胞数目。
1.5.2 炎症因子的测定 7 d后收集3 mL腹动脉血液,离心,分离血清,ELISA法检测肿瘤坏死因子-α(TNF-α)、白介素-1β(IL-1β)、白介素-6(IL-6)以及白介素-18(IL-18)炎症因子水平,严格按照试剂盒说明书操作。
1.5.3 凋亡基因测定 称取200 mg脑组织进行样品制备,trizol法提总RNA,取1 g总RNA进 行逆转录cRNA合成,严格按照逆转录试剂盒和相关引物的说明书加入相应量的试剂进行聚合酶链反应,经1.5%琼脂糖凝胶电泳分离,利用全自动数码凝胶分析仪检测目的cRNA。BCA法测定蛋白浓度,Western blotting检测Bcl-2表达水平,免疫组织化学法检测p53表达水平。
1.6 统计学处理

表1 RT-PCR相关参数
应用SPSS19.0统计软件。计量资料以()表示,采用t检验比较组内和组间差异;计数资料以(%)表示,应用χ2检验。P<0.05为差异具有统计学意义。
2 结 果
2.1 各组大鼠神经功能评分和神经行为学评分比较
见表2。与假手术组比较,模型组大鼠的BBB评分和神经功能评分明显低于假手术组(P<0.05)。给予药物干预后,阳性组和实验组大鼠的BBB评分和神经功能评分明显高于模型组(P<0.05),两组大鼠的BBB评分和神经功能评分间比较均有显著性差异(P<0.05)。
表2 各组大鼠的BBB评分和神经功能评分比较(分,±s)

表2 各组大鼠的BBB评分和神经功能评分比较(分,±s)
与假手术组比较,∗P<0.05;与模型组比较,△P<0.05。下同
组别假手术组模型组阳性组实验组n 10 10 10 10 BBB评分19.40±2.04 8.27±1.34*13.14±0.81*#15.62±0.76*#神经功能评分16.50±2.00 8.08±1.21*12.08±1.19*#14.25±0.92*#
2.2 各组大鼠脑组织梗死体积及神经细胞凋亡情况比较
见表3。假手术组大鼠的脑组织细胞未见明显病理改变、神经元排列紧密整齐,核仁明显可见,居中,细胞膜清晰。模型组脑组织神经元明显减少,结构模糊构型紊乱,不规则出现不同程度变性坏死及炎细胞浸润、核体固缩深染;与模型组相比,阳性组和实验组的神经元均明显增多,有不同程度的缓解恢复,核固缩核体均有不规则程度的减轻,间质水肿减轻,细胞结构较完整,见图1~图2。与假手术组比较,模型组大鼠的脑梗死体积和神经细胞凋亡明显升高(P<0.05),给予药物治疗后,阳性组和实验组的脑梗死体积和神经细胞凋亡水平明显降低(P<0.05),两组间比较均有显著性差异(P<0.05)。
表3 各组大鼠脑梗死体积及神经细胞凋亡比较(±s)

表3 各组大鼠脑梗死体积及神经细胞凋亡比较(±s)
组别假手术组模型组阳性组实验组n 15 15 15 15脑梗死体积(%)0.00±0.00 45.37±4.38*32.03±5.01*#33.95±3.96*#神经细胞凋亡(个)11.12±1.87 65.28±7.26*30.98±3.42*#32.15±4.05*#

图1 各组大鼠的脑组织病理图(TTC,400倍)

图2 各组大鼠的脑组织梗死面积比较
2.3 各组大鼠炎症因子水平比较
见表4。与假手术组比较,模型组大鼠的TNF-α、IL-1β、IL-6以及IL-18水平明显升高(P<0.05)。给予药物干预后,阳性组和实验组大鼠的炎症因子水平明显降低(P<0.05),两组大鼠的炎症因子比较有显著性差异(P<0.05)。
表4 各组大鼠炎症因子水平比较(pg/mL,±s)

表4 各组大鼠炎症因子水平比较(pg/mL,±s)
与阳性组比较,△P<0.05。下同
组别假手术组模型组阳性组实验组n 15 15 15 15 TNF-α 45.89±6.16 124.75±12.08*75.09±9.14*#64.28±7.32*#△IL-1β 34.53±4.67 106.72±13.85*64.66±7.54*#55.69±6.71*#△IL-6 26.12±2.67 78.47±7.86*50.57±4.45*#42.87±3.09*#△IL-18 23.14±2.59 61.23±6.12*40.47±5.74*#35.12±3.26*#△
2.4 各组大鼠凋亡基因Bcl-2和p53表达比较
见表5,图3。与假手术组比较,Bcl-2基因表达和Bcl-2蛋白表达的相对丰度值明显降低,具有显著差异(P<0.05),模型组大鼠的凋亡基因p53基因表达和p53蛋白表达的相对丰度值明显升高(P<0.05)。给予药物干预后,Bcl-2基因表达和Bcl-2蛋白表达的相对丰度值明显高于模型组(P<0.05),阳性组和实验组大鼠的p53基因表达和p53蛋白表达的相对丰度值明显低于模型组,两组比较均有显著性差异(P<0.05)。
表5 各组大鼠凋亡基因Bcl-2和p53表达比较(分,±s)
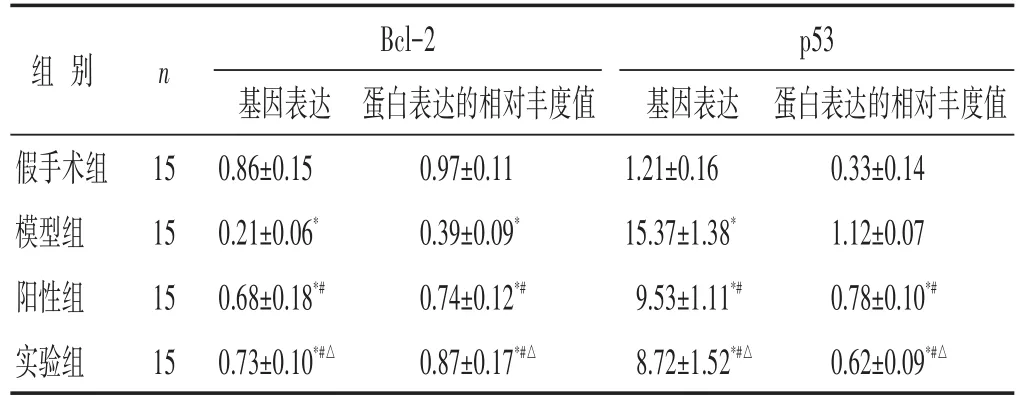
表5 各组大鼠凋亡基因Bcl-2和p53表达比较(分,±s)
组别假手术组模型组阳性组实验组n 15 15 15 15 Bcl-2基因表达0.86±0.15 0.21±0.06*0.68±0.18*#0.73±0.10*#△蛋白表达的相对丰度值0.97±0.11 0.39±0.09*0.74±0.12*#0.87±0.17*#△p53基因表达1.21±0.16 15.37±1.38*9.53±1.11*#8.72±1.52*#△蛋白表达的相对丰度值0.33±0.14 1.12±0.07 0.78±0.10*#0.62±0.09*#△

图3 各组大鼠的凋亡相关蛋白电泳条带
3 讨 论
脑缺血病理生理变化与炎症因子及氧自由基大量产生、细胞内Ca2+超载、凋亡相关蛋白表达的启动等多方面因素密切相关[9]。神经功能和神经行为学指标对脑缺血疾病的研究具有重要作用,可真实反映脑缺血疾病程度。炎症在脑缺血病程进展中发挥着重要作用,脑缺血可打破促炎和抗炎反应间的动态平衡,且炎症标志物水平与预后不良密切相关[10-11],研究发现,脑缺血的炎症反应是一个动态过程,脑部缺血中心区的坏死组织因大量的炎症介质及炎症因子的释放,激活免疫应答,加重炎症反应,而炎症反应释放大量的氧自由基、一氧化氮、兴奋性氨基酸等毒性物质,相互作用明显造成脑组织不可逆的损伤,可诱发神经细胞凋亡,最终导致脑细胞凋亡甚至坏死,加重脑损伤[12]。TNF-α是炎症反应的起始因子,具有多效促炎性及神经毒性作用,导致内皮细胞功能失调,致使内皮细胞屏障的渗透性增加[13]。IL-1β是脑缺血状态下由星形胶质细胞等大量分泌而成的,参与炎症级联扩大反应,是脑缺血早期炎症反应的重要炎症因子,是脑缺血损伤的病理生理基础。而且IL-1β的激活会促进TNF-α分泌,同时二者会增加其他炎症因子表达,导致脑损伤程度加重。IL-6为炎症递质,可加重脑缺再灌注的全身反应和局部损伤。IL-18参与了急性脑损伤的病理生理过程,且其血清中含量与脑损伤程度密切相关,对于临床诊断预后判断和提高患者救治水平有重要意义[14]。细胞凋亡是指机体受刺激后一系列基因参与的细胞自主有序的程序性死亡,Bcl-2、P53等是细胞凋亡启动的关键。Bcl-2为高度同源蛋白中的经典的抗凋亡蛋白,在细胞凋亡进程中发挥着重要的调节作用,在调控细胞自噬的过程中也有重要作用[15]。此外,Bcl-2还能调控氧化应激诱导自噬和凋亡[16]。p53作为转录因子可通过调节多种基因的转录参与诱导细胞凋,是调控的凋亡蛋白中的重要成员之一[17]。
脑缺血属于中医学“中风”范畴,痰瘀互结、脑脉不通为病机,气血、脾胃升降失调,治宜活血醒脑开窍。清开灵注射液方中水牛角粉清热定惊、凉血解毒、为君药。胆酸、猪去氧胆酸清热解毒、息风止痉、开窍豁痰;栀子、板蓝根、黄芩、金银花清热解毒,燥湿泻火,共为臣药。佐以珍珠母清心肝之火而明目。诸药相合,共奏清热解毒、化痰通络、醒神开窍之功。现代药理发现[18-20],水牛角有明显的抗炎作用,可用于炎症性疾病的治疗;黄芩苷可通过调控线粒体自噬减轻胞神经元细胞缺血缺氧再灌注损伤;栀子中的活性成分栀子苷和西红花苷I,可通过改善线粒体的能量代谢抗氧化抗炎抑制细胞凋亡等途径在脑缺血的治疗中发挥作用,而且黄芩苷栀子苷配伍可通过抑制兴奋性氨基酸的释放而发挥脑保护作用。
本研究结果显示,与假手术组比较,模型组大鼠的神经功能评分、神经行为学评分明显降低,大鼠的脑组织神经元明显减少,结构模糊构型紊乱,不规则出现不同程度变性坏死及炎细胞浸润、核体固缩深染,脑梗死体积、神经细胞凋亡、TNF-α、IL-1β、IL-6以及IL18水平。给药后,阳性组和实验组大鼠的神经元均明显增多,有不同程度的缓解恢复,核固缩核体均有不规则程度的减轻,间质水肿减轻,细胞结构较完整,神经功能评分和神经行为学评分明显升高,脑梗死体积、神经细胞凋亡、炎症因子水平明显低于模型组,提示清开灵注射液能有效地提高脑缺血大鼠的神经功能和神经行为学指标,减少脑梗死体积和神经细胞凋亡,降低炎症因子水平。与假手术组比较,模型组大鼠脑部Bcl-2表达显著下调,p53表达显著上调。给予药物干预后,阳性组和实验组的大鼠脑部Bcl-2蛋白水平显著上调,p53表达显著下调,提示清开灵注射液能有效地调整凋亡相关因子表达,减少脑部细胞的死亡,激活脑细胞自我保护。
综上所述,清开灵注射液对脑缺血模型大鼠可有效地减少脑梗死面积,保护脑组织免受炎症因子的损伤,调整凋亡相关因子表达,减少神经细胞的凋亡,激活脑细胞自我保护。
