大孔吸附树脂法吸附桑葚色素及其稳定性研究
2020-07-17许先猛董文宾王芳张增帅黄健马蓉丽
许先猛,董文宾,,王芳,张增帅,黄健,3,马蓉丽
(1.运城职业技术学院,山西运城044000;2.陕西科技大学,陕西西安710021;3.运城学院,山西运城044000)
桑椹(Mulberry),俗称桑果,含有丰富的多酚类、黄酮类、维生素、有机酸、生物碱和矿物质等活性成分[1],桑葚及桑葚提取物具有保护肝肾、降血压、控制肥胖、抗血栓、抗肿瘤、抗衰老、抗病毒和提高免疫力等功效[2-4],且桑葚被我国列为“药食同源”食品。桑葚通体呈黑紫色或紫红色,红色素含量较丰富,色价高。近年来,天然色素的开发和研究已成为部分研究学者的关注重点[5]。桑椹红色素是一种天然色素,因着色效果好,在果酒、果汁、饮料、糖果生产中被广泛应用。本试验采用有机溶剂浸提法提取桑葚色素,研究了大孔吸附树脂法纯化桑葚色素工艺,并对制备和纯化的桑葚色素稳定性进行了测定,以期为桑葚色素提取、纯化和应用研究奠定基础。
1 材料与方法
1.1 材料与仪器
桑椹:采自山西省运城市桑葚农场。
大孔吸附树脂:西安蓝晓科技有限公司;无水乙醇:天津市红岩化学试剂厂;柠檬酸:上海化学试剂公司;氢氧化钠、蔗糖、浓盐酸:天津市天力化学试剂有限公司;酒石酸:天津市北方天医化工试剂厂;醋酸:天津市富宇精细化工有限公司;氯化钾:重庆北培精细化工厂;阿斯巴甜、木糖醇:山东福田科技集团。所有试剂均为分析纯。
FD-T-50真空冷冻干燥机:北京博医康实验仪器有限公司;BS-224型电子天平:德国SARTORIUS公司;722型可见分光光度计、752型紫外可见分光光度计:上海光谱仪器有限公司;RE-52AA型旋转蒸发器、SHZ-III循环水多用真空泵:上海亚荣生化仪器厂;HH-Z2恒温水浴锅:郑州长城科工贸有限公司;PHS-3C精密pH计:上海精密科学仪器有限公司;TDL-5型离心机:上海安亭科学仪器厂;101-1AB电热鼓风干燥箱:天津市泰斯特仪器有限公司;HYG-Ⅱa回转式恒温调速遥瓶柜:上海欣蕊自动化设备有限公司;微量移液器:芬兰Dragonmed公司。
1.2 试验方法
1.2.1 桑葚色素提取和大孔吸附树脂纯化
1)桑葚色素提取:取适量桑椹→制浆→准确称取→加入80%酸性乙醇溶液(pH 2.0),搅拌均匀→50℃避光水浴提取2 h→取上清液,浓缩→醇沉→过滤→真空浓缩→制得桑葚色素溶液(冷藏备用)。
2)桑葚色素大孔吸附树脂纯化:大孔吸附树脂预处理→桑葚色素吸附→桑葚色素解吸→真空浓缩→冷冻真空干燥→桑葚色素冻干粉(室温25℃、密封、避光保存备用)。
1.2.2 桑葚色素测定方法
1)pH示差测定法:分别取1 mL桑葚色素溶液样品置于两根试管之中,分别加入pH(1.0±0.01)的缓冲溶液与pH 4.5的缓冲溶液,静置后得到待测液。平行测定 3组,按式(1)和(2)计算桑葚色素浓度[6]。

式中:ε表示矢车菊花素-3-葡萄糖苷的消光系数,26 900;DF表示稀释因子;MW表示矢车菊花素-3-葡萄糖苷的分子量,449.2;L表示光程,1 cm。以蒸馏水作为参比,用A700nm来消除样液混浊的影响。
1.2.3 大孔吸附树脂的预处理
大孔树脂预处理参考刘玲翠等[7]方法,稍作改动。分别将选用的9种大孔吸附树脂LX-60、LX-36、LXA-8、LSA-10、LSA-21、XDA-8、XDA-7、LS305、LS300用无水乙醇密封浸泡24 h,蒸馏水冲洗乙醇,用1 mol/L的NaOH浸泡24 h,蒸馏水洗至中性,用1 mol/L的HCl浸泡24 h,以蒸馏水洗至中性后备用。
1.2.4 桑椹色素吸附率、解吸率及吸附量的计算
桑葚色素吸附率、解吸率和吸附量计算参照李园园等[8]方法,稍作改动。分别准确称取30.0g预处理后的 9 种大孔吸附树脂 LX-60、LX-36、LXA-8、LSA-10、LSA-21、XDA-8、XDA-7、LS305、LS300 置于 500 mL 具塞锥形瓶中,分别加入200 mL已知浓度的色素溶液,避光和密封处理,30℃下70 r/min振荡4 h,过滤后,记录溶液体积,并测定其吸光度计算桑葚色素浓度。
将吸附色素的树脂置于500 mL具塞锥形瓶中,加入200 mL的80%乙醇,避光和密封处理,30℃下70 r/min解吸振荡60 min,过滤后,记录溶液体积,并测定其吸光度计算桑葚色素浓度。
桑椹色素吸附率、解吸率及吸附量用以下公式计算:

式中:C0表示吸附液中色素浓度,mg/L;V0表示吸附液体积,L;C1表示吸附后上清液中色素浓度,mg/L;V1表示上清液体积,L;C2表示洗脱液中色素浓度,mg/L;V2表示洗脱液体积,L。
1.2.5 桑葚色素大孔树脂吸附
1.2.5.1 桑葚色素大孔树脂吸附单因素试验考察
选取大孔树脂吸附时间、桑葚色素解吸乙醇浓度、桑葚色素解吸时间、解吸次数等单因素进行试验,考察各因素对桑葚色素吸附量的影响。
1.2.5.2 桑葚色素大孔树脂吸附正交试验考察
对吸附时间、解吸乙醇浓度、解吸时间、解吸次数4个因素进行正交试验,选取3个水平,采用L9(34)设计正交试验进行条件优化。试验因素水平表见表1。

表1 正交试验因素水平表Table 1 The factors of the orthogonal test
1.2.6 桑葚色素稳定性研究
1.2.6.1 pH值对桑椹色素稳定性的研究
称取一定量的桑葚色素冻干粉,用蒸馏水溶解制备0.1mg/mL桑葚色素溶液,分别用1 mol/L HCl溶液和1 mol/L NaOH 溶液调节 pH 值分别为 1、2、3、4、5、6、7、8、9、10、11、12、13、14 的桑葚色素溶液,静置 70 min后,扫描在200 nm~800 nm波长范围内不同pH值条件下桑葚色素最大吸收峰。
1.2.6.2 光照对桑椹色素稳定性研究
称取一定量的桑葚色素冻干粉,用蒸馏水溶解制备0.1 mg/mL桑葚色素溶液,室温(25℃)常光下静置5 d,每天测定色素含量。
1.2.6.3 温度对桑椹色素稳定性研究
称取一定量的桑葚色素冻干粉,用蒸馏水溶解制备0.1 mg/mL桑葚色素溶液,将桑椹色素溶液分别置于 20、40、60、80、100 ℃水浴中加热 5 h,每隔 1 h 测定色素含量。
1.2.6.4 甜味剂对桑椹色素稳定性研究
称取一定量的桑葚色素冻干粉,分别溶解在浓度为的10%蔗糖、3.5%木糖醇、0.3%阿斯巴甜溶液中,制备0.1 mg/mL桑葚色素溶液,蒸馏水作对照,室温(25℃)避光静置5 d,每天测定色素含量。
1.2.6.5 酸味剂对桑椹色素稳定性研究
称取一定量的桑葚色素冻干粉,分别溶解在浓度为2%的醋酸、2%柠檬酸、1%酒石酸溶液中,制备0.1 mg/mL桑葚色素溶液,蒸馏水作对照,室温(25℃)避光静置5 d,每天测定色素含量。
1.3 数据处理
2 结果与讨论
2.1 大孔吸附树脂筛选
2.1.1 不同种类大孔吸附树脂对桑葚色素的吸附效果
在30℃、避光、密封、摇床转速为70 r/min条件下,LX-60、LX-36、LXA-8、LSA-10、LSA-21、XDA-8、XDA-7、LS305、LS300等9种大孔吸附树脂对桑葚色素吸附4 h,大孔树脂吸附率如图1所示。

图1 不同大孔吸附树脂吸附率Fig.1 The adsorption of different macroporous
由图 1 可以看出,LX-36、LSA-21、XDA-8、LS-305,4种大孔吸附树脂对桑葚色素吸附率较高,吸附率都超过了90%。
2.1.2 不同种类大孔吸附树脂对桑葚色素的解吸效果
在30℃、避光、密封、摇床转速为70 r/min条件下,用80%乙醇溶液解吸附60 min,大孔吸附树脂解吸率如图2所示。
由图 2 可以看出,LXA-8、LSA-21、XDA-8,3 种大孔树脂对桑葚色素解吸率较高,解吸率都超过了90%。
2.1.3 不同种类大孔吸附树脂对桑葚色素吸附量
大孔树脂对桑葚色素吸附量如图3所示。
由图3可以看出,XDA-8吸附量最高,其吸附量为1.81 mg/g。

图2 不同大孔吸附树脂解吸率Fig.2 The desorption of different macroporous

图3 不同大孔吸附树脂吸附量Fig.3 The adsorption capacity of different macroporous
综合考虑 LX-60、LX-36、LXA-8、LSA-10、LSA-21、XDA-8、XDA-7、LS305、LS300 等 9 种大孔吸附树脂对桑葚色素的吸附率、解吸率和吸附量3个因素,大孔吸附树脂XDA-8效果最好。桑葚色素主要成分为极性物质,在极性溶液中溶解度高,XDA-8大孔吸附树脂是极性树脂,因此XDA-8大孔吸附树脂对桑葚色素吸附效果较为明显。XDA-8为理想的大孔吸附树脂,用于桑葚色素的分离和纯化。
2.2 桑葚色素大孔吸附树脂分离纯
2.2.1 桑葚色素大孔树脂吸附单因素试验
2.2.1.1 吸附时间对桑葚色素吸附量的影响
桑葚色素溶液和XDA-8大孔吸附树脂置于500 mL具塞锥形瓶中避光和密封处理,30℃下70r/min分别振荡吸附 2、4、6、8、10、12 h,过滤,用 80%乙醇在30℃下70 r/min振荡解吸60 min,桑葚色素吸附量如图4所示。

图4 吸附时间对桑葚色素吸附量的影响Fig.4 The influence of adsorption time on the adsorption capacity
由图4可以看出,震荡吸附时间对XDA-8大孔吸附树脂的桑葚色素吸附量影响呈现先上升后趋于平缓的趋势,震荡吸附时间超过4 h后,震荡吸附时间对XDA-8大孔吸附树脂的桑葚色素吸附量影响不明显。李瑞琦[9]研究发现,D101大孔吸附树脂静态吸附桑葚色素3 h后吸附量趋于平稳,吸附达到饱和,这与本试验结果基本一致,本试验选取震荡吸附时间为4 h。
2.2.1.2 解吸乙醇浓度对桑葚色素吸附量的影响
桑葚色素溶液和XDA-8大孔吸附树脂置于500mL具塞锥形瓶中避光和密封处理,30℃下70 r/min振荡吸附4 h,过滤,分别用20%、40%、60%、80%、95%乙醇在30℃下70 r/min振荡解吸60 min,桑葚色素吸附量如图5所示。

图5 解吸乙醇浓度对桑葚色素吸附量影响Fig.5 The influence of desorption ethanol concentration on the adsorption capacity
由图5可以看出,随着解吸乙醇浓度的增加,XDA-8大孔吸附树脂的桑葚色素吸附量影响呈现先上升后下降的趋势,解吸乙醇浓度80%时XDA-8大孔吸附树脂的桑葚色素吸附量最高。解吸溶液为极性溶液,随着解析溶液乙醇浓度的增加解吸溶液极性有所降低,解吸溶液极性介于水和乙醇之间。当乙醇浓度为80%时,解吸溶液极性与桑葚色素极性最为接近,桑葚色素解吸率高,桑葚色素吸附量高,因此本试验选取解吸乙醇浓度为80%。
2.2.1.3 解吸时间对桑葚色素吸附量的影响
桑葚色素溶液和XDA-8大孔吸附树脂置于500mL具塞锥形瓶中避光和密封处理,30℃下70 r/min振荡吸附4 h,过滤,用80%乙醇在30℃下70 r/min分别振荡解吸 30、60、90、120、150 min,桑葚色素吸附量如图6所示。

图6 解吸时间对桑葚色素吸附量影响Fig.6 The influence of desorption time on the adsorption capacity
由图6可以看出,在大孔吸附树脂解吸时间为30 min至150 min范围内,随着解吸时间的延长,桑葚色素吸附量呈现先增加后平稳的趋势。解吸时间超过60 min后,继续延长解吸时间,桑葚色素吸附量基本没有变化。这是由于大孔吸附树脂吸附的桑葚色素量是定量,同时解吸溶液的解吸能力有限,解吸时间超过60 min后大孔吸附树脂中桑葚色素已基本解吸完成,本试验选取解吸时间为60 min。
2.2.1.4 解吸次数对桑葚色素吸附量的影响
桑葚色素溶液和XDA-8大孔吸附树脂置于500mL具塞锥形瓶中避光和密封处理,30℃下70 r/min振荡吸附4 h,过滤,用80%乙醇在30℃下70 r/min振荡解吸 60 min,分别解吸和震荡 1、2、3、4、5 次,桑葚色素吸附量如图7所示。

图7 不同解吸次数对多酚得率影响Fig.7 The influence of desorption times on the adsorption capacity
由图7可以看出,随着解吸次数的增加,桑葚色素吸附量呈现平缓增加的趋势,不同解吸次数对桑葚色素吸附量影响不明显。
2.2.2 桑葚色素大孔树脂吸附正交试验
在上述单因素试验基础上,桑葚色素大孔树脂吸附正交试验结果如表2所示。

表2 正交试验表Table 2 The orthogonal range analysis table
结果显示,影响桑葚色素吸附量的因素大小依次为 RB>RC>RD>RA,即解吸乙醇浓度>解吸时间>解吸次数>吸附时间,桑葚色素大孔树脂吸附最佳工艺为A2B2C3D3,即吸附时间为4 h、解吸乙醇浓度为80%、解吸时间为80 min、解吸次数3次。
2.2.3 验证试验
准确称取30.0 g XDA-8大孔吸附树脂置于500 mL具塞锥形瓶中,加入200 mL色素溶液,避光和密封处理,30℃下70 r/min分别振荡吸附4 h,过滤。将吸附色素的树脂置于500 mL具塞锥形瓶中,加入200 mL的80%乙醇,避光和密封处理,30℃下70 r/min振荡80 min,解吸3次,过滤后,记录溶液体积,重复3次取平均值。结果表明XDA-8大孔吸附树脂桑葚色素吸附量为1.89 mg/g。
2.3 桑椹色素稳定性研究
2.3.1 pH对桑椹色素稳定性影响的研究
调整桑葚色素溶液pH值,静置70min后,在200nm~800 nm波长范围内扫描桑葚色素最大吸收峰,结果如表3所示。

表3 pH值对桑椹色素稳定性的影响Table 3 Effects of pH on stability of mulberry pigments
由表3可以看出,当桑葚色素溶液pH 1.0和桑葚色素溶液为pH2.0时桑葚色素最大吸收峰在535 nm处,在桑葚色素溶液pH2.0至桑葚色素溶液pH6.0范围内,随着pH值的增大,桑葚色素最大吸收峰发生一定位移的红移。在桑葚色素溶液pH7.0至桑葚色素溶液pH14.0范围内,桑葚色素无最大吸收峰。这主要是由于桑葚色素溶液pH值升高会导致桑葚色素中花色苷结构改变,pH值超过6.0且继续升高,花色苷中的黄烊盐阳离子失去质子,花色苷中的醌式碱不断增加,花色苷中醌式结构为主体[10-11]。桑葚色素溶液pH值持续升高,还会导致碱式结构出现开环降解[12]。因此,桑葚色素在pH 2.0左右的酸性环境较为稳定。
2.3.2 光照对桑椹色素稳定性研究
将0.1 mg/mL桑葚色素溶液室温(25℃)常光下静置5 d,每天测定色素含量,结果如图8所示。

图8 光照对桑椹色素稳定性的影响Fig.8 Effects of light on stability of mulberry pigments
由图8可以看出,桑葚色素在不加入其他试剂的条件下随着在常光下静置时间的延长,桑葚色素的含量不断降低,因此桑葚色素在常光照射下结构不稳定,这与张国栋等[13]研究结果一致,因此桑葚色素保存及应用应注意避光处理。
2.3.3 温度对桑椹色素稳定性研究
将0.1 mg/mL桑葚色素溶液分别置于20、40、60、80、100℃水浴中,避光加热5 h,每隔1 h测定色素含量,结果如图9所示。
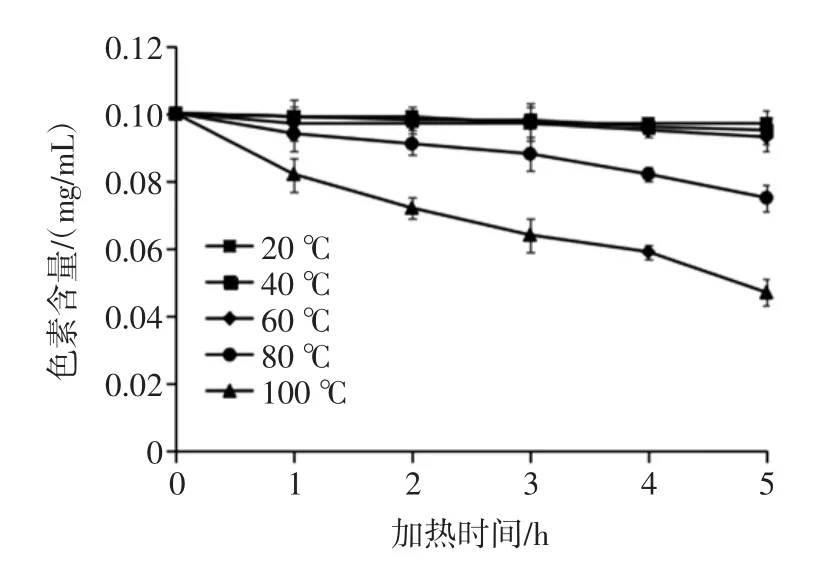
图9 温度对桑椹色素稳定性的影响Fig.9 Effects of temperature on stability of mulberry pigments
由图9可以看出,温度变化对桑葚色素稳定性有一定的影响,在20℃至60℃温度范围内,在5 h内温度对桑葚色素稳影响不大。当温度为80℃至100℃时,温度会破坏桑葚色素结构。桑葚色素长时间处于超过80℃温度下,桑葚色素含量会大幅度降低。
2.3.4 甜味剂对桑椹色素稳定性研究
制备含10%蔗糖、3.5%木糖醇、0.3%阿斯巴甜的0.1 mg/mL桑葚色素溶液,室温(25℃)避光静置5 d,每天测定色素含量,结果如图10所示。
由图10可以看出,常用的蔗糖、木糖醇、阿斯巴甜等甜味剂在一定的浓度下对桑葚色素稳定性影响不明显,食品加工过程中甜味剂的正常使用不会对桑葚色素稳定性产生较大影响。

图10 甜味剂对桑椹色素稳定性的影响Fig.10 Effects of sweeteners on stability of mulberry pigments
2.3.5 酸味剂对桑椹色素稳定性研究
制备含2%的醋酸、2%柠檬酸、1%酒石酸的0.1 mg/mL桑葚色素溶液,室温(25℃)避光静置5 d,每天测定色素含量,结果如图11所示。

图11 酸味剂对桑椹色素稳定性的影响Fig.11 Effects of acidified agent on stability of mulberry pigments
由图11可以看出,常用的醋酸、柠檬酸、酒石酸等酸味剂在一定的浓度下对桑葚色素稳定性影响不明显。桑葚色素在酸性条件下比较稳定,通过酸味剂的添加和使用,可以对桑葚色素起到护色和增色的效果[14],食品加工过程中酸味剂的正常使用不会对桑葚色素稳定性产生较大影响。
3 结论
大孔吸附树脂法吸附桑葚色素,效果良好。XDA-8大孔吸附树脂对桑葚色素吸附率、解吸率和吸附量较高,对桑葚色素吸附量为选取9种大孔吸附树脂中最高,吸附量为1.89 mg/g。
XDA-8大孔吸附树脂对桑葚色素,解吸乙醇浓度对吸附量影响最大,解吸时间、解吸次数、吸附时间对吸附量影响逐渐递减。XDA-8大孔吸附树脂吸附桑葚色素最优工艺为:准确称取30.0 g XDA-8大孔吸附树脂置于500 mL具塞锥形瓶中,加入200 mL色素溶液,避光和密封处理,30℃下70 r/min分别振荡吸附4 h,过滤。将吸附色素的树脂置于500 mL具塞锥形瓶中,加入200 mL的80%乙醇,避光和密封处理,30℃下70 r/min振荡80 min,解吸3次。
桑椹色素稳定性研究表明,pH值、光照和温度等条件对桑葚色素稳定性影响较大,碱性环境、光照和高温都会破坏桑葚色素结构。桑葚色素在pH值为2.0左右的酸性环境较为稳定,桑葚色素溶液pH值升高会导致桑葚色素中花色苷结构改变。桑葚色素在低于60℃温度环境下结构较为稳定,温度继续升高桑葚色素结构也会被破坏。常用的蔗糖、木糖醇、阿斯巴甜等甜味剂和常用的醋酸、柠檬酸、酒石酸等酸味剂在一定的浓度下对桑葚色素稳定性没有明显影响。
