基于对半胱胺保护的金纳米粒子催化活性的抑制检测氰根离子
2020-07-14赵丹李娜许艳杰黄晶晶陈传霞
赵丹 李娜 许艳杰 黄晶晶 陈传霞

摘要利用氰根离子(CN对带正电荷的半胱胺保护的金纳米粒子(cystAuNPs)过氧化物模拟酶催化活性的抑制,建立了一种简单、灵敏测定CN的比色传感方法。CystAuNPs可催化过氧化氢(H2O2)氧化四甲基联苯胺(TMB),生成蓝色的oxTMB,最大吸收波长为652 nm。由于CN对cystAuNPs的蚀刻作用,cystAuNPs的催化活性减弱,导致生成的oxTMB量变少,溶液颜色变浅,652 nm处的吸光度下降,而颜色变浅和吸光度下降的程度与CN的浓度直接相关。基于催化体系的放大效应,此比色方法的灵敏度高,在最佳条件下,检测CN的线性范围为2~10 μmol/L和10~140 μmol/L,检出限为0.33mol/L(S/N=3)。本方法不需要对金纳米粒子表面进行修饰,具有操作简单、成本低、结果可视化等优点,具有潜在的实际应用价值。
关键词氰根离子; 比色方法; 半胱胺保护的金纳米粒子; 过氧化物模拟酶活性
1引 言
氰根离子(CN是一种剧毒的阴离子,进入人体血液循环之后,可与体内细胞色素氧化酶的Fe3+结合,降低细胞利用氧的能力,损害中枢神经系统[1]。作为一种重要的化学原料,CN被广泛应用于冶金、黄金开采、电镀、纤维合成以及农药医药、树脂生产等领域,对生态环境具有潜在的危害性[2]。CN可通过多种途径被人体吸收,包括肺部的呼吸、皮肤的接触以及被氰化物所污染的食物及饮用水的摄入等,极微量的CN便可致人死亡。世界卫生组织和中国的《生活饮用水卫生标准》规定饮用水中的CN的限量值为1.9 μmol/L[3,4]。因此,发展简便快速、灵敏的检测CN的方法,对于环境监测、食品安全和人类健康具有重要意义。
目前,研究人员发展了多种用于检测CN的方法,主要有比色法[5~7]、荧光法[8~11]、离子色谱法[12]、流动注射法[13]和电化学方法[14]等。这些方法大多较繁琐耗时、操作复杂以及需要专业的操作人员。近年来,基于纳米粒子的比色法因其成本低、简单、可视化以及易进行表面修饰等优点而备受关注。利用CN刻蚀贵金属纳米粒子(如金纳米粒子(AuNPs)和银纳米粒子(AgNPs))的能力,已有简便的比色法被报道用于检测CN [15~17]。然而,这种方法灵敏度较低,检测范围较窄,而且需要对纳米粒子表面进行功能化修饰。针对此问题,研究者分别基于CN对碳量子点AuNPs[18]和石墨烯量子点AgNPs[19]传感体系荧光的恢复,发展了高灵敏度检测CN的荧光方法。但是,此类传感体系需要复杂荧光纳米材料的合成与纯化,繁琐费时,且荧光仪器成本较高,不利于快速推广。近年来,基于纳米材料过氧化物模拟酶性质的催化反应成为放大比色檢测信号的主要策略,可实现痕量分析物的高灵敏度检测。研究表明,一些纳米材料,如金属及金属氧化物纳米粒子、碳基纳米材料、金属纳米簇、石墨烯、金属二硫化物纳米片等,具有催化活性,被称为“纳米酶”[20~23]。纳米酶与天然酶在催化活性、表面电荷、形状和尺寸方面具有相似之处,且具有价格低廉、性质稳定、可大量制备等优点,在环境、食品和医药领域具有广阔的应用前景。如Huang等[24]基于SO24对纳米二氧化铈氧化酶活性的激活效应,建立了高灵敏的谷胱甘肽的比色检测方法; 吴亮亮等[25]通过对银/铂纳米簇的表面修饰调控其催化活性,实现了对环境水样中Cu2+的快速痕量检测。然而,以纳米酶催化的显色反应检测CN的比色方法鲜有报道。
根据文献报道,带正电的半胱胺保护的金纳米粒子(cystAuNPs)具有过氧化物模拟酶的催化活性,其表面的金原子是促进其催化活性的主要因素[26,27]。另外,CN与Au具有较强的络合能力,可蚀刻AuNPs [28]。
2实验部分
2.1仪器与试剂
UV1000紫外可见分光光度计(上海龙尼柯仪器有限公司); Tecnai G2 F20透射电子显微镜(美国FEI公司); 力辰超纯水机(力辰科技股份有限公司)。
三水合氯金酸(HAuCl4·3H2O)和半胱胺盐酸盐购于北京国药集团; 四甲基联苯胺(TMB,美国SigmaAldrich公司); 其它试剂均为国产分析纯。通过调节乙酸和乙酸钠的混合比例配制不同pH值的乙酸盐缓冲溶液(0.2 mol/L),并稀释至所需浓度。实验用水为超纯水(18.2 MΩ·cm)。
2.2cystAuNPs的合成
根据文献[29]的方法合成表面带有正电荷的cystAuNPs,步骤如下: 向40 mL HAuCl4溶液(1.42 mmol/L)中加入400 μL半胱胺盐酸盐溶液(213 mmol/L),室温下搅拌20 min后,逐滴快速加入10 μL新配制的NaBH4(10 mmol/L)。剧烈搅拌15 min后,得到酒红色的cystAuNPs溶液。实验全程需避光, 制备的cystAuNPs于4℃保存, 备用,在3个月内不发生团聚,保持相对稳定。
2.3CN
3结果与讨论
3.1检测机理
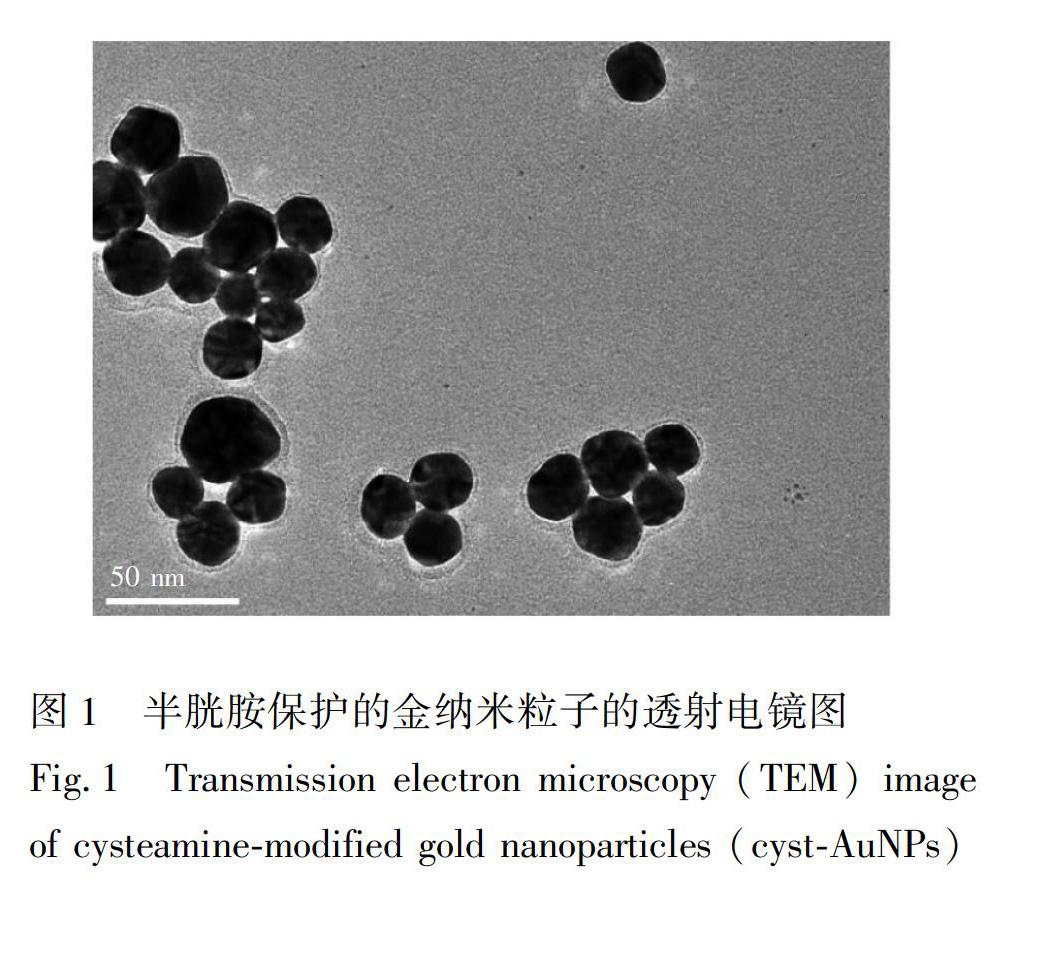
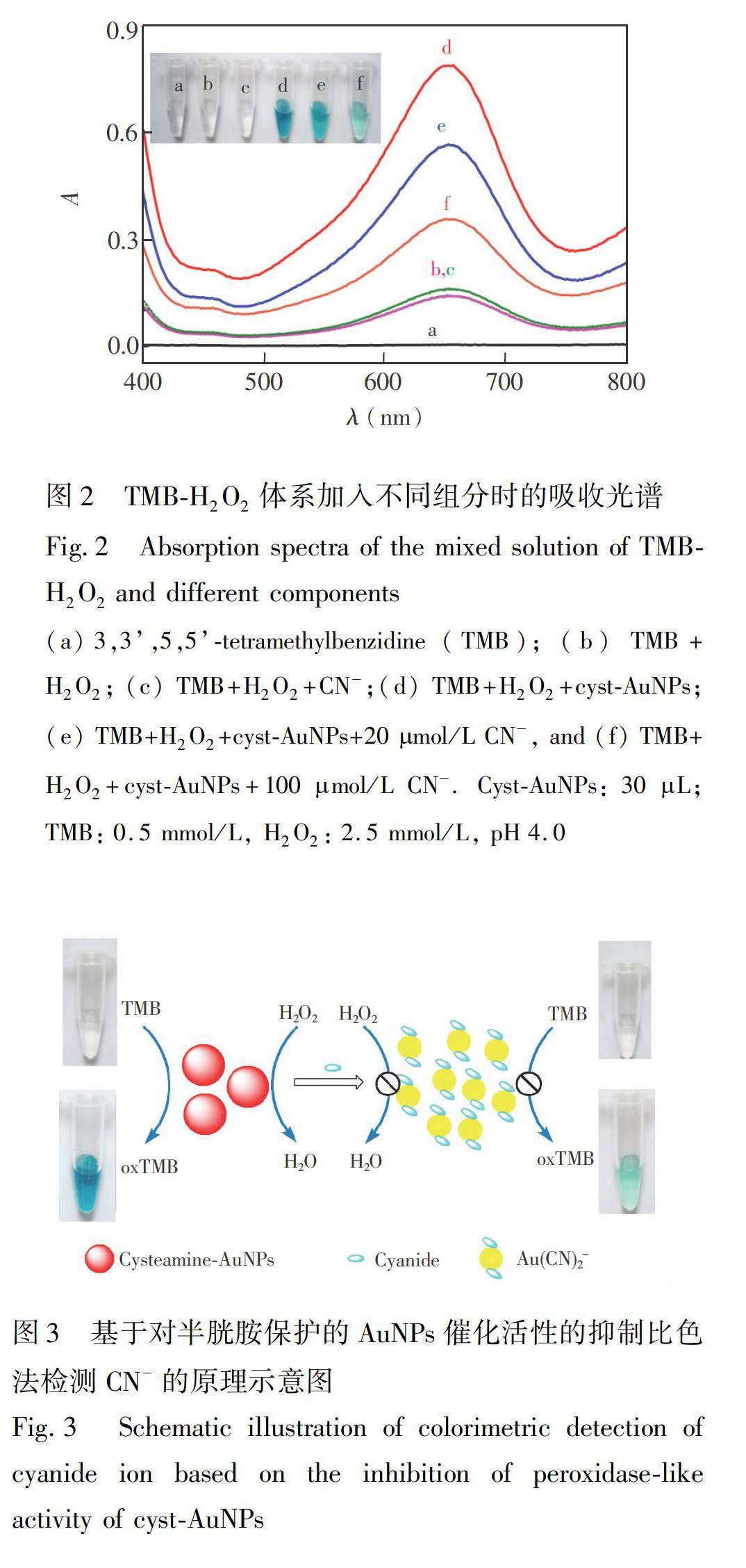
由TEM图(图1)可见,合成的cystAuNPs粒径约为(23±4)nm。不同体系的吸收光谱见图2。单独的TMB无明显的吸收峰(图2曲线a),H2O2与TMB反应后,
体系在652 nm处出现氧化态TMB(oxTMB)的特征吸收峰,但峰强度很弱(图2曲线b),这是由于H2O2与TMB反应很缓慢,此时体系呈无色澄清的溶液(图2插图b)。加入cystAuNPs后,体系在652 nm处的吸收明显增强,同时溶液变为深蓝色(图2曲线d和插图d),说明cystAuNPs具有过氧化物模拟酶的活性,能显著催化H2O2氧化TMB的反应。但是,当体系中存在20
3.2.2pH值的优化pH值影响cystAuNPs的带电状态、 稳定性及催化性能等,对pH值对体系的影响进行了考察。结果表明,只有在酸性条件下,cystAuNPs表面才具有足够的正电荷,保证其稳定性。根据文献[31]报道,H2O2在水中能电离产生过氧根孤对电子,而cystAuNPs中的Au核外电子轨道有空轨道,易与过氧根的孤对电子配位; 在弱酸条件下,过氧根吸附在AuNPs表面,使其OO键断裂,从而持续产生羟基自由基(·OH),在cystAuNPs周围这些活性自由基的局部浓度增高,具有极强的氧化能力[32],显著加快了TMB转化成oxTMB的速率,从而使AuNPs表现出过氧化物模拟酶的特性。如图5A所示,随着pH值增加,ΔA652先增加后减小, pH=4.0时, 加入CNSymbolm@@引起的吸光度差值ΔA652达到最大值,检测的灵敏度最高。因此,本研究选取pH 4.0作为最佳pH值。
3.2.3反应温度和时间的优化与辣根过氧化物酶类似,cystAuNPs的催化活性与体系温度密切相关。分别在25℃、 30℃、 35℃、 40℃、 45℃和50℃的水浴中反应后,测定体系在652 nm处的吸光度。结果表明,体系在40℃时具有最大的催化活性; 继续升高温度,H2O2分解加速,cystAuNPs的催化活性下降。此外,较高温度不利于cystAuNPs与CN之间的相互作用。如图5B所示,随着温度升高,ΔA652先增加后减小,在30℃时达到最大值。因此,选择30℃作为测定CN的最适反应温度。
3.4特异性分析
为了评估cystAuNPsTMBH2O2比色体系对CN的选择性,考察了环境中一些常见的阴、 阳离子
References
1Wang F, Wang L, Chen X Q, Yoon J. Chem. Soc. Rev., 2014, 43(13): 4312-4324
2Hernández Y, Coello Y, Fratila R M, de la Fuente J M, Lionberger T A. Talanta, 2017, 167: 51-58
3Wang S, Hai X, Yang Q, Yan S, Li Y. RSC Adv., 2015, 5(59): 47990-47996
4GB57492006, Standards for Drinking Water Quality. National Standards of the Peoples Republic of China
生活飲用水卫生标准. GB5749-2006. 中华人民共和国国家标准
5Mohammadi A, Sahragard R, Rassa M. J. Photoch. Photobio. A, 2017, 344: 114-120
6Liu C Y, Tseng W L. Chem. Commun., 2011, 47(9): 2550-2552
7Li Y R, Wang Q R, Zhou X M, Wen C Y, Yu J F, Han X G, Li X Y, Yan Z F, Zeng J B. Sens. Actuators B, 2016, 228: 366-372
8Promchat A, Rashatasakhon P, Sukwattanasinitt M. J. Hazard. Mater., 2017, 5(329): 255-261
9Cheng C, Chen H Y, Wu C S, Meena J S, Simon T, Ko F H. Sens. Actuators B, 2016, 227: 283-290
10Liu Y L, Ai K L, Cheng X L, Huo L H, Lu L H. Adv. Funct. Mater., 2010, 20(6): 951-956
11Wei S C, Hsu P H, Lee Y F, Lin Y W, Huang C C.ACS Appl. Mater. Interfaces, 2012, 4(5): 2652-2658
12Christison T T, Rohrer J S. J. Chromatogr. A, 2007, 1155(1): 31-39
13Dai X, Jeffrey M I, Breuer P L. Hydrometallurgy, 2005, 76(1): 87-96
14Meher A K, Labhsetwa N, Bansiwal A. Food Chem., 2017, 240: 131-138
15Yu Y H, Shu T T, Fu C, Yu B J, Zhang D D, Luo H X, Chen J J, Dong C Z. J. Lumi., 2017, 186: 212-218
16Hajizadeh S, Farhadi K, Forough M, Sabzi R E. Anal. Methods, 2011, 3(11): 2599-2603
17Lou X D, Zhang Y, Qin J G, Li Z.Chem. Eur J., 2011, 17(35): 9691-9696
18Zhang J, Dong L, Yu S H. Sci. Bull., 2015, 60(8): 785-791
19Chen C X, Zhao D, Hu T, Sun J, Yang X R. Sens. Actuators B, 2017, 241: 779-788
20Zhang S T, Zhang D X, Zhang X H, Shang D H, Xue Z H, Shan D L, Lu X Q. Anal. Chem., 2017, 89(6): 3538-3544
21Wu J X, Wang X Y, Wang Q, Lou Z P, Li S R, Zhu Y Y, Qin L, Wei H. Chem. Soc. Rev., 2019, 48(4): 1004-1076
22LU LiXia, WANG Yang, LIN XiaoXiao, LI XinYao, XIN MengNa. Chinese J. Anal. Chem., 2018, 46(1): 94-99
路麗霞, 王 洋, 蔺晓晓, 李欣瑶, 辛梦娜. 分析化学, 2018, 46(1): 94-99
23Gao Z Q, Liu G G, Ye H H, Rauschendorfer R, Tang D P, Xia X H. Anal. Chem., 2017, 89(6): 3622-3629
24Huang L J, Zhang W T, Chen K, Zhu W X, Liu X N, Wang R, Zhang X, Hu N, Suo Y R, Wang J L. Chem. Eng. J., 2017, 330: 746-752
25WU LiangLiang, QIAN ZhiJuan, XIE ZhengJun, ZHANG YingYing, PENG ChiFang. Chinese J. Anal. Chem., 2017, 45(4): 471-476
吴亮亮, 钱志娟, 谢正军, 张莹莹, 彭池方. 分析化学, 2017, 45(4): 471-476
26Jv Y, Li B X, Cao R. Chem. Commun., 2010, 46(42): 8017-8019
27Wang S, Chen W, Liu A L, Hong L, Deng H H, Lin X X. Chemphyschem, 2012, 13(5): 1199-1204
28Kim M H, Kim S, Jang H H, Yi S, Seo S H, Han M S. Tetrahedron Lett., 2010, 51(36): 4712-4716
29Zhao D, Chen C X, Lu L X, Yang F, Yang X R. Sens. Actuators B, 2015, 215: 437-444
30Shang L, Jin L, Dong S J. Chem. Commun., 2009, 21(21): 3077-3079
31Zhu R, Zhou Y, Wang X L, Liang L P, Long Y J, Wang Q L, Zhang H J, Huang X X, Zheng H Z. Talanta, 2013, 117: 127-132
32Long Y J, Li Y F, Liu Y, Zheng J J, Tang J, Huang C Z. Chem. Commun., 2011, 47(43): 11939-11941
33Shang L, Dong S J. Anal. Chem., 2009, 81(4): 1465-1470
