原发性肝癌切除术中联合残肝断面射频消融对术后局部复发的预防
2020-07-08朱建平余国华薛晨辉牟东成孙伟光李永猛华玲莉
朱建平,余国华,薛晨辉,牟东成,孙伟光,李永猛,华玲莉
朱建平,牟东成,孙伟光,李永猛,华玲莉, 北京市第一中西医结合医院肿瘤中心肝胆外科 北京市 100018
余国华, 贵州省玉屏侗族自治县人民医院普外科 贵州省玉屏县 554000
薛晨辉, 河北省保定市唐县康定医院外科 河北省保定市 072350
0 引言
我国是世界上原发性肝癌(本文也简称“肝癌”)的高发国家,占世界肝癌发病人数的一半以上,而且大部分发现时已属中晚期,仅小部分早中期患者能行手术切除,但术后复发率依然较高[1,2].肝癌术后复发是制约肝癌手术疗效的重要因素,而且以术后残肝断面复发最常见,如何处理肝脏断面以预防或减少肝癌术后局部复发是提高肝癌手术长期生存疗效的关键因素之一,也是目前研究的热点[3,4].我们回顾性分析2016-10/2019-09期间17例原发性肝癌切除术中残肝断面联合使用射频消融(radiofrequency ablation,RFA)患者的临床资料进行分析,结合文献报告如下.
1 材料和方法
1.1 一般资料 本组男12例,女5例,年龄38-75岁,中位年龄51.5岁±7.8岁,合并乙肝后肝硬化14例,酒精性肝硬化1例,另有2例无明显肝病史; 肝功能Clild-Pugh分级:A级15例,B级2例; 术前均未接受介入、化疗和放疗等,术前影像学没有发现脉管癌栓、也无肝内、肺部、淋巴结和骨等远处转移,全部为单个瘤体; 无心肺脑肾严重伴随疾病,无手术禁忌症,术前向患者及家属充分沟通说明,均签署手术知情同意书.
1.2 术中肝断面RFA方法 患者均给予常规术前准备,包括保肝降酶、纠正低蛋白和腹水等治疗,术后均给予保肝、预防感染和营养支持.采用规划的肝切除方法[5,6],术中均未行肝门阻断,肉眼肝切缘距肿瘤1.0 cm的整块肝脏切除; 手术切除肝脏肿瘤后,肝脏整个断面再联合应用RFA处理,术前影像与术中情况见图1-3所示; 射频设备型号为WB991029 (奥林巴斯Olympus Celon,德国),设定功率为20 W,消融时间9 min,有重点地在肝断面地毯式全覆盖RFA,消融深度1.0-2.0 cm,肝断面形成均匀的凝固性坏死带.
1.3 随访观察指标 所有患者术后每3 mo门诊或住院严密随访1次; 定期复查肝功能、肿瘤标记物(AFP+CEA+Ca199)[7]、胸片和腹部彩超,必要时行肝脏增强计算机断层摄影(computed to mography,CT)/磁共振成像(magnetic resonance imaging,MRI)和正电子发射计算机断层显像(positron emission to mography,PET)等检查[8],如图4所示术后影像情况.
随访关注重点:彩超有阳性发现或虽彩超无阳性发现但肿瘤标记物指标异常升高者,行肝脏增强CT或MRI检查; 如果还没能发现复发癌灶的病例则行数字减影血管造影(digital subtraction angiography,DSA)或PETCT检查,以确定有无复发癌灶的存在.
肝脏局部肿瘤复发判定标准:术中未发现残余癌灶及脉管癌栓、肝周及腹腔无转移; 术后出现的手术部位或肝切缘旁新发的癌灶,以影像检查确认时间作为复发的时间.
2 结果
本组腹腔镜手术8例,开腹手术9例.其中行右半肝切除术4例,左半肝切除术3例,扩大右半肝切除1例,左外叶肝切除3例,右后叶肝切除1例,不规则肝切除5例; 其中有11例同时行胆囊切除术; 手术中位时间157.6 min±30.7 min; 患者术中出血较少,中位出血量120.6 mL±35.5 mL,均没有输血,均顺利完成手术,无手术死亡.
术后病理诊断情况:原发性肝细胞型肝癌(hepatocellular carcinoma,HCC)15例(其中高分化7例、中分化6例、中-低分化2例),中-低分化胆管细胞型肝癌(intrahepatic cholangiocarcinoma,ICC)1例,中-低分化HCC-ICC混合型肝癌合并门静脉脉管癌栓1例; 肿瘤直径1.8-15.5 cm (其中肿瘤直径≥10.0 cm者共3例),中位直径7.8 cm±2.5 cm,BCLC分期:A期2例,B期14例,C期1例.所有患者术后康复顺利,术后无高热,体温、血WBC在3-5 d恢复正常,腹腔引流量少,均在3-6 d拔除腹腔引流管; 肝功能指标在5-8 d恢复正常,无术后大出血、胆瘘、术区感染、肝功能衰竭等手术相关并发症,术后8-15 d均痊愈出院.
所有患者均得到持续随访,无失访,术后每3 mo随访复查,随访时间均超过6 mo,已随访6-36 mo,中位随访时间25.7 mo±4.4 mo,所有患者肝断面局部无复发;术后15 mo腹腔淋巴结转移1例,经放射治疗[9,10]病情稳定; 术后18 mo远离肝断面的新发肝内癌灶1例,经肝动脉化疗栓塞(transcatheter arterial chemoembolization,TACE)[11,12]联合经皮穿刺RFA[13]病情稳定; 所有患者全程坚持采用现代中西医结合治疗,随访期无死亡.
3 讨论
原发性肝癌是临床上常见的恶性肿瘤之一,根治性切除术后1年为复发高峰[3,14],复发率超过40%,术后3年复发率超过60%,5年复发率约80%; 非根治性切除的术后复发更高,吴力群等[15]对528例HCC肝切除术后1年生存分析结果显示,非R0切除(切缘<1.0 cm)术后局部复发率高达78.1%,是导致患者术后早期死亡(1年内死亡率59.3%)的主要因素,局部的复发与瘤体周围微转移灶的存在有关,而绝大部分微转移灶存在于肿瘤周围1.0-2.0 cm范围内,肝癌术后复发是制约肝癌手术疗效的重要因素,如何有效地预防肝癌术后复发是目前研究的重点和难点.完整切除并保证肿瘤边缘有足够的安全距离是肿瘤外科基本原则,目前对肝癌安全肝切缘(R0切除)的标准宽度仍存在争论[1,16-19].一般主张切缘1.0-3.0 cm,无肉眼残癌为R0根治切除条件,切缘>2.0-3.0 cm能有效提高无瘤生存率,但肝硬化及肝脏解剖特点使得切缘往往难以达此标准,但强调1.0 cm切缘是R0切除的最低必需条件.有研究显示广泛切缘有较低的复发率和更好的长远存活预后[20,21],对不同肝硬化背景的患者最佳切缘的宽度很难明确,多数医生支持术中应尽量使肝切缘距肿瘤≥1.0 cm.复旦大学肝癌研究所汤钊猷院士等对距肿瘤边缘2.0 cm及1.0 cm的肝癌切除术进行比较研究[22],结果发现前者局部复发率明显降低,3年及5年生存率明显提高.也有研究表明肝癌术后3-6 mo内出现的肿瘤多为残癌[23-25],源于肿瘤的播散和侵袭,即使是根治性手术,其术后的残癌率亦可高达37.6%,但大部分肝癌患者就诊时病情较晚,肿瘤较大或无完整包膜,或邻近重要血管,而且我国的原发性肝癌大部分合并肝炎后肝硬化,难以耐受较大范围的根治性肝切除术,这类患者切缘很难达到根治切除的标准,切缘残癌阳性率势必较高,而绝大部分微转移灶或变异细胞群存在于肿瘤周围1.0-2.0 cm的移行范围内,这些残留灶由于现有影像学技术的限制而难以在术前或术中发现,是术后肿瘤局部复发的至关重要因素,也是制约原发性肝癌手术远期效果的主要原因.

图1 原发性肝癌术前计算机断层摄影.
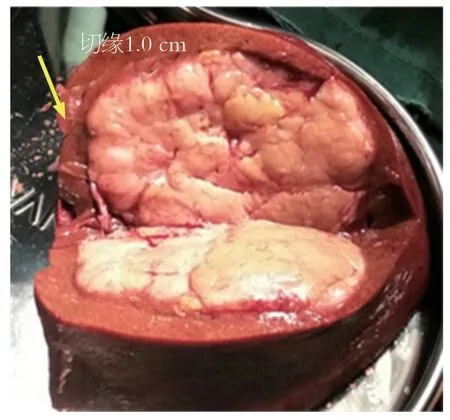
图2 右半肝切除标本.

图3 残肝断面射频消融.

图4 术后6 mo计算机断层摄影示肝断面凝固性坏死带.
因此,对于这类难以完全满足根治切除的原发性肝癌患者或者肿瘤较大、无完整包膜的胆管细胞型肝癌和混合型肝癌,如何处理好肝脏断面,以完全杀灭切缘残留癌细胞或变异细胞群,是降低残癌、减少肿瘤复发以及提高患者远期生存的关键.
RFA治疗原发性肝癌是近年来快速发展的新技术,对不宜进行肝切除的肝癌和复发癌灶均获得了良好的治疗效果[26-28].其原理是通过射频能量的输入,使局部组织达到高温灭活及固化,热辐射范围可累及治疗针周边1.0-2.0 cm,而且微转移灶癌细胞对热敏感性高,容易造成细胞凝固性坏死.术中在直视下完成对残肝断面的RFA,避免了对肝内血管及胆管各分支的损伤,在手术切除1.0 cm的基础上,又增加了1.0-2.0 cm的消融带,满足了肝切缘>2.0-3.0 cm的高标准要求,尤其对ICC或HCC-ICC能增加足够宽的切缘,既提高了手术的安全性,又有效预防了术后残肝断面的局部复发[13,29].
RFA在肝胆外科术中的应用更具有止血速度快,止血彻底,损伤小,术后并发症低和弥补手术不足的优势[30].在肝脏肿瘤手术中用于止血的同时,又能有效杀灭肝断面残留肿瘤细胞,还额外增加了有效切缘深度1.0-2.0 cm,对肝硬化患者明显起到弥补肝切缘距离不足的顾虑,能显著减少术后的肿瘤局部复发.RFA还能诱发宿主抗肿瘤免疫效应,进一步提高了患者临床疗效和生存时间[31].
结合我们的初步体会:在原发性肝癌切除术中联合残肝断面RFA能增加手术切缘的有效深度,对预防肝切除残肝断面局部肿瘤复发有很好的潜在价值,并延长了患者的无瘤生存时间.
在原发性HCC肝切除手术中,如果手术切缘不能满足安全切缘,我们建议术中联合RFA处理这类患者肝脏断面; 对于胆管细胞型肝癌或混合型肝癌,以及合并脉管癌栓患者,除术中积极采用RFA处理残肝断面外,术中术后还应采取更积极的预防措施,术中应酌情再加做标准的淋巴结清扫、术后早期酌情行预防性TACE等.
由于增加了切缘深度,杀灭了更多的残癌细胞或移行的变异细胞群,致使肿瘤局部复发率降低.但因影响患者术后复发及生存情况的因素较多,我们的病例数尚少、对生存时间观察不足够长,尚需增加更多病例数和设计随机对照研究,并结合多因素统计分析及进一步临床对照观察和多中心研究论证.
4 结论
在肝脏储备功能良好、无手术禁忌症的条件下,原发性肝癌根治性切除手术中,对于不能达根治切除标准、切缘残癌可疑阳性的HCC患者,手术中联合应用RFA处理残肝断面,形成良好的凝固性坏死移行带,能更有效的杀灭残肝断面残留的可疑细胞,降低术后肿瘤局部复发; 并且对切缘的正常细小胆管、血管等组织也均被凝固坏死、闭塞,起到更好的止血和防治胆瘘的作用,还能进一步减少肿瘤经血管及胆管扩散转移的机率; 对于胆管细胞型肝癌或混合型肝癌,以及合并脉管癌栓患者,除术中采用RFA处理残肝断面外,术中术后还应采取更积极的预防措施.
因此,原发性肝癌肝切除术中联合应用RFA处理残肝断面对术后肿瘤局部复发有很好的预防作用,在提高患者生存率以及延长生存时间等方面有积极的临床意义,值得临床推广应用.
文章亮点
实验背景
肝癌是我国常见的恶性肿瘤,发病率与病死率均高,严重威胁国人的生命健康.至今传统的手术切除仍是可能治愈肝癌的主要方法,随着现代技术的发展,近年来小肝癌的RFA治疗效果良好、设备和技术发展迅速,已能达到手术切除相同的效果,而且手术操作更趋微创化,但术后的高复发率是制约其远期疗效不佳的主要因素,而且手术区域即残肝断面的复发最为常见.
实验动机
目前国内外研究大多聚焦于如何降低术后局部复发的临床实验研究,本文通过传统手术与现代肿瘤消融技术-射频消融(radiofrequency ablation,RFA)的联合应用,探讨此新方法对患者术后肿瘤局部复发的预防作用.
实验目标
本实验提出的肝癌切除术中联合应用RFA处理残肝断面的方法,目标是为达到降低术后肿瘤局部复发率、提高患者无瘤生存时间.
实验方法
本研究通过回顾应用联合手术治疗的17例原发性肝癌患者的详细临床资料,分析其术后肿瘤局部复发情况.
实验结果
通过17例患者的完整随访资料分析得到初步的良好结果:所有患者无严重术后并发症,中位随访时间25.7 mo±4.4 mo,所有患者残肝断面局部无复发; 仅有术后15 mo腹腔淋巴结转移1例,术后18 mo远离肝断面的新发肝内癌灶1例,这2例患者均采用现代中西医结合模式进一步治疗,现带瘤生存良好,其他患者状况良好,全组无死亡.
实验结论
原发性肝癌肝切除术中联合应用RFA处理残肝断面可显著降低肿瘤局部复发,对术后肿瘤局部复发有很好的预防作用,在提高患者生存率以及延长生存时间等方面有积极的临床意义,值得临床推广应用.
展望前景
我国原发性肝癌患者,大多合并肝炎后肝硬化,在根治性切除手术中,较多患者受到肝脏储备功能的限制,将可能达不到根治切除标准或存在切缘可疑残癌,手术中联合应用RFA处理残肝断面,能有效弥补此类根治不足或切除不够,将会降低术后肿瘤局部复发; 尤其对于近年发病率所有增加的胆管细胞型肝癌或混合型肝癌,以及合并脉管癌栓患者,除术中积极采用RFA处理残肝断面外,术中术后还应采取更积极的预防措施以防治术后的复发转移,此联合手术应用前景广,值得推广应用.
