脊髓小胶质细胞激活参与吗啡诱导瘙痒的机制*
2020-07-04李楠琦黄思婷
汤 洋 李楠琦 彭 哲 黄思婷 万 丽
(1 广州医科大学附属第二医院疼痛科,广州510260;2 广州医科大学麻醉学系,广州510260;3 中山大学附属第一医院麻醉科,广州 510080)
众所周知,疼痛和瘙痒是机体两种截然不同的主观感觉,但两者又彼此密切联系。疼痛和瘙痒所诱发的均为躯体不愉快的主观感觉体验,疼痛可以发生在机体除大脑以外的深部和浅表几乎所有器官组织,而瘙痒仅发生在皮肤和黏膜等浅表组织处。在急性条件下,疼痛和瘙痒的感觉都可以作为警告信号,保护机体免受可能的伤害性刺激造成的损伤[1]。
临床上,瘙痒是吗啡椎管内注射镇痛的常见并发症。其发生率在非妊娠病人占30%~100%,在妊娠病人可高达60%~100%,极大影响了吗啡术后镇痛的舒适度,甚至病人被迫终止镇痛治疗,而引起术后疼痛发生率增加。因此,吗啡术后镇痛所致皮肤瘙痒是临床亟待解决的问题[2,3]。我们想通过研究吗啡所致瘙痒的机制来解决临床上吗啡椎管内注射后瘙痒的并发症。瘙痒产生的机制涉及多方面的介质和因素,虽然目前临床用5-HT3受体拮抗剂、混合型阿片受体激动/拮抗剂、丙泊酚、抗组胺药等预防和减少吗啡鞘内注射所致瘙痒,但临床效果并不理想[4]。吗啡所致急性瘙痒并没有有效的临床用药。近年研究表明,脊髓背角小胶质细胞表达有多种神经递质的受体[5],从而参与疼痛中枢敏化的形成。研究证明介导疼痛与瘙痒产生的机制有很多联系,许多参与疼痛的传导通路也都与瘙痒有关[6]。Zhang 等[7]研究已发现小胶质细胞激活参与2, 4-dinitrofluorobenzene (DNFB)慢性瘙痒和神经病理性疼痛,并伴有小胶质细胞激活及激活后多种趋化因子表达[8]。因此,我们猜测小胶质细胞可能也参与吗啡所致的急性瘙痒。本研究通过鞘内注射吗啡急性瘙痒模型,观察小胶质细胞激活表达标志物OX-42、CD11b 蛋白和p-p38 变化,进一步探讨吗啡诱导急性瘙痒的机制。小胶质细胞涉及吗啡所致急性瘙痒的机制是本研究的一个创新点,为吗啡注射后瘙痒寻找潜在的治疗靶点。
方 法
1.实验动物及分组
雄性C57BL/6J 小鼠,20~30 g,广东省实验动物中心[许可证号SCXK(粤)2013-0002],7~12 周,实验随机分为4 组:正常对照组 (normal control)、吗啡组 (morphine),吗啡加米诺环素组 (morphine plus minocycline)和吗啡加p38 抑制剂组 (morphine plus p38 inhibitor);每组各12 只,其中6只用于行为学测试,6 只用于形态学及分子生物学检测。分笼饲养,自由饮水和取食。实验前适应性饲养1 周,动物行为学观察实验皆于8:00~14:00进行。本研究所有实验操作均符合国际动物伦理规范及精神。
2.试剂与材料
吗啡(东北制药集团沈阳第一制药有限公司,10 mg/ml,中国);米诺环素(M9511-25MG,SIGMA 公司, 美国),为一种小胶质细胞抑制剂;p38 抑制剂(P8139-5MG, SIGMA 公司,美国),可抑制p38 MAPK 通路;Alexa Fluor 488 抗小鼠lgG (H + L) (1890503A 0.5 ml, Thermo Fisher);Alexa Flour594 抗 兔lgG (H + L) (ab150076 500 mg, Abcam);兔抗CD11b 抗体(ab128797 100 µg, Abcam);小鼠抗p-p38 MAPK 抗体(T180/Y182 100 µl, CST,美国);RIPA(71500150 500 ml,北京鼎国);电泳仪、电泳槽(BioRad,美国)。
3.鞘内注射及给药
根据既往实验方法,用微量注射器在小鼠L4-5腰椎间隙行鞘内注射,单次注射小鼠出现甩尾表现则为成功穿刺标志。对照组鞘内注射10 µl生理盐水;吗啡组注射0.6 nmol 吗啡;吗啡加米诺环素组鞘内先注射0.6 nmol 吗啡并依次分别加0.5 nmol、1 nmol、2 nmol 米诺环素鞘内注射。吗啡加p38 抑制剂组鞘内先注射0.6 nmol 吗啡并依次分别加1 nmol、2 nmol、5 nmol p38 抑制剂鞘内注射。注射容量均为10 µl。
4.吗啡所致瘙痒行为学观察
每次鞘内注射后即刻将小鼠置于观察盒内(15 cm×20 cm×15 cm)并连续摄像记录30 min 小鼠瘙痒行为,每组各6 只。小鼠后爪搔抓颈部、背部或脸后,出现舔爪或将爪放至地面记录为1 次瘙痒次数。
5.小胶质细胞标志物CD11b 及p-p38 蛋白水平检测
在吗啡急性瘙痒模型造模后,另取四组中各3只小鼠,即刻快速断头处死,取出L4-S1节段脊髓。提取总蛋白后,应用BCA 方法测量总蛋白浓度并配平。将分装的蛋白样本(25 µg)进行SDS-PAGE (10%)电泳,将蛋白转移至PVDF 膜上,5%脱脂牛奶室温封闭约1 h,按1:500 比例稀释一抗孵育过夜;1:2000 比例稀释与一抗对应的二抗,室温孵育1 h。最后,用化学成像系统照相,对小胶质细胞标记物CD11b、p-p38 检测。目的蛋白检测后,同一张膜测GAPDH。
6.腰段脊髓小胶质细胞激活标志物OX-42 及p-p38 免疫荧光检测
按照行为学测量结果,各组剩余3 只小鼠在吗啡加米诺环素造模后,即刻用混合麻醉剂(100 mg氯胺酮+ 5 mg 咪达唑仑溶于10 ml 生理盐水中,浓度为5 µg/ml,每只小鼠20 g 注射200 µl 混合液)深度麻醉下开胸,插管至左心室,先以0.9%生理盐水40 ml 心内灌注快速冲去血液,再以4%多聚甲醛40 ml 先快速滴注5 min 后慢速滴注30 min 固定。灌注完毕立即取出小鼠L4-S1节段脊髓于多聚甲醛中后固定(4℃过夜),移入20%蔗糖中脱水沉底,再移入30%蔗糖中脱水沉底。冰冻冠状切片,片厚20 μm,采用免疫荧光法,0.01 mol/L PBS 摇床上漂洗10 min 后,加入含2.5%驴血清的封闭液室温下封闭1 h,随后加入兔抗OX-42 (1:400),鼠抗p-p38 (1:500) 4℃孵育过夜。次日PBS 漂洗3 次后加入驴抗鼠绿色,驴抗兔红色荧光标记的二抗,室温避光孵育2 h。用PBS 漂洗后贴于载玻片上,封片,在荧光显微镜下拍照。检测小胶质细胞标志物OX-42 和p-p38 的表达变化。
7.统计学分析
采用GraphPad Prism 软件(版本6.0c)进行统计学分析,实验数据均以均数±标准差(±s)表示,组间比较采用t 检验,组内比较采用方差分析,以P < 0.05 为差异有统计学意义。
结 果
1.吗啡所致瘙痒小鼠脊髓小胶质细胞水平增加
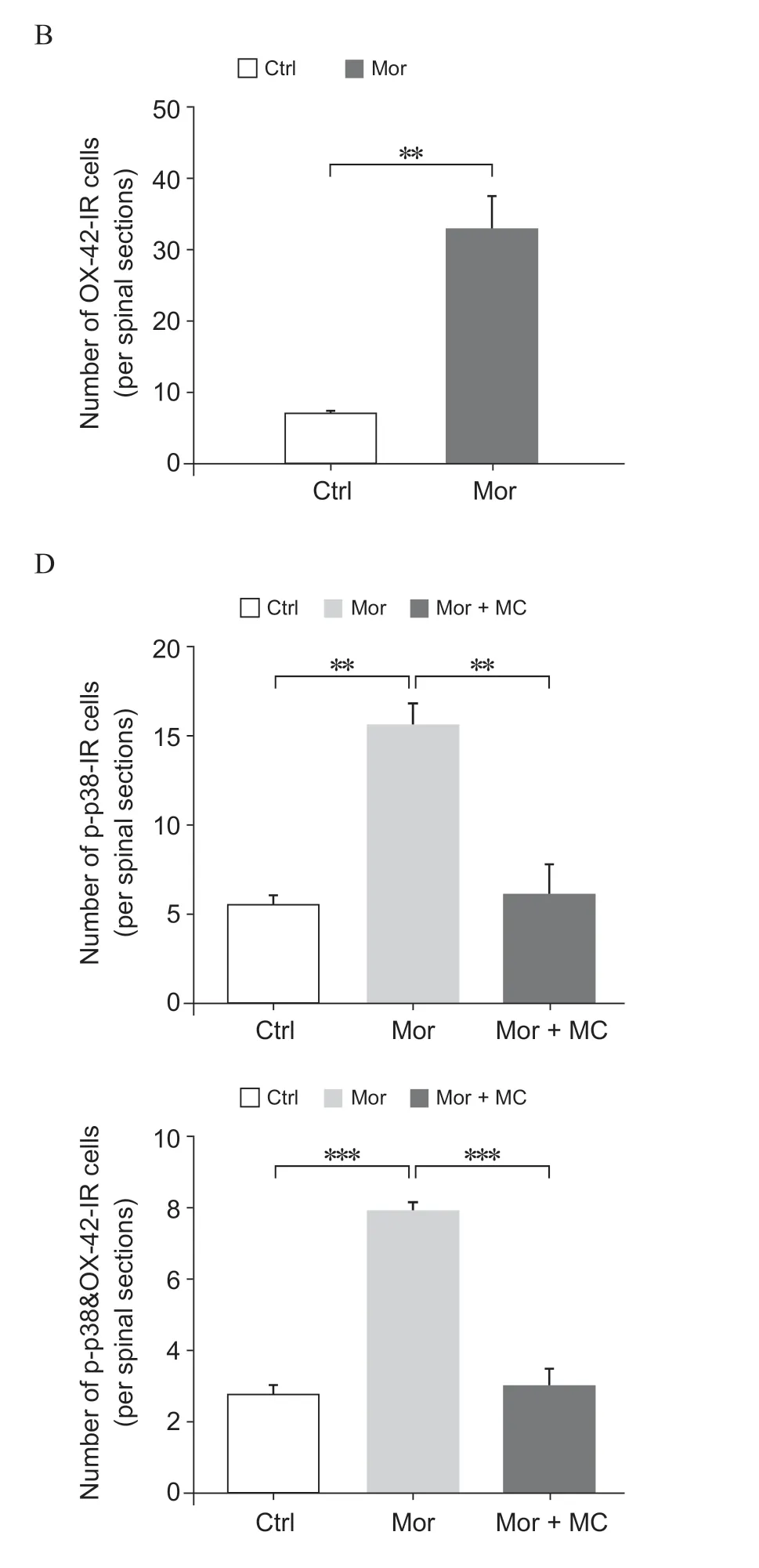
与对照组相比,鞘内注射0.6 nmol 吗啡后小鼠瘙痒次数明显增多。在注射吗啡后10 min~20 min内,小鼠瘙痒次数增多最为显著(P < 0.001,见图1)。之后瘙痒次数逐渐减少;免疫荧光结果显示,与对照组相比,吗啡组小胶质细胞活化数量明显增加,小胶质细胞胞体增大,树突变短;吗啡组脊髓腰段小胶质细胞OX-42 量的表达显著增加。与对照组相比,具有显著性差异(P < 0.05,见图2A, B)。
2.吗啡所致瘙痒小鼠脊髓p-p38 水平增加且与小胶质细胞共表达于脊髓背角
免疫荧光结果显示,与对照组相比,鞘内注射吗啡组小鼠p-p38 表达显著增加且与OX-42 共表达于脊髓背角。同样,吗啡处理组小鼠p-p38 蛋白水平较对照组增高(P < 0.01,见图2C, D)。
3.米诺环素降低吗啡致痒小鼠瘙痒行为及脊髓小胶质细胞CD11b 蛋白和p-p38 水平
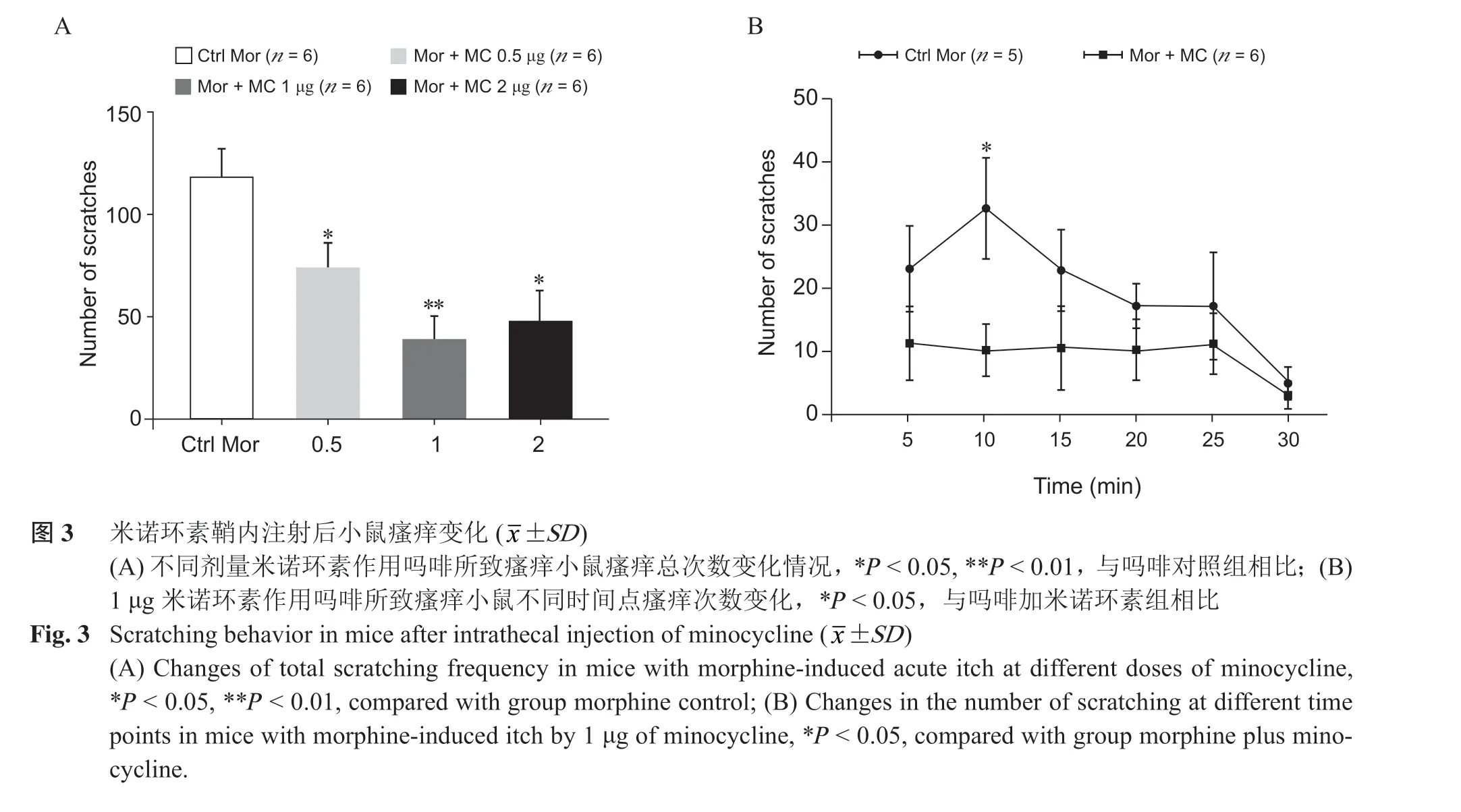
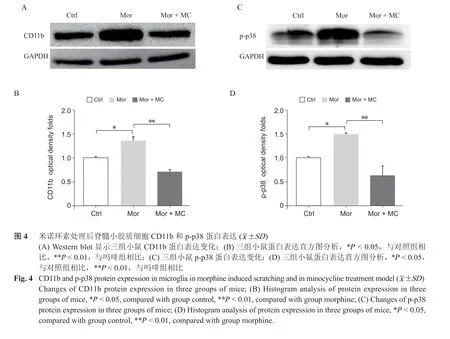
与生理盐水对照组、鞘内注射吗啡组相比,鞘内注射米诺环素后,吗啡所致瘙痒小鼠瘙痒次数明显减少,浓度梯度米诺环素处理后,可发现1 μg 米诺环素对吗啡诱导瘙痒的抑制作用最明显(P < 0.05,见图3A)。其中1 μg 米诺环素注射30 min 内不同瘙痒时间点显示,米诺环素注射10 min 时抑制吗啡瘙痒作用最显著(P < 0.05,见图3B)。Western blot 结果显示,与吗啡组相比,米诺环素处理组小鼠小胶质细胞标记物CD11b 蛋白浓度明显减少,差异有统计学意义(P < 0.05,见图4A, B),p-p38蛋白表达也显著低于单独注射吗啡组(P < 0.01,见图4C, D)。
4. p38 抑制剂减少吗啡致痒小鼠瘙痒行为
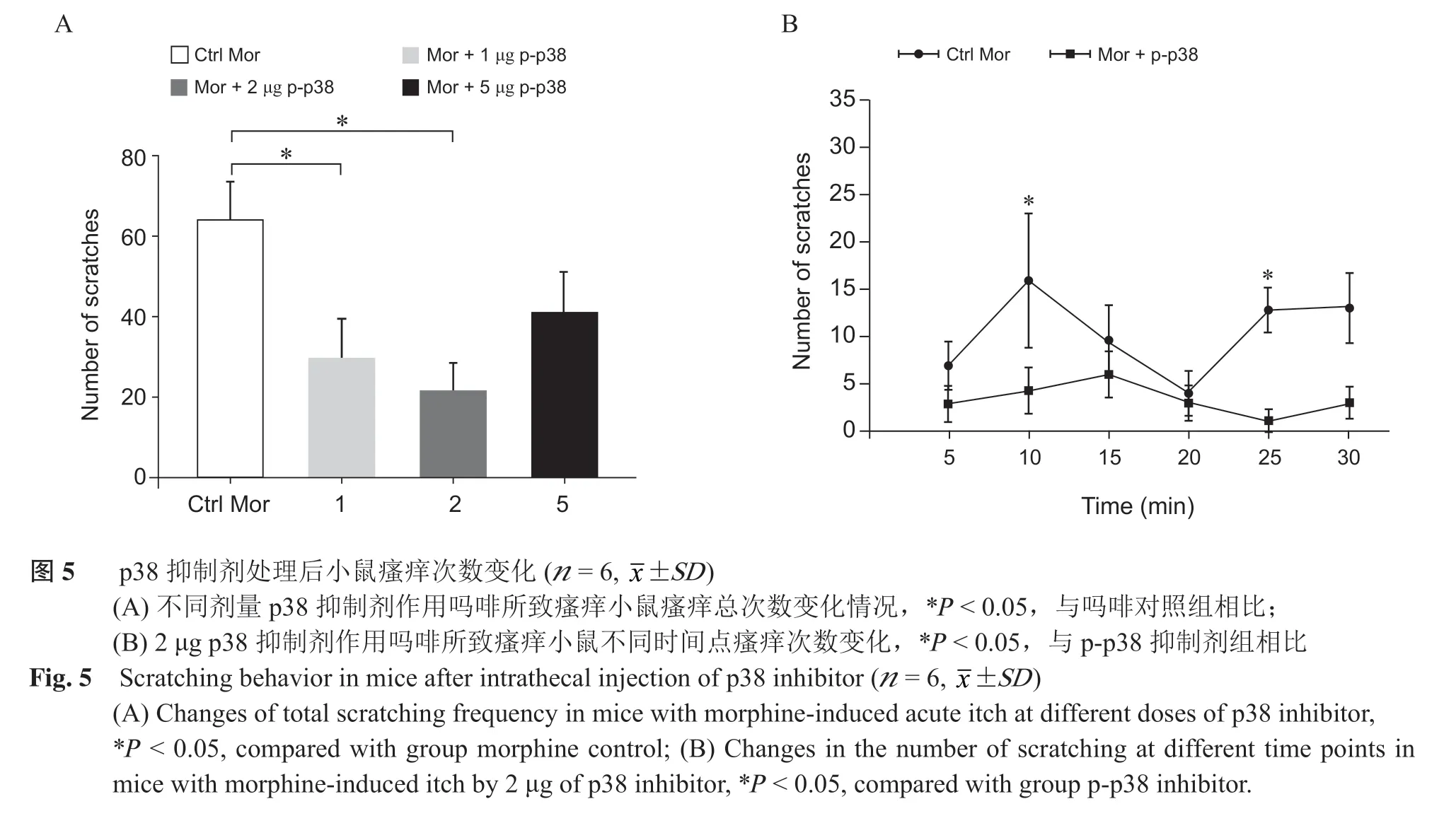
与生理盐水对照组、鞘内注射吗啡组相比,鞘内注射p38 抑制剂后吗啡致痒小鼠瘙痒次数明显减少,不同浓度p38 抑制剂处理后,p38 抑制剂抑制瘙痒效果也不同。其中,2 μg p38 抑制剂抑制作用最显著(P < 0.05,见图5A),2 μg p38 抑制剂抑制吗啡所致瘙痒的30 min 内时间点显示,抑制作用在10 min 和25 min 时最显著(P < 0.05,见图5B)。
讨 论
近年来,大量研究表明脊髓中小胶质细胞不仅参与神经损伤反应及多种神经病理性疼痛过程[9,10],而且在吗啡镇痛中发挥作用[11]。已有研究表明在慢性瘙痒中,小胶质细胞处于活化状态[7]。小胶质细胞对外界环境变化极为敏感,在神经损伤后能迅速活化,并释放一系列细胞因子,从而调节细胞的功能[12],但在急性瘙痒时小胶质细胞是否被调动激活目前尚未报道。因此,在本次研究中,观察吗啡诱导的急性瘙痒中小胶质细胞是否被激活及调控的影响。研究发现,吗啡诱导急性瘙痒15 min 时,小鼠脊髓背角小胶质细胞即被激活,不仅激活状态的小胶质细胞数量增多,而且激活的细胞胞体肥大,树突变短,这与慢性疼痛时脊髓背角胶质细胞激活相似[13]。而使用小胶质细胞的抑制剂米诺环素处理后,小鼠瘙痒次数明显减少,且活化的小胶质细胞数量减少。说明小胶质细胞也参与吗啡诱导急性瘙痒,且小胶质细胞抑制剂米诺环素可拮抗吗啡所致急性瘙痒。
临床上不仅吗啡成瘾,椎管内吗啡所致瘙痒也是亟待解决的问题[14]。虽然椎管内吗啡致痒的具体机制尚不清楚,研究表明其可能与中枢μ 阿片受体、5-HT3 受体、D2 受体及痒觉相关神经递质如胃泌素释放肽(GRP)、P 物质等有关[4]。Liu 等提出吗啡所致瘙痒和镇痛由MOR 不同亚型介导,MOR1 参与吗啡镇痛,而脊髓MOR1D 受体是痒特有的受体[15],临床应用阿片受体拮抗/激动剂纳布啡、5-HT3受体拮抗剂、丙泊酚等治疗吗啡所致瘙痒[16],但遗憾的是,临床效果并不理想。所以,在本次实验中,建立吗啡诱导瘙痒模型来探讨可能与其有关的潜在机制。
相关研究表明,小胶质细胞抑制剂米诺环素可通过抑制脊髓小胶质细胞中的p-38 MAPK 信号通路抑制小胶质细胞表达[17]。王益敏等[18]通过免疫荧光双标技术观察到,在脊髓背角p-38 MAPK 主要表达于小胶质细胞,且小胶质细胞可通过p38 MAPK信号通路参与神经病理性痛的形成。因此,我们猜测小胶质细胞也可能通过p38 MAPK 通路参与吗啡诱导瘙痒的形成。本研究发现,在吗啡诱导瘙痒中,小胶质细胞处于激活状态,且p-p38 信号通路也处于高表达活化状态,这说明小胶质细胞与p38 MAPK分子相关信号通路参与了吗啡诱导急性瘙痒的形成过程。同时,我们发现吗啡注射所致的明显增高p-p38 水平,可被小胶质细胞抑制剂米诺环素处理所抑制,表现为p-p38 表达明显减少。同时p-p38与OX-42 共表达于脊髓背角,p38 抑制剂处理可减少吗啡所致瘙痒,证明p-p38 参与吗啡急性瘙痒的形成过程,且可能作用于小胶质细胞的下游信号通路。然而,p38 MAPK 是否通过炎症因子或趋化因子等其他介质参与小胶质细胞激活,需要进一步的实验研究。
许多研究表明小胶质细胞活化参与神经病理性过程,并包括多种细胞因子,趋化因子和炎症介质的参与[19]。虽然没有直接证据表明小胶质细胞参与人体神经病理性疼痛,但通过以小胶质细胞为靶点来治疗炎症性疼痛有令人兴奋的前景和展望[20]。虽然研究已证明脊髓神经元GRP 参与特定瘙痒回路,以及NMB 等参与神经瘙痒回路[21]。但胶质细胞在瘙痒中的作用仍值得探讨。本研究中发现小胶质细胞参与吗啡诱导的急性瘙痒。除此之外,许多研究已证实小胶质细胞不仅参与神经病理性疼痛,同时也在介导瘙痒传递,如DNFB 慢性瘙痒模型的小鼠和48/80,GNTI 诱发的瘙痒病中小胶质细胞表达都增加[22]。所以本研究选小胶质细胞是否参与吗啡所致急性瘙痒为切入点,并且研究p38 通路的变化,是本研究的一个创新点。
本研究中,吗啡注射后30 min,小鼠瘙痒行为与对照组相比显著增高,与既往报道吗啡鞘内注射所致急性瘙痒模型一致。米诺环素注射后,小鼠瘙痒反应与吗啡组相比明显减少,提示小胶质细胞的激活可作为吗啡所致急性瘙痒的干预靶点。同时,在吗啡注射30 min 内p-p38 水平明显增高,小胶质细胞抑制剂米诺环素及p38 抑制剂注射后30 min内明显抑制p-p38 水平,表明p-p38 可能作为小胶质细胞激活的下游信号通路参与吗啡所致急性瘙痒的形成。过去的研究表明米诺环素通过抑制脊髓小胶质细胞中的p38 MAPK 通路减少吗啡镇痛的耐受性[23],因此推测也可能通过此通路参与吗啡所致急性瘙痒的形成,但其具体机制还需进一步的研究。
综上所述,p38 MAPK 信号通路激活小胶质细胞参与吗啡诱导的瘙痒。小胶质细胞抑制剂米诺环素可通过抑制p38 MAPK 通路抑制吗啡诱导急性瘙痒的产生。提示脊髓小胶质细胞可作为吗啡诱导瘙痒的治疗靶点。其机制可能是通过激活小胶质细胞促进炎性介质的生成等参与瘙痒的形成,对于p-p38上游机制今后还需要给药干预以及分子实验进一步证明该通路在吗啡诱导急性瘙痒的作用,为进一步研究吗啡诱导急性瘙痒提供理论依据。
