柠檬酸改性Hβ分子筛酸性中心的调变与解析
2020-07-01刘金玲秦玉才孙兆林宋丽娟
惠 宇,刘金玲,秦玉才,孙兆林,2,宋丽娟,2
(1.辽宁石油化工大学 辽宁省石油化工催化科学与技术重点实验室,辽宁抚顺113001;2.中国石油大学(华东)化学工程学院,山东青岛266555)
β分子筛的基本单元是由两个六元环通过两个四元环和四个五元环连接而成的双六元环。由于基本结构单元有3种不同的连接方式,且3种不同的连接方式在能量上是相等的,所以形成3种不同的晶体结构。这3种多晶结构是通过层错相关联的,由于层与层之间的层错以及3种晶型的随机堆积而产生的大量缺陷位和随机孔道使β分子筛具有特殊的表面性质和催化活性[1]。
近年来,研究者们采用FTIR和NMR等方法对β分子筛中铝的存在形式及分布进行了大量研究。结果表明,在β分子筛中存在3种状态的铝,其中将具有六配位结构的铝物种归属为非骨架铝,四配位的铝归属为骨架铝,而NMR不可见铝为过渡态 铝[2‐4]。
β分子筛的酸性质与上述3种状态铝的分布密切相关。对于Hβ分子筛而言,骨架硅铝桥羟基是分子筛B酸中心的主要的来源[5]。M.Guisent等[6]认为,β分子筛表面存在两种不同形式的B酸中心,其中包括酸性较强的(SiO)3Si-OH-Al(OSi)3与酸性较弱的(SiO)2(AlO)Si-OH-Al(OSi)3。此外,Hβ分子筛酸中心的种类与性质,在很大程度上也决定于铝的配位状态。六配位的非骨架铝物种和骨架缺陷处的三配位铝均可作为L酸中心。在高温条件下,β分子筛中的骨架铝羟基也会脱水而形成L酸中心;其中某些不稳定的骨架铝则会因高温作用而从骨架上脱落,最终以六配位非骨架铝的形式存在,而某些较稳定的骨架铝则以扭曲四面体的形式存在[7]。上述两种铝的存在形式均具有L酸性,其中扭曲的四面体铝通常在吸附水分子后也会转变成六配位非骨架铝的形式,但对分子筛进行脱水以后,这些铝的配位状态会恢复为四面体形式,并成为B酸中心。
Hβ分子筛在酸处理的过程中会影响分子筛中铝的状态和分布[8],往往非骨架铝和缺陷位上的铝被优先去除,在一定的处理时间内不会对晶体的织构结构造成影响,低浓度酸只能起到清理非骨架铝的作用,只有高浓度酸才能致其骨架脱铝,其中β分子筛中酸性较弱的(SiO)2(AlO)Si-OH-Al(OSi)3被优先脱除,致使分子筛中Si(2Si,2Al)的含量减少,降低了弱B酸酸量。
本研究以商业Hβ分子筛为原料,采用不同浓度柠檬酸进行改性,通过原位红外光谱技术分析柠檬酸改性过程中分子筛活性羟基基团的变化情况;以吡啶为探针分子,分析吡啶分子与分子筛各活性组成单元的作用形式,进而为Hβ分子筛活性位的辨析与定向调控提供理论依据。
1 实验部分
1.1 柠檬酸改性Hβ分子筛的制备
Hβ分子筛原粉(n(Si)/n(Al)=12.5)由南开大学催化剂厂提供,550℃下焙烧4 h除去杂质,浸于一定浓度的柠檬酸溶液中,于60℃回流处理4 h。过滤后用蒸馏水洗涤至pH=7,110℃干燥12 h后550℃焙烧4 h。制备的样品根据柠檬酸的浓度(0.25、0.50、1.00 mol/L)分 别 记 为 0.25CHB,0.50CHB,1.00CHB,未经柠檬酸处理的样品记为HB。
1.2 柠檬酸改性Hβ分子筛的表征
样品的物相分析采用日本理学株式会社D/MAX‐RB型X射线衍射仪(XRD),Cu靶3 Kα射线,入射波长为0.154 nm,管电压30 kV,管电流100 mA,5o~60o扫描,扫描速率 8(o)/min,连续扫描。样品的比表面积和孔体积在美国麦克公司(Micromeritics)生产的ASAP 2020型物理吸附仪上测定,催化剂样品在623 K下抽真空预处理10 h,液氩冷却至77 K,进行低温Ar吸/脱附实验,并利用BET(Brunauer‐Emmett‐Teller)法 计 算 比 表 面 积 ,HK(Horvath‐Kawazoe)法计算微孔的孔容和孔径分布,BJH(Barrett‐Joyner‐Halenda)法计算介孔的孔容和孔径分布。
样品的酸类型、酸强度及总酸量分布采用化学吸附仪(Micromeritics,Auto Chem II)进行氨气程序升温脱附(NH3‐TPD)实验测定;样品中B酸和L酸的酸量和酸强度采用吡啶为探针分子,运用原位傅里叶变换红外光谱技术(in situ‐FTIR)进行表征。其中,在Py‐FTIR中,定义150℃脱附后测得的酸量为总酸量,400℃脱附后测得的酸量为强酸量,两者之差为弱酸量。
1.3 Hβ分子筛活性位与酸性质的关联性
为进一步分析吡啶分子在改性Hβ分子筛不同活性位上的吸附形式,同样采用in situ‐FTIR进行研究。在实验过程中,吡啶的浓度是依次从低浓度到高浓度通入原位池中,150℃条件下,每次在改性β分子筛上吸附0.5 h后再脱气0.5 h。扫描的波数为 4 000~1 200 cm-1,扫描32次,分辨率为 4 cm-1。
2 结果与讨论
2.1 柠檬酸改性β分子筛的织构性质
2.1.1 Hβ分子筛的XRD表征 图1给出了不同浓度柠檬酸处理Hβ分子筛的XRD谱图。由图1可知,经柠檬酸改性后的样品仍保持原粉Hβ分子筛的特征衍射峰,其中位于 2θ=7.80°、22.30°附近的特征衍射峰强度在经过改性后未见明显变化[9]。
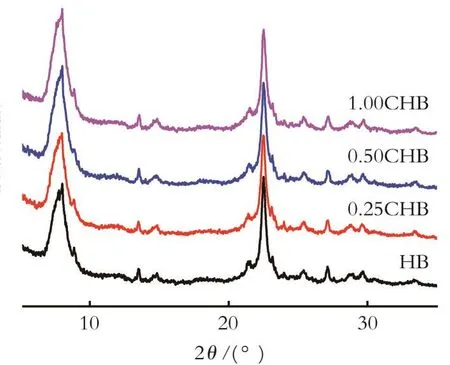
图1 不同浓度柠檬酸处理Hβ分子筛的XRD谱图Fig.1 XRD patterns of modified Hβ zeolites with different concentrations of citric acid
表1给出了不同浓度柠檬酸处理Hβ分子筛的织构性质及骨架不对称振动波数(νTOT)。从表1中样品的相对结晶度结果可以看出,柠檬酸处理的样品均具有较高的结晶度,说明分子筛骨架结构未造成明显破坏,仅对其晶体的精细结构造成一定影响。
2.1.2 Hβ分子筛的Ar吸附‐脱附曲线 图2为不同浓度柠檬酸处理Hβ分子筛的Ar吸附‐脱附曲线。从图2中可以看出,4种分子筛在低压区(p/p0≤0.1)的N2吸附量急剧上升并且在中压区开始出现转折,并在相对压力(p/p0)为0.1~0.4时出现一个平台,这完全符合Ar吸附‐脱附等温线的I型等温线,说明4种分子筛均存在微孔结构。当相对压力(p/p0)在0.4~1.0时,4种分子筛均出现了滞后环现象,这属于Ar吸附‐脱附等温线的IV型等温线,说明4种分子筛中还存在介孔结构。对比上述样品在此两个相对压力区的Ar吸附量来看,经过柠檬酸处理后其微孔及介孔结构并未遭受严重破坏。
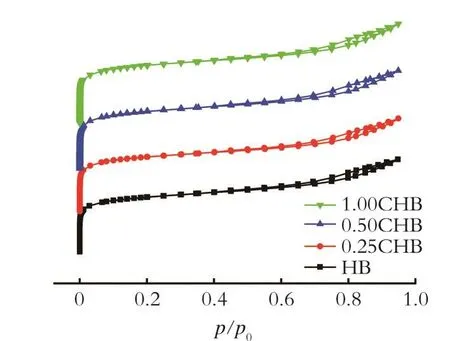
图2 不同浓度柠檬酸处理Hβ分子筛的Ar吸附‐脱附等温线Fig.2 Ar adsorption⁃desorption isotherms of modified Hβ zeolites with different concentrations of citric acid
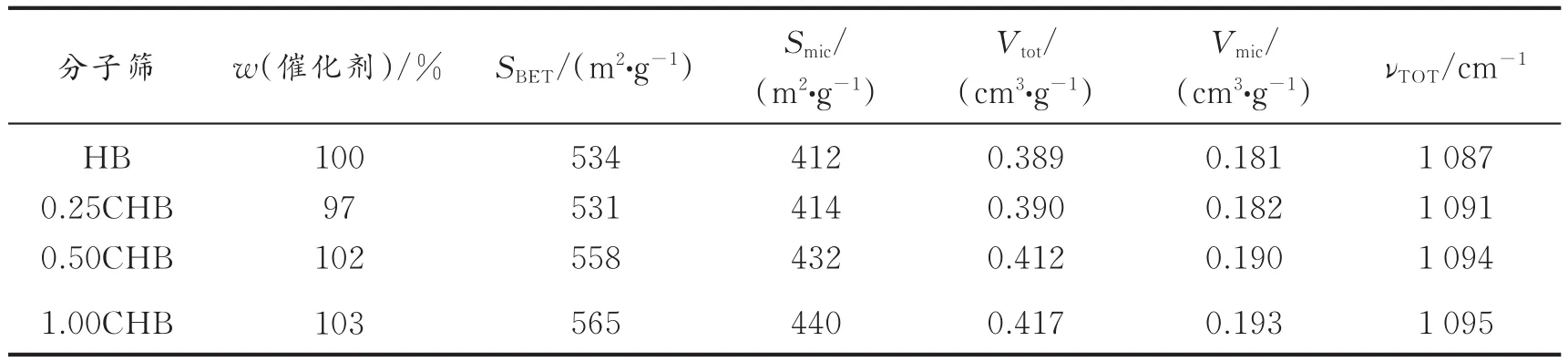
表1 不同浓度柠檬酸处理Hβ分子筛的织构性质及骨架不对称振动波数Table 1 Basic physical parameters and νTOTof modified Hβ zeolites with different concentrations of citric acid
2.1.3 Hβ分子筛的HK孔分布 图3为改性Hβ分子筛HK法测定的微孔分布。
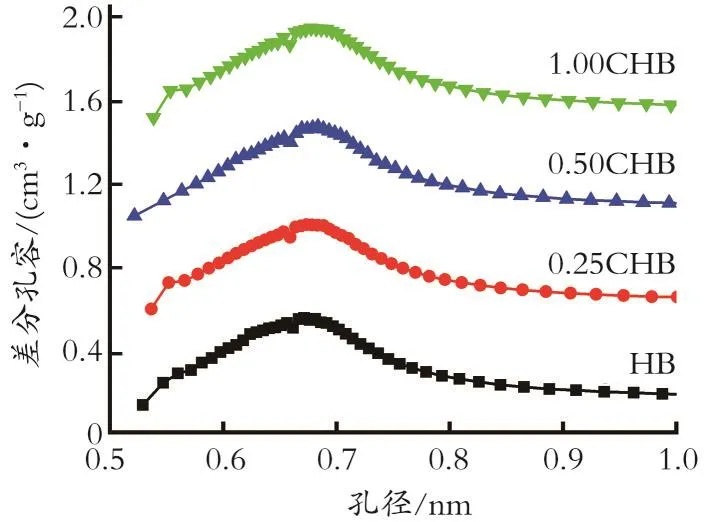
图3 不同浓度柠檬酸改性Hβ分子筛的HK孔分布Fig.3 HK micropore size distributions of modified Hβ zeolites with different concentrations of citric acid
从图3可以看出,4种分子筛均在0.67 nm附近具有最可几孔径分布。但是从表1给出的上述样品的微孔比表面积以及微孔孔容来看,随着柠檬酸浓度的增大,二者均缓慢增加。产生的原因可能是由于柠檬酸并未对分子筛微孔结构造成破坏,而仅对微孔中存在的无定型结构进行选择性移除,也正是由于分子筛内无定型物种的移除,其改性分子筛的相对结晶度稍高于Hβ原粉(见表1)。
2.1.4 Hβ分子筛的BJH法介孔分布 图4为改性Hβ分子筛BJH法测定的介孔分布。从图4可以看出,4种分子筛均在10 nm附近具有最可几孔径分布,此处的孔应归属于分子筛晶粒间的堆积孔,结合表1给出的上述样品的介孔孔容来看,介孔孔容随柠檬酸浓度的提高缓慢增加,这是由于柠檬酸移除了分子筛晶间存在的无定型结构,进而增加了介孔孔容。

图4 不同浓度柠檬酸处理Hβ分子筛的BJH法介孔分布Fig.4 BJH mesopore size distributions of modified Hβ zeolites with different concentrations of citric acid
尽管柠檬酸与分子筛中非骨架物种的作用具有更大的选择性,但是柠檬酸仍然会对骨架铝产生一定的影响。Hβ分子筛在1 100 cm-1附近的吸收峰归属于分子筛骨架四面体的不对称伸缩振动,此吸收峰与分子筛骨架中的铝含量密切相关[9]。由表1中改性Hβ分子筛的红外光谱中骨架四面体不对称振动波数(νTOT)变化不难发现,随着柠檬酸浓度的增加骨架不对称振动波数逐渐向高频移动,说明样品发生了不同程度的骨架脱铝。尽管分子筛发生了骨架脱铝,但是其结晶度仍然保持良好,其原因在于柠檬酸与骨架铝的相互作用。
2.1.5 骨架脱铝与同晶取代机制 柠檬酸改性过程中的骨架脱铝与同晶取代机制如图5所示。
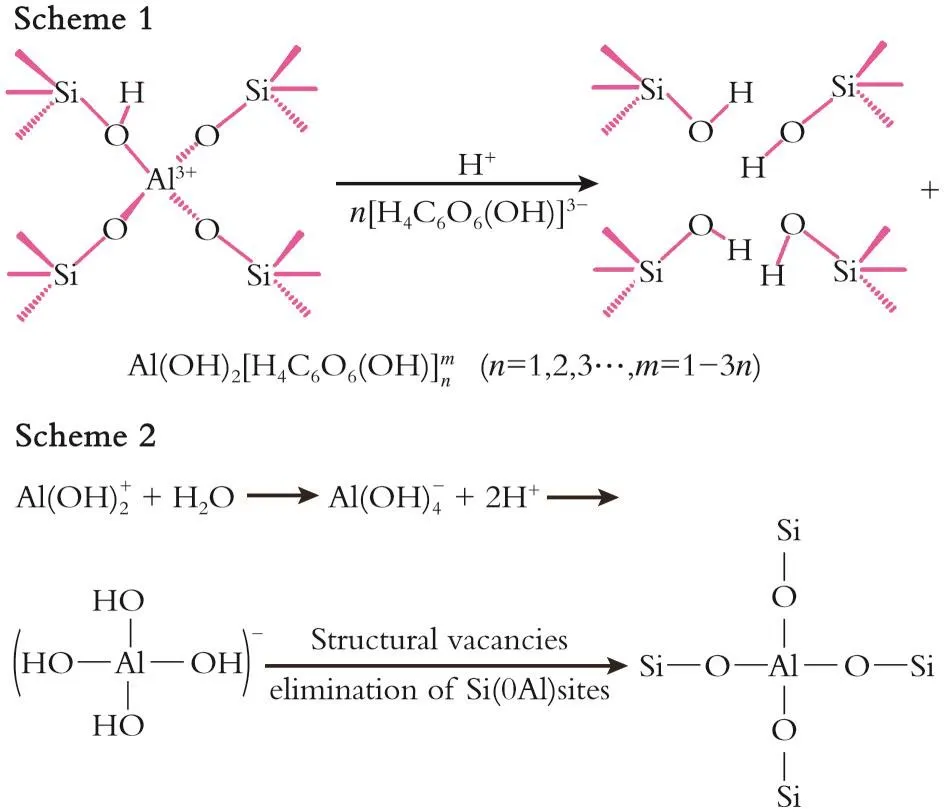
图5 柠檬酸改性过程中的骨架脱铝与同晶取代机制Fig.5 Mechanism of dealumination and aluminium rein⁃sertion on the Hβ zeolite during citric acid treatment
由于Hβ原粉n(Si)/n(Al)较大,分子筛中铝含量少,尽管在酸性环境下可以脱铝,但是基本骨架却仍然保持完整,脱铝产生的硅羟基(Si—OH)稳定,不易与含铝的柠檬酸螯合物进一步作用造成骨架的进一步破坏。与此同时,由于柠檬酸分子除具有—COOH基团外还具有—OH基团,—OH基团会与脱除的骨架Al物种重新形成Al(OH)-4,该物种会重新进入分子筛骨架中,实现分子筛中Al原子的重排,增强了分子筛的骨架稳定性[10]。
2.2 改性β分子筛活性中心与酸性质间的关联性
2.2.1 Hβ分子筛的NH3‐TPD表征 图6为柠檬酸改性Hβ分子筛的NH3‐TPD。由图6可知,4种Hβ分子筛均在150~250℃和250~350℃存在NH3脱附峰,分别对应的是分子筛的弱酸性位和中强酸性位。与未改性的Hβ分子筛相比,经柠檬酸改性的Hβ分子筛的总酸量随柠檬酸的浓度增加逐渐下降,说明分子筛中部分酸性活性中心在柠檬酸处理过程中被选择性移除。其中,柠檬酸主要移除了具有弱酸性的活性物种,其弱酸酸量在下降的同时其NH3脱附峰向左迁移,表明分子筛中可能存在不同类型的弱酸性活性物种,柠檬酸选择性地移除了其中酸性较强活性物种,或在酸处理过程中分子筛产生了新的弱酸中心,进而减弱了Hβ分子筛的弱酸性位。对分子筛的中强酸酸性位而言,其酸量及酸强度变化不大,表明柠檬酸对分子筛的中强酸活性中心影响较小。
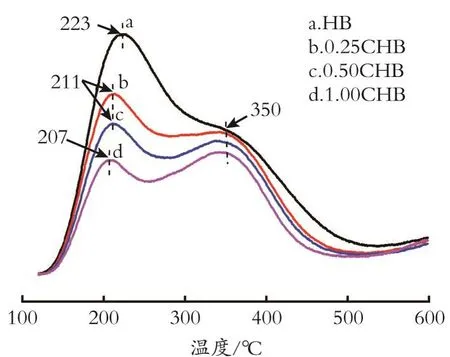
图6 不同浓度柠檬酸处理Hβ分子筛的NH3‐TPD谱图Fig.6 NH3⁃TPD profiles of modified Hβ zeolites with different concentrations of citric acid
2.2.2 Hβ分子筛的吡啶红外表征 图7给出了4种Hβ分子筛的吡啶红外(Py‐FTIR)谱图。由图7可见,3 745、3 735 cm-1分别归属于β分子筛外表面和内表面的硅羟基(Si—OH),与未处理的Hβ分子筛相比,柠檬酸处理后3 740、3 735 cm-1吸收峰均稍有增加且3 735 cm-1峰的变化更为明显,证明了柠檬酸导致了部分骨架脱铝,这个结果与上述柠檬酸处理后分子筛骨架不对称振动波数(νTOT)的蓝移结果可以很好地吻合。随着柠檬酸浓度的增加,归属于骨架硅铝桥羟基的3 607 cm-1的特征峰也发生了不同程度的变化。其中0.25CHB分子筛在3 607 cm-1处的羟基峰稍大于HB分子筛原粉,此时3 662 cm-1处的吸收峰已经完全消失,此处吸收峰与非骨架铝羟基相关,这些非骨架铝作为平衡阳离子往往与骨架氧相连[11]。当上述物种被选择性移除时,为平衡分子筛体系电荷,硅铝桥羟基产生,致使3 607 cm-1处的羟基峰增强。但是,随着柠檬酸浓度的升高,更多的柠檬酸与骨架铝作用,造成骨架脱铝,致使其羟基峰缓慢下降。以上实验结果说明,柠檬酸对于部分非骨架铝羟基物种的脱除能力大于对骨架铝脱除。另外,3 782 cm-1处的特征峰也随酸浓度的增大缓慢减少,其归属于缺陷位三配位的铝羟基物种,此物种与非骨架铝羟基物种相比更难脱除[12]。由此可见,柠檬酸也可以一定程度上对β分子筛中缺陷位的Al物种进行去除而不产生更多缺陷位的Al物种。
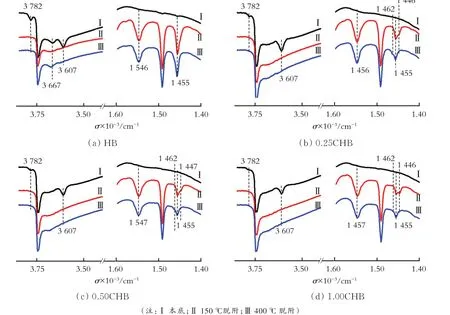
图7 不同浓度柠檬酸处理Hβ分子筛在不同脱附温度下的吡啶红外谱图Fig.7 Py⁃FTIR spectra of modified Hβ zeolites with different concentrations of citric acid after desorption at different temperatures
根据改性Hβ分子筛的吡啶吸附‐脱附红外谱图结果,并结合Hβ分子筛的羟基分布及随温度变化情况,发现经柠檬酸改性后不仅改变了分子筛酸性位的分布,也改变了吡啶与分子筛活性位的作用方式。未经柠檬酸处理的Hβ分子筛中分别归属于骨架硅铝桥羟基峰(3 607 cm-1),非骨架Al羟基峰(3 662 cm-1)和缺陷位三配位骨架Al羟基峰(3 782 cm-1)经150℃吡啶吸附‐脱附后均完全消失。与此同时,出现了在1 546 cm-1附近归属于吡啶吸附在B酸性位的振动吸收峰(PyH+)以及位于1 455 cm-1附近归属于吡啶吸附在L酸性位上的振动吸收峰(PyL)。其中,吡啶在B酸性位的吸附(PyH+)主要与分子筛中的硅铝桥羟基(Si-OH-Al)活性位(3 607 cm-1)相关,而与L酸有关的活性中心的归属却非常复杂,这主要取决于分子筛中非骨架Al物种或缺陷位Al物种的种类。
对比1 455 cm-1吸收峰在150、400℃不同脱附温度下的结果表明,Hβ分子筛存在强弱两种L酸中心。经400℃脱附后,3 662 cm-1附近的吸收峰基本恢复,说明此处存在的非骨架Al羟基物种可能具有弱L酸性;而3 782 cm-1处的吸收峰在高温脱附时未见恢复,证明吡啶与这种碱性的三配位的骨架Al羟基物种作用更强且具有强L酸酸性。对于1 546 cm-1附近的吸收峰而言,经400℃脱附后,此处吸收峰强度减弱,表明Hβ分子筛也存在强弱两种B酸中心,但是3 607 cm-1附近的吸收峰未见恢复,说明吡啶仍然与部分硅铝桥羟基存在作用,这种作用方式并非是吡啶分子与B酸位的直接作用(PyH+)而可能是其他吸附位上吡啶分子与其附近硅铝桥羟基的氢键作用(H‐bond作用)[13]。
Hβ分子筛经柠檬酸酸处理后,1 546 cm-1处的吸收峰并未发生根本性改变,与硅铝桥羟基(Si-OH-Al)活性位的变化相一致,证明柠檬酸处理主要移除了分子筛中的非骨架铝物种,而对骨架铝的移除作用较弱,因此对分子筛中的B酸中心影响不大。相比于1 546 cm-1处吸收峰的变化,在柠檬酸处理后,1 455 cm-1附近的吸收峰发生了显著的变化。随着柠檬酸浓度的提高其峰强度明显减弱,证明柠檬酸在移除非骨架铝物种的同时选择性地移除了一部分L酸中心。这一部分L酸中心与柠檬酸处理后3 662 cm-1处吸收峰的消失有关,再次证明了具有单核或者多核的非骨架铝羟基物种是分子筛L酸中心的重要组成部分。另外,分子筛经柠檬酸处理后仍然存在强L酸中心,位于3 782 cm-1处的吸收峰在吡啶吸附前仍然存在且在400℃吡啶脱附后未见恢复,再次证明了缺陷位三配位骨架Al羟基物种具有强L酸酸性且不易在柠檬酸作用下移除。另外,分子筛中也可能存在不具有羟基的非骨架铝物种(AlO+),此类物种不能被原位红外光谱检测,但是与吡啶分子存在强吸附作用。
经柠檬酸处理后,在150℃脱附温度下,在1 447 cm-1附近出现了一个明显的吸收峰,此吸收峰在400℃脱附温度下消失,而在1 462 cm-1处出现了一个新的吸收峰。J.P.Marques等[4]将1 445 cm-1附近的吸收峰归属为吸附在L酸中心并与临近的羟基有键合的吡啶分子振动吸收峰,并将经高温脱附后出现的1 462 cm-1处吸收峰与前者进行关联,归属于同时与B酸和L酸中心发生协同作用的亚胺离子的振动吸收峰。
2.2.3 吡啶吸附在Hβ分子筛上的红外表征 图8为150℃、不同浓度下吡啶吸附在Hβ分子筛上的原位红外谱图,进一步分析吡啶与分子筛各活性组成单元的作用形式。从图8中可以看出,当吡啶的浓度在较低时,已经出现了吡啶在B酸中心的吸附(对应于1 636、1 546 cm-1吸收峰的出现)和在L酸中心上的吸附(对应于1 621、1 455 cm-1吸收峰的出现)。与此同时,归属于分子筛中的硅羟基吸收峰(3 745、3 735 cm-1),硅铝桥羟基峰(3 607 cm-1),以及缺陷位处三配位的骨架Al羟基峰(3 782 cm-1)均发生了不同程度的减弱,而非骨架Al羟基峰(3 662 cm-1)却没有发生明显变化。证明了吡啶分子会优先吸附在酸性较强的活性位上,其吡啶分子与各活性位的吸附形式见图9。
另外,分子筛中的末端硅羟基(Si-OH)也可能具有酸性,与吡啶在B酸中心和L酸中心上的作用形式不同,吡啶分子会与硅羟基发生氢键作用(PyH)[13],导致吡啶浓度继续增加时此处羟基峰红移而在3 700~3 660 cm-1内形成宽峰,其吡啶分子与末端硅羟基基团的吸附形式见图10。
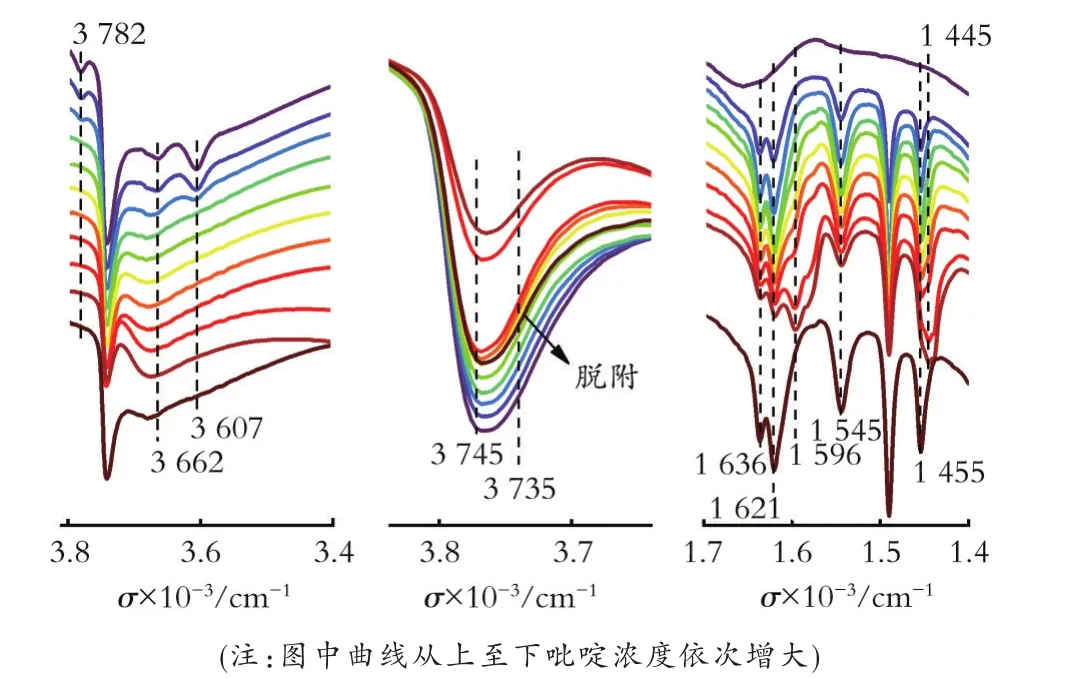
图8 150℃和不同浓度下吡啶吸附在Hβ分子筛上的原位红外光谱Fig.8 FTIR spectra of pyridine dosed on the Hβ zeolite at 150℃with different concentration and at degassingtemperature of 150℃for each dose
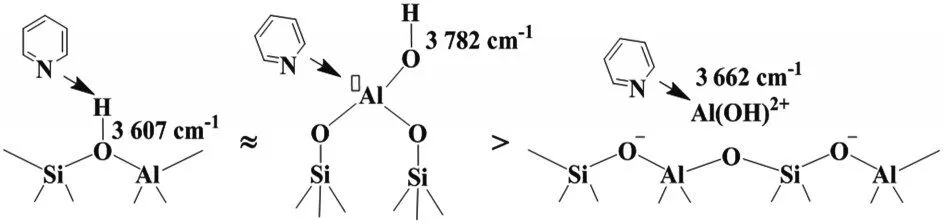
图9 吡啶与Hβ分子筛不同活性组成单元的作用机制Fig.9 Mechanisms of pyridine absorpted on constitument unit of active site in the Hβ zeolite
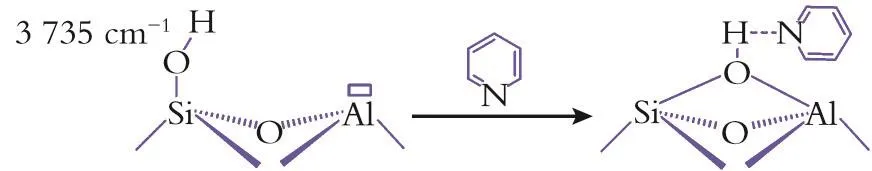
图10 吡啶与Hβ分子筛末端硅羟基基团的作用机制Fig.10 Mechanisms of pyridine absorpted on terminal silicon hydroxyl in the Hβ zeolite
随着浓度逐渐增加,上述羟基活性基团的峰强度逐渐减弱,吡啶与B酸性位和L酸性位的作用增强。但是,当浓度达到一定量时,归属于吡啶与硅羟基弱相互作用的吸收峰(1 596、1 445 cm-1)逐渐增强,而归属于吡啶吸附在B酸性位的振动吸收峰(1 636、1 546 cm-1)以及归属于吡啶吸附在L酸性位上的振动吸收峰(1 621、1 455 cm-1)逐渐减弱,发生这一现象的原因是由于当更多的吡啶分子进入到分子筛时,多个吡啶分子会同时吸附在同一活性位上(PyH…Py),受分子间相互作用的影响其吡啶在活性位上的吸收振动峰减弱[13‐14](吸附形式见图11)。经吡啶饱和吸附‐脱附后,硅羟基吸收峰部分恢复且1 596、1 445 cm-1吸收峰消失;吡啶吸附在B酸性位的振动吸收峰以及吡啶吸附在L酸性位上的振动吸收峰得以恢复,证明了上述提到两种吡啶与酸性位的作用形式很弱,更容易脱附。
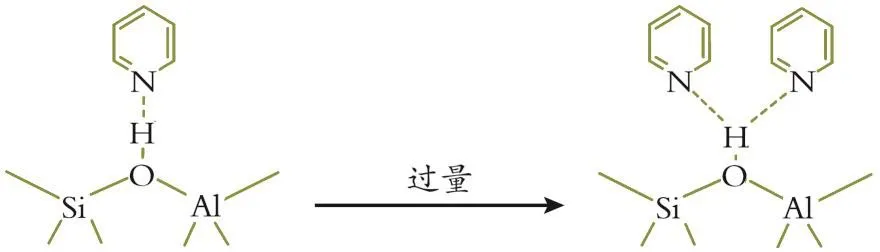
图11 吡啶与Hβ分子筛硅铝桥羟基基团的作用机制Fig.11 Mechanisms of pyridine absorpted on bridging hydroxyl(Si-OH-Al)in the Hβ zeolite
3 结 论
Hβ分子筛除存在与硅铝桥羟基相关的B酸中心外,还存在与非骨架铝羟基基团有关的弱L酸中心以及与缺陷位处三配位的Al羟基物种和AlO+有关的强L酸中心。非骨架铝物种与临近的硅铝桥羟基间存在协同作用,吡啶分子可以吸附在其L酸中心处并与临近B酸中心产生键合,在高温时更不易脱附。吡啶分子会优先吸附在酸性较强的硅铝桥羟基和缺陷位处三配位的Al羟基活性位上,而与非骨架铝羟基基团作用较弱。经柠檬酸处理后,分子筛中部分非骨架铝羟基物种被选择性移除,且未对骨架铝造成严重破坏。Hβ分子筛经柠檬酸处理后仍存在强L酸中心,此强L酸中心的存在方式可能与AlO+和缺陷位的三配位的Al物种有关。
